Способ моделирования полиорганной патологии у крыс
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к экспериментальной патофизиологии, и может быть использовано для изучения механизмов формирования, прогрессирования и терапии заболеваний внутренних органов. Для моделирования полиорганной патологии крысам ежедневно в течение 180 суток с кормом вводят 33 г сухого молока, 42,5 г свиного сала и 4,3 г чистого порошкового холестерина из расчета на 1000 г массы животного. Способ позволяет получить простую, воспроизводимую модель полиорганной патологии, наиболее точно отражающую структурно-функциональную реорганизацию печени, почек, сердца, характеризующуюся формированием системного фиброза, некроза тканей органов-мишений, сопровождающуюся ожирением, дислипидемией, гипергликемией. 3 табл., 3 ил.
Реферат
Изобретение относится к медицине, а именно к экспериментальной патофизиологии, и может быть использовано для изучения механизмов формирования, прогрессирования и терапии заболеваний внутренних органов.
В настоящее время отмечается рост сочетанной патологии в структуре заболеваемости [Буеверова Е.Л., Драпкина О.М., Ивашкин В.Т. Атерогенная дислипидемия и печень // Рос. мед. вести. 2008. №1. С.17-23; Лопаткин Н.А., Яковенко Э.К. Мочекаменная болезнь // Рус. мед. журн. 2000. Т.8, №3. С.117-120; Chitturi S., Farrell G.C. Etiopathogenesis of non-alcoholic steatohepatitis // Semin. Liver. Dis. 2001. N 21. P.27-41; Vasan R.S. Cardiac function and obesity // Heart. 2003. Vol.89. P.1127-1129]. На сегодняшний день рассматривать монопатологию приходится все реже. Изучение патогенетических и саногенетических аспектов заболеваний внутренних органов обычно проводится с использованием экспериментальных моделей конкретных заболеваний органов-мишений.
Известен способ моделирования кардиовазоренальной гипертензии у крыс, основанный на введении экспериментальным животным кардиовазо-нефропатогенной полусинтетической диеты, обогащенной холестерином, солями двузамещенного фосфорнокислого водного натрия при дефиците калия и магния [Пат. RU 2327228. Способ моделирования кардиовазоренальной артериальной гипертензии у крыс. Новгородцева Т.П., Антонюк М.В., Котельников В.Н и др. Опубл. 20.06.2008]. Одновременно осуществляют замену питьевой воды 1% раствором хлорида натрия с последующим холодовым воздействием через 2 недели в условиях содержания крыс в течение 4 ч при 4°С. В результате развивается органическое поражение сердечной ткани и эпителия почек.
Известен способ моделирования цирроза печени путем интрагастрального введения лабораторному животному два раза в неделю в течение месяца 50%-ный раствор совтола-1 на оливковом масле из расчета 0,25 мл на 100 г массы тела и 10%-ный раствор этанола вместо воды для питья [Пат. RU 2197018. Способ моделирования цирроза печени. Мышкин В.А., Ибатуллина Р.Б., Савлуков А.И. и др. Опубл. 20.01.2003].
Перечисленные выше способы заболеваний внутренних органов способствуют органическому поражению конкретного органа-мишени.
Известен способ моделирования системного фиброза у экспериментальных животных путем 4-6-кратного с перерывами в 1 неделю введения смеси четыреххлористого углерода в вазелиновом масле в соотношении 1:1 в объеме 0,3-0,4 мл подкожно. Предварительно за 15-20 мин до каждого введения смеси вводят купренил в дозе 0,1-0,2 мг/кг [Пат. RU 2371778. Способ моделирования системного фиброза. Лазебник Л.Б., Потапова В.Б., Лычкова А.Э., опубл. 27.10.2009]. В результате чего развивается фиброз печени, почек, сердца, поджелудочной железы.
Однако недостатком этого способа является то, что патогенетическим фактором развития системного фиброза оказывается высокотоксичные химические вещества, что в значительной степени отличается от реальных причин, способствующих формированию полиорганной патологии (ПП) у людей.
Одной из главных причин патогенеза заболеваний внутренних органов является алиментарный фактор [Гонсалес Д.Э. Питание как фактор риска развития гипертонической болезни легких и ишемической болезни сердца // Вопр. питания. 2008. Т.77. №3. С.15-20]. Известно, что гиперхолестеринемия, системное воспаление становятся триггерными механизмами развития патологии гепатобилиарной, сердечно-сосудистой, мочевыделительной систем. Следовательно, существуют трудности в экстрополяции экспериментальных данных по изучению механизмов развития полиорганной патологии на человека. В связи с этим для изучения механизмов формирования ПП, разработки новых подходов в профилактики и лечения с применением современных достижений науки и техники исследователям требуются экспериментальные модели, наиболее приближенные к реальным клиническим условиям.
По результатам проведенных патентных исследований и анализа научной медицинской литературы авторы изобретения не выявили конкретных рекомендаций по моделированию ПП, характерных для реальных условий развития данных заболеваний у людей.
Наиболее близким техническим решением, принятым за прототип, является способ формирования алиментарной гиперхолестеринемии по Koichi А. Согласно этому способу экспериментальных крыс содержат в течение 11 недель на гиперхолестериновом рационе (3,5 г холестерина на 1000 г массы тела животного). В результате у крыс формируется гиперхолестеринемия, нарушение функции печени [Koichi A., Kazuhisa F., Takhi О. Simultaneous occurrence of hypercholesterolemia // Life Sci. 1986. Vol.39, N 6. P.499-505]. В данном способе-прототипе нарушение структуры и функции сердца, почек не происходит.Следовательно, с помощью известного способа-прототипа невозможно воспроизвести полиорганную патологию.
Учитывая возможность развития патологии внутренних органов при несбалансированном гиперкалорийном питании, а также принимая во внимание, что гиперхолестеринемия является ведущим фактором развития заболеваний органов-мишений, представляет интерес разработка способа моделирования полиорганной патологии путем воздействия на экспериментальных животных гиперкалорийным рационом.
Задача изобретения состоит в том, чтобы создать более простой способ моделирования полиорганной патологии у крыс с повышенной точности воспроизведения полиорганной патологии, за счет высокого приближения к клиническому течению заболевания внутренних органов, путем воздействия на животных алиментарными патогенетическими факторами.
Для этого в способе моделирования полиорганной патологии у крыс, путем скармливания экспериментальным животным патогенного корма, согласно изобретению в течение 180 суток каждые сутки в основной рацион животным добавляют 33 г сухого молока, 42,5 г свиного сала и 4,3 г чистого порошкового холестерина из расчета на 1000 г массы крыс.
По истечении 180 суток от начала вскармливания патогенным рационом у крыс методом гистологического исследования тканей печени, почек, сердца выявляют структурные нарушения данных органов, характеризующиеся разрастанием соединительной ткани, появлением некротических участков, тромбозов.
Общими с прототипом признаками являются следующие:
- скармливание экспериментальным животным патогенного корма (гиперхолестериновый рацион).
Отличительными признаками являются следующие:
- длительной алиментарной нагрузки возрастает до 180 суток;
- в течение 180 суток каждый день с кормом животным вводят 33 г сухого молока, 42,5 г свиного сала и 4,3 г чистого порошкового холестерина из расчета на 1000 г массы крыс.
При использовании изобретения увеличивается общий калораж рациона за счет нагрузки холестерином, сухим молоком, свиным салом, пролонгируется срок воздействия алиментарной гипержировой нагрузкой, отмечается стабильная прибавка в весе у крыс в течение всего периода эксперимента. Помимо структурной реорганизации печени, почек, сердца предложенный способ моделирования полиорганной патологии сопровождается многими метаболическими нарушениями (гипертриглицеридемия, гиперхолестеринемия, гипергликемия), являющимися основополагающими патогенетическими факторами заболеваний внутренних органов. Изобретение дает возможность изучения механизмов формирования алиментарнозависимых заболеваний.
Проведенные патентные исследования и анализ научной медицинской информации, отражающие методологию создания экспериментальных моделей полиорганной патологии с сопутствующими метаболическими нарушениями, не выявили технологий моделирования ПП на экспериментальных животных, содержащих всю совокупность существенных признаков заявленного изобретения. Таким образом, заявленное техническое решение соответствует критерию «новизна». Заявляемое изобретение может быть использовано в экспериментальной медицине и биологии согласно своему назначению и на этом основании оно соответствует критерию «промышленная применимость».
Сделать вывод о том, что заявляемое изобретение для специалиста явным образом не следует из уровня техники позволяет тот факт, что до настоящего времени проблемы профилактики, лечения и механизма развития заболеваний внутренних органов окончательно не решены. Предложенное решение не является простой модификацией известных способов, оно дает неожиданно высокий результат и 100%-ную воспроизводимость у подопытных животных. Предлагаемый способ моделирования ПП несложен в техническом воспроизведении и создает условия для проведения совершенно оригинальных и имеющих огромное практическое значение для медицины и биологии работ по выяснению патогенетических механизмов формирования болезни печени, сердца, почек и причин, способствующих запуску процессов фиброгенеза. На этом основании можно заключить, что заявляемый способ соответствует критерию «изобретательский уровень».
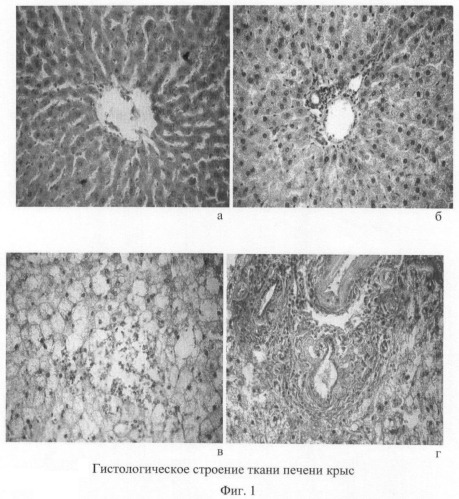
На фиг.1 представлено гистологическое строение ткани печени крыс, получавших алиментарную патогенную нагрузку:
а - контрольная группа. На гистологическом препарате представлена центральная зона печени с центральной веной, от которой радиально отходят печеночные балки и синусоидные капилляры. Окраска гематоксилином и эозином. Ув. ×150;
б - контрольная группа. На препарате представлена портальная зона печени крыс. Коллагеновые волокна обнаруживаются в незначительных количествах вокруг портальных трактов. Окраска пикрофуксином по Ван-Гизону. Ув. ×150;
в - опытная группа (180 суток патогенной нагрузки). Очаговый некроз. Окраска гематоксилином и эозином. Ув. ×150;
г - опытная группа (180 суток патогенной нагрузки). Гистологический срез ткани печени с разросшейся соединительной тканью вокруг триады. Окраса пикрофуксином по Ван-Гизону. Ув. ×150.
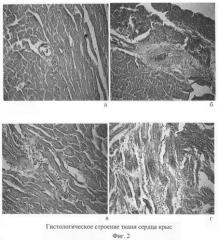
На фиг.2 представлено гистологическое строение ткани сердца крыс, получавших алиментарную патогенную нагрузку:
а - контрольная группа. Окраска гематоксилином и эозином. Ув. ×150;
б - опытная группа (180 суток патогенной нагрузки). На препарате показано утолщение стенок, сужение просвета сосуда. Застой крови в венуле. Окраска гематоксилином и эозином. Ув. ×100;
в - опытная группа (180 суток патогенной нагрузки). На гистологическом препарате показан инфарктоидный участок миокарда. Окраска гематоксилином и эозином. Ув. ×150;
г - опытная группа (180 суток патогенной нагрузки). На препарате показано увеличение доли стромы в миокарде крыс. Выявляется большое количество тонких извитых, беспорядочно расположенных коллагеновых волокон. Окраска гематоксилином и эозином. Ув. ×150.
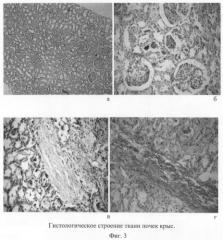
На фиг.3 представлено гистологическое строение ткани почек крыс, получавших алиментарную патогенную нагрузку:
а - контрольная группа; гистологический срез окрашен гематоксилином и эозином. Ув. ×150;
б - опытная группа (180 суток патогенной нагрузки). На препарате корковый слой почки. Деструкция канальцев. Крупные очаги кровоизлияния. Окраска гематоксилином и эозином. Ув. ×150;
в - опытная группа (180 суток патогенной нагрузки). Гистологический срез почки крыс с хорошо видимыми соединительнотканными тяжями. Окраска гематоксилином и эозином. Ув. ×150;
г - опытная группа (180 суток патогенной нагрузки). Гистологический срез почки крыс со склерозом клубочковой зоны. Окраска пикрофуксином по Ван-Гизону. Ув. ×150.
Для создания модели полиорганной патологии использовались белые крысы линии Вистар. Для воспроизведения экспериментальной модели использованы половозрелые особи мужского пола, средней массой 180,5±10,6 г. При разработке модели отрабатывалось воспроизведение нескольких аналогичных экспериментальных состояний, все варианты модификаций воспроизводимых моделей анализировались на основании гистологических исследований ткани печени, почек, сердца. Отобраны были те модели, при воспроизведении которых достигались стойкие структурные нарушения органов-мишений, сопровождающиеся жировой инфильтрацией, образованием некроза, фиброза при отсутствии смертности экспериментальных животных.
Способ моделирования полиорганной патологии осуществляют следующим образом. Животные в течение 180 суток (6 месяцев) находятся на специальной гиперкалорийной патогенной диете, обогащенной насыщенными жирами животного происхождения (сухое молоко, свиной жир, холестерин) (табл.1).
| Таблица 1 | ||
| Суточный рацион крыс (г/1000 г массы животного) | ||
| Ингредиенты | Экспериментальный рацион | Общевиварный рацион |
| Свиное сало | 42,5 | 5 |
| Холестерин | 4,3 | - |
| Сухое молоко | 33 | - |
| Подсолнечное масло | 5 | 50 |
| Смесь зерновая | 50 | 5 |
| Хлеб пшеничный (сухари) | 20 | 20 |
| Крупа овсяная | 13 | 13 |
| Мясо говяжье второй категории | 20 | 20 |
| Морковь | 33 | 33 |
| Зелень | 33 | 33 |
| Дрожжи пивные | 0,5 | 0,5 |
| Соль поваренная | 1 | 1 |
В диету включен холестерин, как один из факторов, активизирующих липидные нарушения, процессы жировой инфильтрации, патологическую структурную реорганизацию внутренних органов. Среди патогететически ориентированных факторов базовой являлась жировая нагрузка сухим молоком и свиным салом, увеличивающим общий калораж рациона патогенной диеты. То есть в модели полиорганной патологии инициируются механизмы, характеризующиеся ожирением, дислипидемией, гипергликемией.
Для обоснования заявленного изобретения в лаборатории биомедицинских исследований НИИ Медицинской климатологии и восстановительного лечения (г.Владивосток) были проведены экспериментальные работы на крысах линии Вистар.
Для исследования выделялось 2 группы крыс:
контрольная группа - интактные крысы, содержащиеся на стандартном рационе вивария (20 голов);
опытная группа - крысы, содержащиеся на экспериментальном гиперкалорийном рационе в течение 180 суток (10 голов).
Животные ежедневно осматривались, учитывалась поедаемость корма. За время опыта не было случаев падежа и заболеваний животных. Эвтаназию животных осуществляли путем декапитации под эфирным наркозом в соответствии с требованиями Европейской конвенции по защите экспериментальных животных 86/609 EEC [European Convention for the Protection of Vertebrate Animals used for exsperimental and other scientific purposes. Strasburg: Council of Europe, 1986: 51]. Оценивались биометрические показатели: вес крысы, индекс Кетле, относительная и абсолютная масса печени, почек, сердца, висцерального жира. Уровень липидов, глюкозы и активность аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), лактатдегидрогеназы (ЛДГ) в сыворотке крови исследовали с помощью биохимического анализатора FP-901 (Финляндия) с помощью наборов фирмы «Ольвекс» (Россия). Определяли уровень общего холестерина (ОХС), триглицеридов (ТГ), ХС липопротеидов высокой плотности (ХС ЛПВП), результаты выражали в ммоль/л. Холестерин липопротеидов низкой (ЛПНП) и очень низкой плотности (ЛПОНП) определяли расчетным методом по формулам Фридвальда. Индекс атерогенности (ИА) рассчитывали по формуле ОХС-ХС ЛПВП/ХС ЛПВП [Климов А.Н., Никульчева Н.Г. Обмен липидов, липопротеидов и его нарушения. СПб.: Питер Ком, 1999, 512]. Для проведения гистологического исследования ткани печени (центральной части правой доли органа), почек, сердца небольшие фрагменты фиксировались в 10%-ном растворе нейтрального формалина, приготовленного на 0,07 М фосфатном буфере (рН=6,98). Обезвоживание тканей проводили в этиловом спирте возрастающей концентрации и заливали в парапласт. Далее с помощью микротома (МЗП-01 «ТЕХНОМ») готовили срезы исследуемых органов толщиной 7 мкм. Для гистологических исследований срезы тканей печени, почек, сердца окрашивали гематоксилином и эозином по Романовскому, пикрофуксином по Ван-Гизону на выявление коллагеновых волокон [Пирс Э. Гистохимия. М.: Изд-во иностр. литературы, 1962. 967]. Препараты исследовали при помощи микроскопа фирмы «Carl Zeiss» (Германия) (ув. об. ×10, ×40 и ×90).
Данные, полученные в результате исследований, приведены в графических и табличных материалах.
Весоростовые параметры крыс представлены в таблице 2. У всех крыс опытной группы по сравнению с интактной группой выявлено увеличение массы тела, индекса Кетле, массы висцеральной жировой ткани и внутренних органов. Результаты исследования продемонстрировали формирования алиментарного ожирения, гипертрофии органов в условии воздействия патогенным высокожировым рационом.
Изучение показателей липидного обмена показало, что у крыс под влиянием патогенного рациона формировалась алиментарная дислипидемия, проявляющаяся повышением уровня ОХС, ТГ в сыворотке крови (табл.3). При этом ХС ЛПВП снижался более чем в 2 раза, а индекс атерогенности увеличился на порядок (р<0,001). Обнаруженные низкие значения ХС ЛПОНП у крыс опытной группы являются одним из критериев метаболических нарушений в печени и развития стеатогепатита [Буеверова Е.Л., Драпкина О.М., Ивашкин В.Т. Атерогенная дислипидемия и печень // Рос. мед. вести. 2008. №1. С.17-23]. Формирование ПП сопровождалось развитием гипергликемии, доказательством чего явилось повышение уровня глюкозы в крови опытной группы крыс. Морфофункциональное состояние печени и ткани сердца крыс опытных групп оценивали по активности в сыворотке крови ферментов - АЛТ, ACT, ЛДГ. У животных, содержавшихся на экспериментальном рационе, наблюдалось повышение активности ферментов трансаминаз (АЛТ, ACT) и ЛДГ (р<0,001), что свидетельствовало о повреждении целостности клеток, развитии цитолитического синдрома. Интерпретация выявленных изменений говорит о формировании заболеваний внутренних органов [11]. Причем снижение соотношения АСТ/АЛТ (коэффициент де Ритиса) на 180 сутки эксперимента свидетельствует о хроническом течении патологического процесса.
| Таблица 2 | ||
| Весоростовые параметры крыс при моделировании ПП, М±m | ||
| Показатели | Контрольная группа, n=20 | Опытная группа, n=10 |
| Вес крысы до эксперимента, г | 168,0±4,1 | 180±28 |
| Вес крысы после окончания эксперимента, г | 250,0±8,9 | 471,2±67,9** |
| Прирост массы тела, г | 82±4,2 | 280,2±65,7*** |
| Рост крысы, см | 19,4±0,1 | 26,3±0,3* |
| Индекс Кетле, у.е. | 6,7±0,2 | 8,4±1,2** |
| Масса печени, г | 8,16±0,23 | 27,9±4,1*** |
| Масса висцерального жира, г | 5,91±0,68 | 12,5±3,4*** |
| Масса почек, г | 2,10±0,07 | 2,9±0,3* |
| Масса сердца, г | 1,08±0,03 | 1,3±0,1* |
| Примечание здесь и далее: (*) - статистическая значимость различий относительно контрольной группы: * - р<0,05; ** - р<0,01; *** - р<0,001. |
| Таблица 3 | ||
| Биохимические показатели крови крыс при моделировании ПП, М±m | ||
| Показатели | Контрольная группа, n=20 | Опытная группа, n=10 |
| ОХС, ммоль/л | 1,57±0,04 | 2,04±0,17* |
| ТГ, ммоль/л | 1,12±0,04 | 1,95±0,06*** |
| ХС ЛПВП, ммоль/л | 0,67±0,04 | 0,26±0,02*** |
| ХС ЛПНП, ммоль/л | 0,7±0,16 | 0,9±0,06 |
| ХС ЛПОНП, ммоль/л | 0,65±0,19 | 0,20±0,03*** |
| ИА, у.е. | 1,43±0,15 | 7,4±0,8*** |
| Глюкоза, ммоль/л | 5,4±0,1 | 12,0±0,3*** |
| АЛТ, ммоль/л | 52,2±3,5 | 172±12*** |
| ACT, ммоль/л | 118,6±6,1 | 165,6±2,5*** |
| ЛДГ, ммоль/л | 936±133 | 1285±56,1*** |
| АСТ/АЛТ, у.е. | 2,26±0,10 | 0,96±0,07*** |
Доказательством развития модели полиорганной патологии у животных служило исследование гистологических срезов ткани печени, почек, сердца, окрашенных гематоксилином и эозином по Романовскому и пикрофуксином по Ван-Гизону на выявление коллагена.
Печень. Структура ткани печени крыс опытной группы подверглась значительным деструктивно-дистрофическим изменениям, выразившимся в увеличении площади некротизированных участков (10-15% от общей площади исследуемых участков печени) (фиг.1в). Деструктивные изменения гепатоцитов сопровождались увеличением мезанхимально-клеточной реакцией, особенно заметной в зонах портальных трактов, где обнаруживалось скопление круглоклеточной инфильтрации. Гепатоциты не образовывали трабекул, располагались беспорядочно, синусоиды резко сужены. Было отмечено расширение крупных портальных трактов за счет разрастания стромы и заполнения ее воспалительным инфильтратом. Некоторые портальные тракты были с некротическими изменениями сосудов. Стенки таких сосудов слабо различались. Выявлялась деструкция желчных протоков. Паренхима печени крыс имела вид жировой и гидропической дистрофии. На препаратах, окрашенных по Ван-Гизону, обнаруживались соединительнотканные тяжи, протянувшиеся от триад к центральной вене, перемоделирующие печеночную дольку, что является прямым доказательством сформировавшегося фиброза печени (фиг.1г).
Сердце. На гистологических препаратах ткани сердца крыс опытной группы обнаруживались коронарные сосуды с неравномерно утолщенными стенками артериол и венул, на отдельных участках с нарушением целостности эндотелия (фиг.2б). На поверхности поврежденных эндотелиоцитов наблюдалась адгезия эритроцитов, что свидетельствовало о тромбообразовании. В участках повреждения отмечалась «изъеденность» эндотелия, пикноз ядра эндотелиоцитов. Определялось мукоидное и фибриноидное набухание стенок сосудов. В части венул был виден тромбоз, гомогенизация и вакуолизация мышечной оболочки сосудистой стенки с явлениями ангиосклероза. Вокруг подобных сосудов наблюдались дистрофия и цитоз кардиомиоцитов с потерей ими поперечной исчерченности. В миокарде определялись мелкие диапедезные кровоизлияния. Под эпикардом имелось полнокровие сосудов. Обнаруживалось инфарктоидное повреждение кардиомиоцитов, некроз, потеря поперечной исчерченности и ядер клеток сердечной мышцы, нейтрофильная инфильтрация (фиг.2в). Были выявлены участки с плотной, светло-серой рубцовой тканью, что указывает на инфаркт миокарда. В периваскулярной ткани вокруг крупных артерий и вен наблюдалось разрастание соединительной ткани (фиг.2г).
Почки. Результаты исследования гистологического строения почек крыс опытной группы продемонстрировали формирование нефропатии, нефросклероза. Наблюдалось уменьшение мочевого пространства, появление в клубочках между капиллярами и капсулой спаек. Канальцы были выстланы уплощенным кубическим и призматическим эпителием с дистрофическими изменениями. В перитубулярных сосудах отмечался множественный гемостаз с тромбозами, в межканальцевой интерстиции - очаги кровоизлияний (фиг.2б). Граница между корковым и мозговым слоем сглажена. Клубочки средней величины, в отдельных клубочках расширено мочевое пространство. Встречались клубочки с обширной эндокапилярной пролиферацией и накоплением полиморфоядерных лейкоцитов. Обнаруживались сосуды с диффузно утолщенной стенкой. На гистологических препаратах почки, окрашенных по Ван-Гизону, отмечалось утолщение базальной мембраны боуменовой капсулы и образование соединительнотканных тяжей (фиг.2в, 2г).
Таким образом, удалось получить модель полиорганной патологии, характеризующуюся ожирением, дислипидемией, гипергликемией, нарушением структурной организации, некрозом ткани, формированием фиброза органов-мишеней (почки, печень, сердце). Разработанная модель полиорганной патологии позволяет изучать механизмы развития патологии внутренних органов. Развитие модели ПП учитывает большинство клинически значимых факторов повреждения органов, наиболее часто встречающиеся в патогенезе заболеваний внутренних органов.
Способ подтверждается следующим примером.
Крысе линии Вистар весом 220 г каждый день в течение 180 суток с кормом вводят 33 г сухого молока, 42,5 г свиного сала и 4,3 г чистого порошкового холестерина из расчета на 1000 г массы крыс.
Через 180 суток вес крысы увеличивается до 450 г. Отбирают биоптаты печени, почек, сердца.
Печень. При обзорной окраске гематоксилином и эозином балочная структура печени не сохранена. Обнаруживаются соединительнотканные тяжи, протянувшиеся от триад к центральной вене, перемоделирующие печеночную дольку. Большая часть гепатоцитов находится в состоянии жировой дистрофии. Цитоплазма оптически прозрачна; ядра гепатоцитов уплотнены и уменьшены в размере. Имеются двуядерные гепатоциты. Выявляется деструкция желчных протоков. Вокруг вен наблюдается скопление стромальных клеток и умеренно расширенные синусоиды. Ядерная область эндотелиальных клеток вен и артерий триад выбухает в просвет сосуда. В области умеренно расширенных центральных вен находятся дилатированные синусоиды с купферовскими клетками. Обнаруживаются участки полнокровия печени с наличием эритроцитов в синусоидах. При окрашивании по Ван-Гизону наблюдается окаймление сосудов центральных вен коллагенсодержащими структурами. В отдельных областях соединительнотканные волокна окаймляют группы гепатоцитов и отдельные гепатоциты. Из периваскулярного пространства узкие тяжи соединительнотканных волокон проникают в паренхиму печени. Вблизи отдельных резко расширенных синусоидов располагаются пучки коллагеновых волокон, которые прослеживаются и в пространстве Диссе.
Сердце. При окраске гематоксилином и эозином мышечные клетки преимущественно нормального строения, в отдельных кардиомиоцитах в околоядерной области выявляется зернистая дистрофия. Поперечная исчерченность кардиомиоцитов нарушена. Сосуды капиллярного типа, несколько расширенные, содержат эритроциты. При окраске по Ван-Гизону в отдельных участках миокарда преимущественно по ходу капилляров и прекапилляров расположены прослойки соединительной ткани. Обнаруживаются участки окрашенной перисарколеммальной ткани за счет содержащихся коллагеновых волокон. В мелких сосудах в дупликатурах базальной мембраны находятся адвентициальные клетки. Адвентициальные клетки (перициты) по ходу сосудов дифференцируются в фибробласты с последующим образованием коллагеновых волокон. В периваскулярной ткани вокруг крупных артерий и вен наблюдается разрастание соединительной ткани. Вокруг мелких сосудов коллагеновых волокон немного, вены расширены, кровенаполнены. Вокруг артерий находится много коллагеновых волокон, проникающих в мышечные пучки.
Почка. При окраске гематоксилином и эозином в мозговом слое почки канальцы расширены в разной степени. Нисходящий и восходящий отделы петли Генле также расширены. Эпителий канальцев уплощен из-за их растяжения; эпителиоцитов нормального строения немного. Мелкие сосуды содержат эритроциты. Эндотелий выбухает в просвет артерии вследствие сокращения ее стенки. При специальной окраске на коллагеновые волокна выявляются сохранные клубочки с отслоенной от клубочков капсулой. Капсула тонкая, коллагенизированная. Вокруг канальцев обнаружены коллагеновые волокна. Вокруг вен находится коллагенсодержащая ткань. Периваскулярная область крупных артерий содержит большое количество коллагеновых волокон. Наибольшее развитие соединительной ткани наблюдается в периваскулярной области.
Проведено моделирование полиорганной патологии у 10 крыс.
Морфологическое исследование подтвердило успешное решение поставленной задачи изобретения.
Отмечаемые в настоящее время негативные тенденции в питании населения характеризуются дефицитом нутриентов - снижением в рационе полноценных белков, недостатком большинства витаминов, дефицитом полиненасыщенных жирных кислот, нерационально высоким потреблением животных жиров и низким уровнем пищевых волокон [Доценко В.А. Теоретические и практические проблемы питания здорового и больного человека // Вопр. питания. 2004. №6. С.36-39]. Разбалансированность рациона питания неизбежно влечет за собой нарушение и сбои обменных процессов, следствием которых является гипергликемия, дислипидемия, избыточная масса тела и ожирение [Доценко В.А., Мосийчук Л.В., Парамонов А.И. Ожирение у детей и подростков: современные аспекты // Вопр. детской диетологии. 2004. Т.2, №3. С.25-32]. Алиментарные факторы играют важную роль в этиопатогенезе заболеваний сердечно-сосудистой (атеросклероз, ишемическая болезнь сердца, инфаркт миокарда, мозговой инсульт), гепатобилиарной (стеатоз печени, стеатогепатит, острый или хронический панкреатит), мочевыделительной (нефрокальциноз, нефросклероз) систем [Гонсалес Д.Э. Питание как фактор риска развития гипертонической болезни легких и ишемической болезни сердца // Вопр. питания. 2008. Т.77. №3. С.15-20]. Нередко нарушение липидного обмена способствует формированию полиорганой патологии. В предложенном способе моделирования ПП были инициированы основные патогенетические триггерные механизмы, запускающие процессы системного фиброгенеза. Таким образом, полученные данные свидетельствует об идентичности экспериментально вызванных патогенетических изменений предложенной модели ПП описанным в литературе механизмам.
Результаты исследования свидетельствуют о несомненной экономической привлекательности использования данной модели. В первую очередь модель ПП может позиционироваться в области хронических экспериментов для оценки степени нарушения функционального состояния внутренних органов и поиска эффективных фармакотерапевтических органотропных средств. Кроме этого создание модели проводится при отсутствии смертности животных, а также используется наиболее доступный биологический вид - крысы, что является важным и соответствует поставленной цели. Создание такой модели делает возможным проведение экспериментов, постановка которых в клинике является практически неосуществимой. Новая модель ПП может быть использована для проведения поиска и испытания действия вновь синтезированных или полученных из естественных источников органотропных препаратов.
Таким образом, проведенные исследования позволили получить новую экспериментальную модель полиорганной патологии, в основе которой лежит комплексное сочетание патологических факторов, инициирующих каскад повреждений в печени, сердце, почках, приводящих к развитию стойких морфофункциональных нарушений. Предложенная модель проста в исполнении, отличается хорошей воспроизводимостью, отсутствием летального исхода экспериментальных животных.
Техническим результатом изобретения является повышение воспроизводимости, упрощение способа и приближение к клиническому течению патологии органов-мишений.
Предлагаемый способ моделирования позволяет в большей мере приблизиться к клиническому течению патологического процесса в органах гепатобилиарной, мочевыделительной, сердечно-сосудистой систем.
Предлагаемым способом воспроизводится надежная модель патологии внутренних органов, что подтверждено морфологическим анализом печени, почек, сердца и биохимическими показателями крови. Кроме того, способ обеспечивает возможность изучения механизмов развития алиментарнозависимых заболеваний.
Способ моделирования полиорганной патологии у крыс путем скармливания экспериментальным животным патогенного корма, отличающийся тем, что ежедневно в течение 180 суток с кормом животным вводят 33 г сухого молока, 42,5 г свиного сала и 4,3 г чистого порошкового холестерина из расчета на 1000 г массы крысы.