Способы и системы для получения многоатомных спиртов
Иллюстрации
Показать всеОписаны способы получения пропиленгликоля, этиленгликоля и других многоатомных спиртов, двухатомных спиртов, кетонов, альдегидов, карбоновых кислот и спиртов из биомассы, с использованием водорода, получаемого из биомассы. Способы включают реагирование части водного потока сырьевого раствора биомассы в присутствии катализатора в условиях реформинга водной фазы с получением водорода, и затем взаимодействие водорода и сырьевого водного раствора в присутствии катализатора с получением пропиленгликоля, этиленгликоля и других многоатомных спиртов, двухатомных спиртов, кетонов, альдегидов, карбоновых кислот и спиртов. Описанные способы можно проводить при более низкой температуре и давлении, и они позволяют обеспечить получение кислородсодержащих углеводородов без необходимости подачи водорода из внешнего источника. 6 н. и 56 з.п. ф-лы, 16 пр., 11 ил.
Реферат
Данное изобретение было осуществлено при поддержке правительства Соединенных Штатов с помощью DOC NIST Grant No. 70NANB3H3014 и DOE Grant No.DE-FG36-05GO15046. Соединенные Штаты обладают определенными правами на это изобретение.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способам, катализаторам и реакционным системам для получения одного или более кислородсодержащих углеводородных продуктов из водного потока сырья, содержащего водорастворимый кислородсодержащий углеводород. Предпочтительно, продукты реакции включают двухатомные спирты и другие многоатомные спирты, кетоны, альдегиды, карбоновые кислоты и/или спирты, получаемые путем гидрогенизации водорастворимых многоатомных спиртов (таких как глицерин) в сырье, полученном из биомассы, с использованием водорода, получаемого в пределах реакционной системы из части потока сырьевой биомассы.
УРОВЕНЬ ТЕХНИКИ
Биомасса (материал, полученный из живых или недавно умерших биологических материалов) становится одним из наиболее важных возобновляемых ресурсов. Ожидают, что возможность преобразования биомассы в топливо, химикаты, энергию и другие материалы укрепит экономику сельского хозяйства, понизит зависимость от нефтяных и газовых ресурсов и уменьшит загрязнение воздуха и воды. Получение энергии и химикатов из возобновляемых ресурсов, таких как биомасса, также снижает чистую производительность по диоксиду углерода - важному парниковому газу, который вносит вклад в глобальное потепление.
Ключевой проблемой для продвижения и поддержки применения биомассы в промышленном секторе является необходимость разработки эффективных и экологически благоприятных технологий переработки биомассы в полезные продукты. Настоящие технологии переработки биомассы, к сожалению, имеют тенденцию к привнесению дополнительных затрат, что делает затруднительной конкуренцию с продуктами, полученными при использовании традиционных ресурсов, таких как ископаемые топлива. Такие затраты часто включают капитальные вложения на оборудование и обрабатывающие системы, способные выдерживать экстремальные температуры и высокие давления, и необходимые текущие расходы на нагревательное топливо и на реакционные продукты, такие как ферментационные организмы, энзимные материалы, катализаторы и другие реакционные химикаты.
Одна технология альтернативного топлива, привлекающая значительное внимание, представляет собой биодизельное топливо, получаемое посредством этерификации растительных масел или животных жиров. В США производство биодизельного топлива ежегодно достигает 114-151 миллионов литров (30-40 миллионов галлонов), но к 2012 году прогнозируют возрастание его производства до намеченных 1,51 миллиарда литров (400 миллионов галлонов) в год. В Европе было произведено свыше 1,4 метрических тонн биодизельного топлива в 2003 г., и множество проектов находятся в процессе разработки в Бразилии и Азии.
Побочным продуктом способа получения биодизельного топлива является неочищенный глицерин, который без дополнительной очистки имеет лишь небольшую ценность или вообще не имеет никакой ценности. Вопрос, составляющий предмет спора, состоит в том, что делать с растущим предложением неочищенного глицерина. Очистка неочищенного глицерина является одним вариантом решения вопроса, однако очистка неочищенного глицерина, который содержит катализатор, органические примеси и остаточный метанол, является трудоемкой и часто слишком дорогой для производителей биодизельного топлива в небольших масштабах. Рассматриваемые проблемы осложняются тем, что спрос на чистый глицерин также остается постоянным, а цены сильно падают по мере того, как большее предложение поступает на рынок, особенно в Европе.
Разработка эффективных способов преобразования неочищенного глицерина в альтернативные продукты, такие как двухатомные спирты и другие многоатомные спирты, кетоны, альдегиды, карбоновые кислоты и спирты, может предоставить дополнительные возможности для повышения экономической эффективности и экологических преимуществ получения биодизельного топлива. Например, сегодня в США более 400 миллионов кг (миллиарда фунтов) пропиленгликоля производят и используют в производстве многих промышленных продуктов и потребительских товаров, включая антиобледенители для воздушных судов и взлетно-посадочных полос, антифризы, охлаждающие агенты, жидкие теплоносители, растворители, ароматизаторы и душистые вещества, косметические добавки, фармацевтические препараты, гидравлические жидкости, химические полуфабрикаты и термореактивные пластмассы. В настоящее время пропиленгликоль получают посредством частичного окисления пропилена, получаемого из ископаемого топлива, с образованием пропиленоксида, который затем приводят во взаимодействие с водой для образования пропиленгликоля.
Исследователи недавно разработали способы осуществления взаимодействия чистого водорода с более высокомолекулярными многоатомными спиртами, получаемыми из биомассы (глицерин, ксилит и сорбит), и сахарами (глюкоза и ксилоза) в присутствии каталитических материалов гидрогенизации и гидрогенолиза с получением пропиленгликоля. В то время как биомассу получают из возобновляемых источников, чистый водород как таковой обычно получают посредством парового реформинга невозобновляемого природного газа. В силу его происхождения, чистый водород также необходимо транспортировать и вводить в поток производства при повышенных давлениях из внешнего источника, таким образом уменьшая эффективность способа и вызывая увеличение общей стоимости итогового конечного продукта.
Например, в патентах США 6841085, 6677385 и 6479713, принадлежащих Werpy et al., описаны способы гидрогенолиза как углерод-кислородных, так и углерод-углеродных связей при использовании мультиметаллического катализатора, содержащего рений, в присутствии подаваемого извне водорода с получением таких продуктов, как пропиленгликоль (ПГ). Катализаторы, содержащие рений, могут также включать Ni, Pd, Ru, Со, Ag, Au, Rh, Pt, Ir, Os и Cu. Конверсия происходит при температурах от 140°С до 250°С и, более предпочтительно, от 170°С до 220°С, а давление водорода составляет от 4,14 МПа до 11,03 МПа (от 600 до 1600 фунт/кв. дюйм) по водороду.
Dasari et. al также описывают гидрогенолиз глицерина с получением ПГ в присутствии водорода из внешнего источника при температурах от 150°С до 260°С и давлении водорода 1,38 МПа (200 фунт/кв. дюйм) на никелевом, палладиевом, платиновом, медном катализаторах и катализаторе на основе хромита меди. Данные авторы сообщают об увеличении выхода пропиленгликоля при снижении концентрации воды и снижении селективности по ПГ при температурах выше 200°С и давлении водорода 1,38 МПа (200 фунт/кв. дюйм). Авторы дополнительно сообщают, что никель, рутений и палладий не являлись очень эффективными для гидрогенизации глицерина (Dasari M.A., Kiatsimkul P.-P, Sutterlin W.R., Suppes G.J. Low-pressure hydrogenolysis of glycerol to propylene glycol, Applied Catalysis, A: General, 281 (1-2), p.225 (2005)).
В патентной заявке США Na 11/088603 (публ. US 2005/0244312 А1) описан способ конверсии глицерина в низшие спирты, обладающие температурами кипения менее 200°С, с высокими выходами. Данный способ включает конверсию натурального глицерина в пропиленгликоль через промежуточный продукт ацетол при температуре от 150°С до 250°С и при давлении от 0,1 до 2,5 МПа (от 1 до 25 бар) и предпочтительно от 0,5 до 0,8 МПа (от 5 до 8 бар) в присутствии палладиевого, никелевого, родиевого, цинкового, медного или хромового катализатора. Реакция протекает в присутствии или в отсутствие водорода, причем водород поставляют из внешнего источника. Реакцию глицерина осуществляют в растворе, содержащем 50% масс. или менее воды, и предпочтительно только от 5% масс. до 15% масс. воды.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на способы образования кислородсодержащих углеводородов, таких как многоатомные спирты, двухатомные спирты, кетоны, альдегиды, карбоновые кислоты и спирты, из водного сырьевого раствора при использовании водорода, получаемого из части сырьевого раствора. Способ включает реакцию части сырьевого раствора на первом катализаторе при условиях реформинга водной фазы с получением водорода и взаимодействие водорода с по меньшей мере второй частью сырьевого раствора на втором катализаторе при условиях, подходящих для получения требуемых продуктов (например, путем гидрогенизации). В одном воплощении способ включает стадии: (а) приведение первого каталитического материала в контакт с водным сырьевым раствором, содержащим воду и по меньшей мере один водорастворимый кислородсодержащий углеводород, имеющий два или более атомов углерода, с получением водорода и (б) взаимодействие водорода с оставшимися кислородсодержащими углеводородами на втором каталитическом материале, выбираемом для ускорения гидрогенизации кислородсодержащих углеводородов до требуемых продуктов реакции.
Водный сырьевой раствор предпочтительно включает воду и кислородсодержащий углеводород, имеющий по меньшей мере два атома углерода, такой как любой из ряда многоатомных спиртов, сахаров, сахарных спиртов, спиртов, крахмалов, лигнинов, целлюлозных полимеров и водорастворимых сахаридов. Предпочтительно сырьевой раствор включает глицерин.
Первый каталитический материал желательно является гетерогенным катализатором, содержащим один или более материалов, способных к производству водорода при условиях реформинга в водной фазе, таких как металлы Группы VIIIB по отдельности, либо в сочетании с металлами Группы VIIB, металлами Группы VIB, металлами Группы VB, металлами Группы IVB, металлами Группы IIB, металлами Группы IB, металлами Группы IVA или металлами Группы VA. Второй каталитический материал предпочтительно является гетерогенным катализатором, содержащим один или более материалов, способных ускорять реакцию между получаемым водородом и сырьевым раствором с получением двухатомных спиртов или других многоатомных спиртов, кетонов, альдегидов, карбоновых кислот и/или спиртов. Предпочтительные примеры второго каталитического материала включают медь, металлы Группы VIII, их смеси и сплавы и различные бифункциональные катализаторы. Второй каталитический материал может включать эти металлы по отдельности или в сочетании с одним или более металлами Группы VIIIB, Группы VIIB, металлами Группы VIB, металлами Группы VB, металлами Группы IVB, металлами Группы IIB, металлами Группы IB, металлами Группы IVA или металлами Группы VA. Предпочтительно второй каталитический материал включает железо, рутений, медь, рений, кобальт или никель.
В одном воплощении многоатомные спирты, двухатомные спирты, кетоны, альдегиды, карбоновые кислоты и/или спирты образуют путем получения водорода из части водного сырьевого раствора, приведенного в контакт с первым каталитическим материалом при температуре от примерно 80°С до 400°С, при массовой часовой объемной скорости (МЧОС) по меньшей мере примерно 1,0 г кислородсодержащего углеводорода на грамм первого каталитического материала в час и давлении, при котором вода и кислородсодержащие углеводороды являются конденсированными жидкостями, и затем взаимодействия водорода со второй частью сырьевого раствора на втором каталитическом материале при условиях температуры, давления и массовой часовой объемной скорости, эффективных для получения одного или более кислородсодержащих углеводородов, таких как двухатомные спирты и другие многоатомные спирты, кетоны, альдегиды, карбоновые кислоты и/или спирты. Вторая часть сырьевого раствора обычно включает как первоначальные кислородсодержащие углеводороды, так и кислородсодержащие углеводороды, получаемые из стадии получения водорода, и ее можно приводить в контакт со вторым каталитическим материалом при температуре примерно от 100°С до 300°С, при избыточном давлении от примерно 1,38 МПа (200 фунтов на кв. дюйм изб.) до примерно 12,42 МПа (1200 фунтов на кв. дюйм изб.) и при массовой часовой объемной скорости по меньшей мере примерно 1,0 г кислородсодержащего углеводорода на грамм каталитического материала в час. Получающаяся композиция обычно может включать, не ограничиваясь этим, многофазную композицию веществ, включающую твердую фазу с каталитической композицией, содержащей первый каталитический материал и второй каталитический материал, предпочтительно платину и железо, и жидкую фазу, содержащую воду, глицерин, карбоновую кислоту, пропиленгликоль и диоксид углерода.
В другом воплощении предложены реакционные системы для получения кислородсодержащих соединений, таких как двухатомные спирты и другие многоатомные спирты, кетоны, альдегиды, карбоновые кислоты и/или спирты, из многоатомного спирта. Реакционная система включает по меньшей мере первый реакционный слой, приспособленный для получения водного сырьевого раствора для получения водорода, и второй реакционный слой, приспособленный для получения кислородсодержащих соединений из водорода и части сырьевого раствора. Первый реакционный слой скомпонован для контактирования водного сырьевого раствора в конденсированной фазе с первым каталитическим материалом (описанным выше) для обеспечения водорода в потоке реагентов. Второй реакционный слой скомпонован так, чтобы принимать поток реагентов для контактирования со вторым каталитическим материалом (описанным выше) и получать требуемые кислородсодержащие соединения. В одном предпочтительном воплощении первый каталитический материал включает металл Группы VIII, в то время как второй каталитический материал представляет собой либо железо, рутений, медь, кобальт, никель, либо их сплавы или смеси. Второй реакционный слой может быть расположен внутри того же реакционного сосуда вместе с первым реакционным слоем или во втором реакционном сосуде, сообщающемся с первым реакционным сосудом, содержащим первый реакционный слой. Реакционный сосуд предпочтительно включает выпускное отверстие, приспособленное для удаления потока продукта из реакционного сосуда.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
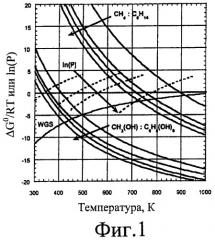
На Фиг.1 представлен график, на котором показана термодинамика (ΔG°/RT в зависимости от температуры) получения СО или Н2 путем реформинга в паровой фазе СН4, С2Н6, С3Н8 и C6H14; СН3(ОН), С2Н4(ОН)2, С3Н5(ОН)3 и С6Н8(ОН)6; а также сдвига равновесия в водяном газе. Пунктирные линии показывают значения In(Р) для давлений паров СН3(ОН), С2Н4(ОН)2, С3Н5(ОН)3 и С6Н8(ОН)6 (единицы давления выражены в атмосферах) в зависимости от температуры.
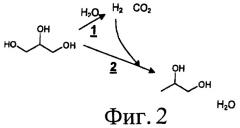
На Фиг.2 представлено схематическое изображение путей реакции получения H2 и пропиленгликоля из глицерина.
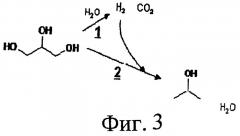
На Фиг.3 представлено схематическое изображение путей реакции получения Н2 и пропилового спирта из глицерина.
На Фиг.4 представлено схематическое изображение путей реакции получения Н2 и гексанола из сорбита.
На Фиг.5 представлена схема, иллюстрирующая способ преобразования многоатомного спирта в диол или спирт, используя полученный in situ водород.
На Фиг.6 представлена схема, иллюстрирующая способ образования продуктов реакции из многоатомного спирта, используя реактор, имеющий первую реакционную камеру для получения водорода и вторую камеру гидрогенизации.
На Фиг.7 представлена схема, иллюстрирующая способ образования продуктов реакции из многоатомного спирта с вводимой добавкой при использовании реактора, имеющего первую реакционную камеру для получения водорода и вторую камеру для гидрогенизации.
На Фиг.8 представлена схема реакционной системы, которую можно использовать для оценки образования многоатомных спиртов из глицерина посредством реформинга в водной фазе.
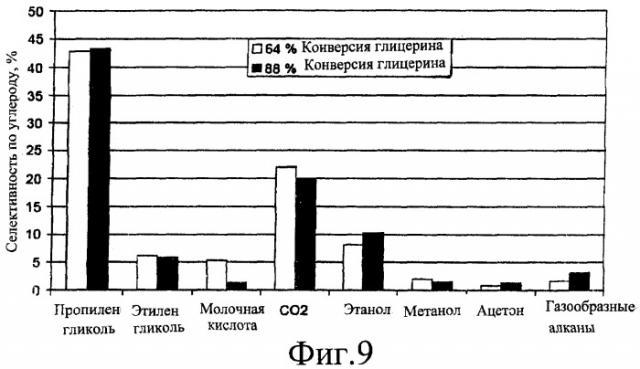
На Фиг.9 представлено графическое изображение распределения углеродных продуктов в ходе реформинга глицерина в водной фазе на модифицированном платиновом катализаторе.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее описание относится к способам и системам реформинга концентратов биомассы с водой при низких температурах с получением пропиленгликоля, этиленгликоля и других многоатомных спиртов, двухатомных спиртов, кетонов, альдегидов, карбоновых кислот и/или спиртов при использовании водорода, получаемого in situ. Водород можно получить путем взаимодействия части водного сырьевого раствора, содержащего биомассу и воду на катализаторе, при условиях реформинга в водной фазе (РВФ). Водород, получаемый посредством РВФ, можно затем использовать для взаимодействия со второй частью сырьевого раствора, включающей кислородсодержащие углеводороды, получаемые из производства водорода на стадии РВФ, на втором катализаторе при условиях, подходящих для получения требуемых продуктов.
Сокращения и определения
ГХ = газовый хроматограф или газовая хроматография.
ЧОСГ = часовая объемная скорость газа.
МПа избыт. (фунт/кв. дюйм избыт.) = МПа (фунтов на квадратный дюйм) свыше атмосферного давления (то есть избыточное давление).
Объемная скорость = отношение массы/объема реагентов на единицу катализатора в единицу времени.
ЧО = частота оборота.
МЧОС = массовая часовая объемная скорость = масса кислородсодержащего соединения на массу катализатора в час.
СВГ = сдвиг в водяном газе.
Реформинг в водной фазе (РВФ) является способом каталитического реформинга, в котором получают обогащенное водородом топливо из кислородсодержащих соединений, полученных из биомассы (глицерин, сахара, сахарные спирты и т.д.). Различные способы и технологии РВФ описаны в патентах США 6699457, 6964757 и 6964758 и в патентной заявке США 11/234727 (все они принадлежат Cortright et al. и озаглавлены «Низкотемпературное получение водорода из кислородсодержащих углеводородов»), и в патентной заявке США 6953873 (принадлежащей Cortright et al. и озаглавленной «Низкотемпературное получение водорода из кислородсодержащих углеводородов») и совместной одновременно поданной международной патентной заявке PCT/US2006/048030 (принадлежащей Cortright et al. и озаглавленной «Катализаторы и способы реформинга кислородсодержащих соединений»), которые все включены в этот документ посредством ссылки. Термины «реформинг в водной фазе» и «РВФ» обобщенно обозначают полную реакцию кислородсодержащего соединения и воды с образованием потока водорода, вне зависимости от того, протекают ли реакции в газовой фазе или в конденсированной жидкой фазе. Когда отличие является важным, это должно быть отмечено. «Водород РВФ» обобщенно относится к водороду, полученному посредством способа РВФ.
Способ РВФ предпочтительно выполняют в жидкой фазе, хотя его можно также выполнять в паровой фазе реакции. РВФ может протекать при температурах, при которых реакция сдвига в водяном газе является предпочтительной (например, от 80°С до 400°С), делая возможным образование водорода с небольшим количеством СО в одном химическом реакторе. Преимущества способа РВФ включают: (1) выполнение реакции при более низких давлениях (обычно от 1,38 до 5 МПа избыт. (от 200 до 725 фунт/кв. дюйм избыт.)), (2) способность к образованию сырья, обогащенного водородом, при более низких температурах без необходимости испарения воды, что обеспечивает значительную экономию энергии, (3) способность работать при температурах, которые минимизируют нежелательные реакции разложения, обычно встречающиеся, когда углеводы нагревают до повышенных температур, и (4) утилизацию сырья, полученного из сельского хозяйства. Способ РВФ использует преимущество уникальных термодинамических свойств кислородсодержащих соединений, обладающих благоприятным стехиометрическим отношением углерода к кислороду, в особенности углеводородов, имеющих соотношение С:O, равное 1:1 (предпочтительное соотношение) для образования водорода при относительно низких температурах за одну реакционную стадию.
Стехиометрическая реакция реформинга кислородсодержащего углеводорода, имеющего отношение С:O, равное 1:1, для получения СО и H2, представлена реакцией (1):
Условия реакции для получения водорода из углеводородов могут определяться термодинамикой парового реформинга алканов с образованием СО и Н2 (реакция (2)) и реакции сдвига в водяном газе с образованием CO2 и Н2 из СО (реакция (3)).
На Фиг.1 (созданном на основе термодинамических данных, полученных из Chemical Properties Handbook, C.L.Yaws, McGraw Hill, 1999) показаны изменения стандартной свободной энергии Гиббса (ΔG°/RT), связанной с уравнением (2), для серии алканов (СН4, С2Н6, С3Н8 и С6Н14), нормализованной на моль получаемого СО. Можно видеть, что паровой реформинг алканов является термодинамически благоприятным (то есть имеет отрицательное значение ΔG°/RT) только при температурах выше 675 К (402°С).
Также показаны важные кислородсодержащие углеводороды, имеющие отношение С:O, равное 1:1, такие как метанол (СН3(ОН)), этиленгликоль (C2H4(OH)2), глицерин (С3Н5(ОН)3) и сорбитол (С6Н8(ОН)6). На Фиг.1 пунктирными линиями показаны величины In(Р) для давления паров СН3(ОН), С2Н4(ОН)2, С3Н5(ОН)3 и С6Н8(ОН)6 (единицы давления выражены в атмосферах) в зависимости от температуры. На Фиг.1 показано, что паровой реформинг этих кислородсодержащих углеводородов с получением СО и Н2 является термодинамически благоприятным при значительно более низких температурах, чем те, которые требуются для алканов с таким же количеством атомов углерода. На Фиг.1 также показано, что значение ΔG°/RT для сдвига в водяном газе от СО к CO2 и Н2 является более благоприятным при таких же низких температурах. Следовательно, возможно преобразовать кислородсодержащие углеводороды с благоприятными отношениями С:O при низких температурах с образованием СО и Н2 и, следовательно, Н2 и CO2 в однофазном каталитическом способе.
В то же время, на Фиг.1 показано, что конверсия кислородсодержащих соединений в присутствии воды в Н2 и CO2 является чрезвычайно благоприятной при низких температурах, причем последующая реакция Н2 и кислородсодержащих соединений с образованием алканов (CnH2n+2) и воды является также чрезвычайно благоприятной при низких температурах.
В первом варианте воплощения предложены способы получения кислородсодержащих соединений. Способы предпочтительно включают стадии: (а) приведения первого каталитического материала в контакт с первой частью водного сырьевого раствора, содержащего воду и растворимые в воде кислородсодержащие углеводороды, с получением водорода РВФ, и (б) приведение в контакт водорода РВФ со второй частью сырьевого раствора на втором каталитическом материале с получением продукта реакции, который включает, не ограничиваясь этим, многоатомный спирт, двухатомный спирт, кетон, альдегид, карбоновую кислоту и/или спирт. Вторая часть сырьевого раствора предпочтительно включает кислородсодержащие углеводороды, полученные из производства водорода РВФ, в дополнение к кислородсодержащим углеводородам, включенным в первоначальный сырьевой раствор, однако может также включать части сырьевого раствора без кислородсодержащих углеводородов, полученных в течение образования водорода РВФ. Первый каталитический материал предпочтительно является катализатором реформинга в водной фазе (РВФ) и второй каталитический материал предпочтительно является материалом, способным ускорять реакции гидрогенизации. Если не указано другое, то любые обсуждаемые здесь катализаторы гидрогенизации и катализаторы РВФ представляют собой неограничивающие примеры подходящих каталитических материалов.
Как более полно описано ниже, более термодинамически благоприятная реакция потребляет водород РВФ с образованием многоатомных спиртов, двухатомных спиртов, кетонов, альдегидов и/или спиртов. При благоприятных условиях способы и реакционные системы, описанные ниже, могут обеспечивать получение смесей, в основном включающих одно или более кислородсодержащих соединений, таких как двухатомные спирты или другие многоатомные спирты, кетоны, альдегиды, карбоновые кислоты и/или спирты. Например, способы и реакционные системы, описанные здесь, могут обеспечивать получение углеродсодержащего продукта реакции с более чем 50% одного или более многоатомных спиртов, таких как пропиленгликоль. Предпочтительно, по существу, весь водород РВФ, полученный in situ посредством способа РВФ, расходуется в течение реакции с кислородсодержащими углеводородами на втором каталитическом материале без добавления чистого водорода из внешнего источника.
На Фиг.2, 3 и 4 схематически показаны возможные маршруты реакций образования как Н2, так и многоатомных спиртов, двухатомных спиртов, кетонов, альдегидов и/или спиртов из кислородсодержащих углеводородов на металлическом катализаторе. В общем, образование водорода включает дегидрогенизацию и последующие стадии перегруппировки, которые образуют промежуточные продукты, содержащие атомы углерода, несвязанные с атомами кислорода. Углеводы сначала подвергаются дегидрогенизации для обеспечения адсорбированных промежуточных продуктов, до расщепления связей С-С или С-O. Последующее расщепление связей С-С приводит к образованию СО и H2, при этом СО затем взаимодействует с водой с образованием CO2 и Н2 посредством реакции сдвига в водяном газе (СВГ). Затем происходит образование многоатомных спиртов, двухатомных спиртов, кетонов, альдегидов и/или спиртов, в местах, где гидроксильные группы кислородсодержащих углеводородов удаляются через механизм дегидратации с последующей гидрогенизацией ранее образованным водородом. Также возможно образовывать многоатомные спирты, двухатомные спирты, кетоны и/или спирты на металлическом катализаторе вначале путем расщепления связей C-O в адсорбированных промежуточных углеводах. Промежуточные продукты можно затем преобразовать в многоатомные спирты, двухатомные спирты, кетоны, альдегиды и/или спирты в зависимости от катализатора и условий реакции.
СЫРЬЕВОЙ РАСТВОР
Предпочтительное сырье включает растворимые в воде кислородсодержащие углеводороды, полученные из биомассы. Используемый здесь термин «биомасса» относится, не ограничиваясь перечисленным, к органическим материалам, полученным из растений (таким, как листья, корни, семена и стебли), и метаболическим отходам микроорганизмов и животных. Распространенные источники биомассы включают: (1) сельскохозяйственные отходы, такие как стебли кукурузы, солома, шелуху семян, отходы сахарного тростника, жмых, скорлупу орехов и навоз крупного рогатого скота, домашней птицы и домашних свиней, (2) древесные материалы, такие как древесина или кора, опилки, древесный распил и заводской скрап, (3) городские отходы, такие как макулатура и складские обрезки и (4) энергетические культуры, такие как тополь, ива, просо, люцерна, бородач степной (prairie bluestream), зерно, соя и т.п. Сырье можно получить из биомассы путем любых известных в настоящее время или разработанных в будущем средств или оно может представлять собой простые побочные продукты других процессов, такие как неочищенный глицерин из производства биодизельного топлива.
Кислородсодержащие углеводороды могут быть любыми углеводородами, имеющими по меньшей мере два атома углерода и по меньшей мере один атом кислорода. В предпочтительном воплощении кислородсодержащий углеводород является растворимым в воде и содержит от 2 до 12 атомов углерода, и более предпочтительно от 2 до 6 атомов углерода. Кислородсодержащий углеводород также предпочтительно имеет отношение кислорода к углероду от 0,5:1 до 1,5:1, включая отношения 0,75:1,0, 1,0:1,0, 1,25:1,0, 1,5:1,0 и другие отношения, существующие между ними. В наиболее предпочтительном воплощении кислородсодержащие углеводороды имеют отношение кислорода к углероду 1:1. Неограничивающие примеры предпочтительных растворимых в воде кислородсодержащих углеводородов включают этандиол, этандион, уксусную кислоту, пропанол, пропандиол, пропионовую кислоту, глицерин, глицеральдегид, дигидроксиацетон, молочную кислоту, пировиноградную кислоту, малоновую кислоту, бутандиолы, бутановую кислоту, альдотетрозы, таутаровую кислоту, альдопентозы, кетотетрозы, кетопентозы, кетогексозы, альдитолы, сахара, сахарные спирты, целлюлозы, лигноцеллюлозы, сахариды, крахмалы, многоатомные спирты и т.п. Наиболее предпочтительно кислородсодержащий углеводород является сахаром, сахарным спиртом, целлюлозой, сахаридами и глицерином.
Кислородсодержащий углеводород соединяют с водой для получения водного сырьевого раствора, имеющего концентрацию, эффективную для того, чтобы вызвать образование требуемых продуктов реакции. Воду можно добавлять либо перед контактом кислородсодержащего углеводорода с катализатором РВФ, либо в то же самое время, когда происходит контакт кислородсодержащего углеводорода с катализатором РВФ. В предпочтительном воплощении воду соединяют с кислородсодержащим углеводородом с образованием водного раствора перед контактом с катализатором РВФ для облегчения обработки, но также было обнаружено, что кислородсодержащий углеводород можно также помещать в раствор и затем дополнительно добавлять воду во время контакта с катализатором РВФ для образования водного сырьевого раствора. Предпочтительно, оставшаяся часть сырьевого раствора является водой. В некоторых воплощениях сырьевой раствор состоит преимущественно из воды, одного или более кислородсодержащих углеводородов и, возможно, одного или более описанных здесь модификаторов сырья, таких как щелочи или гидроксиды щелочных или щелочноземельных металлов, солей или кислот. Сырьевой раствор может также содержать незначительное количество водорода, предпочтительно менее примерно 0,1 МПа (1 бар). В предпочтительных воплощениях водород не добавляют в сырье.
Отношение воды к углероду в растворе предпочтительно составляет от примерно 0,5:1 до примерно 7:1, включая отношения, находящиеся между этими величинами, такие как 1:1, 2:1, 3:1, 4:1, 5:1, 6:1 и любые величины отношений, существующие между ними. Сырьевой раствор можно также характеризовать как раствор, имеющий по меньшей мере 20% масс. от общего количества раствора в виде кислородсодержащего углеводорода. Например, раствор может включать один или более кислородсодержащих углеводородов с общей концентрацией кислородсодержащих углеводородов в растворе, составляющей по меньшей мере 20%, 30%, 40%, 50%, 60% масс. или выше, включая любые процентные содержания, находящиеся между указанными значениями, и в зависимости от используемых кислородсодержащих углеводородов. Более предпочтительно, сырьевой раствор включает по меньшей мере примерно 20%, 30%, 40%, 50% или 60% масс. глицерина, включая любые процентные содержания, находящиеся между указанными значениями. Отношения воды к углероду и процентные содержания за пределами вышеуказанных диапазонов также включены в объем изобретения.
ПОЛУЧЕНИЕ ВОДОРОДА
Водород РВФ получают из сырья при условиях реформинга в водной фазе. Температуру и давление реакции предпочтительно выбирают так, чтобы поддерживать сырье в жидкой фазе. Однако следует понимать, что условия температуры и давления также можно выбирать для более благоприятного получения водорода в паровой фазе. Вообще, реакцию РВФ и последующие реакции гидрогенизации необходимо выполнять при температуре, при которой термодинамика предлагаемой реакции является благоприятной. Давление изменяется с температурой. Для реакций в конденсированной жидкой фазе давление внутри реактора должно быть достаточным для поддержания реагентов в конденсированной жидкой фазе на входе в реактор.
Для реакций в паровой фазе реакцию следует проводить при температуре, при которой давление пара соединения кислородсодержащего углеводорода составляет по меньшей мере примерно 10 кПа (0,1 атм) (и предпочтительно намного выше), и термодинамика реакции является благоприятной. Эта температура изменяется в зависимости от конкретного используемого соединения кислородсодержащего углеводорода, однако обычно она составляет от примерно 100°С до примерно 450°С для реакций, протекающих в паровой фазе, и более предпочтительно, от примерно 100°С до примерно 300°С для реакций в паровой фазе.
Для реакций в жидкой фазе температура реакции может составлять от примерно 80°С до примерно 400°С, и давление реакции от примерно 0,5 МПа избыт. до примерно 9 МПа избыт. (от 72 до 1300 фунт/кв. дюйм избыт.). Предпочтительно, температура реакции составляет от примерно 120°С до примерно 300°С, и более предпочтительно от примерно 150°С до примерно 270°С. Давление реакции предпочтительно составляет примерно от 0,5 до 8,3 МПа избыт. (от 72 до 1200 фунт/кв. дюйм избыт.), или примерно от 1 до 8,3 МПа избыт. (от 145 до 1200 фунт/кв. дюйм избыт.), или примерно от 1,4 до 5 МПа избыт. (от 200 до 725 фунт/кв. дюйм избыт.), или примерно от 2,5 до 4,1 МПа избыт. (от 365 до 600 фунт/кв. дюйм избыт.). Так как водород получают in situ, давление обеспечивают посредством механизма накачки, с помощью которого также осуществляют перемещение сырьевого раствора через реакционную систему.
Способ в конденсированной жидкой фазе возможно также осуществлять, используя модификатор, который увеличивает активность и/или стабильность первого и/или второго каталитического материала(ов) (то есть каталитической системы). Предпочтительно, чтобы вода и кислородсодержащий углеводород реагировали при подходящем рН от примерно 1,0 до примерно 10,0, включая величины рН между ними с инкрементом 0,1 и 0,05, и более предпочтительно, при рН от примерно 4,0 до примерно 10,0. Обычно модификатор добавляют к сырьевому раствору в количестве от примерно 0,1% до примерно 10% масс. по сравнению с общей массой используемой каталитической системы, хотя количества за пределами этого диапазона включены в настоящее изобретение.
Для оптимизации доли водорода в продуктах реакции в сырьевой раствор также можно добавлять соли щелочных или щелочноземельных металлов. Примеры подходящих растворимых в воде солей включают одно или более соединений, выбираемых из группы, состоящей из гидроксида, карбоната, нитрата или хлорида щелочного или щелочноземельного металла. Например, добавление щелочных (основных) солей для обеспечения рН от примерно 4,0 до примерно 10,0 может улучшить селективность реакций реформинга по водороду.
Добавление кислых соединений может также обеспечивать увеличение селективности по отношению к требуемым продуктам реакции в описанных ниже реакциях гидрогенизации. Предпочтительно, растворимую в воде кислоту выбирают из группы, состоящей из нитратных, фосфатных, сульфатных и хлоридных солей и их смесей. Если используют возможный кислый модификатор, предпочтительно, чтобы он присутствовал в количестве, достаточном для уменьшения рН потока водного сырья до значения от примерно 1,0 до примерно 4,0. Уменьшение рН потока сырья таким образом может увеличить долю двухатомных спиртов, многоатомных спиртов, кетонов, карбоновых кислот, альдегидов, спиртов или алканов в конечных продуктах реакции.
В общем, реакцию следует проводить при условиях, при которых время пребывания сырьевого раствора на катализаторе РВФ соответствует производству количества водорода РВФ, достаточного для реакции со второй частью сырьевого раствора на катализаторе гидрогенизации с получением требуемых продуктов. Например, в одном воплощении, МЧОС реакции может составлять по меньшей мере 1,0 г кислородсодержащего углеводорода на грамм катализатора РВФ и, предпочтительно, от примерно 1,0 до 5,0 г кислородсодержащего углеводорода на грамм катализатора РВФ, и более предпочтительно от примерно 1,9 до 4,0 г кислородсодержащего углеводорода на грамм катализатора РВФ.
КАТАЛИЗАТОР РВФ
Первый каталитический материал предпочтительно является катализатором РВФ, обычно гетерогенным катализатором, способным ускорять взаимодействие воды и кислородсодержащих углеводородов с образованием водорода при описанных выше условиях. Предпочтительный катализатор РВФ включает по меньшей мере один пере