Способ прогнозирования эффективности противовирусной терапии (пвт) хронического гепатита в (хгв)
Иллюстрации
Показать всеИзобретение относится к области медицины и предназначено для прогнозирования вирусологического ответа у больных хронической сочетанной HBV/HCV-инфекцией при проведении противовирусной терапии хронического гепатита В. Определяют содержание цитокина ФНО-α в сыворотке крови до и во время лечения на 4-5 неделе и на 7-8 неделе. При превышении исходного уровня цитокина ФНО-α в 1,5 раза и более на 4-5 неделе терапии с последующим снижением в 1,5 раза и более от исходного уровня на 7-8 неделе терапии прогнозируют хорошую эффективность назначенного лечения. При превышении исходного уровня менее чем в 1,5 раза на 4-5 неделе или при наличии снижения ФНО-α менее чем в 1,5 раза от исходного уровня на 7-8 неделе терапии прогнозируют неэффективность проводимой терапии. Способ позволяет спрогнозировать результаты противовирусной терапии в ранние сроки лечения - через 4-8 недель от начала терапии. 2 ил., 2 пр.
Реферат
Предлагаемое изобретение относится к области медицины, а именно к исследованию биологических жидкостей (крови) с помощью физических и химических методов, и может быть использовано для прогнозирования вирусологического ответа у больных хронической сочетанной HBV/HCV-инфекцией при проведении противовирусной терапии (ПВТ).
Гепатиты сочетанной этиологии занимают значительную долю в структуре инфекционных поражений печени (Дудик Т.В и др. Случаи вирусных гепатитов сочетанной этиологии // Российский гастроэнтерологический журнал. - 2001. - №1). Наиболее часто встречается инфекция вирусами гепатита В и С, при хронизации которой наблюдается повышенный риск развития цирроза печени и гепатоцеллюлярной карциномы. Почти у ¼ больных наблюдается активная репликация HBV на фоне низкой репликативной активности вируса гепатита С (Мироджов Г.К. и др. Особенности клинического течения хронических гепатитов смешанной (HBV+HCV) этиологии // Российский журн. гастроэнтер., гепатол., колопр. - 2009. - №5; Арямкина О.Л. и др. Клиническая характеристика больных диффузными хроническими заболеваниями печени вирусной HBV- и НСУ-этиологии // Российский журн. гастроэнтер., гепатол., колопр. - 2001. - №1 (Прил.12):5). В этом случае противовирусное действие препаратов направлено на вирус гепатита В. При этом используют методики лечения, которые применяют при лечении моноинфекции ХГВ. Реже (5-7%) регистрируют одновременное обнаружение HBV ДНК и HCV РНК. При таком варианте микст-гепатита рекомендуют применение тритерапии (ИНФ-α2, рибавирин, препарат из группы атипичных нуклеозидов) или «золотого стандарта» лечения хронического гепатита С (ХГС) (ИНФ-α2, рибавирин), так как ИНФ-α2 обладает антивирусной активностью и против вируса гепатита В. Создание надежных прогностических критериев эффективности лечения ХГВ и ХГС в силу высокой стоимости и наличия большого количества побочных эффектов противовирусных препаратов, в частности интерферонов, представляет важную практическую задачу.
Известен способ прогнозирования эффективности ПВТ при ХГВ, включающий проведение оценки анамнеза заболевания, состояния больного, иммунологических показателей, свойств вируса (С.Н.Соринсон. Вирусные гепатиты. - Спб.: ТЕЗА. 1998. с.147, 234; В.Т.Ивашкин. Комбинированное лечение хронического гепатита В // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 1998. - №5. - с.57-60). Так ретроспективный метаанализ показал, что вероятность положительного ответа на ПВТ коррелирует с некоторыми клинико-биохимическими показателями и данными полимеразной цепной реакции (ПЦР), которые составляют благоприятные критерии эффективного противовирусного лечения. Они включают: молодой возраст, женский пол, парентеральное заражение, инфицирование в зрелом возрасте и предпочтительнее «диким» штаммом (наличие HBeAg), отсутствие клинико-биохимических признаков холестаза и аутоиммунного компонента воспаления, низкая концентрация HBV ДНК, повышенный уровень АлАТ, отсутствие выраженного фиброза печени.
Однако эти критерии можно считать ориентировочными, так как данный подход к прогнозированию эффективности ПВТ основан на совокупной оценке самых различных показателей здоровья пациента, что обычно представляет сложную задачу и не исключает элемент субъективизма при окончательной оценке. Кроме этого, к недостаткам известного способа можно отнести высокую стоимость и сложность определения и особенно генотипирования HBV ДНК, так как возможны спонтанные колебания показателя вирусной нагрузки даже в течение суток в зависимости от физической нагрузки, приема алкоголя, уровня инсоляции. Известный способ не позволяет провести гистологическое исследование в нужное время для оценки активности морфологического и инфекционного процесса в печени. Отсроченность оценки такого показателя, как цитолитический криз, возможное влияние внешних факторов (употребления алкоголя, физической нагрузки, нарушения диеты) на уровень АлАТ.
За прототип предлагаемого изобретения выбран известный способ прогнозирования эффективности противовирусной терапии при хроническом гепатите В, включающий определение содержания ФНО-α в сыворотке крови до и во время проведения противовирусной терапии (см. патент на изобретение RU №2287826, публ. 20.11.2006 г., бюл. №32).
Известный способ осуществляют следующим образом.
У больного в утренние часы натощак проводят забор венозной крови, а также через 4,5 часа после первого введения препарата интерферона - на пике его терапевтической активности. Сыворотку крови отделяют центрифугированием. Мононуклеарные клетки выделяют на градиенте плотности фиколл-верографин, полученную популяцию стандартизируют и инкубируют 24 часа в питательной среде RPMI-1640 с добавлением L-глутамина, 2% фетальной телячьей сыворотки и гентамицина во влажной обогащенной СО2 атмосфере при 37°С. Содержание ИФН-γ в супернатантах после центрифугирования и ФНО-α в сыворотке крови определяют методом ИФА с помощью тест-наборов «Цитокин» (Россия). Спонтанная продукция ИФН-γ МНК у здоровых составила 34,82±4,03 пг/2×106 клеток (колебания от 22,09 до 46,85), содержание ФНО-α в сыворотке крови - 22,41±3,67 пг/мл (колебания от 10,82 до 34,0).
При содержании ФНО-α в сыворотке крови, не превышающем 59,31 пг/мл, и хорошей реакции показателя ФНО-α и синтеза ИФН-γ клетками в ответ на первое введение интерферона-α (повышение ФНО-α более 46,1% и ИФН-γ более 70,25% от исходных уровней) прогнозируют вирусологический ответ (респондерство). При содержании ФНО-α в сыворотке крови выше 74,51 nr/мл и в случае ограниченной либо негативной реакции цитокинов на первую инъекцию интерферона-α (повышение ФНО-α не более 24,9%, ИФН-γ не более 70% или снижение обоих показателей) прогнозируют отсутствие вирусологического ответа (нон-респондерство).
Использование способа по мнению авторов позволяет уже после первого введения препарата интерферона-α прогнозировать результаты интерферонотерапии при хроническом вирусном гепатите В.
Однако известный способ позволяет прогнозировать вирусологический ответ только при лечении больного интерфероном-α2 (исключая комбинированную терапию с использованием препаратов из группы противовирусных для лечения ХГВ - атипичные нуклеозиды) и только при моногепатите ХГВ, поэтому известный способ не может быть точным и объективным для прогнозирования вирусологического ответа у больных хронической сочетанной HBV/HCV. Кроме этого, почти у 95% больных после первых 3-4 инъекций ИНФ-α2, наблюдается выраженный побочный эффект в виде гриппоподобного синдрома с температурной реакцией до 38-40°С. Он также влияет на динамику уровня цитокинов, что сказывается на точности прогнозирования.
Задачей предлагаемого изобретения является обеспечение возможности прогноза результатов ПВТ при лечении ХГВ у больных хронической сочетанной HBV/HCV-инфекцией в ранние сроки лечения - через 4-8 недель от начала терапии.
Поставленная задача достигается тем, что в известном способе прогнозирования эффективности противовирусной терапии хронического гепатита В, включающем определение содержания цитокина ФНО-α в сыворотке крови до и во время лечения, у больных хронической сочетанной HBV/HCV-инфекцией содержание цитокина ФНО-α в сыворотке крови исследуют до начала противовирусной терапии, на 4-5 неделе и на 7-8 неделе противовирусной терапии, и при превышении исходного уровня цитокина ФНО-α в 1,5 раза и более на 4-5 неделе терапии с последующим снижением в 1,5 раза и более от исходного уровня на 7-8 неделе терапии прогнозируют хорошую эффективность назначенного лечения, при превышении исходного уровня менее чем в 1,5 раза на 4-5 неделе или при наличии снижения ФНО-α менее чем в 1,5 раза от исходного уровня на 7-8 неделе терапии прогнозируют неэффективность проводимой терапии.
Предлагаемое изобретение отвечает критерию изобретения «новизна», так как в процессе проведения патентно-информационных исследований не выявлено технических решений, порочащих новизну предлагаемого способа.
Предлагаемое изобретение отвечает критерию «изобретательский уровень», так как не выявлено технических решений с существенными признаками предлагаемого изобретения.
Из научных источников известно, что ведущая роль в хронизации и дальнейшем течении как гепатита С, так и гепатита В принадлежит именно Т-клеточному иммунному ответу, в частности участию провоспалительных и противовоспалительных цитокинов в формировании Th 1 или Th 2 типа иммунного ответа (Кетлинский С.А. Роль Т-хелперов типов 1 и 2 в регуляции клеточного и гуморального иммунитета // Иммунология. - 2002. - Т.23. - №2). Особую роль в формировании противовирусного иммунного ответа играет фактор некроза опухоли альфа (ФНО-α) (Гаврилова Н.И. и др. Уровень ФНО-α в сыворотке крови у детей с моно- и сочетанными формами хронических вирусных гепатитов // Аллергология и иммунология. - 2000. - Т.1. - №2; Курамшин Д.Х. и др. Показатели эффекторного звена иммунитета и содержание цитокинов в сыворотке при вирусном гепатите С и сочетанной форме инфекции С+В // Аллергология и иммунология. - 2000. - Т.1. - №2). ФНО-α - многофункциональный цитокин с выраженной плейотропностью принимает участие в формировании защитных реакций организма, стимулирует фагоцитарную и цитотоксическую активность клеток, регулирует процессы иммунного воспаления, способствует утилизации деструктивного материала, а также регулирует апоптоз клеток (Пигузова Е.А. Система фактора некроза опухоли альфа и его рецепторов в иммунопатогенезе персистентных вирусных инфекций // Автореферат дисс. на соиск.уч.ст.канд.биол.наук. - 2006).
Указанные в формуле параметры для прогнозирования получены эмпирическим путем.
Предлагаемое изобретение было разработано в ходе исследования, включающего изучение достоверного количества иммунологических, иммунохимических, биохимических показателей при динамическом наблюдении. В результате был отобран наиболее важный для прогноза показатель - цитокин ФНО-α, а также наиболее информативные сроки проведения определения его содержания - перед ПВТ, на 4-5 и 7-8 неделе лечения.
Для более полного описания хода исследований представлен графический материал.
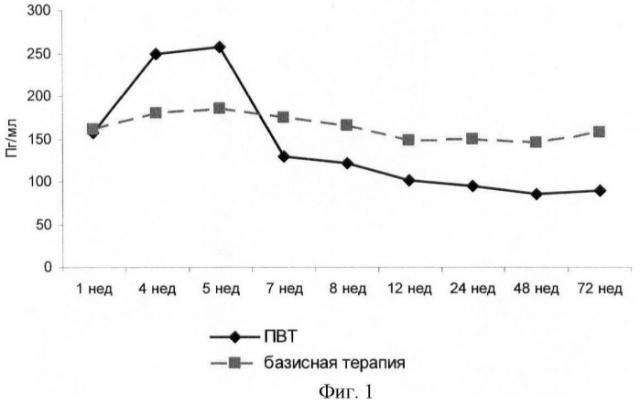
На фигуре 1 приведен график динамики содержания ФНО-α при базисной и противовирусной терапии ХГВ (в структуре сочетанной инфекции).
На фигуре 2 показана динамика содержания ФНО-α у больных хроническим микст-гепатитом В+С с разными результатами противовирусной терапии ХГВ (в структуре смешанной инфекции).
Диагноз хронического микст-гепатита В+С устанавливали на основании данных анамнеза, клинико-лабораторных показателей. Всем больным проводилось УЗИ органов брюшной полости. Маркеры HBV и HCV в сыворотке крови определяли иммуноферментным методом. Полимеразной цепной реакцией исследовали в крови HBV ДНК и HCV РНК.
Медиаторы иммунного ответа определялись иммуноферментным методом с использованием тест-систем производства «Протеиновый контур», Санкт-Петербург. В целях уточнения пределов нормальных колебаний значений всех изучавшихся показателей медиаторов были проведены исследования у 60 здоровых доноров, мужчин и женщин в возрасте от 20 до 50 лет. Средние показатели ИЛ-1β, ИЛ-6, ФНО-α у них составили: 153,4±10,4 пг/мл, 58,4±4,3 пг/мл, 44,3±3,1 пг/мл. Половые и возрастные характеристики этой группы соответствовали таковым у больных сочетанной хронической HBV/HCV-инфекцией.
Исследование содержания цитокинов проведено у 31 больного хроническим сочетанным гепатитом В+С, которые получали ПВТ (1 группа). Сравнительную группу составили 30 больных хроническим сочетанным гепатитом В+С, получавших базисное лечение (2 группа) в стационаре и/или амбулаторно. Базисная терапия включала: диету - стол №5а-5, гепатопротекторы, желчегонные, поливитамины. Противовирусная терапия (препараты назначались в общепринятых дозах) в течение 48 недель включала: 14 больных получали ламивудин (или энтакавир) ежедневно и реальдирон через день (или пег-ИНФ-α2 1 раз в неделю), 10 - пег-ИНФ-α2 1 раз в неделю, остальные 6 больных, у которых были обнаружены в сыворотке крови оба вируса, получали тритерапию: пег-ИНФ-α2, рибавирин, ламивудин (или энтакавир). Изучение содержания медиаторов иммунного ответа проводили до начала ПВТ и в процессе ПВТ на 4-5 и на 7-8 неделе.
Первым этапом анализа была оценка изучаемых показателей в процессе ПВТ. Важно отметить, что до начала лечения HBV ДНК выявлялась у всех больных обеих групп в разной концентрации (от 102 до более 107 копий/мл). В 1 группе уже на 4-6 неделе ПВТ у большей части больных (19 из 31, 61,3%) отмечено исчезновение HBV ДНК. У оставшихся 12 человек зарегистрировано уменьшение концентрации HBV ДНК.
Иная картина отмечалась во 2 группе больных. На 4-5 неделе базисного лечения у всех больных сохранялась ДНК в сыворотке крови. Высокая вирусная нагрузка (105 копий/мл и более) в эти сроки лечения свидетельствовала о сохранении виремии на прежнем уровне у преимущественного большинства больных (24 из 30-80%). У 6 больных (20%) концентрация HBV уменьшилась.
Изменения содержания HBV ДНК и активности инфекционного процесса у больных 1 и 2 группы определяли динамику АлАТ в процессе лечения. В 1 группе у 21 больного из 31 (67,7%) был зарегистрирован «цитолитический кризис» на 10-11 неделе болезни. То есть достоверное увеличение уровня АлАТ по сравнению с исходным (перед ПВТ 1,8±0,18 ммоль/л·ч и через 10-11 недель 3,8±0,26 ммоль/л·ч, р=0,035) с последующим снижением до исходного или нормального к 12 -13 неделе лечения. Во 2 группе аналогичной динамики не отмечено ни у кого из больных. К окончанию ПВТ средние показатели АлАТ не превышали нормальные (0,6±0,08 ммоль/л·ч). На 10-11 неделе наблюдения во 2 группе больных средний уровень АлАТ был значительно ниже (1,9±0,18 ммоль/л·ч, р=0,028), чем в 1 группе.
При анализе спектра медиаторов иммунного ответа можно отметить, что у больных 1 группы на 4-5 неделе ПВТ выявлены незначительные динамические изменения уровня ИЛ-1β и ИЛ-6 (снижение ИЛ-1β, увеличение ИЛ-6). С другой стороны, изменения в динамике ФНО-α были достоверными: ФНО-α перед лечением 158,5±9,7 пг/мл, на 4-5 неделе лечения 258,6±16,4 пг/мл (р=0,038). Увеличение показателя ФНО-α характеризовало усиление мезенхимально-воспалительного синдрома и некровоспалительных изменений в печени, что являлось предвестником развития «цитолитического кризиса». При дальнейшем наблюдении отмечалось значительное уменьшение содержания ФНО-α на 7-8 неделе лечения (118,4±8,2 пг/мл, р=0,031). У пациентов, получавших только базисную терапию, изучаемые медиаторы иммунного ответа оставались практически на прежнем уровне (фиг.1).
Следующим этапом анализа явилось установление закономерностей, определяющих эффективность ПВТ хронического гепатита В в структуре хронической сочетанной HBV/HCV-инфекции. С учетом результатов лечения все больные были разделены на 2 группы. В 1 группу вошли 15 (48,4%) больных из 31, у которых наблюдался вирусологический ответ. У 16 пациентов (51,2%) были отмечены положительные результаты индикации HBV ДНК к окончанию лечения или в процессе наблюдения в течение 2 лет.
В 1 группе у преимущественного большинства 13 из 15 больных (86,7%) зарегистрировано исчезновение ДНК вируса на 4-6 неделе ПВТ. У 2 оставшихся больных отрицательный результат индикации HBV ДНК отмечен на 8 и 9 неделе противовирусного лечения. Можно отметить, что у этих двух больных исходно вирусная нагрузка была высокой - 105 и 106 копий/мл. Тем не менее в дальнейшем не было зарегистрировано рецидива.
Другая картина динамики HBV ДНК наблюдалась у больных с отсутствием положительного ответа на ПВТ (2-я группа). На 6 неделе лечения у всех 16 больных ДНК вируса сохранялась в сыворотке крови. Необходимо отметить, что у большинства из них (13 из 16 больных) зарегистрирована высокая концентрация ДНК (более 105 копий/мл). Повторное исследование сыворотки методом ПЦР на 12 неделе лечения показало сохранение виремии у 12 из 16 больных (75%). Из них снижение вирусной нагрузки отмечалось только у 4 человек. У оставшихся 4 пациентов, у которых наблюдалось исчезновение HBV ДНК в процессе лечения, обнаружение ДНК вновь зарегистрировано на 2, 3 и 6 месяце от момента окончания ПВТ соответственно.
Была исследована также динамика уровня АлАТ в процессе проведения противовирусного лечения. Перед началом лечения показатель цитолиза был повышен у 12 из 15 больных 1-й группы (80%) и у 9 из 16 больных 2-й группы (56,3%). Средний уровень АлАТ в 1 группе составил 2,0±0,15 ммоль/л·ч, во 2-й - 1,6±0,13 ммоль/л·ч (р=0,22). Через 10-11 недель от начала ПВТ у всех больных 1 группы и 3 больных 2-й группы отмечено повышение уровня АлАТ в 1,5-2 раза от исходного с последующей нормализацией (1 группа больных) или снижением данного показателя ниже исходного (3 больных 2-й группы). В дальнейшем в 1 группе уровень АлАТ оставался стойко нормальным и к концу противовирусного лечения и на протяжении последующих 2 лет наблюдения, а во 2 группе у всех больных отмечались постоянные колебания содержания показателя цитолиза от 1,5 до 7 норм в те же сроки наблюдения. Сохранение гиперферментемии часто (у 62,5% больных 2 группы) соответствовало появлению ДНК в сыворотке крови или повышению вирусной нагрузки.
В соответствии с задачами нашей работы была проведена оценка ряда цитокинов у больных хроническим сочетанным гепатитом В (с высокой репликативной активностью HBV) + С с разными результатами ПВТ. По данным первичного обследования перед ПВТ не выявлено существенных различий между показателями ФНО-α в 1 и 2 группах (156,6±11,8 пг/мл и 162,4±12,4 пг/мл, р=0,257). Оценивая динамику состояния реактивности иммунной системы в 1 группе, отмечалось значительное - в 1,5 раза и более повышение уровня ФНО-α на 4-5 неделе от начала лечения у 14 из 15 больных (156,1±11,5 пг/мл и 303,7±20,9 пг/мл, р=0,032) (фиг.2). При дальнейшем наблюдении на 7-8 неделе от начала ПВТ отмечено снижение показателя ФНО-α (в 1,5 раза или ниже исходного).
С другой стороны, у большей части больных 2 группы (13 из 16, 81,2%) отсутствовало повышение уровня ФНО-α, лишь у оставшихся 3 больных отмечено незначительное увеличение содержания данного медиатора без какой-либо существенной динамики в дальнейшем.
Динамические изменения уровня ИЛ-1β и ИЛ-6 в те же сроки наблюдения достоверных показателей не выявили.
Таким образом, предлагаемый способ прогнозирования эффективности ПВТ хронического гепатита В у больных хронической сочетанной HBV/HCV-инфекцией: 1) позволяет оценить предполагаемый результат ПВТ хронического гепатита В задолго до окончания лечения (в частности в сочетании с оценкой других показателей с целью возможного изменения схемы лечения), 2) применим у больных ХГВ при наличии ко-инфекции ХГС, 3) применим для оценки эффективности лечения не только интерфероном-2а, но и на фоне комбинированной ПВТ (с использованием атипичных нуклеозидов), в том числе при наличии высокой репликации HCV.
Предлагаемый способ осуществляют следующим образом.
У больного натощак из срединной локтевой вены проводят забор крови в количестве 5,0 мл. Кровь центрифугируют 20 минут со скоростью 3000 оборотов в 1 минуту. В полученной сыворотке крови определяют содержание цитокина ФНО-α с помощью набора реагентов ProConlFgamma твердофазовым иммуноферментным методом (ООО «Протеиновый контур», Санкт-Петербург).
Прогноз осуществляют следующим образом: у больного при поступлении определяют в сыворотке крови содержание ФНО-α. Затем исследуют содержание этого показателя на 4-5 и 7-8 неделе: при содержании ФНО-α на 4-5 неделе от начала ПВТ, превышающем исходный уровень в 1,5 раза и больше с последующим снижением в 1,5 раза и более от исходного уровня на 7-8 неделе, прогнозируют положительный ответ на противовирусное лечение. При превышении исходного уровня менее чем в 1,5 раза на 4-5 неделе ПВТ или при наличии снижения ФНО-α менее чем в 1,5 раза от исходного уровня на 7-8 неделе терапии прогнозируют неэффективность проводимой терапии.
Примеры конкретного исполнения приведены в виде выписок из историй болезни.
Пример 1
Больная О., 30 лет (ИБ №207) - указания на перенесенный острый гепатит отсутствуют. В анамнезе 2 года назад были роды, 1,5 года назад - медицинский аборт. Год назад был обнаружен HBsAg. Стационарного лечения не проводилось. Поступила с жалобами на слабость, сниженный аппетит, чувство тяжести в правом подреберье, умеренные боли в крупных суставах. Общее состояние удовлетворительное. Гепатомегалия. Лабораторные данные: общее содержание билирубина - 22 мкмоль/л (свободный - 12, связанный -10), АлАТ - 1,8 ммоль/л·ч, тимоловая проба - 8,3 ед. В сыворотке крови обнаружены HBsAg в титре 1/512, HBeAg, суммарные анти-HBcore, анти-HBcore IgM, HBV ДНК (1*104 копий/мл), суммарные антиНСV, антиНСVсоre IgM, антиНСVсоre IgG, антиНСV NS3, антиНСV NS4, HCV РНК (1*103 вирусных частиц/мл), генотип - 1в. Диагноз: хронический сочетанный гепатит В (с высокой репликативной активностью) + С (с высокой репликацией), умеренной биохимической активностью.
Больной была назначена тритерапия (48 недель): Пегасис 180 мкг 1 раз в неделю, рибаверин 1200 мг ежедневно, энтакавир по 0,5 мг ежедневно.
Перед началом ПВТ уровень ФНО-α составлял 148,4 пг/мл, на 5 неделе лечения - 170,7 пг/мл (повышение менее чем в 1,5 раза), на 8 неделе лечения - содержание ФНО-α практически прежний (164,8 пг/мл), что говорило о плохом прогнозе эффективности терапии.
На 4 месяце от начала лечения было зарегистрировано исчезновение HBV ДНК и незначительное снижение АлАТ - 1,2 ммоль/л.ч. Однако сразу после окончания 48-недельного курса ПВТ зарегистрировано вновь появление ДНК вируса (отсутствие вирусологического ответа), что соответствовало слабой реакции Т-клеточного иммунитета в ответ на воздействие HBV. В отношении хронического гепатита С в структуре сочетанной инфекции - HCV РНК исчезла, то есть был зарегистрирован устойчивый вирусологический ответ
Пример 2
Больная З., 35 лет (ИБ №1275) - 2 года назад перенесла легкую форму ОГВ, была выписана с остаточными явлениями (гепатомегалия, уровень АлАТ превышал норму в 4 раза) и сохранявшимся HBsAg. Динамического наблюдения не проводилось. В анамнезе - удаление зубов, периодически посещает маникюрный салон. Поступила с жалобами на слабость, снижение аппетита, темное окрашивание мочи. При поступлении состояние удовлетворительное. Гепатоспленомегалия, консистенция печени плотная. Единичные сосудистые звездочки на коже грудной клетки. Лабораторные данные: общее содержание билирубина 28 мкмоль/л (свободный - 14, связанный - 14), АлАТ - 2,3 ммоль/л.ч. В сыворотке крови обнаружены HBsAg в титре 1/8192, HBeAg, суммарные антиНВсоrе, антиНВсоre IgM, HBV ДНК (1*105 вирусных частиц/мл), суммарные антиНСV, антиНСVсоre IgG, антиНСV NS4, антиНСV NS3. Диагноз: хронический сочетанный гепатит В (с высокой репликативной активностью)+С (с низкой репликацией), умеренной биохимической активностью.
Больной был назначен Пегасис 180 мкг 1 раз неделю и ламивудин по 100 мг ежедневно - 48 недель. Перед началом ПВТ уровень ФНО-α составлял 152,8 пг/мл, на 4 неделе лечения - 283,7 пг/мл (повышение почти в 2 раза), на 8 неделе лечения - содержание ФНО-α значительно меньше исходного (89,2 пг/мл). Данная динамика характеризовала положительный эффект ПВТ.
На 6 неделе от начала лечения было зарегистрировано исчезновение HBV ДНК. На 11 неделе лечения зарегистрировано повышение АлАТ до 3,5 ммоль/л·ч, к концу 3 месяца лечения - нормализация АлАТ. После проведенного противовирусного лечения на протяжении срока наблюдения в течение 2 лет не было выявлено появления HBV ДНК и повышения уровня трансаминаз, что характеризовало вирусологический ответ на противовирусную терапию ХГВ. Назначение ПВТ способствовало формированию стабильной ремиссии с последующим вирусологическим ответом у пациентки, что характеризовало высокую реактивность Т-клеточного иммунитета в ответ на воздействие HBV и способствовало элиминации HBV. В отношении хронического гепатита С в структуре микст-инфекции - серологический профиль был прежним.
Способ прогнозирования эффективности противовирусной терапии (ПВТ) хронического гепатита В (ХГВ), включающий определение содержания цитокина ФНО-α в сыворотке крови до и во время лечения, отличающийся тем, что у больных хронической сочетанной HBV/HCV - инфекцией содержание цитокина ФНО-α в сыворотке крови исследуют до начала противовирусной терапии, на 4-5 неделе и на 7-8 неделе противовирусной терапии и при превышении исходного уровня цитокина ФНО-α в 1,5 раза и более на 4-5 неделе терапии с последующим снижением в 1,5 раза и более на 7-8 неделе терапии прогнозируют хорошую эффективность назначенного лечения, при превышении исходного уровня менее чем в 1,5 раза на 4-5 неделе или при наличии снижения ФНО-α менее чем в 1,5 раза на 7-8 неделе терапии от исходного уровня прогнозируют неэффективность проводимой терапии.