Тетрациклические антибиотические производные антрахинона с высокой активностью, способ их получения и их применение
Иллюстрации
Показать всеИзобретение относится к тетрациклическим антибиотическим производным антрахинона с противораковой активностью. Тетрациклические антибиотические производные антрахинона, описываемые в настоящем изобретении, обладают такой же или более высокой активностью, чем активность известных лекарственных средств, таких как доксорубицин, даунорубицин и тому подобное, на клеточном уровне, и в то же время обладают лучшей толерантностью, чем толерантность доксорубицина и даунорубицина, для организма животного. 4 н. и 11 з.п.ф-лы, 54 прим., 3 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к тетрациклическим антибиотическим производным антрахинона с противораковой активностью, способу их получения и применению при получении лекарственного средства для лечения опухоли или рака.
Уровень техники
Тетрациклические антрахиноновые антибиотики, в особенности доксорубицин и даунорубицин, являются широко применяемыми противораковыми лекарственными средствами. Доксорубицин обладает значительными лечебными действиями для многих солидных опухолей, включающих рак печени, рак желудка, рак молочной железы, рак легких, рак яичников и множественные лейкозы. Даунорубицин является одним из наиболее эффективных лекарственных средств для лечения лейкоза. Однако, вследствие их побочных действий, таких как тяжелая миелосупрессия, кардиотоксичность, побочные реакции пищеварительного тракта и тому подобное, их клинические применения ограничиваются. До сих пор уже много тетрациклических производных антрахинона было выделено из природных источников или получено искусственно. Предполагается получить новое поколение противораковых лекарственных средств с высокой активностью и низкой токсичностью из этих производных. Активность на клеточном уровне производного доксорубицина, 2-пирролинилдоксорубицина (AN-201), полученного Attilla A. Nagy, et al., в 300-1000 раз больше активности доксорубицина. Однако, вследствие высокой токсичности AN-201, противораковую активность не изучали при максимально толерантной дозе на патологической моделе трансплантированной опухоли у мыши.
Сущность изобретения
Настоящее изобретение относится к антибиотическим тетрациклическим производным антрахинона с противораковой активностью. Антибиотические тетрациклические производные антрахинона, предлагаемые в настоящем изобретении, обладают такой же или более высокой активностью, чем активность известных лекарственных средств, таких как диоксорубицин, даунорубицин и тому подобное на клеточном уровне, в то время как являются более переносимыми, чем доксорубицин и даунорубицина для организма животного.
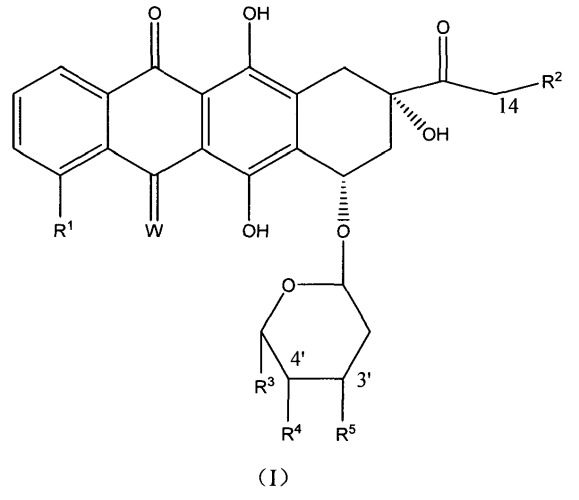
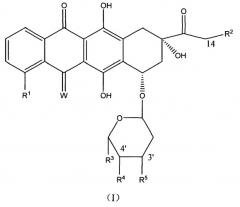
Соответственно этому, настоящее изобретение относится к соединению, представленному формулой (I), и его соли или сольвату
где
R1 представляет собой H, C1-4гидрокарбил или OC1-4гидрокарбил;
R2 представляет собой H или OR6, где R6 выбран из группы, состоящей из H, C(O)R8, пептидной цепи, C(O)NH2, C(O)NR8R9, C(O)Ar-R27, C(O)(C2-4гидрокарбилиден)COOH и остатка, представленного формулой (II); R8 и R9, каждый независимо, представляет собой H или C1-6гидрокарбил, или NR8R9 представляет собой пирролидин-1-ил, пиперидин-1-ил или морфолин-1-ил; Ar представляет собой ароматическое кольцо или ароматическое гетероциклическое кольцо; R27 представляет собой 0-5 одинаковых или разных групп, выбранных из группы, состоящей из F, Cl, NO2, CN, OH, SH, COOH, NH2, NR8R9, C1-6гидрокарбила, OC1-6гидрокарбила, OC(O)C1-6гидрокарбила, C(O)OC1-6гидрокарбила, SC1-6гидрокарбила, S(O)C1-6гидрокарбила и S(O)2C1-6гидрокарбила; пептидная цепь представляет собой одну природную аминокислоту, одну неприродную аминокислоту или пептидную цепь, состоящую из 2-4 природных аминокислот и/или неприродных аминокислот;
W представляет собой O или NH;
R3 представляет собой H, F, OC1-4гидрокарбил или C1-4гидрокарбил;
R4 представляет собой H, F, C1-4гидрокарбил или OR7, где R7 представляет собой H, 2-пиранил или R6;
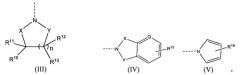
R5 представляет собой остаток, представленный формулой (III), остаток, представленный формулой (IV), остаток, представленный формулой (V), или малеимидо;
где
n равно 1 или 2;
X и Y, каждый независимо, представляет собой C=O или CR21R22;
Q представляет собой CH или N;
R10, R11, R12, R13, R15 и R16, каждый независимо, выбраны из группы, состоящей из H, F, Cl, CN, NO2, NH2, OH, C(O)OC1-4гидрокарбила, OC(O)C1-4гидрокарбила, OC1-4гидрокарбила, C1-4гидрокарбила, SC1-6гидрокарбила, S(O)C1-6гидрокарбила, S(O)2C1-6гидрокарбила, (C0-4гидрокарбилиден)Ar-R27 и NR8R9; и
R21 и R22, каждый независимо, представляют собой H или C1-4гидрокарбил.
Применяемый в контексте C1-4гидрокарбил может быть неразветвленным насыщенным или ненасыщенным гидрокарбилом или разветвленным насыщенным или ненасыщенным гидрокарбилом и может быть замещен 0-4 одинаковыми или разными заместителями, выбранными из группы, состоящей из F, Cl, CN, OH, NO2, COOH, C1-4гидрокарбила, NHC(O)C1-6гидрокарбила, NHC(O)Ar-R27 и NR8R9. R8 и R9, каждый независимо, представляют собой H или C1-6гидрокарбил или NR8R9 выбран из группы, состоящей из пирролидин-1-ила, пиперидин-1-ила и морфолин-1-ила.
Применяемый в контексте C2-4гидрокарбилиден может быть неразветвленным насыщенным или ненасыщенным гидрокарбилиденом или разветвленным насыщенным или ненасыщенным гидрокарбилиденом и может быть замещен 0-3 одинаковыми или разными заместителями, выбранными из группы, состоящей из F, Cl, CN, OH, NO2, COOH, C1-4гидрокарбила, NHC(O)C1-6гидрокарбила, NHC(O)Ar-R27 и NR8R9. R8 и R9, каждый независимо, представляют собой H или C1-6гидрокарбил или NR8R9 выбран из группы, состоящей из пирролидин-1-ила, пиперидин-1-ила и морфолин-1-ила.
Применяемый в контексте термин C0-4гидрокарбилиден может быть неразветвленным насыщенным или ненасыщенным гидрокарбилиденом или разветвленным насыщенным или ненасыщенным гидрокарбилиденом и может быть замещен 0-3 одинаковыми или разными заместителями, выбранными из группы, состоящей из F, Cl, CN, OH, NO2, COOH, C1-4гидрокарбила, NHC(O)C1-6гидрокарбила, NHC(O)Ar-R27 и NR8R9. R8 и R9, каждый независимо, представляют собой H или C1-6гидрокарбил или NR8R9 выбран из группы, состоящей из пирролидин-1-ила, пиперидин-1-ила и морфолин-1-ила.
Применяемый в контексте, C1-6гидрокарбил может быть неразветвленным насыщенным или ненасыщенным гидрокарбилом или разветвленным насыщенным или ненасыщенным гидрокарбилом и может быть замещен 0-4 одинаковыми или разными заместителями, выбранными из группы, состоящей из F, Cl, CN, OH, NO2, COOH, C1-4гидрокарбила, NHC(O)C1-6гидрокарбила, NHC(O)Ar-R27 и NR8R9. R8 и R9, каждый независимо, представляют собой H или C1-6гидрокарбил или NR8R9 выбран из группы, состоящей из пирролидин-1-ила, пиперидин-1-ила и морфолин-1-ила.
Применяемое в контексте ароматическое кольцо или ароматическое гетероциклическое кольцо выбрано из группы, состоящей из бензола, нафталина, пиридина, пиррола, тиофена, фурана, пиримидина и пиразина.
Соединение, представленное формулой (I), которое является подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R1 выбран из группы, состоящей из H, CH3 и OCH3. Соединением формулы (I), которое является наиболее подходящим для получения лекарственного средства для лечения опухоли или рака, является соединение, где R1 представляет собой H или ОСН3.
Соединение, представленное формулой (I), которое является подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R2 представляет собой H или OR6, где R6 выбран из группы, состоящей из H, глицила, аланила, валила, лейцинила, изолейцинила, фенилаланила, серинила, треонила, тирозинила, лизинила, 2-N,N-диметиламиноацетила, 2-N,N-диэтиламиноацетила, 2-пиперидилацетила, 2-морфолинилацетила, 2,2-диметилглицила, 2,2-диметил-2-метиламиноацетила, 2,2-диметил-2-(N,N-диметиламино)ацетила, 2,2-диметил-2-этиламиноацетила, 2,2-диметил-2-(N,N-диэтиламино)ацетила, 2,2-диметил-2-(N,N-дипропиламино)ацетила, 2,2-диметил-2-пиперидилацетила, 2,2-диметил-2-пирролинилацетила, 2,2-диметил-2-морфолинилацетила, 2,2-диметил-2-(N-метил-N-этиламино)ацетила, 2-фенилглицила, 2-фенил-2-метиламиноацетила, 2-фенил-2-(N,N-диметиламино)ацетила, 2-фенил-2-этиламиноацетила, 2-фенил-2-(N,N-диэтиламино)ацетила, 2-фенил-2-(N,N-дипропиламино)ацетила, 2-фенил-2-пиперидилацетила, 2-фенил-2-пирролинилацетила, 2-фенил-2-морфолинилацетила, 2-фенил-2-(N-метил-N-этиламино)ацетила, ацетила, пропионила, бутаноила, пентаноила, 3-метиламинопропионила, 3-этиламинопропионила, 3-N,N-диметиламинопропионила, 3-N,N-диэтиламинопропионила, 3-пиперидилпропионила, 3-пирролидинилпропионила, 3-морфолинилпропионила, N-глицилглицила, N-аланилглицила, N-валилглицила, N-серинилглицила, N-глицилаланила, N-аланилаланила, N-валилаланила, N-серинилаланила, N-глицилвалила, N-аланилвалила, N-валилвалила, N-серинилвалила, гидросукцинатной группы, (3-нитро-2-карбокси)бензоатной группы, (2-карбокси)бензоатной группы, (2,4-дикарбокси)бензоатной группы, (3,4,5,6-тетрафтор-2-карбокси)бензоатной группы, (2-карбокси-6-фтор)бензоатной группы и (3-фтор-2-карбокси)бензоатной группы. Соединение, представленное формулой (I), которое является более подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R2 представляет собой H или OR6, где R6 выбран из группы, состоящей из H, глицила, аланила, валила, лейцинила, изолейцинила, фенилаланила, серинила, треонила, тирозинила, лизинила, 2-N,N-диметиламиноацетила, 2-N,N-диэтиламиноацетила, 2-пиперидилацетила, 2-морфолинилацетила, 2,2-диметилглицила, 2-фенилглицила, 3-метиламинопропионила, 3-этиламинопропионила, гидросукцинатной группы, (3-нитро-2-карбокси)бензоатной группы, (2-карбокси)бензоатной группы, (2,4-дикарбокси)бензоатной группы, (3,4,5,6-тетрафтор-2-карбокси)бензоатной группы, (2-карбокси-6-фтор)бензоатной группы и (3-фтор-2-карбокси)бензоатной группы. Соединение, представленное формулой (I), которое является наиболее подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R2 представляет собой H или OR6, где R6 выбран из группы, состоящей из H, глицила, аланила, валила, лейцинила, изолейцинила, фенилаланила, серинила, треонила, тирозинила, лизинила, 2-N,N-диметиламиноацетила, 2-N,N-диэтиламиноацетила, 2-пиперидилацетила, 2-морфолинилацетила, 2,2-диметилглицила, 2-фенилглицила, гидросукцинатной группы, (3-нитро-2-карбокси)бензоатной группы, (2-карбокси)бензоатной группы, (2,4-дикарбокси)бензоатной группы, (3,4,5,6-тетрафтор-2-карбокси)бензоатной группы, (2-карбокси-6-фтор)бензоатной группы и (3-фтор-2-карбокси)бензоатной группы.
Соединение, представленное формулой (I), которое является подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где W представляет собой O или NH. Соединение, представленное формулой (I), которое является наиболее подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где W представляет собой O.
Соединение, представленное формулой (I), которое является подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R3 выбран из группы, состоящей из H, F, CH3, CH2CH3, OCH3 и OCH2CH3. Соединение, представленное формулой (I), которое является более подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R3 выбран из группы, состоящей из H, CH3, CH2CH3 и OCH3. Соединение, представленное формулой (I), которое является наиболее подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R3 представляет собой CH3.
Соединение, представленное формулой (I), которое является подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R4 выбран из группы, состоящей из H, F, OH, CH3, OCH3, 2-пиранила, гидросукцинатной группы, (3-нитро-2-карбокси)бензоатной группы, (2-карбокси)бензоатной группы, (2,4-дикарбокси)бензоатной группы, (3,4,5,6-тетрафтор-2-карбокси)бензоатной группы, (2-карбокси-6-фтор)бензоатной группы и (3-фтор-2-карбокси)бензоатной группы. Соединение, представленное формулой (I), которое является более подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R4 выбран из группы, состоящей из OH, OCH3, 2-пиранила и гидросукцинатной группы. Соединение, представленное формулой (I), которое является наиболее подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R4 выбран из группы, состоящей из OH, 2-пиранила и гидросукцинатной группы.
Соединение, представленное формулой (I), которое является подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R5 выбран из группы, состоящей из пиррол-1-ила, сукцинимидо, глутаримидо, бутиролактам-1-ила, валеролактам-1-ила, 3-метилпиррол-1-ила, 3-метоксипиррол-1-ила, 3-метилсукцинимидо, 3-метоксисукцинимидо, 3-метилглутаримидо, 3-метоксиглутаримидо, 3-метилбутиролактам-1-ила, 3-метоксибутиролактам-1-ила, 3-метилвалеролактам-1-ила, 3-метоксивалеролактам-1-ила, 4-метилвалеролактам-1-ила, 4-метоксивалеролактам-1-ила, бензосукцинимидо-1-ила и пиридосукцинимидо-1-ила. Соединение, представленное формулой (I), которое является наиболее подходящим для получения лекарственного средства для лечения опухоли или рака, является соединением, где R5 выбран из группы, состоящей из пиррол-1-ила, сукцинимидо, глутаримидо, бутиролактам-1-ила и валеролактам-1-ила.
В настоящем изобретении соединение, которое имеет хиральный центр и конкретно не идентифицировано как имеющее R- или S-конфигурацию в структурной формуле в описании и формуле изобретения, может быть соединением с R-конфигурацией, соединением с S-конфигурацией или их смесью.
Объем защиты настоящего изобретения должен включать также пролекарство, соль или активный метаболит соединения, описанного в настоящем изобретении.
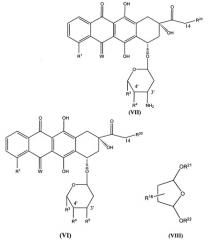
В настоящем изобретении описано несколько способов получения соединения, представленного формулой (VI), которое является важным промежуточным соединением для получения соединения, представленного формулой (I).
Способ 1
Группы, представленные R1, R3, R4 и W в соединении, представленном формулой (VII), являются такими же, как группы, представленные R1, R3, R4 и W в соединении, представленном формулой (I). R20 представляет собой H или OH. Группы, представленные R1, R3, R4, R5 и W в соединении, представленном формулой (VI), являются такими же, как группы, представленные R1, R3, R4, R5 и W в соединении, представленном формулой (I). R20 представляет собой Н или ОН. Группа, представленная R16 в соединении, представленном формулой (VIII), является такой же, как группа, представленная R16 в формуле (V). R21 и R22, каждый независимо, представляют собой Н или С1-4гидрокарбил.
Описываемой в контексте солью соединения, представленного формулой (VII), является соль соединения, представленного формулой (VII), полученная реакцией с кислотой, которая выбрана из группы, состоящей из хлористоводородной кислоты, серной кислоты, фосфорной кислоты, муравьиной кислоты, уксусной кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты и их смеси.
Соединение, представленное формулой (VI), получают реакцией соединения, представленного формулой (VII), или его соли с соединением, представленным формулой (VIII), в присутствии кислотного и/или основного реагента, где кислотный реагент выбран из группы, состоящей из хлористоводородной кислоты, серной кислоты, фосфорной кислоты, муравьиной кислоты, уксусной кислоты, пропионовой кислоты, масляной кислоты, пентановой кислоты, гексановой кислоты, метилсульфоновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты, лимонной кислоты, винной кислоты, молочной кислоты, яблочной кислоты и их смеси. Количеством кислотного реагента является 0,05-500-кратное количество (в молях) соединения, представленного формулой (VII). Более подходящим количеством кислотного реагента является 0,2-50-кратное количество (в молях) соединения, представленного формулой (VII). Наиболее подходящим количеством кислотного реагента является 0,7-5-кратное количество (в молях) соединения, представленного формулой (VII). Основный реагент выбран из группы, состоящей из карбоната калия, карбоната цезия, карбоната натрия, бикарбоната натрия, бикарбоната калия, гидроксида натрия, гидроксида калия, ацетата натрия, ацетата калия, фосфата натрия, фосфата калия, гидрофосфата натрия, гидрофосфата калия, лактата натрия, лактата калия, цитрата натрия, цитрата калия, тартрата натрия, тартрата калия, малата натрия, малата калия, пропионата натрия, пропионата калия, бутирата натрия, бутирата калия, сукцината натрия, сукцината калия, валерата натрия, валерата калия, глутарата натрия, глутарата, калия, триэтиламина, триметиламина, диизопропилэтиламина, 4-диметиламинопиридина, 4-(пирролидин-1-ил)пиридина, пиридина, N-метилморфолина и их смеси. Количеством основного реагента является 0,05-500-кратное количество (в молях) соединения, представленного формулой (VII). Более подходящим количеством основного реагента является 0,2-50-кратное количество (в молях) соединения, представленного формулой (VII). Наиболее подходящим количеством основного реагента является 0,7-5-кратное количество (в молях) соединения, представленного формулой (VII). Температура реакции от -20 до 150°С. Более подходящая температура реакции от -10 до 100°С. Наиболее подходящая температура реакции от -10 до 80°С. Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, N,N-диметилформамид, диметилсульфоксид, диметиловый эфир этиленгликоля, монометиловый эфир этиленгликоля, этанол, метанол, изопропанол, тетрагидрофуран, этилацетат, метилацетат, метилпропионат, этилпропионат, диэтиловый эфир этиленгликоля, моноэтиловый эфир этиленгликоля, N,N-диэтилформамид, 1,2-дихлорэтан, ацетонитрил, вода, соединение, представленное формулой (VIII), или их смесь. Если необходимо, в качестве катализатора в реакции можно применять триэтиламин, триметиламин, диизопропилэтиламин, 4-диметиламинопиридин, 4-(пирролидин-1-ил)пиридин, пиридин, N-метилморфолин и тому подобное. Когда органическое основание применяют в качестве катализатора, молярным количеством органического основания является 0,01-2-кратное количество соединения, представленного формулой (VII). Более подходящим молярным количеством органического основания является 0,05-0,2-кратное количество соединения, представленного формулой (VII). Молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (VIII), составляет от 1:0,1 до 1:10000. Более подходящее молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (VIII), составляет от 1:0,5 до 1:1000. Наиболее подходящее молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (VIII), составляет от 1:1 до 1:500.
В настоящем изобретении описан второй способ получения соединения, представленного формулой (VI).
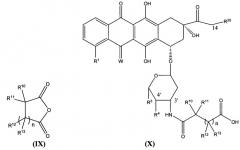
где группы, представленные R10, R11, R12, R13 и n в соединении, представленном формулой (IX), являются такими же, как группы, представленные R10, R11, R12, R13 и n в формуле (III); группы, представленные R10, R11, R12, R13 и n в соединении, представленном формулой (X), являются такими же как группы, представленные R10, R11, R12, R13 и n в формуле (III); группы, представленные R1, R3, R4 и W в соединении, представленном формулой (X), являются такими же, как группы, представленные R1, R3, R4 и W в соединении, представленном формулой (VII); R20 представляет собой H или OH.
Соединение, представленное формулой (X), получают реакцией соединения, представленного формулой (VII) или его соли с соединением, представленным формулой (IX). Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, тетрахлорид углерода, этилацетат, метилацетат, метилпропионат, этилпропионат, 1,2-дихлорэтан, ацетон, тетрагидрофуран, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, N,N-диметилформамида, N,N-диэтилформамида, диметилсульфоксид, ацетонитрил, вода или их смесь. Пиридин, 4-диметиламинопиридин, 4-диэтиламинопиридин, 4-(пирролидин-1-ил)пиридин или их смесь можно необязательно добавлять в реакционную смесь в качестве катализатора. Молярным количеством катализатора является 0,01-10-кратное количество соединения, представленного формулой (VII). Более подходящим молярным количеством катализатора является 0,02-5-кратное количество соединения, представленного формулой (VII). Оптимальным молярным количеством катализатора является 0,05-1-кратное количество соединения, представленного формулой (VII). В качестве агента, связывающего кислоту в реакционную смесь можно добавлять триэтиламин, триметиламин, пиридин, диизопропилэтиламин, N-метилморфолин, N-метилпиперидин, N-этилпиперидин, 4-диметиламинопиридин, 4-диэтиламинопиридин, 4-(пирролидин-1-ил)пиридин, карбонат калия, карбонат натрия, бикарбонат натрия, бикарбонат калия, карбонат цезия, гидроксид натрия, гидроксид калия или их смесь. Молярным количеством агента, связывающего кислоту, является 0,4-20-кратное количество соединения, представленного формулой (VII). Более подходящим молярным количеством агента, связывающего кислоту, является 0,8-10-кратное количество соединения, представленного формулой (VII). Оптимальным молярным количеством агента, связывающего кислоту, является 1-5-кратное количество соединения, представленного формулой (VII). Температура реакции от -20 до 100°С. Более подходящая температура реакции от -10 до 80°С. Наиболее подходящая температура реакции от -5 до 80°С. Молярное отношение в сырье соединения, представленного формулой (IX), к соединению, представленному формулой (VII), или его соли составляет от 1:0,1 до 1:10. Более подходящее молярное отношение в сырье соединения, представленного формулой (IX), к соединению, представленному формулой (VII), или соли составляет от 1:0,5 до 1:5. Наиболее подходящее молярное отношение в сырье соединения, представленного формулой (IX), к соединению, представленному формулой (VII), составляет от 1:0,8 до 1:3.
Соединение, представленное формулой (VI), получают с применением соединения, представленного формулой (Х) в присутствии дегидратирующего агента. Дегидратирующий агент выбран из группы, состоящей из DCC (дициклогексилкарбодиимид), EDC HCl (гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида), CDI (N,N'-карбонилдиимидазол) и DIC (N,N'-диизопропилкарбодиимид).
Молярным количеством дегидратирующего агента является 0,1-10-кратное количество соединения, представленного формулой (Х). Более подходящим молярным количеством дегидратирующего агента является 0,5-5-кратное количество соединения, представленного формулой (Х). Оптимальным молярным количеством катализатора является 1-3-кратное количество соединения, представленного формулой (Х). Температура реакции от -10 до 120°С. Более подходящая температура реакции от 0 до 100°С. Наиболее подходящая температура реакции от 0 до 80°С. Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, этилацетат, метилацетат, этилпропионат, метилпропионат, ацетон, тетрагидрофуран, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, N,N-диметилформамид, N,N-диэтилформамид, диметилсульфоксид или ацетонитрил или их смесь.
В настоящем изобретении описан третий способ получения соединения, представленного формулой (VI).
где группы, представленные R10, R11, R12, R13, R21, R22 и n в соединении, представленном формулой (XI), являются такими же, как группы, представленные R10, R11, R12, R13, R21, R22 и n в формуле (III); U выбран из группы, состоящей из Cl, Br, I, OTs (п-толуолсульфонатной группы) и OMs (метансульфонатной группы); T выбран из группы, состоящей из F, Cl, Br, OSu, OBt и OAt. Группы, представленные R10, R11, R12, R13, R21, R22, n и U в соединении, представленном формулой (XIII), являются такими же, как группы, представленные R10, R11, R12, R13, R21, R22, n и U в соединении, представленном формулой (XI). Группы, представленные R1, R3, R4, R20 и W в соединении, представленном формулой (X), являются такими же, как группы, представленные R1, R3, R4, R20 и W в соединении, представленном формулой (VII).
Соединение, представленное формулой (XIII), получают реакцией соединения, представленного формулой (VII), или его соли с соединением, представленным формулой (XI), в присутствии основания. Основание выбрано из группы, состоящей из триэтиламина, триметиламина, диизопропилэтиламина, пиридина, 4-диметиламинопиридина, 4-диэтиламинопиридина, 4-(пирролидин-1-ил)пиридина, N-метилморфолина, N-метилпиперидина, N-этилпиперидина, карбоната цезия, карбоната калия, карбоната натрия, бикарбоната натрия, бикарбоната калия, гидроксида натрия, гидроксида калия и их смеси. Молярным количеством основания является 0,5-10-кратное количество соединения, представленного формулой (VII), или его соли. Более подходящим молярным количеством основания является 0,8-7-кратное количество соединения, представленного формулой (VII), или его соли. Наиболее подходящим молярным количеством основания является 1-5-кратное количество соединения, представленного формулой (VII), или его соли. Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, 1,2-дихлорэтан, ацетон, этилацетат, изопропанол, метилацетат, пропилацетат, метилпропионат, этилпропионат, ацетонитрил, этанол, N,N-диметилформамид, N,N-диэтилформамид, диметилсульфоксид, тетрагидрофуран, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, монометиловый эфир этиленгликоля, моноэтиловый эфир этиленгликоля, этиленгликоль, этанол, пропанол, вода или их смесь. Температура реакции от -20 до 120°С. Более подходящая температура реакции от -10 до 100°С. Наиболее подходящая температура реакции от 0 до 80°С. Молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (XI), составляет от 1:0,2 до 1:10. Более предпочтительное молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (XI), составляет от 1:0,5 до 1:5. Оптимальное молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (XI), составляет от 1:0,8 до 1:3.
Соединение, представленное формулой (VI), получают реакцией соединения, представленного формулой (XIII), в присутствии основного реагента. Основный реагент выбран из группы, состоящей из триэтиламина, триметиламина, диизопропилэтиламина, пиридина, 4-диметиламинопиридина, 4-диэтиламинопиридина, 4-(пирролидин-1-ил)пиридина, N-метилморфолина, N-метилпиперидина, N-этилпиперидина, карбоната цезия, карбоната калия, карбоната натрия, бикарбоната натрия, бикарбоната калия, гидроксида натрия, гидроксида калия, гидрида натрия, гидрида калия, гексаметилдисилазида лития, гексаметилдисилазида калия, гексаметилдисилазида натрия и их смеси. Молярным количеством основного реагента является 0,5-3-кратное количество соединения, представленного формулой (XIII), или его соли. Более подходящим молярным количеством основного реагента является 0,8-2-кратное количество соединения, представленного формулой (XIII), или его соли. Наиболее подходящим молярным количеством основного реагента является 1-1,5-кратное количество соединения, представленного формулой (XIII), или его соли. Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, 1,2-дихлорэтан, ацетон, этилацетат, изопропанол, метилацетат, пропилацетат, метилпропионат, этилпропионат, ацетонитрил, этанол, N,N-диметилформамид, N,N-диэтилформамид, диметилсульфоксид, тетрагидрофуран, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля или их смесь. Температура реакции от -20 до 120°С. Более подходящая температура реакции от -10 до 100°С. Наиболее подходящая температура реакции от 0 до 80°С.
В настоящем изобретении описан четвертый способ получения соединения, представленного формулой (VI).
Группы, представленные R10, R11, R12, R13, R21, R22 и n в соединении, представленном формулой (XIV), являются такими же, как группы, представленные R10, R11, R12, R13, R21, R22 и n в формуле (III).
Соединение, представленное формулой (VI), получают реакцией соединения, представленного формулой (XIV), или его соли с соединением, представленным формулой (VII), в присутствии кислотного и/или основного реагента, в которой основный реагент выбран из группы, состоящей из триметиламина, триэтиламина, пиридина, N-метилморфолина, N-метилпиперидина, N-этилпиперидина, диизопропилэтиламина, карбоната калия, карбоната натрия, карбоната цезия, бикарбоната натрия, бикарбоната калия и их смеси. Молярным количеством основного реагента является 0,5-10-кратное количество соединения, представленного формулой (VII), или его соли. Более подходящим молярным количеством основного реагента является 0,8-5-кратное количество соединения, представленного формулой (VII), или его соли. Наиболее подходящим молярным количеством основного реагента является 1-3-кратное количество соединения, представленного формулой (VII), или его соли. Кислотный реагент выбран из группы, состоящей из хлористоводородной кислоты, серной кислоты, фосфорной кислоты, муравьиной кислоты, уксусной кислоты, пропионовой кислоты, масляной кислоты, пентановой кислоты, гексановой кислоты, метилсульфоновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты, лимонной кислоты, винной кислоты, молочной кислоты, яблочной кислоты и их смеси. Количеством кислотного реагента является 0,05-500-кратное количество (в молях) соединения, представленного формулой (VII). Более подходящим количеством кислотного реагента является 0,2-50-кратное количество (в молях) соединения, представленного формулой (VII). Наиболее подходящим количеством кислотного реагента является 0,7-5-кратное количество (в молях) соединения, представленного формулой (VII). Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, ацетон, ацетонитрил, этилацетат, метанол, этанол, пропанол, изопропанол, бутанол, этиленгликоль, тетрагидрофуран, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, монометиловый эфир этиленгликоля, моноэтиловый эфир этиленгликоля, метилацетат, пропилацетат, метилпропионат, этилпропионат, N,N-диметилформамид, N,N-диэтилформамид, диметилсульфоксид или их смесь. Температура реакции от -20 до 100°С. Более подходящая температура реакции от -10 до 80°С. Наиболее подходящая температура реакции от 0 до 50°С.
В настоящем изобретении описан пятый способ получения соединения, представленного формулой (VI).
где группы, представленные R15 и Q в формуле (XV), являются такими же, как группы, представленные R15 и Q в формуле (IV). Группы, представленные R15 и Q в формуле (XVI), являются такими же, как группы, представленные R15 и Q в формуле (IV). Группы, представленные R1, R3, R4, R20 и W в формуле (XVI), являются такими же, как группы, представленные R1, R3, R4, R20 и W в соединении, представленном формулой (VII). Группы, представленные R15 и Q в формуле (XVII), являются такими же, как группы, представленные R15 и Q в формуле (IV). Группы, представленные R1, R3, R4, R20 и W в формуле (XVII), являются такими же, как группы, представленные R1, R3, R4, R20 и W в соединении, представленном формулой (VII).
Соединение, представленное формулой (XVI) или формулой (XVII), получают реакцией соединения, представленного формулой (VII), или его соли с соединением, представленным формулой (XV). Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, тетрахлорид углерода, этилацетат, метилацетат, метилпропионат, этилпропионат, 1,2-дихлорэтан, ацетон, тетрагидрофуран, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, N,N-диметилформамид, N,N-диэтилформамид, диметилсульфоксид, ацетонитрил, вода или их смесь. В реакционную смесь в качестве катализатора можно необязательно добавлять пиридин, 4-диметиламинопиридин, 4-диэтиламинопиридин, 4-(пирролидин-1-ил)пиридин или их смесь. Молярным количеством катализатора является 0,01-10-кратное количество соединения, представленного формулой (VII). Более подходящим молярным количеством катализатора является 0,02-5-кратное количество соединения, представленного формулой (VII). Оптимальным молярным количеством катализатора является 0,05-1-кратное количество соединения, представленного формулой (VII). В реакцию в качестве связывающего кислоту агента можно необязательно добавлять триэтиламин, триметиламин, пиридин, диизопропилэтиламин, N-метилморфолин, N-метилпиперидин, N-этилпиперидин, 4-диметиламинопиридин, 4-диэтиламинопиридин, 4-(пирролидин-1-ил)пиридин, карбонат калия, карбонат натрия, бикарбонат натрия, бикарбонат калия, карбонат цезия, гидроксид натрия, гидроксид калия или их смесь. Молярное количество агента, связывающего кислоту, составляет 0,4-20-кратное количество соединения, представленного формулой (VII). Более подходящее молярное количество агента, связывающего кислоту, составляет 0,8-10-кратное количество соединения, представленного формулой (VII). Оптимальное молярное количество агента, связывающего кислоту, составляет 1-5-кратное количество соединения, представленного формулой (VII). Температура реакции от -20 до 100°С. Более подходящая температура реакции от -10 до 80°С. Наиболее подходящая температура реакции от 0 до 80°С. Молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (XV), составляет от 1:0,2 до 1:10. Более подходящее молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (XV), составляет от 1:0,5 до 1:5. Наиболее подходящее молярное отношение в сырье соединения, представленного формулой (VII), или его соли к соединению, представленному формулой (XV), составляет от 1:0,8 до 1:3.
Соединение, представленное формулой (VI), можно получить из соединения, представленного формулой (XVI) или формулой (XVII), в присутствии дегидратирующего агента. Дегидратирующий агент выбран из группы, состоящей из DCC (дициклогексилкарбодиимид), EDC HCl (гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида), CDI (N,N'-карбонилдиимидазол) и DIC (N,N'-диизопропилкарбодиимид). Молярным количеством дегидратирующего агента является 0,1-10-кратное количество соединения, представленного формулой (XVI) или (XVII). Более подходящим молярным количеством дегидратирующего агента является 0,5-5-кратное количество соединения, представленного формулой (XVI) или (XVII). Оптимальным молярным количеством дегидратирующего агента является 1-3-кратное количество соединения, представленного формулой (XVI) или (XVII). Температура реакции от -10 до 120°С. Более подходящая температура реакции от 0 до 100°С. Наиболее подходящая температура реакции от 20 до 100°С. Реакцию проводят в растворителе, таком как дихлорметан, хлороформ, этилацетат, метилацетат, этилпропионат, метилпропионат, ацетон, тетрагидрофуран, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, N,N-диметилформамид, N,N-диэтилформамид, диметилсульфоксид, ацетонитрил или их смесь. В реакционную смесь в качестве катализатора можно добавлять пиридин, 4-диметиламинопиридин, 4-диэтиламинопиридин, 4-(пирролидин-1-ил)пиридин или их смесь. Молярным количеством катализатора является 0,01-1-кратное количество соединения, представленного форм