Способ диагностики хронического риносинусита
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к оториноларингологии. Для диагностики хронического риносинусита проводят морфологическое исследование зон структуризации, которые образуются последовательно при клиновидной дегидратации биологической жидкости полости носа и околоносовых пазух. В качестве критериев оценки процесса в норме и при патологии берут временные параметры образования структур, при этом длительность всего периода дегидратации с формированием окончательного рисунка фации определяют по формуле: tобщ=t1+t2+t3, где t1 - время образования периферической краевой зоны; t2 - время образования радиальных трещин и секторов; t3 - время образования поперечных трещин с формированием отдельностей и образованием в них центров кристаллизации. При t1 от 30 до 50 минут, t2 от 50 до 90 минут, t3 от 60 до 90 минут, tобщ от 2,5 до 4,5 часов диагностируют хронический риносинусит. Способ повышает эффективность диагностики воспалительных заболеваний верхних дыхательных путей за счет получения параметров времени образования структур твердой фации носового секрета при клиновидной дегидратации. 8 ил., 3 пр.
Реферат
Изобретение относится к медицине, а именно к оториноларингологии, и может найти применение при диагностике патологических процессов или заболеваний слизистой оболочки полости носа и околоносовых пазух.
Известно, что состав носового секрета является индикатором всех процессов, в том числе и патологических, которые протекают в слизистой оболочке верхних дыхательных путей.
В настоящее время в клинической практике исследование носового секрета на качественное и количественное содержание в нем различных органических и неорганических компонентов, а также его свойств с помощью биохимических, иммунологических, физических методов, цитологическое исследование его состава имеет большое диагностическое и прогностическое значение.
Секрет слизистой оболочки дыхательных путей - второй после респираторного эпителия неотъемлемый компонент мукоцилиарной системы и мукоцилиарного клиренса. Он покрывает эпителий на всем протяжении от верхних отделов дыхательных путей до нижних и вместе с ресничками принимает участие в сохранении гомеостаза внутренней среды организма с помощью удаления продуктов метаболизма, инородных частиц, микроорганизмов наружу из дыхательных путей.
Двигательная активность ресничек может осуществляться только в жидкой среде, роль которой выполняет секрет слизистой оболочки дыхательных путей. Это обосновывает их структурно-функциональное единство в осуществлении мукоцилиарного клиренса.
В секрете слизистой оболочки содержится ряд неспецифических и специфических защитных факторов, способствующих обезвреживанию и удалению микроорганизмов. К первым относятся гликопротеиды, лизоцим, лактоферрин, комплемент, протеазы-ингибиторы, секреторные глюкозидазы, интерферон.
Специфические факторы представлены иммуноглобулинами, выполняющими роль защиты от микроорганизмов. Благодаря деятельности тех и других факторов происходит нейтрализация вирусов, токсинов, лизис бактерий.
Выработка слизистой оболочкой секрета - один из основных защитных механизмов респираторного тракта. Объем носовой секреции у здоровых людей составляет от 100 мл до 1-2 л в сутки. Около 3/4 жидкой части носового секрета расходуется на увлажнение вдыхаемого воздуха, остальная же часть необходима для обеспечения мукоцилиарного транспорта.
Секрет слизистой оболочки дыхательных путей в норме по химическому составу состоит из: воды (95%), белков (1%-3%), углеводов - мукогликопротеидов (1%), липидов - фосфолипидов, нуклеиновых кислот (1%), сурфактанта (0,8%), ионов электролитов (Na, Cl, P, Са), антипротеаз, антиоксидантов (1%).
По данным Y.Sakakura (1979) носовой секрет у здоровых людей имеет РН 7,4±0,3; вязкость 1,17±0,1; содержание электролитов: Na - 34,2±3,7 мэкв/л; К - 5,96±1,33 мэкв/л; Са - 3,9±0,9 мэкв/л. Общий белок - 14,5±7,4 мг/мл; полисахариды - 2,62±0,8 мг/мл. Сухая масса секрета составляет 19,7 мг/мл. Он представляет собой щелочной протеид, который при РН=7,5-7,6 превращается из золя в гель (Рихельманн Г., Лопатин А.С., 1994; Федосеев Г.Б., 1995; Blake J.B., Winet H., 1980; Macchione M. et al., 1995).
Секрет слизистой оболочки дыхательных путей имеет двухфазную структуру (Lucas A.M., Douglas L.C., 1934; Reissing, Bang B.G. et al., 1978). Реснички находятся и движутся в более глубоком слое, так называемой перицилиарной серозной жидкости, обладающей свойствами золя. Поверхностный слой - гель, расположен над золем и над ресничками и непосредственно контактирует с воздухом.
По данным В.Barnet, С.Е.Miller (1966); W.C.Hulbert et al. (1982), общая толщина слоя секрета полости носа составляет 5-10 мкм, перицилиарной жидкости (золь) - 6-8 мкм, слоя гель - 0,5-2 мкм. По данным L.Giheber, Z.Priel (1989) толщина слоя золь находится в пределах от 7 до 10 мкм.
Золь, имеющий низкую вязкость, близкую к вязкости воды, действует как вспомогательная среда, координирующая движение ресничек, которые транспортируют слой гель, вязкость которого примерно в 1000 раз больше вязкости слоя золь.
Одним из основных компонентов секрета респираторного тракта являются мукогликопротеиды (муцины), которые секретируются бокаловидными клетками эпителия и железами слизистой оболочки дыхательных путей. Они содержат около 80% сахара и имеют особый аминокислотный состав. Муцины - гликопротеиды с низким содержанием аминокислот и высоким содержанием углеводов: фукозы, галактозы, N-ацетилглюкозаминов, N-ацетилгалактозаминов и сиаловой кислоты. Гистохимический состав муцина меняется в зависимости от нахождения его в различных отделах дыхательных путей. Образование и выделение муцина обусловлено генетически. Известно около восьми специфических генов, отвечающих за образование различных эпителиальных мукогликопротеидов - муцинов, связанных карбонгидратными цепями соответственно их белковой молекуле.
Составная часть мукогликопротеидов - мукополисахариды выполняют в организме комплекс функций: а) структурной основы опорной покровной и соединительной ткани; б) факторов, определяющих содержание воды и проницаемость соединительной ткани; в) слизистой составляющей секретов покрывающих и защищающих слизистые оболочки; г) составных элементов иммунных реакций организма.
В зависимости от химического состава входящих в них мукополисахаридов, композиция мукогликопротеидов, состоящая из кислой и нейтральной фракций, подразделяется на три группы: сиаломуцины, сульфомуцины (кислые) и фукомуцины (нейтральные). Кислая фракция состоит из большого количества альфа-сиаловых кислот и значительно меньшего количества сульфамуцинов. Кислые муцины непосредственно влияют на состояние сетчатой структуры слизи и на ее способность к гидратации. Сиаломуцины могут ингибировать процессы воспаления в бронхах. Их защитная роль состоит в образовании каркаса слизистого чехла, покрывающего эпителий.
Нейтральная фракция представлена белково-полисахаридными соединениями, которые имеют довольно прочную связь между белковой и углеводными частями.
Особое свойство секрета слизистой оболочки - вязкость - обусловлено наличием в нем мукогликопротеидов.
Кислотная характеристика содержимого клеток слизистой оболочки дыхательных путей подвержена значительным колебаниям - от нейтральной до кислой. Одновременно наблюдается разное содержание в клетках сульфата и сиаловой кислоты. Для секрета слизистой оболочки при воспалительных процессах нижних дыхательных путей характерно содержание нейтральных муцинов и муцинов с высоким содержанием сульфата, в то время как для здоровых характерно наличие в секрете слизистой оболочки кислых муцинов с большим содержанием сиаловой кислоты.
Известно, что изменение физических свойств секрета эпителия слизистой оболочки дыхательных путей, соотношения вязкости слоев золь и гель - одна из основных причин нарушения защитной функции мукоцилиарной системы и мукоцилиарного транспорта. При воспалении слизистой оболочки увеличивается продукция слизи бокаловидными клетками и железами подслизистого слоя. Биологическая целесообразность такой реакции заключается в увеличении толщины слоя, защищающего эпителиоциты. При этом в зону воспаления мигрируют фагоцитирующие клетки крови, в ткани увеличивается уровень противовоспалительных цитокинов.
В результате активации фагоцитов существенным образом увеличивается продукция прооксидантов. Наблюдается сдвиг окислительно-восстановительного потенциала в сторону окислительных значений. Гиперпродукция слизи - изначально защитная реакция - может превращаться в патогенный фактор, этому способствуют: снижение МЦТ за счет уменьшения реснитчатых клеток и увеличения бокаловидных; изменение реологии слизи вследствие формирования дисульфидных связей между молекулами муцинов в условиях окислительных значений редокс-потенциала среды. Активация синтеза оксида азота, обусловливает вазодилатацию, уменьшение активности ресничек, увеличение проницаемости тканевых барьеров. Все это приводит к стазу большого объема вязкой мокроты и создает условия для колонизации слизистой оболочки микробами, их размножению, более глубокому проникновению в толщу ткани и хронизации воспаления.
Содержание в секрете слизистой оболочки дыхательных путей мукогликопротеидов, ансамбль извитых молекул которых создает молекулярную структуру слизи, определяет физические свойства секрета (Lucas A.M., Douglas L.C., 1934). Эти гетерогенные цепи захватывают чужеродные частицы, которые затем транспортируются к глотке посредством цилиарной активности (Jacquot J. et al., 1992; Murase M., Shimizu H., 1986). В мукогликопротеидах выявляется большое количество перекрестных связей, дисульфидных мостиков, ионных, водородных связей и сил Ван дер Ваальса. Благодаря этим гликопротеидным связям, секрет имеет физические характеристики жидкости - вязкость, и твердого тела - эластичность (Carlson D.M., 1976; Puchelle E. et al., 1985).
Физические свойства секрета эпителия слизистой оболочки укладываются в понятия и принципы реологии - науки о текучести жидкостей. В норме время релаксации слизистого секрета θ очень большое (до 30 мс), что дает возможность слизи свободно захватывать и удерживать посторонние частицы (Gilboa A., Silberberg A., 1976).
С другой стороны, реснички совершают эффективный удар в секрете быстрее, чем время релаксации. Таким образом, ресничка сталкивается с секретом и перемещает его как твердое тело. Известно, что коэффициент переноса слизи пропорционален вязкости и упругости слизи (Ross S.M., CorrsinS., 1974).
Установлено, что соотношение между вязкими и упругими свойствами является показателем транспортабельности слизи in vitro и in vivo (Lorenzi G. et al., 1992; Macchione M. et al., 1995). Оптимальными реологическими параметрами слизи являются: динамическая вязкость η=1-1,5·10-3 Па·с, и время релаксации вязких напряжений θ. Его значение зависит от внутренней структуры слизи и в норме достигает 40 мс, а при патологии увеличивается до 200 мс (Raptis A., Perdikis С., 1983; Rautiainen M.E.P., 1988.).
Соотношение вязкости слоев золь и гель оказывает большое влияние на мукоцилиарный транспорт. Как правило, при хроническом бронхите и других неспецифических заболеваниях легких отмечается увеличение вязкости, что обычно соответствует снижению гидратации мокроты, увеличению в ней концентрации органических и неорганических веществ. Причем увеличение вязкости - пропорционально тяжести течения заболевания.
Известно, что переходу золя в гель и ухудшению мукоцилиарного транспорта способствует увеличение концентрации мукогликопротеидов в секрете, сопровождающееся уменьшением скрученности и увеличением длины молекул муцина, увеличением осмолярности секрета, уменьшением глубины слоя золь и увеличением вязкости слоя гель (Man S.P. et al., 1979; Puchell E. et al., 1983; Puchelle E. et al., 1985; Verdugo P., 1991).
Влияние изменения реологических свойств бронхиального секрета человека (вязкости и упругости) на мукоцилиарный транспорт и частоту биения ресничек отмечают Е.Puchell et al. (1983); Е.Puchelle, J.M.Zahm, 1984; E.Puchell et al. (1985). Максимальная скорость транспорта слизистого секрета достигается при определенных вязкоупругих его свойствах, толщине слоя гель, составляющей 2 мкм в сочетании с оптимальной механической координацией движения ресничек (Barton С., Raynor S., 1967; Puchelle E. et al., 1985; Puchelle E. et al., 1987).
Таким образом, секрет дыхательных путей имеет большое значение в функционировании органов дыхания и сохранении гомеостаза внутренней среды организма. Состав секрета полости носа и околоносовых пазух рассматривается как фактор патогенеза и индикатор патологического процесса в дыхательных путях (Веремеенко К.Н. 1982; Плужников М.С., Лавренова Г.В., 1990; Drettner В., 1982; Mitchell - Heggs 1982; Mygind N., Winter В., 1987; Demoly P. et al., 1994).
Однако, несмотря на значимость секрета слизистой оболочки верхних дыхательных путей в нормальной жизнедеятельности организма человека, в настоящее время он представляет наименее обследованный объект мукоцилиарной системы. Большая часть информации, заложенной в секрете слизистой оболочки верхних дыхательных путей, остается недоступной для прочитывания, что связано с несовершенством существующих методов его получения и исследования.
В настоящее время разработка новых способов получения и исследования носового секрета представляет несомненную актуальность. В клинической практике исследование носового секрета на качественное и количественное содержание в нем различных органических и неорганических компонентов, а также его свойств с помощью биохимических, иммунологических, физических методов, цитологическое исследование его состава имеет большое диагностическое и прогностическое значение.
С помощью этих исследований секрета полости носа и околоносовых пазух проводится диагностика наличия воспалительного процесса в слизистой оболочке дыхательных путей. Однако для достоверной диагностики характера воспалительного процесса необходимо комплексное определение целого ряда иммунологических и биохимических параметров воспалительного процесса. Это представляет достаточно трудоемкий метод исследования, требующий затрат времени и дорогостоящих реактивов.
Применение нами нового в медицине методологического направления - морфологического исследования структур твердой фазы биологических жидкостей - позволило изучить секрет верхних дыхательных путей на принципиально новом, до настоящего времени не доступном, вследствие отсутствия методологии, молекулярном уровне и дать характеристику его морфотипов в норме и при патологии.
Одним из перспективных новых направлений исследования в биологии и медицине служит «функциональная морфология» биологических жидкостей. Теоретической основой к исследованию «функциональной морфологии» биологических жидкостей явилось учение о самоорганизации и поведении сложных систем, разработанное школами нобелевского лауреата И.Пригожина и Г.Хакена.
За последнее десятилетие Шабалин В.Н. и Шатохина С.Н. установили, что при переходе в твердую фазу в процессе самоорганизации (дегидратация) биологические жидкости структурируются и приобретают устойчивые морфологические формы. Этими авторами разработана методологическая основа исследования морфологических структур биологических жидкостей, а именно методы клиновидной и краевой дегидратации.
Биологические жидкости выполняют широкий спектр жизненно важных функций в жизнедеятельности организма человека на всех его уровнях. При переходе биологической жидкости в твердую фазу образуются кристаллические структуры, морфотип которых представляет интегральную картину взаимодействия молекулярного и атомарного состава в жидкой фазе биологической жидкости. Анализ структур твердой фазы биологической жидкости позволяет проводить диагностику физиологического и патофизиологического состояния организма даже на самых ранних (доклинических) этапах заболевания. «Функциональная морфология» биологических жидкостей представляет кардинально новое научное направление, отличающееся принципиальной новизной по своим теоретическим основам, методике исследования, виду получаемой информации, подходу к диагностике и лечению заболеваний. Соответственно дальнейшее развитие методологии «функционального морфологического» исследования биологических жидкостей человека представляет несомненную актуальность для различных областей клинической медицины, в том числе и оториноларингологии.
Диагностика патологического процесса с помощью «функциональной морфологии» до настоящего времени основывалась преимущественно на описании и оценке морфотипов фаций различных биожидкостей, полученных с помощью методов клиновидной и краевой дегидратации. Для диагностики заболевания опираются на описания характерных для нормы и патологии состояний структур твердой фазы различных БЖ по определенным морфологическим критериям и маркерам патологического процесса. В настоящее время большая часть функциональной морфологической диагностики основана на изучении текстур фаций различных биожидкостей при физиологических и патологических состояниях.
Активно продолжается набор базы статистических данных морфотипов структур твердой фазы биологических жидкостей у здоровых и при различных заболеваниях, что в дальнейшем позволит разработать критерии и алгоритмы диагностики, а также выявить маркеры различных патологических процессов в организме человека.
Установлено, что патологическое состояние организма проявляется в нарушении образования структур твердой фазы биологических жидкостей в виде: асимметричности расположения структур, отсутствия характерных для нормы и образования патологических структур. Одним из механизмов нарушения структуризации при патологии является образование патологически прочных белково-солевых и других комплексов и агрегатов, которые не распадаются при дегидратации, что отражается на структуре фации. При этом структуры, характерные для нормы (радиальные трещины, аркады, секторы, отдельности, конкреции), могут отсутствовать, проявлять полиморфизм и асимметрию.
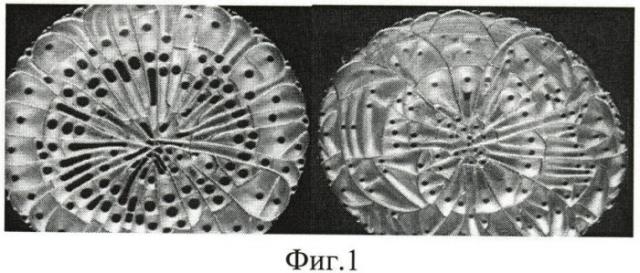
Известно использование морфологического исследования сыворотки крови человека для диагностики различных патологических состояний (Шабалин В.Н., Шатохина С.Н., 1986, 2001). Анализ видеоизображений фаций сыворотки крови позволил определить характерные для физиологического и патологического состояния организма структуры. Физиологическое состояние организма характеризовалось симметричным расположением радиальных трещин, отдельностей, конкреций и других формообразующих элементов фации (см. фиг.1).
Патологические изменения относились к системным и подсистемным элементам структуризации. Системные нарушения фации сыворотки крови проявлялись в асимметричности расположения основных ее элементов, изменении их формы или полном отсутствии основных формообразующих элементов фации (см. фиг.2).
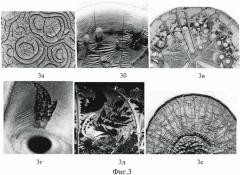
Подсистемные нарушения проявлялись характерными патологическими структурами, которые являлись маркерами патологических процессов. К маркерам патологических состояний отнесены: жгуты, указывающие на гипоксию (см. фиг.3а), бляшкообразные структуры (см. фиг.3б), свидетельствующие об интоксикации эндогенного или экзогенного происхождения; воронкообразные трещины (см. фиг.3в), указывающие на высокое напряжение защитных механизмов; морщины - маркеры повышенного содержания липидов (см. фиг.3е).
Аномальные поля типа «языков Арнольда» (см. фиг.3г), «ковров Серпинского» (см. фиг.3д) являлись признаками воспалительного процесса и были обнаружены в сыворотке крови больных острыми и хроническими неспецифическими воспалительными заболеваниями внутренних органов.
На фиг.4 представлены структурные образования, сформированные грибами рода Candida (см. фиг.4а), врожденный системный кандидоз (см. фиг.4б), с бобовидными споровыми образованиями (см. фиг.4в).
Представленные данные свидетельствуют, что морфологическая картина сыворотки крови отражает патологические изменения, происходящие в организме человека, и может быть использована в качестве диагностического метода в различных клинических специальностях.
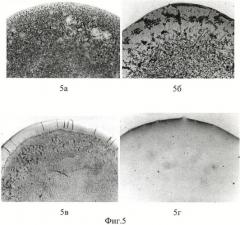
Также известно морфологическое исследование мочи (Тарусинов Г.А. «Кристаллографическое исследование мочи в диагностике и дифференциальной диагностике диффузных заболеваний соединительной ткани у детей», Педиатрия, 1994, №1, стр.55-57) в диагностике различных патологических состояний (см. фиг.5).
Микроскопическая картина фаций мочи в норме имеет идентичную картину: их поверхность покрыта кристаллическим налетом солей. Кристаллы солей могут быть мелкими (до 100 мкм), средними (до 0,1 мм) и крупными (до 0,5 мм). В последнем случае визуально просматривается их структура. При микроскопии фации - центр ее образован более мелкими, четкими кристаллическими структурами, в направлении к периферии размер кристаллов увеличивается (см. фиг.5а).
Фации мочи больных с протеинурией, как правило, имеют 2 зоны: центральную - в виде налета солей и краевую - аморфную прозрачную (см. фиг.5в). Краевая белковая зона, как правило, имеет небольшое число аркадных трещин. Минимальное количество белка, при котором в образце визуально выявляется краевая прозрачная зона, составляет, по данным (Шабалин В.Н., Шатохина С.Н, 2001), менее 0,022 г/л.
Следовательно, появление прозрачной краевой зоны при клиновидной дегидратации мочи является ценным информативным признаком, свидетельствующим о присутствии белка в исследуемом материале.
Таким образом, метод клиновидной дегидратации пригоден для обнаружения белка в моче. В норме при клиновидной дегидратации соли как обладатели более мощных осмотических сил кристаллизуются в центральной зоне капли биологической жидкости, а белковые компоненты формируют периферическую аморфную зону.
У больных мочекаменной болезнью с протеинурией устанавливаются патологически прочные связи камнеобразующих солей с белками. Эти связи настолько прочные, что даже при клиновидной дегидратации, когда активизируются осмотические и онкотические силы, они не в состоянии их разрушить. В результате аномальные белково-солевые агрегаты перемещаются в высыхающей капле как единый комплекс. Только по окончании процесса дегидратации (завершении испарения связанной воды), соли отрываются от белковых компонентов и кристаллизуются в белковой среде краевой зоны (см. фиг.5б).
Особая структура фации выявляется при наличии глюкозы в моче (см. фиг.5г). При высоких концентрациях глюкозы фация имеет вид стекловидной пленки. Такой характер структуризации связан с тем, что глюкоза при дегидратации не кристаллизуется сама и препятствует кристаллизации солей, находящихся вместе с ней в растворе. При высокой концентрации глюкоза полностью блокирует кристаллизацию всех солей, растворенных в моче, в результате фация представляет собой прозрачную аморфную пленку. При низких концентрациях в условиях метода клиновидной дегидратации глюкоза вытесняется из массы капли мочи на периферию и образует прозрачное аморфное кольцо. Таким образом, метод клиновидной дегидратации может иметь самостоятельное значение в диагностике глюкозурии.
Нами разработан метод диагностики хронического риносинусита по характеристике морфотипов структур твердой фазы биологических жидкостей полости носа и околоносовых пазух.
Перевод биологических жидкостей в твердую фазу для последующего их морфологического исследования проводился нами с помощью метода клиновидной дегидратации.
Качественная оценка фаций секрета слизистой оболочки полости носа здоровых людей выявила характерный для них морфотип структур фаций. В большинстве образцов фаций наблюдались две четко выраженные зоны: центральная и периферическая (см. фиг.6).
Центральная зона во всех препаратах занимала большую часть фации. В ней были расположены древовидные или звездообразные кристаллические структуры, с ветвлениями 1-4 порядка (см. фиг.6а, 6б). В периферической зоне наблюдались: мелкодисперсные, аморфные белковые структуры (см. фиг.6а), симметричные радиальные трещины с аркадами (см. фиг.6б). Представленный морфотип структур твердой фазы секрета слизистой оболочки полости носа здоровых отражает характерный для физиологического состояния состав носового секрета.
У больных хроническим гнойным риносинуситом в ряде образцов фаций достаточно часто наблюдались различного рода включения (см. фиг.7а). Образование включений может быть обусловлено взаимодействием различных компонентов секрета воспалительной и противовоспалительной направленности, приводящим к образованию диссипативных патологических структур. Кристаллические структуры солей в центральной зоне фаций больных были представлены хаотично расположенными, короткими, палочкообразными, прямыми и V-образно разветвленными элементами (см. фиг.7а), редко сохраняющими радиальную направленность, что значительно отличало фации больных от фаций здоровых. В ряде образцов наблюдались дендритные структуры с разветвлениями 1-2 порядка (см. фиг.7б и г, 7а). Разветвление кристаллов до 3-4 порядка встречалось крайне редко.
Кристаллы солей в центральной зоне фаций больных часто прослеживались с трудом вследствие скопления вокруг них аморфных белковых элементов, что свидетельствовало о нарушении процесса кристаллизации солей центральной зоны, обусловленного присутствием не характерного для нормы состава белков (см. фиг.7а, 7б и 7в).
Перенос белков в центральную зону фации при структуризации может быть связан с количественным и качественным изменением их состава в жидкой фазе секрета, приводящим к образованию в процессе структуризации прочных белково-солевых комплексов. Это может препятствовать характерному для системной самоорганизации биологической жидкости в норме переносу белков в периферическую зону. Избыточно прочные комплексы оседают в центральной зоне.
В центральной зоне фаций ряда образцов больных хроническим гнойным риносинуситом при рассмотрении под большим увеличением микроскопа наблюдались сетчатые, паутинообразные с разорванными нитями, кляксообразные, булавовидные структуры, зернистые и мелкозернистые аморфные белковые образования (см. фиг.8в). Они представляли структуры белковых комплексов, которые не встречались в образцах фаций секрета слизистой оболочки полости носа здоровых.
В ряде препаратов текстур фаций секрета слизистой оболочки полости носа группы больных хроническим гнойным риносинуситом наблюдалось значительное преобладание ширины периферической зоны по сравнению с центральной, что не наблюдалось у здоровых и также свидетельствует об изменении структурно-компонентного состава и нарушении физиологических процессов, протекающих в биологических жидкостях в норме.
В периферической зоне фаций секрета полости носа больных хроническим гнойным риносинуситом в отличие от контрольной группы наблюдалась асимметричность расположения элементов структуризации радиальных трещин и аркад (см. фиг.8а). В периферической зоне части образцов присутствовало значительное количество (от 3 до 9) четко выраженных рядов концентрационных волн различной интенсивности и ширины.
На фиг.8б представлен образец фации слизисто-гнойного секрета больного хроническим гнойным риносинуситом, полученного из верхнечелюстной пазухи во время операции. Периферическая зона занимает более половины радиуса фации и содержит пять четко различающихся по интенсивности затемнения концентрационных зон различной ширины, образование которых обусловлено отложением элементов с одинаковыми структурно-функциональными свойствами. Такая картина свидетельствует о многокомпонентном биохимическом составе секрета в первую очередь белковом и выраженной интенсивности протекающих в нем биохимических процессов. Возможно, это обусловлено активизацией компенсаторных механизмов и имеет защитно-приспособительную направленность.
Образование структур твердой фазы секрета слизистой оболочки полости носа в группе здоровых обусловлено количественным и качественным компонентным составом секрета, который обеспечивает физиологический характер протекающих в его жидкой фазе процессов. Описанные структуры могут быть отнесены к характерным для нормы элементам секрета слизистой оболочки полости носа.
Качественная оценка текстур фаций секрета слизистой оболочки полости носа у больных хроническим гнойным риносинуситом обнаружила значительное отличие морфотипа больных от морфотипа здоровых. Полученные находки свидетельствуют о нарушении кристаллизации солей центральной зоны в фациях секрета слизистой оболочки полости носа у больных хроническим гнойным риносинуситом. Они свидетельствуют о количественном и качественном изменении состава секрета и в первую очередь структурно-функциональных характеристик белков, диктующих специфику структур твердой фазы секрета, и указывают на патофизиологический характер протекающих в жидкой фазе исследованных биологических жидкостей реакций.
Таким образом, основными отличительными особенностями морфотипа фаций секрета полости носа больных хроническим гнойным риносинуситом от здоровых служит нарушение кристаллизации солей в центральной зоне фации, которое проявляется в аморфизации центральной зоны белковыми компонентами, не свойственной для здоровых.
Кроме того, в образцах фаций больных хроническим гнойным риносинуситом наблюдаются структуры, указывающие на активацию протекающих в биологической жидкости биохимических процессов, возможно имеющих защитную направленность (наличие нескольких рядов концентрационных волн белковых отложений в периферической зоне).
Перечисленные особенности морфотипа фаций носового секрета больных хроническим риносинуситом свидетельствуют об изменении количественного и качественного состава белков в жидкой фазе исследуемых биологических жидкостей.
Однако визуальная описательная оценка структур биологических жидкостей носит субъективный характер.
В настоящее время морфологическое исследование биологических жидкостей имеет несколько направлений своего развития, включая: тезиграфию, хромографию и другие направления.
Тезиграфия изучает кристаллогенез биологических жидкостей с использованием кристаллообразующих веществ, усиливающих кристаллизицию (см. Камакин Н.Ф., Мартусевич А.К. и соавт. «Основные и дополнительные критерии тезограмм», Вятский медицинский вестник, 2003, №2, стр.22-24).
Хромография изучает кристаллогенез с использованием красителей избирательно окрашивающих отдельные компоненты биологических жидкостей, что позволяет определить их компонентный состав. Примером может служить исследование интерпретации результатов анализа биологических жидкостей методом клиновидной дегидратации с использованием красителей избирательно окрашивающих белки, входящие в состав биологических жидкостей.
Наиболее близким по технической сущности к заявляемому способу является способ выявления воспалительного заболевания путем определения локализации групп белков в высохшей капле сыворотки крови при помощи красителей (см. Обухова Л.М., Конторщикова К.Н. - Вест. Нижегор. универ. им. Н.И.Лобачевского. - 2008. - №3. - С.116-119).
Способ включает анализ структур твердой фазы, полученной методом клиновидной дегидратации сыворотки крови, после предварительного перемешивания ее с красителями. Проводился анализ корреляции между шириной зон окраски и концентрацией белковых фракций сыворотки. Это позволило определить локализацию и количество различных типов белков в высохшей капле сыворотки крови, что определяет реакцию воспаления.
При осуществлении данного способа проводили исследование сыворотки крови больных с нарушением процентного соотношения белковых фракций, с повышенным содержанием холестерина и практически здоровых людей.
В каждом образце определяли общее количество белка, процентное соотношение белковых фракций, общего холестерина и холестерина липопротеидов высокой и низкой плотности. Изучали структурный макропортрет сыворотки крови при добавлении различных красителей, применяемых в биохимии, гистохимии для выявления белков: метиленовый синий, толуидиновый синий, кармин, альциановый голубой, амидочерный 10В, кумасси бриллиантовый синий R-250, бромфеноловый синий.
После перемешивания сыворотку с добавлением красителя в объемном соотношении 3:1 исследовали методом клиновидной дегидратации, для чего каплю высушивали на горизонтально расположенном предметном стекле при комнатной температуре в течение 18-24 часов, а затем анализировали структуру полученной дегидратированной капли в световом микроскопе. Высохшие капли фотографировали и рассчитывали соотношение ширины различных зон окраски по их радиусу.
Затем определяли коэффициент корреляции между этими показателями и значениями концентраций белковых фракций сыворотки, общего холестерина, холестеринов. Проведенный корреляционный анализ между шириной зон окраски и концентрацией белковых фракций сыворотки обнаружил: прямую взаимосвязь между содержанием альбуминов в сыворотке крови и шириной краевой зоны при использовании амидочерного 10В (r=0,495). При обратной взаимосвязи с шириной центральной зоны (r=-0,441).
Это указывает на то, что при высыхании капли сыворотки крови альбумины располагаются в краевой зоне. При этом содержание глобулинов коррелировало с шириной центральной зоны (амидочерный 10В r=0,486), промежуточной зоны толуидиновый синий и кармин). Обратная связь наблюдалась с шириной краевой зоны (амидочерный 10В r=-0,412).
Из полученных данных следует, что глобулины располагаются в центральной и промежуточных зонах, высохшей капли сыворотки крови. Содержание гамма-глобулинов (иммуноглобулинов) прямо зависит от размеров центральной зоны (амидочерный r=0,603, бромфеноловый синий r=0,439) и обратно с шириной краевой зоны (амидочерный r=-0,571, толуидиновый синий r=-0,516, бромфеноловый синий r=-0,414).
При увеличении уровня гамма-глобулинов структурный макропортрет сыворотки крови с добавлением красителя отличался более широкой центральной зоной по сравнению с таковой у здорового человека.
С размерами промежуточной зоны (окраска амидочерным 10В и толуидиновым синим) прямо коррелировало содержание глобулинов α1, α2 и β. Содержание глобулинов α прямо связано с шириной первой ближней к краю промежуточной зоны высохшей капли крови: амидочерный 10В r=0,575; толуидиновый синий r=0,459. Содержание глобулинов β прямо связано с шириной второй (ближней к центру) промежуточной зоны: амидочерный 10В r=0,552; толуидиновый синий r=0,443.
Таким образом, в результате проведенных исследований с использованием красителей, традиционно применяемых в биохимии и гистохимии для определения белков, была выявлена локализация различных типов белков в высохшей капле сыворотки крови: альбумины - краевая зона, α и β-глобулины, включая липопротеины, - в промежуточной и иммуноглобулины - в центральной зоне.
В настоящее время перспектива развития функциональной морфологии биологических жидкостей направлена в первую очередь на объективизацию оценки результатов исследования с дальнейшей их математической компьютерной обработкой.
Недостатком указанного способа является его достаточная сложность и трудоемкость (использование серии красителей).
Технический результат заявляемого решения заключается в повышении эффективности проводимого исследования при неинвазивной диагностике воспалительных заболеваний дыхательных путей путем определения временных параметров образования структур твердой фазы носового секрета при клиновидной дегидратации.
Технический результат заявляемого решения заключается в повышении эффективности проводимого исследования при неинвазивной диагностике острого и хронического риносинусита путем определения интегрального параметра образования структур твердой фазы носового секрета при клиновидной дегидратации.
Для достижения указанного результата в способе, согласно изобретению, нами изучались временные параметры динамики процесса высыхания капли биологической жидкости (секрета полости носа) на стандартном предметном стекле по методу клиновидной дегидратации.
Получение секрета полости носа проводили с помощью разработанного нами способа по патенту RU №2287161.
Способ осуществляют следующим образом.
Забор носового секрета выполняют щеточкой с помощью нескольких легких движений в области носовой перегородки и нижней носовой раковины, в переднезаднем направлении, отступая 1-1,5 см от переднего края, в месте расположения мерцательного эпителия. Затем его смешивают с 0,5 мл физиологического раствора хлорида натрия, производят центрифугирование в течение 15 минут при 900 g, нанесение надосадочной жидкости в объеме 2,0-2,5 мкл на поверхность стекла в виде капли и осуществляют высушивание ее методом клиновидной или краевой дегидратации до получения структуры твердой фазы.
Метод клиновидной дегидратации состоит в следующем: на обезжиренное предметное стекло, расположенное строго горизонтально, наносят каплю исследуемой жидкости в объеме 0,02 мл (20 мкл). При этом диаметр капли составляет 5-7 мм. Затем каплю высушивают при температуре 20-25°С и относительной влажности 65-70% при минимальной влажности окружающего воздуха. При высыхании капля должна быть неподвижной. Продолжительность периода высыхания (до момента анализа структуры) составляет 12-24 часа.
Картина высыхания капли наблюдалась нами с помощью