Способ профилактики раневых осложнений после протезирующей герниопластики при ущемленных вентральных грыжах
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к хирургии, и может использоваться при проведении протезирующей герниопластики при ущемленных вентральных грыжах. Для этого осуществляют установку эндопротеза и проводят антибиотикопрофилактику. При этом по обе стороны от доступа в проекции края сетчатого эндопротеза выполняют отдельные проколы кожи, которые располагают от угла сетчатого эндопротеза на расстоянии, равном 1/3 длины стороны. В проколы параллельно доступу в перипротезные ткани вводят полихлорвиниловые трубки диаметром 0,9-1,0 мм с отверстиями диаметром 0,3 мм, расположенными на боковой поверхности трубки через каждые 20 мм. Длина трубок соответствует длине сетчатого эндопротеза. Трубки располагают над плоскостью сетчатого эндопротеза. В первые и третьи сутки послеоперационного периода у пациента производят забор 400 мл крови в систему «Гемакон». Разделяют полученную кровь центрифугированием в режиме 3700 оборотов в минуту в течение 20 мин на плазму, лейко-тромбоцитарную и эритроцитарную массы. Эритроцитарную массу и плазму возвращают пациенту, в лейко-тромбоцитарную массу добавляют 200 мл 0,9% раствора NaCl, повторяют цетрифугирование в том же режиме с удалением надосадочного слоя. Лейко-тромбоцитарную массу культивируют с 500000 ME рекомбинантного интерлейкина-2 и 200 мл 0,9% раствора NaCl в течение 60 минут при температуре 37°С с последующим центрифугированием в том же режиме с выделением надосадочной жидкости, содержащей комплекс аутологичных цитокинов. Полученный комплекс вводят в полихлорвиниловые трубки из расчета 1 мл на каждый см2 площади сетчатого эндопротеза в 1 и 3 сутки после операции. Лейко-тромбоцитарную массу возвращают пациенту. Способ обеспечивает предупреждение развития раневых осложнений и ускорение процесса заживления в области сетчатого эндопротеза за счет влияния на первично-асептическую воспалительную реакцию в перипротезных тканях. 1 з.п. ф-лы, 3 ил., 2 пр.
Реферат
Изобретение относится к области медицины, а именно к области хирургии, и может использоваться с целью профилактики раневых (воспалительных, инфекционных и гнойных) осложнений у больных после грыжесечения с пластикой сетчатым эндопротезом при ущемленных вентральных грыжах и у больных с высоким риском развития раневых осложнений после планового грыжесечения с пластикой сетчатым эндопротезом.
Известен способ лечения с использованием интерлейкина-2 при расширенных бактериальных инфекциях (патент Германии №3910011, А61К 37/02, 1990). По этому способу введение интерлейкина-2 внутривенно, подкожно, внутрибрюшинно, внутримышечно приводит к усилению неспецифического клеточного ответа, что способствует снижению числа бактерий в перитонеальной полости и снижению эндотоксинов в плазме крови. Способ по патенту может быть использован путем введения интерлейкина-2 в дозе 1-3,5·10 в 6-й степени ЕД/кг в послеоперационном периоде, состояниях после тяжелой травмы, распространенной грамположительной и грамотрицательной инфекции, перитоните.
Известен также способ (РСТ №94/04174, кл. А61К 37/02, 1992 г.), при котором с целью усиления иммунной реакции на патоген используются природные ксеногенные цитокины.
Однако при данных способах использования цитокинов происходит их быстрое выведение, что диктует необходимость использования цитокинов в высоких дозах, что может вызывать выраженные побочные токсические реакции.
Известен способ адаптивной иммунотерапии для лечения больных с гнойно-септическими процессами (RU №2098125 C1, A61К 38/20, А61К 38/00), при котором выделяют мононуклеарные клетки, культивируют их с интерлейкином-2 и возвращают парэнтерально пациенту, а имеющиеся гнойные полости промывают раствором, содержащим комбинацию цитокинов, полученных при культивировании мононуклеарных клеток с интерлейкином-2.
Данный способ применяется только в комбинации с внутривенным введением и не используется как самостоятельный способ только местной цитокинотерапии; используется только при лечении гнойных ран, а не в профилактических целях. Низкая проницаемость препарата при промывании, требующая более высокой концентрации препарата, частоты и длительности применения, а также увеличения сроков лечения является недостатком данного способа.
Известен способ профилактики послеоперационных гнойных осложнений области хирургического вмешательства и лечения инфицированных послеоперационных ран без гнойного отделяемого с использованием комплекса аутологичных цитокинов, в котором используются подкожные инъекции, для создания инфильтрационного вала в зоне операции на расстоянии 1,5 см от краев раны (Патент РФ №2394602, МПК А61М 1/38; А61К 31/7042; А61К 38/19; А61Р 37/00; А61Р 41/00. Бюл. №20 от 20.07.2010 г.). Данный способ применяется для профилактики только гнойных осложнений и лечения инфицированных послеоперационных ран. Инъекции препарата в поверхностный слой подкожно-жировой клетчатки не создают высокой концентрации в зоне интереса, такой как место установки эндопротеза, а также связаны с дополнительными болевыми ощущениями для пациентов.
Основным способом профилактики раневых осложнений в хирургической практике, в том числе и хирургии грыж, является антибиотикопрофилактика (Антибактериальные препараты в клинической практике, Козлов С.Н., М., 2009 г., стр.207-211; Клиническая хирургия, национальное руководство, под редакцией В.С.Савельева, М., 2008 г., том 1, стр.158-162). Антибиотикопрофилактика в современной хирургии стала рутинным методом. В хирургии ущемленных вентральных грыж обычно используют ультракороткую или короткую схемы антибиотикопрофилактики; антибиотикопрофилактика средней продолжительности или длительная могут потребоваться при наличии осложнений ущемленных вентральных грыж, таких как некроз кишки, либо при развитии инфекционных осложений в послеоперационном периоде; преимущественно применяют внутривенное введение цефалоспоринов 1-2 поколений: цефозалина, цефуроксима (Л.С.Страчунский, С.Н.Козлов, Современная антимикробная химиотерапия. Руководство для врачей. - М.: Боргес, 2002).
К недостаткам антибиотикопрофилактики в хирургии ущемленных грыж следует отнести недостаточную эффективность в условиях полиантибиотикорезистентности нозокомиальной микрофлоры, возможность формирования антибиотикорезистентности микробов в ране вследствие кратковременного воздействия антибиотика, необходимость системного воздействия антибиотика, дороговизна метода при его рутинном применении (Носов В.Г., 2007 г. Профилактика инфекции в области хирургического вмешательства при аллопластике паховых и инцизионных вентральных грыж). Рандомизированными исследованиями не доказано достоверного снижения частоты развития инфекции в области хирургического вмешательства при применении антибиотикопрофилактики при грыжесечениях (Периоперационная антибиотикопрофилактика в абдоминальной хирургии, пособие для врачей, под редакцией В.Д.Федорова, В.Г.Плешкова, Л.С.Страчунского, М., 2004 г.). Применение антибиотиков при протезирующей герниопластике не оказывает никакого влияния на первично-асептическую воспалительную реакцию в зоне эндопротеза, являющуюся субстратом воспалительно-инфекционных осложнений в данном случае.
Задача настоящего изобретения - повышение эффективности способа профилактики раневых осложнений у пациентов после герниопластики ущемленных вентральных грыж сетчатым эндопротезом с использованием местной цитокиновой терапии за счет влияния на первично-асептическую воспалительную реакцию в перипротезных тканях при протезирующей герниопластике.
Поставленная задача решается способом профилактики раневых осложнений после протезирующей герниопластики при ущемленных вентральных грыжах, включающим установку эндопротеза и проведение антибиотикопрофилактики.
Выполняют отдельные проколы кожи по обе стороны от доступа в проекции края сетчатого эндопротеза, которые располагают от угла сетчатого эндопротеза на расстоянии, равном 1/3 длины стороны сетчатого эндопротеза, в проколы параллельно доступу в перипротезные ткани вводят полихлорвиниловые трубки с отверстиями, длина которых соответствует длине сетчатого эндопротеза. Трубки располагают над плоскостью сетчатого эндопротеза. Проводят иммунотерапию, для чего у пациента производят забор 400 мл крови в систему «Гемакон», разделяют полученную кровь центрифугированием в режиме 3700 оборотов/мин в течение 20 мин на плазму, лейко-тромбоцитарную и эритроцитаную массы. Эритроцитарную массу и плазму возвращают пациенту. В лейко-тромбоцитарную массу добавляют 200 мл 0,9% раствора NaCl, повторяют цетрифугирование в том же режиме, удаляют надосадочный слой, лейко-тромбоцитарную массу культивируют с 500000 ME рекомбинантного интерлейкина-2 и 200 мл 0,9% раствора NaCl в течение 60 минут при температуре 37°С, затем вновь центрифугируют в том же режиме с выделением надосадочной жидкости, содержащей комплекс аутологичных цитокинов, которую вводят в полихлорвиниловые трубки из расчета 1 мл на каждый см2 площади эндопротеза в 1 и 3 сутки после операции, лейко-тромбоцитарную массу возвращают пациенту.
Используют полихлорвиниловые трубки диаметром 0,9-1,0 мм с отверстиями диаметром 0,3 мм, расположенными на боковой поверхности трубки через каждые 20 мм.
Новизна изобретения
Выполняют отдельные проколы кожи по обе стороны от доступа в проекции края сетчатого эндопротеза, которые располагают от угла сетчатого эндопротеза на расстоянии, равном 1/3 длины стороны сетчатого эндопротеза. В проколы параллельно доступу в перипротезные ткани вводят полихлорвиниловые трубки с отверстиями, длина которых соответствует длине сетчатого эндопротеза. Трубки располагают над плоскостью сетчатого эндопротеза.
Трубки в перипротезных тканях проводятся на всю длину эндопротеза, что способствует равномерному распределению раствора в перипротезных тканях. Введение раствора через предварительно установленные трубки позволяет минимизировать неприятные ощущения больного. Трубки вводятся непосредственно в перипротезные ткани - в предбрюшинную клетчатку через кожу, подкожно-жировую клетчатку и апоневроз широких мышц живота при подапоневротической пластике или в глубокий слой подкожно-жировой клетчатки через поверхностный слой подкожно-жировой клетчатки и поверхностную фасцию живота при надапоневротической пластике. Такое положение трубок позволяет создать наибольшую концентрацию вводимого раствора именно в тех тканях, где развивается воспалительная реакция на сетчатый эндопротез, таким образом оказывать влияние на воспалительную реакцию.
Проводят иммунотерапию, для чего у пациента производят забор 400 мл крови в систему «Гемакон», разделяют полученную кровь центрифугированием в режиме 3700 оборотов/мин в течение 20 мин на плазму, лейко-тромбоцитарную и эритроцитарную массы, эритроцитарную массу и плазму возвращают пациенту, в лейко-тромбоцитарную массу добавляют 200 мл 0,9 % раствора NaCl, повторяют цетрифугирование в том же режиме, удаляют надосадочный слой, лейко-тромбоцитарную массу культивируют с 500000 ME рекомбинантного интерлейкина-2 и 200 мл 0,9% раствора NaCl в течение 60 минут при температуре 37°С, затем вновь центрифугируют в том же режиме с выделением надосадочной жидкости, содержащей комплекс аутологичных цитокинов.
Раствор с комплексом аутологичных цитокинов вводится из расчета 1 мл на каждый см2 площади эндопротеза, так как данным объемом раствора производится достаточное пропитывание перипротезных тканей. Расчет объема раствора на площадь сетчатого эндопротеза объясняется тем, что выраженность воспалительной реакции на протез непосредственно зависит от площади протеза.
Используют полихлорвиниловые трубки диаметром 0,9-1,0 мм с отверстиями диаметром 0,3 мм, расположенными на боковой поверхности через каждые 20 мм. Наличие отверстий в трубках позволяет равномерно распределить вводимый раствор в перипротезных тканях.
Введение раствора с комплексом аутологичных цитокинов в первые и третьи сутки послеоперационного периода объясняется длительностью фазы воспаления в послеоперационной ране, которая составляет 5-7 суток, тогда как наибольшая выраженность воспаления наблюдается в 1-4 сутки послеоперационного периода.
Совокупность существенных признаков позволяет получить новый технический результат, заключающийся в создании высокой коцентрации комплекса аутологичных цитокинов непосредственно в зоне развития воспалительной реакции на сетчатый эндопротез как на инородное тело, что позволяет путем иммунокоррекции местной воспалительной реакции оптимизировать процессы заживления, тем самым уменьшить риск развития раневых осложнений и ускорить прорастание тканями сетчатого эндопротеза.
Известные ранее способы были направлены на профилактику именно гнойных осложнений со стороны раны, тогда как предлагаемый нами способ подразумевает наличие в ране сетчатого эндопротеза как объекта асептической воспалительной реакции, которая приводит к образованию сером, инфильтратов и нагноений. С учетом влияния сетчатого эндопротеза на раневой процесс введение аутологичных цитокинов в область сетчатого эндопротеза позволяет оптимизировать процессы воспаления, стимулировать иммуннозависимые реакции репарации, тем самым предупреждать развитие раневых осложнений и ускорять процесс заживления в области сетчатого эндопротеза.
Впервые в хирургической практике применена с целью профилактики развития осложнений со стороны послеоперационной раны передней брюшной стенки в условиях установки сетчатого эндопротеза при ущемленных вентральных грыжах местная цитокиновая терапия с учетом роли местной первично-асептической воспалительной реакции на эндопротез в патогенезе послеоперационных раневых осложнений. Использование полихлорвиниловых трубок позволяет обеспечить равномерное распределение препарата непосредственно в месте расположения эндопротеза и минимизировать болевую реакцию пациента на инъекции. Введение препарата в расчете 1 мл раствора на каждый см2 площади сетчатого эндопротеза обусловлено тем, что при этом создается достаточное пропитывание перипротезных тканей.
Способ введения, непосредственно в перипротезные ткани, используя предварительно установленные трубки, в отличие от внутривенного, внутримышечного, аппликационного и традиционного введения в поверхностный слой подкожно-жировой клетчатки, позволяет быстро создать более высокую концентрацию препарата в перипротезных тканях. Также способ позволяет добиться более равномерного распределения препарата в них, что повышает эффективность действия комплеска аутологичных цитокинов именно в тканях, непосредственно контактирующих с сетчатым эндопротезом как причиной воспалительной реакции.
Препарат вводится непосредственно в перипротезные ткани, а именно в глубокий слой подкожно-жировой клетчатки при расположении протеза над апоневрозом широких мышц живота, либо в предбрюшинную клетчатку при расположении эндопротеза под апоневрозом, где и формируется местный иммунный ответ и повышение иммунологической реактивности.
Совокупность существенных признаков в доступной нам литературе не найдена, следовательно, изобретение соответствует критерию «новизна».
Способ поясняется рисунками, представленными на Фиг.1-3.
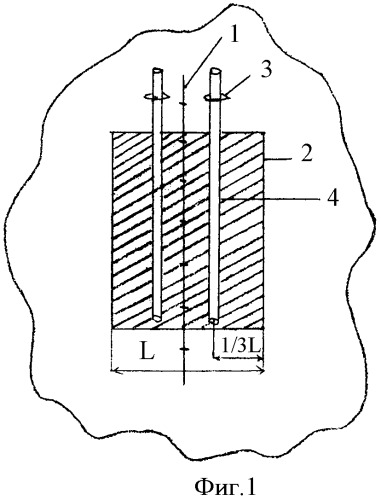
На Фиг.1 показано расположение проколов и трубок.
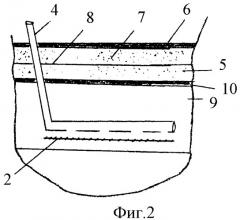
На Фиг.2 показано размещение сетчатого эндопротеза и трубок при надапоневротической пластике.
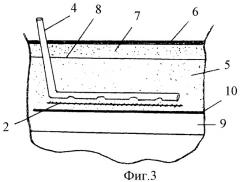
На Фиг.3 показано размещение сетчатого эндопротеза и трубок при подапоневротической пластике.
Способ осуществляется следующим образом.
При выполнении герниопластики сетчатым эндопротезом у больных с ущемленными вентральными грыжами интраоперационно после выполнения основной части герниопластики перед ушиванием операционной раны по обе стороны от оперативного доступа 1 в проекции края сетчатого эндопротеза 2 на расстоянии, равном 1/3 длины стороны L от угла сетчатого эндопротеза, выполняют проколы кожи. Через проколы кожи 3 параллельно доступу другой стороне сетчатого эндопротеза в перипротезные ткани вводят полихлорвиниловые трубки 4 диаметром 0,9-1,0 мм с отверстиями диаметром 0,3 мм, расположенными на боковой поверхности трубки через каждые 20 мм. Длина трубок соответствует длине сетчатого эндопротеза (Фиг.1). Трубки вводят в перипротезные ткани - в глубокий слой подкожно-жировой клетчатки 5 через кожу 6, поверхностный слой подкожно-жировой клетчатки 7 и поверхностную фасцию живота 8 при надапоневротической пластике (Фиг.3) или в предбрюшинную клетчатку 9 через кожу 6, поверхностный слой подкожно-жировой клетчатки 7, поверхностную фасцию живота 8 и глубокий слой подкожно-жировой клетчатки 5 и апоневроз широких мышц живота 10 при подапоневротической пластике (Фиг.3). Трубки располагают над плоскостью сетчатого эндопротеза.
В первые и третьи сутки послеоперационного периода у больного в систему «Гемакон» производят забор 400 мл крови из локтевой вены. Кровь центрифугируется при 3700 оборотов/мин в течение 20 мин, затем из системы удаляют плазму и эритроцитарную массу. Далее в полученную лейко-тромбоцитарную массу добавляют 200 мл 0,9% раствора NaCl, после чего производят центрифугирование в том же режиме и удаление надосадочной жидкости с оставлением лейко-тромбоцитарной массы, в которую добавляют 500000 ME рекомбинантного интерлейкина-2 и 200 мл 0,9% раствора NaCl, полученный раствор инкубируют в течение часа при температуре 37°С. Далее раствор центрифугируют в прежнем режиме, надосадочный слой, содержащий аутологичные цитокины, забирается в стерильные флаконы, а оставшаяся лейко-тромбоцитарная масса возвращается пациенту.
Инъекция комплекса аутологичных цитокинов в предварительно установленные трубки осуществляют в первые сутки послеоперационного периода из расчета 1 мл раствора на каждый см2 сетчатого эндопротеза.
На третьи сутки послеоперационного периода забор крови, центрифугирование, инкубирование с интерлейкином-2 и инъекцию комплекса аутологичных цитокинов через трубки повторяют.
Клинический пример 1
Пациентка К. 68 лет (история болезни №2015) поступила в хирургическое отделение в экстренном порядке 17.05.2010 в 11:35 с диагнозом: ущемленная вентральная грыжа; сопутствующий: гипертоническая болезнь III стадии риск 3.
Грыженоситель в течение 10 лет. Ущемление в течение 72 часов. В анамнезе отмечает подъем температуры тела до 38°С.
Состояние средней степени тяжести, выраженный болевой синдром в области грыжевого выпячивания, температура 37,7°С, гемодинамика стабильная, тахикардии нет.
В общем анализе крови: лейкоциты 5,8·10%, палочкоядерные нейтрофилы - 15, сегментоядерные нейтрофилы - 66, моноциты - 2, лимфоциты - 16, эозинофилы - 1, показатели красной крови и тромбоциты в пределах нормы.
В биохимическом анализе крови все показатели в пределах нормы.
По ЭКГ: систолическая перегрузка левых отделов сердца, синдром укороченного PQ.
После предоперационной подготовки, антибиотикопрофилактики внутривенным введением цефазолина 2,0 г внутривенно перед операцией, профилактики тромбоэмболических осложнений в экстренном порядке 17.05.2010 произведена операция: грыжесечение, резекция ущемленной некротизированной предбрюшинной клетчатки, герниопластика грыжевых ворот с установкой сетчатого протеза под апоневроз широких мышц живота, апоневроз над протезом ушит без натяжения. Размер установленного эндопротеза составил 10×7,5 см - площадь 75 см2. Сетчатый эндопротез более длинной стороной ориентирован вдоль операционного доступа.
Интраоперационно в предбрюшинную клетчатку над эндопротезом через отдельные проколы кожи на расстоянии 2,5 см от углов сетчатого эндопротеза, с двух сторон от доступа, параллельно ему и другой, длинной стороне эндопротеза установлены трубки для проведения местной цитокиновой терапии. Трубки длиной 100 мм диаметром 1,0 мм с отверстиями диаметром 0,3 мм расположены на боковой поверхности трубки через каждые 20 мм. Трубки ориентированы в данном случае параллельно более длинной стороне сетчатого эндопротеза и проведены на всю ее длину - 10 см.
Диагноз после операции: ущемленная грыжа белой линии живота с ущемлением и некрозом предбрюшинной клетчатки.
Дальнейшее лечение в условиях экстренного хирургического отделения, коррекция лечения сопутствующей патологии, антибиотикопрофилактика средней продолжительности: цефазолин 2,0 г 2 раза в день внутримышечно в течение 3 суток.
В первые и третьи сутки послеоперационного периода был произведен забор крови в объеме по 400 мл и приготовлен раствор аутологичных цитокинов по вышеописанной методике.
Введение комплекса аутологичных цитокинов через установленные трубки производилось двукратно предложенным способом в первые и третьи сутки послеоперационного периода по 75 мл на каждое введение. Осложнений при введении не наблюдалось.
После операции общее состояние средней степени тяжести, субфебрилитет в первые трое суток после операции, максимальный подъем температуры тела до 37,3°С. Гиперлейкоцитоза и нейтрофильного палочкоядерного сдвига в общем анализе крови не наблюдалось, биохимические показатели в пределах нормы.
Течение послеоперационного периода благоприятное. Осложнений со стороны послеоперационной раны не наблюдалось, заживление раны первичным натяжением. Больная выписана на 9-е сутки после операции в удовлетворительном состоянии.
Клинический пример 2
Пациентка У. 54 лет (история болезни №3124) поступила в хирургическое отделение в экстренном порядке 21.07.2010 в 16:30 с диагнозом: ущемленная послеоперационная вентральная грыжа; сопутствующий: гипертоническая болезнь II стадии риск 4, ожирение 3 степени.
Грыженоситель в течение 12 лет. Грыжа сформировалась после операции верхне-срединной лапаротомии, холецистэктомии по поводу острого калькулезного холецистита. Ущемление в течение 20 часов.
Состояние средней степени тяжести, выраженный болевой синдром в области грыжевого выпячивания, также имеются боли в нижних отделах живота, температура 37,2°С, гемодинамика стабильная, тахикардии нет.
В общем анализе крови: лейкоциты 7,9·10%, палочкоядерные нейтрофилы - 10, сегментоядерные нейтрофилы - 49, моноциты - 5, лимфоциты - 18, показатели красной крови и тромбоциты в пределах нормы.
В биохимическом анализе крови все показатели в пределах нормы.
По ЭКГ: систолическая перегрузка левых отделов сердца, умеренные метаболические изменения миокарда.
После предоперационной подготовки, антибиотикопрофилактики внутривенным введением цефазолина 2,0 г внутривенно перед операцией, профилактики тромбоэмболических осложнений в экстренном порядке 21.07.2010 произведена операция: герниолапаротомия, резекция ущемленной некротизированной петли тонкой кишки с наложением энтеро-энтероанастомоза бок-в-бок, герниопластика грыжевых ворот с установкой сетчатого эндопротеза на апоневроз широких мышц живота, апоневроз под сетчатым эндопротезом ушит без натяжения. Размер установленного сетчатого эндопротеза составил 12×9 см - площадь 108 см2. Сетчатый эндопротез более длинной стороной расположен параллельно операционному доступу.
Интраоперационно в глубокий слой подкожно-жировой клетчатки над более коротким краем сетчатого эндопротеза через отдельные проколы кожи на расстоянии 3 см от углов сетчатого эндопротеза и параллельно доступу установлены трубки для проведения местной цитокиновой терапии. Трубки длиной 120 мм диаметром 1,0 мм с отверстиями диаметром 0,3 мм, расположенными на боковой поверхности через каждые 20 мм. Трубки ориентированы параллельно другой стороне эндопротеза и проведены на всю его длину 12 см.
Диагноз после операции: ущемленная послеоперационная вентральная грыжа с ущемлением и некрозом петли тонкой кишки.
Дальнейшее лечение в условиях экстренного хирургического отделения, антибиотикопрофилактика средней продолжительности: цефазолин 2,0 г 2 раза в день внутримышечно в течение 3 суток.
В первые и третьи сутки послеоперационного периода был произведен забор крови в объеме по 400 мл и приготовлен раствор аутологичных цитокинов по вышеописанной методике.
Введение комплекса аутологичных цитокинов через установленные трубки двукратно предложенным способом в первые и третьи сутки послеоперационного периода по 108 мл раствора на каждое введение. Осложнений при введении не наблюдалось.
После операции общее состояние средней степени тяжести, субфебрилитет в первые четверо суток после операции, максимальный подъем температуры тела до 37,8°С. Гиперлейкоцитоза в общем анализе крови не наблюдалось, палочкоядерный сдвиг на вторые сутки после операции - 10%, биохимические показатели в пределах нормы.
Течение послеоперационного периода благоприятное. Осложнений со стороны послеоперационной раны не наблюдалось, заживление раны первичным натяжением. Больная выписана на 11-е сутки после операции в удовлетворительном состоянии.
Таким образом, использование предложенного способа местной цитокиновой терапии в качестве способа профилактики развития раневых осложнений позволяет существенно повысить результаты лечения пациентов после герниопластики ущемленных вентральных грыж сетчатыми эндопротезами.
1. Способ профилактики раневых осложнений после протезирующей герниопластики при ущемленных вентральных грыжах, включающий установку эндопротеза и проведение антибиотикопрофилактики, отличающийся тем, что выполняют отдельные проколы кожи по обе стороны от доступа в проекции края сетчатого эндопротеза, которые располагают от угла сетчатого эндопротеза на расстоянии, равном 1/3 длины стороны, в проколы параллельно доступу в перипротезные ткани вводят полихлорвиниловые трубки с отверстиями, длина которых соответствует длине сетчатого эндопротеза, трубки располагают над плоскостью сетчатого эндопротеза; проводят иммунотерапию, для чего у пациента производят забор 400 мл крови в систему «Гемакон», разделяют полученную кровь центрифугированием в режиме 3700 об/мин в течение 20 мин на плазму, лейко-тромбоцитарную и эритроцитаную массы, эритроцитарную массу и плазму возвращают пациенту, в лейко-тромбоцитарную массу добавляют 200 мл 0,9%-ного раствора NaCl, повторяют цетрифугирование в том же режиме, удаляют надосадочный слой, лейко-тромбоцитарную массу культивируют с 500000 ME рекомбинантного интерлейкина-2 и 200 мл 0,9%-ного раствора NaCl в течение 60 мин при температуре 37°С, затем вновь центрифугируют в том же режиме с выделением надосадочной жидкости, содержащей комплекс аутологичных цитокинов, которую вводят в полихлорвиниловые трубки из расчета 1 мл на каждый см2 площади сетчатого эндопротеза в 1 и 3 сутки после операции, лейко-тромбоцитарную массу возвращают пациенту.
2. Способ профилактики раневых осложнений после протезирующей герниопластики при ущемленных вентральных грыжах по п.1, отличающийся тем, что используют полихлорвиниловые трубки диаметром 0,9-1,0 мм с отверстиями диаметром 0,3 мм, расположенными на боковой поверхности трубки через каждые 20 мм.