Индометацин на основе фосфолипидных наночастиц для применения в офтальмологии
Иллюстрации
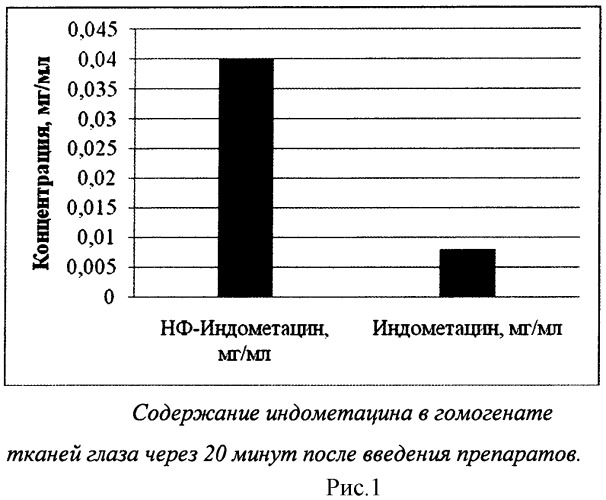
Показать всеИзобретение относится к области офтальмологии. Фармацевтическая композиция для применения в офтальмологии включает нестероидное противовоспалительное средство индометацин и фосфолипидное с размером наночастиц 10-30 нм - фосфатидилхолин растительного происхождения, мальтозу при следующем соотношении компонентов, мас.%: фосфатидилхолина 20-43, мальтозы 55-78, индометацина 2-8. Композиция на основе индометацина и фосфолипидов сои представляет собой лиофильно высушенный порошок. Изобретение обеспечивает стабильность композиции при длительном хранении. 2 ил., 1 пр.
Реферат
Изобретение относится к медицине и фармакологии и касается стабильной при хранении и эффективной по своему специфическому действию лекарственной композиции в виде наночастиц на основе растительных фосфолипидов, включающих противовоспалительный препарат индометацин.
Индометацин входит в группу нестероидных противовоспалительных средств и обладает также обезболивающим и жаропонижающим действием.
Механизм действия индометацина связан, в основном, с ингибированием биосинтеза ряда провоспалительных факторов, в том числе некоторых простагландинов, вызывающих в очаге воспаления развитие боли, повышение температуры и увеличение тканевой проницаемости.
Индометацин широко используется при острых и хронических артритах различного генеза, при спондилоартритах, артрозах, внесуставных ревматических заболеваниях мягких тканей (бурсит, миозит), а также при отеках и воспалениях после травм и оперативных вмешательств (общехирургических, гинекологических, стоматологических и др.). Выпускается индометацин в виде таблеток, растворов для внутривенного или внутримышечного введения, ректальных суппозиториев и в формах для наружного применения (мазь, гель), используемых для локального противовоспалительного воздействия.
Кроме того, индометацин выпускается в виде порошка для приготовления глазных капель (0,1%), также оказывающих противовоспалительное действие.
Критериями оценки эффективности новых создаваемых форм в условиях in vivo служит или внутриглазное накопление лекарства, или, в ряде случаев, измерение внутриглазного давления.
Для повышения биодоступности офтальмологических лекарств используются различные фармацевтические подходы, например использование микроэмульсий, наносуспензий, наночастиц, липосом, дендримеров, циклодекстринов.
Была показана способность наночастиц из поликапролактона взаимодействовать со слизистой оболочкой глаза, что стимулировало серию исследований в этой области, особенно в отношении противовоспалительных препаратов. Так, была показана способность наночастиц из хитозана, содержащих С14-индометацин или циклоспорин А, транспортировать лекарство в роговицу и водянистую влагу, что объясняли улучшенным взаимодействием и проникновением частиц в эпителий рогового слоя.
Для получения наночастиц использовали природные полимеры (альбумин, хитозан, желатин, производные крахмала или желатина) или биодеградируемые полимеры (полиалкил-цианоакрилаты, полиакрилаты). Например, включение тимолола в частицы на основе производного желатина повышало его биодоступность в водянистой влаге в 5.6 раза.
Включение тимолол-малеата в гель-образующую систему, основанную на плюронике F-127 (полиоксиэтилен+полиоксипропилен) резко повышало его окулярную биодоступность при введении кроликам - до 25% по сравнению с 2.5% для свободного лекарства.
Имеются сообщения о включении в лекарственные липидные наноформы и ряда других офтальмологических препаратов. Исследуются возможности применения для этих целей липосом, особенно содержащих положительный заряд, способствующего взаимодействию с роговицей. Например, включение в липосомы пенициллина G повышало в 4 раза его транспорт через роговой слой на изолированной роговице кролика.
Для доставки глюкокортикоидов используются наносуспензии, получаемые гомогенизацией под высоким давлением. При этом наибольший эффект такой формы при введении кроликам достигался при снижении размера частиц.
Разрабатывается также доставка дексаметазона через полиоксиэтилметакрилатный гель, используя его в сочетании с контактными линзами.
В последние годы появились данные об использовании для глазных капель и гелей липидных форм - твердых липидных наночастиц (SLN) и т.н. наноструктурных липидных носителей (NLC), получаемых путем смешивания твердых и жидких липидов, при специально разрабатываемых соотношениях и технологических условиях. Используют комбинации таких частиц с неионными сурфактантами, называемые рядом авторов как «ниосомы» или «десмосомы». Липидные наноформы способствуют также солюбилизации липофильных лекарств. Например, твердые липидные наночастицы использовали для загрузки тобрамицином. Для глазных капель препараты подобных частиц с включаемым лекарством приготовляют в форме наноэмульсий. При включении индометацина в наноэмульсии наблюдали большее проникновение в роговицу по сравнению с его коммерческой формой, особенно для положительно заряженных частиц.
Фосфолипидные наночастицы - лиотропные жидкие кристаллы, химическая структура которых позволяет использовать их в качестве переносчиков как для растворимых, так и для нерастворимых в биологических жидкостях лекарственных препаратов. Встраивание лекарственных соединений в фосфолипидные наночастицы позволяет получить новые формы лекарственных препаратов с высокой эффективностью, биодоступностью и сниженными побочными действиями.
Эффективность композиций лекарственных средств на основе фосфолипидных наночастиц определяется в основном их размерами - менее 100 нм, что обеспечивает большую «рабочую поверхность» частицы и за счет этого способствует увеличению их «емкости» для встраивания лекарственных веществ. Увеличение эффективной площади поверхности в сочетании с наноразмерами создает оптимальные условия для взаимодействия таких частиц с клеткой. По сравнению с липосомами диаметром 250-400 нм при средних размерах клетки 1-5 микрон одновременно возможно единичное количество точек контакта с клеткой. Для наночастиц диаметром 10-30 нм эта величина значительно выше, что, соответственно, повышает вероятности их эндоцитоза. Кроме того, для таких частиц возникает уникальная возможность внедрения в область межклеточных контактов, ширина которых в некоторых участках может достигать 50 нм. Таким образом, появляется возможность доставки биологически активных субстанций к недоступным для других лекарственных форм участкам пораженной ткани.
Известна фосфолипидная транспортная наносистема с размером частиц до 30 нм и показана возможность включения в нее лекарственных соединений разного химического строения (Патент РФ 2373924). Было разработано несколько новых лекарственных композиций пероральной и инъекционной форм и в экспериментах in vivo доказана их высокая биодоступность и специфическая терапевтическая активность по сравнению с исходными субстанциями.
Таким образом, представляется целесообразным использование известных лекарственных субстанций, встроенных в фосфолипидные наночастицы размером меньше 30 нм в решении вопросов контролируемой доставки лекарственных препаратов для использования в офтальмологии. Благодаря развитию нанотехнологий современные подходы позволяют получать фосфолипидные наночастицы столь малого размера. Один из факторов, определяющих растущий интерес к реализации этого направления в фармацевтической промышленности - возможность получения стабильных наночастиц с включенными лекарственными субстанциями, за счет чего у препарата появляется ряд дополнительных положительных свойств: эффект пассивного нацеливания; улучшенная биодоступность, устойчивость к преждевременной деградации; способность проникать через клеточную мембрану и т.д.
Целью изобретения является получение лекарственной композиции на основе индометацина включенного в фосфолипидные наночастицы для применения в офтальмологии.
Состав на один флакон:
| Фосфолипида | 500 мг |
| Индометацина | 25 мг |
| Мальтозы | 1975 мг |
| Воды для инъекций | 10 мл |
Способ получения лекарственной композиции характеризуется следующим
примером:
Пример 1.
А. 25 мг индометацина растворяют в 50 мл медицинского спирта при нагревании. К полученному раствору при интенсивном перемешивании прибавляют 250 мг фосфолипида и доводят до полного растворения.
Полученный раствор переносят в круглодонную колбу объемом 0,5 л и упаривают на роторном испарителе при поддержании температуры водяной бани и вакуума на уровне, не допускающем интенсивное кипение. После упаривания полученную пленку собирают с колбы и взвешивают.
Б. Навеску мальтозы 500 мг растворяют в 150 мл деионизированной воды, к полученному раствору добавляют пленку, полученную на этапе А и 250 мг фосфолипида. Проводят первичную гомогенизацию смеси и доводят ее объем до 7,4 мл.
Смесь, полученную на стадии первичной гомогенизации, подвергают гомогенизации высокого давления до достижения узкого распределения частиц по размерам (IP 0,2-0,3).
В. Навеску мальтозы 1475 мг растворяют в 1,7 мл воды.
Г. Растворы, полученные на этапах Б и В фильтруют через фильтры 0,22 мкм и затем смешивают, путем постепенного вливания раствора мальтозы в раствор фосфолипидных наночастиц. Полученный раствор разливают по флаконам объемом 10 мл и высушивают в лиофильной сушке.
Для изучения фармакокинетики фосфолипидной лекарственной композиции в экспериментах in vivo в качестве экспериментальных животных использовались крысы породы Wistar, содержащиеся в стандартных условиях и на стандартной диете, весом 300-400 г.
Изучение лекарственной композиции в экспериментах in vitro и in vivo
Изучение биодоступности лекарственной композиции на основе фосфолипидных наночастиц проводили в сравнении со свободной лекарственной субстанцией индометацина. Введение препаратов осуществляли путем закапывания 25 мкл исследуемого препарата.
Схема эксперимента.
1. В правый глаз закапывали лекарственную композицию, полученную способом, описанным в примере 1 (НФ-Индометацин).
2. В левый глаз-контроль.
Приготовление контрольного раствора.
Навеску индометацина 0,025 г суспендируют в 10 мл воды на ультразвуковой бане в течение 40 минут до образования тонкой суспензии. К 10 мл полученной суспензии добавляют 1 г мальтозы, тщательно перемешивают на магнитной мешалке.
3. Через 20 минут осуществляют забор глаза. Для этого производят круговой разрез конъюнктивы, конъюнктиву сепарируют от склеры, накладывают зажим на зрительный нерв, центральные артерию и вену сетчатки, глазное яблоко подтягивают, ножницами пересекают зрительный нерв и сосуды.
4. После декапитации глаза его измельчают. К навеске ткани добавляют метанол из расчета на 100 мг ткани 900 мкл растворителя и гомогенизируют до однородного состояния. Далее к 180 мкл гомогената добавляют 20 мкл раствора диклофенака натрия в метаноле с концентрацией 5000 нг/мл и интенсивно перемешивают. Гомогенат центрифугируют в течение 7 минут при 13000 об/мин. Супернатант отбирают и используют для анализа. Полученные образцы анализируют с помощью ВЭЖХ/МС для определения в них лекарственной субстанции.
На рисунке 1 показано, что через 20 минут после введения препаратов (индометацина в составе фосфолипидных наночастиц - НФ индометацина и свободного индометацина) содержание НФ индометацина в гомогенате тканей глаза было более чем в 7 раз выше.
Для изучения специфической активности разработанной лекарственной композиции был выбрана модель неиммуногенного увеита. В качестве экспериментальных животных были взяты здоровые кролики альбиносы, самцы, весом 1,5-2 кг.
Изучение специфической активности лекарственной композиции на основе фосфолипидных наночастиц (условное название НФ-Индометацин) проводили с препаратом сравнения - лекарственной субстанцией индометацина (Индометацин).
Для постановки этой модели кроликам подкожно вводили 5 мл альбумина бычьей сыворотки, а затем, на 9-й день, вводили 10 мкл альбумина бычьей сыворотки (25 мкг/мл) интравитреально.
Закапывание исследуемого препарата и препарата сравнения производили в количестве 100 мкл четырехкратно с интервалом 1, 5 часа, в течение 12 дней.
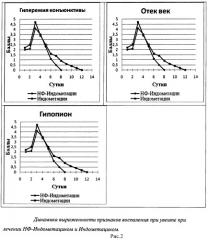
Клиническую оценку течения воспалительного процесса глаз кроликов проводили визуально. Клинические проявления воспаления регистрировали на 1-10 сутки (после введения альбумина бычьей сыворотки) в условных баллах по следующим признакам: гиперемия конъюнктивы, отек век, количество гипопиона (рис.2).
Из рисунка 2 видно, что при лечении лекарственной композиций НФ Индометацин уменьшение признаков воспаления происходило на 5-6 сутки после введения и полное выздоровление животных наблюдалось на 8 сутки, в то время как при лечении Индометацином уменьшение признаков воспаления наблюдалось на 9 сутки и полное выздоровление на 12 сутки.
Фармацевтическая композиция для применения в офтальмологии на основе индометацина и фосфолипидных наночастиц размером 10-30 нм, включающая 78-95%-ный фосфатидилхолин растительного происхождения, мальтозу и индометацин при следующем соотношении компонентов, мас.%:
| Фосфатидилхолин | 20-43 |
| Мальтоза | 55-78 |
| Индометацин | 2-8 |