Гидратированные n-фуллерен-аминокислоты, способ их получения и фармацевтические композиции на их основе
Иллюстрации
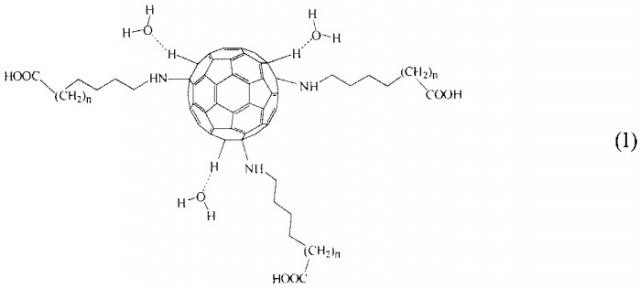
Показать всеИзобретение относится к новым гидратированным N-фуллерен-аминокислотам общей формулы
C60(Н)3{NH(СН2)nCOOH}3·xH2O, где С60 представляет фуллерен, n=5-7, x=8-10, которые обладают активностью против вируса герпеса, вирусов гриппа различной природы, ВИЧ, а также противоопухолевой и противопсориатической активностью. Изобретение относится также к способу получения указанных фуллеренаминокислот и фармацевтическим композициям на их основе. 3 н. и 2 з.п. ф-лы, 28 табл., 10 пр.
Реферат
Изобретение относится к фармацевтической промышленности и медицине и касается новых гидратированных аминокислотных производных фуллерена С60 формулы (I), а также способа их получения и создания фармацевтических композиций на их основе.
Возможность использования фуллеренов как биологически активных соединений вызвало интенсивное развитие химии функциональных производных фуллерена, особенно после того, как было показано, что ряд водорастворимых производных фуллерена проявляют высокую антивирусную активность (Partha R, Conyers JL, "Biomedical applications of functionalized fullerene-based nanomaterials" Int. J. Nanomedicine, 2009, 4, 261-75 Pat US 6204391, 2005, "Water soluble fullerenes with antiviral activity", R.Bakry et al., "Medicinal application of fullerenes" International Journal of Nanomedecine, 2007 (4) 639-649, Z.Zhu, D.I.Schuster, M.Tuckermann, "Molecular Dynamics Study of the Connection between Flap Closing and Binding of Fulleren-Based Inhibitors of the HIV-1 Protease", Biochemistry, 2003, v.42, 1326-1333).
Применение производных фуллерена в медицине основано на липофильных свойствах фуллеренового ядра, позволяющих фуллереновым производным проникать через клеточные мембраны, и способности фуллерена с высоким квантовым выходом генерировать синглетный кислород, расщепляющий ДНК. Эти свойства обеспечивают функциональным производным фуллерена проявление цитотоксических, антивирусных и других свойств (Bedrov D., Smith G.D., Davande Н., "Passive transport of fullerenes through a lipid membrane." J. Phys. Chem., B, 2008, v.112., p.2078-84, Qiao R., Roberts A.E., "Translocation of fullerene and its derivatives across a lipid bilayer", Nano Lett., 2007, v.7, p.614-9. Nelsen G.D., и др., "In vivo biology and toxicology of fullerenes and their derivatives", Basic and Clinical Pharmacology and Toxicology, 2008, v.103, p.197-208).
Гидратированные формы фуллерена проявляют высокую биологическую активность как биоантиоксиданты, что обусловлено образованием активных структурных форм водных кластеров, координированных на сфере фуллерена (Andrievsky G.V., Brushkov V.I., Tykhonov А.А., Gudkov S.V. "Peculiarities of the antioxidant and radioprotective effects of hydrated C60 fullerene nanostructures in vitro and in vivo". Free Radical Biology and Medicine, 2009, v.47, p.786-793).
Основной проблемой, затрудняющей биологические исследования фуллеренов и их производных и создание лечебных препаратов на их основе, является сложность введения фуллереновых систем в водные растворы.
Перспективным методом получения водорастворимых фуллереновых композиций является химическая модификация сферы фуллерена введением гидрофильных солюбилизирующих лигандов. В настоящее время получен большой ряд функционализированных фуллеренов, содержащих гидрофильные фрагменты как в боковой цепи присоединенных к фуллерену лигандов (детергентный тип комплексов), так и сферический тип производных, когда имеются полярные группы, распределенные по фуллереновой сфере (такой тип включает фуллеренолы, аминоаддукты).
Наиболее перспективными для использования являются аминокислотные производные фуллерена.
Неприродные аминокислоты алифатического ряда, содержащие 6 и более метиленовых групп, проявляют ряд особенностей, проявляющихся в процессах их гидратации и их биохимической активности. Спектральные исследования структуры воды в водных растворах аминокислот показывают, что увеличение числа метиленовых групп между амино- и карбоксильной группами приводит к увеличению деструкции водных кластеров. Исследования фармакологических свойств производных аминокислот широкого ряда R-(СН)nCOOH показали более высокую активность систем с n больше и равным 6.
Производные фуллерена С60 с аминокислотами сферического типа, полученные по реакции нуклеофильного присоединения аминокислот по аминогруппе к сфере фуллерена описаны в патентах РФ №№2196602, 2124022, 2236852, которые можно предложить в качестве аналогов настоящего изобретения.
В патенте РФ №2196602 предложен способ ингибирования репродукции ВИЧ и ЦМВ-инфекций при помощи соединений на основе аминокислотных и дипептидных производных фуллерена. В качестве аминокислотного производного фуллерена использованы натриевые соли фуллерен-аминокапроновой и фуллерен-аминомасляной кислот.
В патенте РФ №2124022 для получения фуллерен-аминокапроновой кислоты к раствору фуллерена в о-дихлорбензоле добавляют водный раствор калиевой соли аминокапроновой кислоты и 18-краун-6. Реакционную массу перемешивают 6-8 часов при 60°С. Затем растворители отгоняют, остаток обрабатывают насыщенным раствором хлористого калия и остаток фуллеренового производного промывают водой. Выход целевого продукта количественный. Полученная (моногидро)N-фуллерен-аминокапроновая кислота растворима в диметилсульфоксиде, диметилформамиде, пиридине. В заявленном методе синтеза не определены условия выделения конечного продукта.
Основным недостатком полученных соединений, которые представляют собой продукты моноприсоединения, является их нерастворимость в воде. Другим недостатком изобретения является использование в их синтезе краун-эфира в качестве межфазного катализатора, который сложно отделять от получаемых продуктов реакции.
В патенте РФ №2236852 защищается средство для ингибирования репродукции оболочечных вирусов, представляющее собой фуллеренполикарбоновые анионы общей формулы C60Hn[NH(СН2)mC(O)O-]n, полученные в результате взаимодействия фуллерена с солью аминокислоты в среде органического растворителя в присутствии полиалкиленоксида.
Для получения этих соединений к раствору фуллерена в о-дихлорбензоле (толуоле или любом другом органическом растворителе) вносят аминокислоту в виде соли (калиевой или натриевой), затем добавляют солюбилизатор. Порядок внесения в реакционную среду аминокислоты и солюбилизатора не важен, можно вносить их в виде комплекса, предварительно смешав. В качестве солюбилизатора используют различные полиалкиленоксиды: полиэтиленгликоли мол. массы от 150 до 400 и выше 400 (например, ПЭГ-1500), а также полиэтиленгликоли, имеющие свободные концевые группы, но и с замещенными (например, диметиловый эфир полиэтиленгликоля мол. массы 500). Для увеличения скорости реакции добавляют любой сильный восстановитель (щелочные металлы). Соотношение фуллерена и аминокислоты увеличено более чем в 50 раз. Превращение в желаемую фармацевтически приемлемую соль, особенно натриевую или калиевую, выполнялась путем обработки кислоты подходящим основанием или путем добавления соли слабой летучей кислоты. В частности, не растворимая в воде фуллеренполикарбоновая кислота превращается в более предпочтительные фармацевтически приемлемые соли, такие как натриевая соль, которые растворимы в воде. Добавление соли слабой летучей кислоты происходит путем обработки раствора солью щелочного металла и слабой летучей кислоты. При концентрировании раствора путем выпаривания или лиофилизации слабая кислота удаляется, а смесь фуллеренполикарбоновых кислот выделяется в виде смесей их солей щелочных металлов. Целевой продукт по данному изобретению характеризуется постоянством состава, содержание в целевом продукте основного вещества составляет всего 87,8%.
Основными недостатками фуллерен-аминокислотных производных, полученных представленным в патенте методом получения, является то, что данным способом получают смесь фуллеренкарбоксилатных анионов как солевых, так и кислотных форм. Получить индивидуальное соединение способом, описанным в патенте, не представляется возможным. Также фуллеренполиаминокислоты, полученные запатентованным способом, в кислотной форме практически нерастворимы в воде. Получить стабильную фармацевтическую композицию с фуллеренполикарбоновыми анионами не удалось, т.к. в процессе хранения соединения выпадают в осадок. Фуллеренполиаминокислоты оказывают влияние на лейкопоэз: вызывают сдвиг лейкоцитарной формулы и индуцируют появление молодых форм нейтрофилов - нейтрофильных метамиелоцитов у подопытных животных (крыс и кроликов). С точки зрения безопасности (безвредности) это свидетельствует о наличии у данных субстанций токсичности, вызывающей указанные изменения. Применение в синтезе большого избытка калиевой или натриевой солей аминокислот и больших избытков растворителей приводит к возникновению экологических проблем, связанных с утилизацией отходов производства, а также к удорожанию процесса производства. Использование щелочных металлов для увеличения скорости реакции является технологически невозможным при использовании хлорированных ароматических растворителей.
Задачей заявляемого технического решения является получение индивидуальных гидратированных соединений фуллерена С60 с аминокарбоновыми кислотами, обладающих активностью против вируса герпеса, вируса гепатита С, вирусов гриппа различной природы, ВИЧ, а также противоопухолевой и противопсориатической активностью, не оказывающих токсического действия на организм; способ получения данных соединений и фармацевтические композиции, включающие данные соединения.
Для решения поставленной задачи предложена группа изобретений, объединенных единым изобретательским замыслом: соединение, способ его получения и фармацевтические композиции, содержащие указанное соединение.
Поставленная задача решается индивидуальным гидратированным соединением фуллерена С60 с аминокарбоновыми кислотами общей формулы (II), характеризующееся тем, что на одну молекулу фуллерена приходится три ковалентно связанных аминокислотных фрагмента, имеющих в своей структуре активные центры гидратации, приводящие к образованию водорастворимых гидратов, и длинные углеводородные цепи, позволяющие удерживать молекулы воды во внутренней координационной сфере фуллереновых комплексов.
Указанная задача решается тем, что гидратированные фуллереновые производные аминокислот формулы (II) образуются при взаимодействии фуллерена с 15-кратным мольным избытком безводных калиевых солей аминокислот в среде органического ароматического растворителя при медленном добавлении к полученной суспензии межфазного катализатора при перемешивании и нагревании до температуры не выше 60-80°С до полного обесцвечивания раствора и формирования твердого осадка, который затем выделяют, после чего осуществляют обработку 0,8 М водных растворов калиевых солей фуллерен-аминокислот 0,1 Н раствором органических или минеральных кислот с последующим центрифугированием, промывкой и высушиванием осадка.
Также согласно изобретению безводные калиевые соли аминокислот используют в мелкодисперсном состоянии, что позволяет повысить реакционную способность процесса, его эффективность и экономичность, а выделение твердого осадка калиевых солей фуллерен-аминокислот осуществляют фильтрованием, промывкой этиловым спиртом и высушиванием. В качестве межфазного катализатора используют метиловые эфиры полиэтиленоксидов молекулярной массы 200, 400, 500 как наиболее доступные и безопасные катализаторы.
Указанная задача решается также созданием фармацевтических композиций, содержащих в качестве активного вещества водорастворимые гидратированные фуллерен-аминокислоты формулы (II), обладающих активностью против вируса герпеса, вируса гепатита С, вирусов гриппа различной природы, ВИЧ, а также противоопухолевой и противопсориатической активностью.
Фармацевтические композиции по предложенному техническому решению содержат соединение общей формулы (II) в количестве, эффективном для достижения желаемого результата, и могут быть введены в виде стандартных лекарственных форм (например, в твердой, полутвердой или жидкой формах), содержащих соединения предложенного технического решения в качестве активного ингредиента в смеси с носителем или наполнителем, пригодным для внутримышечного, внутривенного, перорального, сублингвального, ингаляционного, местного, интраназального и интраректального введения. Активный ингредиент может быть включен в композицию вместе с обычно используемыми нетоксичными фармацевтически приемлемыми носителями, пригодными для изготовления растворов, таблеток, пилюль, капсул, драже, суппозиториев, эмульсий, суспензий, мазей, гелей и любых других лекарственных форм.
Конкретный уровень дозировок и частота приема лекарства для каждого конкретного пациента будет зависеть от большого числа факторов, включая активность конкретного производного фуллерена, метаболическую стабильность и длительность действия, скорость выделения, возраст пациента, вес тела, общее состояние здоровья, пол, лекарственные комбинации, а также тяжесть заболевания у данного индивида, подвергаемого лечению.
Для орального применения в виде суспензий композиции готовят согласно методам, широко известным в области приготовления фармацевтических рецептур, и они могут содержать микрокристаллическую целлюлозу или ее производные для обеспечения массы, альгиновую кислоту или альгинат натрия в качестве суспендирующего агента, метилцеллюлозу в качестве усилителя вязкости и подслащивающие агенты и/или отдушки, известные в этой области. В форме таблеток такие композиции могут содержать микрокристаллическую целлюлозу, кальций фосфат, крахмал, стеарат магния и лактозу и/или другие эксципиенты, связующие вещества, расширители, дезинтеграторы, разбавители и смазывающие вещества, известные в данной области.
При применении в виде назальных аэрозолей или путем ингаляции такие композиции готовят методами, хорошо известными в области фармацевтических рецептур, и они могут выпускаться в виде растворов на физиологическом растворе с использованием бензойной кислоты или других подходящих консервантов, промоторов адсорбции для усиления биоприменимости и/или других солюбилизирующих или диспергирующих агентов, известных в данной области.
Растворы или суспензии для инъекций могут формироваться согласно известным методам с использованием нетоксичных, парентерально применимых разбавителей или растворителей, таких как маннит, 1,3-бутандиол, вода, раствор Рингера или изотонический раствор хлористого натрия или подходящих диспергирующих или смачивающих и суспендирующих агентов, таких как стерильные мягкие устойчивые масла, включая синтетические моно- или диглицериды, или жирные кислоты, включая олеиновую кислоту.
При ректальном применении в виде свечей такие композиции могут готовиться путем смешивания лекарства с таким нераздражающим эксципиентом, как масло какао, синтетические глицеридные сложные эфиры или полиэтиленгликоли, которые являются твердыми веществами при обычных температурах, но сжижаются и/или растворяются в ректальной полости с выделением лекарства.
При местном применении в виде мазей, гелей, кремов, линиментов и т.д. такие композиции могут готовиться путем смешивания активных ингредиентов с приемлемой мазевой основой.
В качестве мазевой основы могут быть использованы жировые, углеводородные или гидрофильные основы, например вазелин, вазелиновое масло, парафин, воск, ланолин, полиэтиленгликоль и др.
В качестве основы для гелей могут быть использованы метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы, оксипропилцеллюлоза, полиэтиленгликоль или полиэтиленоксид, карбопол, поливинилпирролидон, поливиниловый спирт и т.д.
Предложенное изобретение касается соединений, способа получения этих соединений и их фармацевтически приемлемых ассоциатов с полярными реагентами. Полученные соединения не оказывают влияния на лейкопоэз: не вызывают сдвига лейкоцитарной формулы и не индуцируют появление молодых форм нейтрофилов - нейтрофильных метамиелоцитов у подопытных животных (крыс и кроликов). С точки зрения безопасности (безвредности) это свидетельствует об отсутствии у данных соединений токсичности, вызывающей указанные изменения. Заявляемый способ позволяет получить различные по составу композиции на основе фуллерен-аминокислот в зависимости от соотношения реагентов и условий проведения процесса, а именно: водорастворимые гидратированные фуллерен-аминокислоты общей формулы (II).
Способ основан на использовании в стадии синтеза оптимальных соотношений исходных реагентов, минимальных количеств органического растворителя и межфазного катализатора с последующем выделением заявляемых соединений с использованием концентрированных растворов органических и минеральных кислот, что приводит к количественному получению фуллерен-аминокислотных композиций определенного состава и возможности применения заявляемого способа для их промышленного синтеза, отличающегося эффективностью и экологичностью.
Технический результат предлагаемого технического решения состоит в получении устойчивых индивидуальных водорастворимых гидратированных соединений фуллерена С60 с аминокарбоновыми кислотами, не оказывающих токсического воздействия на организм. Разработан эффективный способ получения индивидуальных устойчивых гидратированных производных фуллерена, обладающих противовирусной, противоопухолевой и противопсориатической активностью.
Заявляемое изобретение иллюстрируется следующими примерами.
Пример 1. Получение гидрата N-фуллерен-(трис-ε-аминокапроновой кислоты) (по номенклатуре ИЮПАК - гидрат N-фуллерен-(трис-6-аминогексановой кислоты) формулы: N-C60{NH(CH2)5COOH}3·10H2O.
К раствору 60 г (0,08 моля) фуллерена С60 в 4,5 л о-дихлорбензола добавляют 204 г (1,2 молей) тонкоизмельченной безводной калийной соли ε-аминокапроновой кислоты. К полученной суспензии при перемешивании и нагревании не выше 60°С прибавляют в течение 2-х часов смесь о-дихлобензола и метилового эфира полиэтиленгликоля 500 в соотношении 5:1. Реакционную смесь перемешивают при температуре не выше 60°С в течение 5 часов до полного обесцвечивания раствора и формирования твердого осадка. Затем смесь фильтруют, осадок на фильтре промывают несколькими порциями этилового спирта и высушивают в вакууме при температуре не выше 60°С. Выделенную смесь калиевых солей фуллерен-аминогексановой кислоты и аминогексановой кислоты растворяют в 100 л дистиллированной воды. В раствор медленно при перемешивании добавляют 0,1 Н раствор соляной кислоты до рН 5,1. Смесь отстаивают до полного высаживания продукта, Затем водный слой декантируют. Осадок, представляющий собой тонкую взвесь твердого продукта в воде, центрифугируют и промывают водой до рН 6. Осадок высушивают при температуре не выше 60°С в вакуумном сушильном шкафу.
Выход продукта количественный и составляет 115 г.
Соединение представляет собой темно-коричневое твердое вещество, растворимое в воде, растворимое в смесях CH3CN:H2O - 1:10 и ДМФА:H2O - 1:100.
По данным термогравиметрического анализа полученное соединение содержит 10 молей H2O. При температуре 350°С происходит интенсивное разрушение комплекса. Остаток после разложения содержит фуллерен и продукты его окисления.
ИК-спектр продукта (I) содержит полосы поглощения, характерные для N-замещенных аминокислот: группа -СООН- 1704 см-1, 1658 см-1, N-H-валентные колебания 3400 см-1, N-Н-деформационные - 1552 см-1, полосы поглощения C60-NH-R- 1104 см-1, 930 см-1, 830 см-1.
Электронный спектр поглощения не содержит полос поглощения свободного фуллерена.
Элементный анализ соединения показывает следующие соотношения элементов: % С=72,75; % Н=4,70; % N=2,32; рассчитано для брутто-формулы C78H39O6N310H2O: % С=72,38, % Н=4,3, % N=3,24.
Количество карбоксильных групп в продукте определялось по реакциям с солями металлов и аминами. По реакции с азотнокислым серебром количественно выделен комплекс состава C60(H)3{NH(CH2)5COOAg}310H2O. (Найдено: % Ag=20,88, % C=57,80, % N=2,51, % Н=3,32; рассчитано для: C78H36O6N3Ag3(10H2O) - % Ag=20,00, % C=57,88, % N=2,60, % Н=3,46).
По реакции с трисамином получен водорастворимый комплекс состава C60(H)3{NH(CH2)nCOO-NH3 +C(CH2OH)3}3 (найдено % C=64,88, % Н=4,56, % N=5,08, рассчитано для C90H72O15N610H2O: % С=65,2, % Н=4,34, % N=5,10).
Пример 2. Получение гидрата N-фуллерен-(трис-ω-аминоэнантовой кислоты) (по номенклатуре ИЮПАК - гидрат N-фуллерен-(трис-7-аминогептановой кислоты) формулы: N-C60(H)3{NH(CH2)6COOH}3·8H2O.
К раствору 72 г (0,1 моля) фуллерена С60 в 4 л о-дихлорбензола добавляют 182 г (1,2 молей) тонкоизмельченной безводной калийной соли ω-аминоэнантовой кислоты. К полученной суспензии при перемешивании и нагревании не выше 80°С прибавляют в течение 3-х часов смесь о-дихлобензола и метилового эфира полиэтиленгликоля 500 в соотношении 5:1. Реакционную смесь перемешивают при температуре не выше 80°С в течение 8 часов до полного обесцвечивания раствора и формирования твердого осадка. Затем смесь фильтруют, осадок на фильтре промывают несколькими порциями этилового спирта и высушивают в вакууме при температуре не выше 60°С. Выделенную смесь калиевых солей фуллерен-аминоэнантовой и аминоэнантовой кислот растворяют в 120 л дистиллированной воды. В раствор медленно при перемешивании добавляют 0,1 Н раствор соляной кислоты до рН 5,1. Смесь отстаивают до полного высаживания продукта, затем водный слой декантируют. Осадок, представляющий собой тонкую взвесь твердого продукта в воде, центрифугируют и промывают водой до рН 6. Осадок высушивают при температуре не выше 60°С в вакуумном сушильном шкафу.
Выход продукта количественный и составляет 130 г.
Соединение представляет собой темно-коричневое твердое вещество, растворимое в воде, растворимое в смесях CH3CN:H2O - 1:10 и ДМФА:H2O - 1:100.
По данным термогравиметрического анализа полученное соединение содержит 8 молей H2O. При температуре 450°С происходит интенсивное разрушение комплекса. Остаток после разложения содержит фуллерен и продукты его окисления.
ИК-спектр продукта содержит полосы поглощения, характерные для N-замещенных аминокислот: группа -СООН- 1707 см-1 1650 см-1, N-H-вал. колебания - 3400 см-1, N-H-деформационные - 1552 см-1, полосы поглощения С60-NH-R- 1104 см-1, 930 см-1, 830 см-1.
Электронный спектр поглощения содержит полосу поглощения при 260 нм.
Элементный анализ продукта показывает следующие соотношения элементов: % C=73,55; % Н=4,60; % N=3,18; рассчитанные значения для брутто-формулы C81H45O6N3(8H2O) - % С=74,82, % Н=4,69, % N=3,23.
По реакции с азотнокислым серебром выделена серебряная соль фуллерен-аминокислоты, количественно доказывающая наличие трех аминокислотных фрагментов в составе полученного продукта.
Пример 3. Получение гидрата N-фуллерен-(трис-8-аминооктановой кислоты) формулы: N-C60(H)3{NH(CH2)7COOH}3·10H2O.
Проводят аналогично примеру 1 только вместо тонкоизмельченной безводной калийной соли ε-аминокапроновой кислоты (ω-аминоэнантовой кислоты) используют калиевую соль аминооктановой кислоты. Анализ полученного соединения доказывает представляемый состав комплекса.
Была изучена противовирусная активность соединения в отношении ВИЧ, ВПГ, вируса гриппа, а также противоопухолевая активность. Соединение обладает высокой противоопухолевой и противовирусной активностью в отношении всех названных вирусов. Ниже приведены лучшие примеры осуществления изобретения. В приведенных ниже примерах соединение, полученное способом, описанным в примере 1, названо по тексту препарат №1 (фуллерен-трис-аминокапроновой кислоты гидрат).
Пример 4. Изучение активности фуллерен-трис-аминокапроновой кислоты в отношении вируса иммунодефицита человека.
Исследования проводились в ГУ НИИ вирусологии им. Д.И.Ивановского РАМН, г.Москва. В задачу исследований входило изучение активности препарата в отношении вируса иммунодефицита человека.
К клеткам добавляли исследуемый препарат и инфицировали вирусом в дозе 0,01 ТЦИД50/клетка. Инкубировали культуры клеток при 37°С в атмосфере с 5% CO2 и 98%
влажности 4-5 дней. Учет результатов проводили окрашиванием клеток с помощью красителя и световой микроскопии: исследование цитопатического эффекта вируса (ЦПД) и вирусиндуцируемого синцитийобразования (синцитий - конгломерат нескольких клеток с общей клеточной оболочкой, образовавшейся в результате слияния их мембран).
Степень цитодеструкции оценивали под микроскопом по общепринятой четырехкрестовой системе знаками + или - соответственно количеству погибших клеток в каждой из четырех лунок, соответствующих одному исследуемому показателю.
++++ - 100%ая гибель клеток в четырех лунках, использованных в опыте на одно разведение
+++ - 75%ая гибель клеток в каждой из четырех лунок,
++ - 50%ая гибель клеток в каждой из четырех лунок,
+ - 25%ая гибель клеток в каждой из четырех лунок,
+- - начало дегенерации,
- отсутствие цитодеструкции.
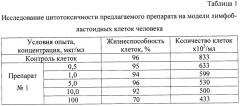
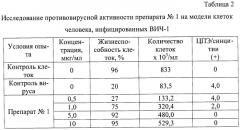
Результаты исследования представлены в таблицах 1-2.
Полученные данные (таблица 1, 2) показали, что препарат №1 обладает противовирусной активностью в отношении вируса иммунодефицита человека типа 1 в концентрации 1-10 мкг/мл. ЭК50 (50%-эффективная концентрация) предлагаемого препарата 5,0 мкг/мл.
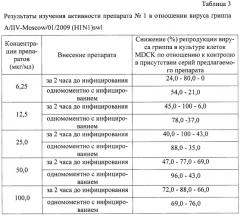
Пример 5. Изучение активности фуллерен-трис-аминокапроновой кислоты в отношении вируса гриппа.
Исследования проводились в ГУ НИИ вирусологии им. Д.И.Ивановского РАМН, г.Москва. В задачу исследований входило изучение противовирусной активности препарата в культуре клеток MDCK в отношении вируса гриппа A/IIV-Moscow/01/2009 (H1N1)sw1.
Препарат разводили в диметилсульфоксиде (ДМСО) (5 мг субстанции + 0,5 мл ДМСО) с последующим добавлением 4,5 мл среды для культур клеток MEM, получая т.о. сток в концентрации 1,0 мг/мл. В последующем проводили разведения стоков средой MEM до рабочих концентраций 6,5 мкг/мл - 12,5 - 25,0 - 50,0 - 100 мкг/мл.
Определение противовирусной активности вещества проводили по снижению репродукции вируса гриппа в культуре клеток MDCK, выявляемой ИФА.
С этой целью клетки МДСК выращивали в 96-луночных планшетах до полного монослоя, отмывали от ростовой среды и вносили вещества в двукратной концентрации в 100 мкл среды MEM. Инфицирование вирусом в рабочей дозе 100-1000 ТЦИД50 проводили в двух режимах: через 2 часа после внесения веществ и одномоментно. Планшеты инкубировали в термостате с СО2 в течение 24 часов при 37°С. После инкубации среду удаляли и клетки фиксировали 80% ацетоном в PBS в течение 15 минут, хорошо высушивали и осуществляли постановку ИФА, проводя последовательно адсорбцию специфических реагентов - моноклональных антител, конъюгата и субстрата (ортофенилендиамин). Реакцию учитывали по оптической плотности при 492 нМ на спектрофотометре фирмы «Биоком». Каждое разведения вируса исследовали в 3-х повторах, для которых вычисляли среднее значение оптической плотности (ОП). Процент ингибирования определяли как отношение между разницей ОП опыта и ОП клеточного контроля, деленное на разницу ОП вирусного контроля и ОП клеточного контроля, умноженное на 100%. На основании полученных данных определены значения минимальной концентрации вещества, вызывающей 50,0% ингибирование вирусной репродукции (МИК50).
Оценку подавления репродукции вируса гриппа A(H1N1) проводили в 3-х опытах при разной множественности заражения. Результаты представлены в табл.3 (протоколы 3-х опытов) и табл.4 (средние значения полученных результатов 3-х опытов).
Как видно из таблицы 4, наибольшую активность по снижению репродукции вируса гриппа в культуре клеток MDCK проявила серия препарата 1. Четко прослеживается зависимость степени репродукции и концентрации препарата: с повышением концентрации снижается репродукция вируса. Кроме того, значительных отличий в показателях при разных режимах инфицирования (через 2 часа после внесения препарата или одномоментно) не отмечено. При этом показатели минимальной ингибирующей репродукцию вируса в 2 раза концентрации (МИК50), составили: в режиме внесения препарата за 2 часа - 9,5 мкг/мл и при одномоментном внесении - 12,5 мкг/мл. Расчет проведен при графическом построении полученных данных.
Таким образом, полученные результаты изучения активности разных серий препарата №1 в отношении вируса гриппа A/IIV-Moscow/01/2009 (H1N1)sw1 выявили высокую активность подавления его репродукции в культуре клеток MDCK серией 1 при средней активности - серии 2. При этом режимы внесения препаратов за 2 часа до инфицирования или одновременно с инфицированием не влияли на их активность в культуре клеток MDCK.
Пример 6. Изучение противовирусной активности фуллерен-трис-аминокапроновой кислоты на модели гриппозной пневмонии мышей.
Исследования выполнялись в центре химии лекарственных средств (ЦХЛС - ВНИХФИ), г.Москва.
В работе использовали препарат №1 в виде темно-коричневого порошка. Для перорального применения готовили необходимые дозы препарата, растворяя навески в 1% растворе крахмала, сваренного на воде. Для внутрибрюшинного и внутримышечного применения навески препарата №1 растворяли в 1,5% растворе диметилсульфоксида.
В работе был использован вирус гриппа А/Аичи/2/69 (H3N2), адаптированный к мышам. Данный вирус широко используется для определения эффективности противовирусных препаратов на модели гриппозной пневмонии мышей и был получен из музея вирусных штаммов и клеточных культур ГУ НИИ вирусологии РАМН. Для подготовки инфицирующего материала мышей заражали интраназально аллантоисным вирусом, после проявления признаков болезни их забивали и в стерильных условиях получали гомогенат легочной ткани. Далее этот гомогенат использовали для заражения 10-дневных куриных эмбрионов, из которых получали аллантоисный вирус и после титрования на его мышах использовали для инфицирования животных.
Белых беспородных мышей (самки) массой 12-14 г получали из питомника «Андреевка» (Московская обл.) и содержали на стандартном рационе в регламентированных условиях вивария.
Предварительно взвешенные мыши (самки нелинейные, средний вес 12-14 г) инфицировались интраназально под легким эфирным наркозом вирусом гриппа А/Аичи/2/69 (H3N2) (10 ЛД50 в 100 мкл). В предварительном опыте было проведено определение ЛД50 путем титрования аллантоисного вируса на таких же мышах, которые затем использовались в основном опыте. Была использована следующая схема лечения исследуемым препаратом: за 24 часа до инфицирования, за 1 час до инфицирования, через 24 часа и далее 1 раз в день через 24 часа в течение 5 дней. Для перорального введения использовали одноразовый инсулиновый шприц со специальной иглой (лаваж), каждую дозу вводили в объеме 100 мкл. Для внутрибрюшинного и внутримышечного лечения также каждую дозу вводили в объеме 100 мкл. Группа вирусного контроля представляла собой 10 мышей, инфицированных вирусом, но не леченных препаратами. Также в опыте было две группы по 10 неинфицированных мышей, которым вводили внутрибрюшинно и внутримышечно по 100 мкл 1,5% DMSO, который использовался в качестве растворителя препаратов. В остальных группах также изначально было по 10 животных. За лечеными и контрольными животными велось ежедневное наблюдение, в первые 5 дней после инфицирования мыши взвешивались каждый день, далее - через день. Химиотерапевтическую активность препарата №1 на модели гриппозной пневмонии мышей оценивали по трем критериям: показатель защиты от смертельной вирусной инфекции, увеличение средней продолжительности жизни и уменьшение снижение веса в группах животных, леченных препаратом, по сравнению с контрольной группой.
Лечение препаратом №1 было эффективно, уменьшая смертность мышей от гриппозной пневмонии и потерю их веса и увеличивая среднюю продолжительность жизни по сравнению с вирусным контролем. Эффективность данного лечения зависела от дозы препарата и способа лечения. Эффективность перорального лечения фуллерен-трис-аминокапроновой кислотой гидрат увеличивалась с увеличением дозы препарата. Пероральное лечение препаратом №1 было эффективно, увеличивая среднюю продолжительность жизни в 1,6-1,7 раз. Наиболее эффективным по всем трем параметрам (показатель защиты от смертности, средняя продолжительность жизни и потеря веса) было лечение фуллерен-трис-аминокапроновой кислотой гидрат внутримышечно, которое в дозах 100 и 200 мг/кг/день предотвращало гибель 70-80% зараженных животных и потерю их веса, а также увеличивало продолжительность их жизни почти в 2 раза.
Внутрибрюшинное лечение фуллерен-трис-аминокапроновой кислотой было эффективно только в дозах 50 и 100 мг/кг/день. Гибель животных, значительное снижение средней продолжительности жизни и веса мышей при внутрибрюшинном лечении их препаратом №1 в дозе 200 мг/кг/день дают основание полагать, что данная доза при этом способе введения является токсичной для инфицированных мышей. Результаты представлены в таблицах 5-6.
Пример №7. Изучение протективной активности фуллерен-трис-аминокапроновой кислоты при экспериментальной летальной гриппозной инфекции у белых мышей, вызванной вирусами различного происхождения.
Исследования выполнялись в научно-исследовательском институте гриппа, г.Санкт-Петербург.
В работе использовали препарат №1 в виде черного мелкодисперсного порошка. Навески препарата были растворены в среде для клеточных культур Игла MEM (БиолоТ, Санкт-Петербург, кат. №1.3.3). Из полученного раствора были приготовлены серии разведений на среде MEM для определения противовирусной активности образцов в опытах на животных.
В качестве референс-препаратов использовали Ремантадин (1-(1-адамантил)-аминоэтил гидрохлорид, Aldrich Chem. Co., Milw., WI, cat. №39.059-3) и Тамифлю (Этил(3R,4R,5S)-4-ацетамидо-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоксилат фосфат, Hoffmann LaRoche, Швейцария).
Вирусы. В работе были использованы адаптированные к мышам вирусы гриппа следующих штаммов:
- A/Swine/1976/31 (H1N1) - свиного происхождения;
- A/Puerto Rico/8/34 (H1N1) - человеческого происхождения (ремантадин-устойчивый);
- А/Владивосток/2/09 (H1N1) - человеческого происхождения (Тамифлю-устойчивый). Вирусы пассировали в аллантоисной полости 10-12 дневных куриных эмбрионов в течение 48 часов при 36°С. Штамм А/Владивосток/2/09 (H1N1) предварительно адаптировали к мышам путем трех пар чередующихся пассажей на животных и в куриных эмбрионах.
Для заражения животных была использована вируссодержащая аллантоисная жидкость куриных эмбрионов. Из нее готовили серию 10-кратных разведений на физиологическом растворе, после чего инфекционная активность вируса в заражающем материале была определена в отдельном эксперименте при помощи титрования по летальности на животных. Титр вируса рассчитывали по методу Рида и Менча (Am. J. Hyg., 1938, 27: 493-497).
Белых беспородных мышей (самки) массой 14-16 г получали из питомника «Рапполово» (Ленинградская обл.) и содержали на стандартном рационе в регламентированных условиях вивария НИИ гриппа РАМН. Подбор животных в группы опыта проводили методом случайной выборки. До начала испытаний животные находились под наблюдением 2 недели.
Исследуемые препараты вводили животным внутрибрюшинно в объеме 0,2 мл в следующих дозах: Препарат №1 - 300, 100 и 30 мг/кг, Ремантадин - 50 мг/кг, Тамифлю - 20 мг/кг веса животных. Препараты вводили по лечебно-профилактической схеме: за 24 часа и 1 час до заражения и через 24, 48 и 72 часа после заражения. В качестве плацебо контрольной группе животных вводили физиологический фосфатный буфер. В качестве отрицательного контроля использовали интактных животных, которые содержались в тех же условиях, что и опытные группы.
Вирусы вводили животным интраназально под легким эфирным наркозом в дозе 1 и 10 LD50. В каждую группу наблюдения брали по 25 мышей. На 3 день после заражения 10 животных из каждой группы умерщвляли, вскрывали и изолировали легкие. Из этих 10 легких 5 использовали для выделения вируса (замораживали и хранили при -20°С до постановки соответствующих экспериментов), оставшиеся 5 фиксировали 10% формалином и использовали для гистологического анализа (см. ниже).
Наблюдение за оставшимися животными осуществляли в течение 14 дней, т.е. срока, в течение которого при экспериментальном гриппе отмечается смертность животных. Ежедневно фиксировали смертность животных в контрольных и опытных группах. На основании полученных показателей смертности в каждой группе рассчитывали процент смертности (М, отношение числа павших за 14 дней животных к общему числу зараженных животных в группе), индекс защиты (IP, отношение разницы процентов смертности в контрольной и опытной группах к проценту смертности в контрольной