Производные гидроксибензамида и их применение в качестве ингибиторов hsp90
Иллюстрации
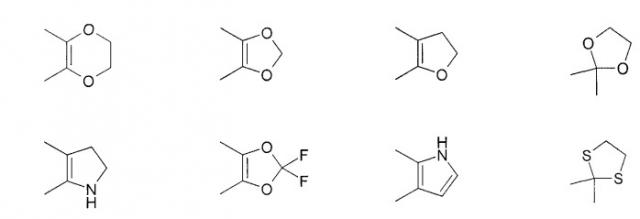
Показать всеИзобретение относится к новым соединениям формулы (VI):
или его фармацевтически приемлемым солям; где n равно 0, 1, 2 или 3; R1 означает-ОН, Н; R2a означает ОН, -СН3, при условии, что по меньшей мере один из R1 и R2a является -OH; R3 означает Cl, Br, циклопропил, разветвленный C3-5алкил; R4a означает Н; R8 означает Н; где фрагмент:
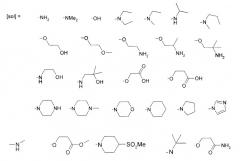
может быть одной из групп В8, В35, В36, В37, В38, В39, В40, В41, В42, В43, В45, В46, В48, В54, В56, В58, В59, В61, В62, В71, В72, В74, В75, В76, В77, В78, В79, В80, В81, В82, В84, В86, В87, В88, В89, В90, В91, В93, В94, В95, В96, В97, В98, В99, В100 и В101, где значения раскрыты в пункте 1 формулы. Соединения обладают Hsp90 ингибирующей активностью, что позволяет использовать их для лечения заболеваний, возникающих из-за аномального клеточного роста у млекопитающих. 8 н. и 18 з.п. ф-лы, 8 схем, 2 табл. 82 пр.
Реферат
Изобретение относится к соединениям, которые ингибируют или модулируют активность белка теплового шока Hsp90, к применению соединений при лечении или профилактике болезненных состояний, опосредованных Hsp90, и к новым соединениям, обладающим активностью, ингибирующей или модулирующей Hsp90. Также представлены фармацевтические композиции, содержащие соединения, и новые химические промежуточные соединения.
Предпосылки создания изобретения
В ответ на клеточные стрессы, включая тепловой, токсины, облучение, инфекцию, воспаление и окислители, все клетки продуцируют стандартный набор белков теплового шока (Hsp) (Macario и de Macario 2000). Большинство белков теплового шока действуют как молекулярные шапероны. Шапероны связывают и стабилизируют белки на промежуточных стадиях укладки и дают возможность белкам свернуться до их функциональных состояний. Hsp90 представляет собой наиболее распространенный цитозольный Hsp в нормальных условиях. Существуют две изоформы Hsp90 человека, основная форма Hsp90α и минорная форма Hsp90ß. Hsp90 связывает белки на последней стадии сворачивания и отличается от других Hsp, тем, что большинство его белковых субстратов вовлечены в сигнальную трансдукцию. Hsp90 имеет особый АТФ-связывающий сайт, включая особенность упаковки по Бергерату (Bergerat) бактериальной гиразы, топоизомераз и гистидиновых киназ. Было показано, что АТФ, связанный в N-концевом кармане Hsp90, гидролизуется. Такая АТФ-фазная активность приводит к конформационным изменениям в Hsp90, которые необходимы для того, чтобы сделать возможными конформационные изменения в клиентном белке.
Домен димеризации и второй АТФ-связывающий сайт, который может регулировать АТФ-азную активность, обнаружен вблизи c-конца Hsp90. Димеризация HSP90 представляется критически важной для гидролиза АТФ. Активация Hsp90 дополнительно регулируется через взаимодействия с другими разнообразными шаперонными белками и может быть отделена в комплексе с другими шаперонами, включая Hsp70, Hip, Hop, p23, и p50cdc37. Было продемонстрировано, что ряд других сошаперонных белков связывают HSP90. Появилась упрощенная модель, в которой АТФ-связывание с амино-концевым карманом изменяет конформацию Hsp90 с тем, чтобы сделать возможной ассоциацию с мультишаперонным комплексом. Первый клиентный белок связывается с комплексом Hsp70/Hsp40. Этот комплекс затем ассоциируется с Hsp90 через Hop. Когда ADP заменен АТФ, конформация Hsp90 изменяется, Hop и Hsp70 высвобождаются и обновляется различный набор сошаперонов, включая p50cdc37 и p23. Гидролиз АТФ приводит к высвобождению указанных сошаперонов и клиентного белка из зрелого комплекса. Ансамициновые антибиотики гербимицин, гельданамицин (GA) и 17-аллиламино-17-дезметоксигельданамицин (17-AAG) представляют собой ингибиторы АТФ-связывающего сайта, которые блокируют связывание АТФ и предотвращают преобразование в зрелый комплекс (Grenert et. al., 1997, J. Biol. Chem., 272:23834-23850).
Несмотря на то, что Hsp90 экспрессирован повсеместно, GA имеет более высокую аффинность связывания с Hsp90, полученному из опухолевых клеточных линий по сравнению с нормальными (Kamal et. al., Nature 2003; 425: 407-410). GA также показывает более мощную цитотоксическую активность в опухолевых клетках и обнаружена при более высоких концентрациях в опухолях на моделях ксенотрансплантатных мышей (Brazidec J. Med. Chem. 2004, 47, 3865-3873). Кроме того, АТФ-азная активность Hsp90 повышена в раковых клетках и является указанием на повышенный уровень стресса в данных клетках. Также сообщается, что амплификация гена Hsp90 имеет место на последних стадиях рака (Jolly и Morimoto JNCI Vol.92, No.19, 1564-1572, 2000).
Повышенная генетическая нестабильность, ассоциированная с раковым фенотипом, ведет к повышению продукции ненативных или мутантных белков. Убихитиновый путь также служит для защиты клетки от ненативных или неправильно упакованных белков путем направления таких белков на протесомальную деградацию. Мутантные белки не являются по их природе нативными и, следовательно, имеют возможность обнаруживать структурную нестабильность и повышенную потребность в шаперонной системе. (Giannini et al., Mol Cell. Biol. 2004; 24(13):5667-76).
Существует некоторое количество данных, что Hsp90 найден первоначально в "активированных" мультишаперонных комплексах в опухолевых клетках в противоположность "латентным" комплексам в нормальных клетках. Один компонент мультишаперонного комплекса представляет собой сошаперон cdc37. Cdc37 связывается с Hsp90 в основании АТФ-связывающего сайта и может воздействовать на скорости дезактивации для ингибиторов, связывающихся с Hsp90 в "активированном" состоянии (Roe et. al., Cell 116, (2004), pp.87-98). Клиентный белок, связанный с Hsp90-Hsp70 формой шаперонного комплекса, как предполагается, является более восприимчивым к убихитинированию и направлению в протеосому для деградации. E3-убихитин-лигазы были идентифицированы с мотивами, взаимодействующими с шапероном, и один них (CHIP), как было показано, промотирует убихитинацию и деградацию Hsp90-клиентных белков (Connell et al., 2001, Xu et al., 2002).
Hsp90-клиентные белки
Количество опубликованных Hsp90-клиентных белков к настоящему времени превышает 100. Поскольку многие из его клиентных белков вовлечены в клеточную сигнальную пролиферацию и выживаемость, Hsp90 остается основным предметом, представляющим интерес, в качестве онкологической мишени. Две группы клиентных белков, клеточные сигнальные белковые киназы и факторы транскрипции, в особенности допускают, что регуляция Hsp90 может иметь потенциальное преимущество при противораковой терапии.
Клиентные белки Hsp90 протеинкиназы, участвующие в клеточной пролиферации и выживаемости, включают следующие:
c-Src
Клеточная Src (c-Src) представляет собой рецепторную тирозинкиназу, необходимую для митогенеза, инициируемого множественными рецепторами фактора роста, включая рецепторы, такие как рецептор эпидермиального фактора роста (EGFR), рецептор тромбоцитарного фактора роста (PDGFR), рецептор колониестимулирующего фактора-1 (CSF-IR) и рецептор основного фактора роста фибробластов (bFGFR). C-Src также сверхэкспрессирована и активирована в многочисленных карциномах человека, которые сверхэкспрессируют EGFR и ErbB2. Src также требуется для поддержания нормального костного гомеостаза через его регуляцию остеокластной функции.
p185erbB2
ErbB2 (Her2/neu) представляет собой рецепторную тирозинкиназу, сверхэкспрессированную в разнообразных злокачественных образованиях, включая рак груди, яичника, простаты и желудка. ErbB2 изначально идентифицировали как онкоген, и ингибирование Hsp90 приводит к полиубихитинации и деградации erbB2.
Polo-митотические киназы
Polo-подобные киназы (Plk) являются важными регуляторами продвижения клеточного цикла в M-фазе. Plk вовлечены в сборку митотического веретенного аппарата и в активацию комплексов CDK/циклин. Plk1 регулирует дефосфорилирование тирозина CDK через фосфорилирование и активацию Cdc25C. Активация CDK1, в свою очередь, ведет к образованию веретена и вхождению в M-фазу.
Akt (PKB)
Akt вовлечен в пути, которые регулируют клеточный рост путем стимулирования клеточной пролиферации и подавления апоптоза. Ингибирование Hsp90 под действием ансамицинов приводит к уменьшению периода полужизни Akt через убихитинирование и протесомальное разложение. Связывание cdc37 с Hsp90 также требуется для подавления Akt. После обработки ансамицином раковые клетки задерживаются в G2/M-фазе клеточного цикла на 24 часа после обработки и переходят к апоптозу через 24-48 часов. Нормальные клетки также задерживаются на 24 часа после обработки ансамицином, но не переходят к апоптозу.
c-Raf, B-RAF, Mek
RAS-RAF-MEK-ERK-MAP киназный путь опосредует клеточные ответы на сигналы роста. RAS мутирован в онкогенную форму приблизительно у 15% раковых новообразований человека. Три гена RAF представляют собой серин/треонининовые киназы, которые осуществляют регуляцию путем связывания RAS.
EGFR
Рецептор эпидермального фактора роста (EGFR) участвует в клеточном росте, дифференциации, пролиферации, выживаемости, апоптозе и миграции. Сверхэкспрессия EGFR была обнаружена во многих различных видах рака и активирующие мутации его киназного домена, как представляется, являются патогенными в подмножестве аденокарцином легкого.
Flt3
FMS-подобная тирозинкиназа 3 (FLT3) представляет собой рецепторную тирозинкиназу, участвующую в клеточной пролиферации, дифференциации и апоптозе. Flt3 активация также ведет к активации фосфатидилинозитол-3-киназы (PI3k) и RAS-каскадах сигнальной трансдукции.
c-Met
c-Met представляет собой рецепторную тирозинкиназу, которая связывает фактор роста гепатоцитов (HGF) и регулирует как клеточную подвижность, так и клеточный рост; c-Met сверхэкспрессирована в опухолях, включая рак щитовидной железы, желудка, поджелудочной железы и толстой кишки. HGF также детектируется вокруг опухолей, включая метастазы печени. Это дает возможность предположить, что c-Met и HGF играют важную роль при инвазии и метастазировании.
Cdkl, Cdk2, Cdk4, Cdk6
Cdkl, Cdk2, Cdk4 и Cdk6 управляют клеточным циклом. Активность CDK регулируется их связыванием со специфическими субъединицами, такими как циклины, факторы ингибирования и сборки. Субстратная специфичность и распределение во времени CDK-активностей определяется их взаимодействием со специфическим циклинами. Cdk4/циклин D и Cdk6/циклин D активны в G1-фазе, Cdk2/циклин E и Cdk2/циклин A в S-фазе, и Cdc2/циклин A и Cdc2/циклин B в G2/M-фазе.
Циклинзависимая киназа типа 4 (CDK4) играет ключевую роль в возможности клеток переходить из G1- в S-фазу клеточного цикла и существенно активироваться во многих раковых новообразованиях человека. Активатор CDK4, циклин Dl, сверхэкспрессирован и CDK4 ингибитор, p16, отсутствует в разнообразных опухолях человека.
Разработаны Cdkl/Cdk2 ингибиторы, которые обратимо блокируют нормальные клетки в Gl/S-фазе или на G2/M-границе. G2/M-задержка обычно менее хорошо переносится клетками и, как следствие, они претерпевают апоптотическую смерть клетки. Поскольку также известно, что Hsp90 воздействует на пути клеточного выживания, этот эффект может быть дополнительно усилен ингибиторами Hsp90.
Wee-1
Протеинкиназа Wee-1 осуществляет подавляющее фосфорилирование CDC2 на тирозине-15 (Tyrl5). Это требуется для активации контрольной точки G2-фазы в ответ на повреждение ДНК.
Hsp90 факторы транскрипций, участвующие в клеточной пролиферации и выживаемости, включают следующие:
Мутантный p53
P53 представляет собой опухолевый супрессорный белок, который вызывает задержку клеточного цикла и индуцирует апоптоз. P53 мутирован в приблизительно половине всех видов рака. Мутантный p53 связывается с Hsp90 и действует как понижающий регулятор в раковых линиях, обработанных ингибиторами Hsp90, в то время как уровни p53 дикого типа остаются незатронутыми.
Прогестероновый рецептор/эстрогенный рецептор/рецептор андрогенного гормона
В отсутствие гормонов, рецепторы прогестерона и андрогенного гормона связываются Hsp90 в неактивную форму. После связывания с их родственными гормонами, рецепторы претерпевают конформационные изменения и диссоциацию из hsp90. Затем связанные лигандом рецепторы способны к димеризации, фосфорилированию и транслокации в ядро. Активированные рецепторы затем связываются с элементами гормонального ответа (HRE) в пределах регуляторных участков генов-мишеней, вовлеченных в поддержание клеточной пролиферации.
Hif-1a
Индуцируемый гипоксией фактор-1a (HIF-1a) представляет собой фактор транскрипции, который контролирует экспрессию генов, которые играют роль в ангиогенезе. HIF-1a экспрессирован в большинстве метастазов и, как известно, ассоциирован с Hsp90. Обработка ансамицином клеточных линий почечной карциномы ведет к убихитинированию и протесомальной деградации HIF-1a.
Ингтбиторы Hsp90 способны воздействовать на большое число мишеней, важных для сигнальной трансдукции при пролиферации опухолевых клеток. Ингибиторы сигнальной трансдукции, которые регулируют активности отдельной мишени, могут не являться такими эффективными благодаря избыточности сигнальных путей и быстрому развитию резистентности. Путем регулирования множественных мишеней, вовлеченных в клеточный сигнальный процесс и клеточную пролиферацию, ингибиторы Hsp90 могут предоставлять преимущество при лечении широкого спектра пролиферативных расстройств.
hERG
В конце 1990-х, ряд лекарственных средств, допущенных Управлением по контролю за продуктами и лекарственными средствами (США), были отозваны из торговли в США, когда было обнаружено, что они приводят к смертным случаям, вызванным дисфункцией сердца. Впоследствии было обнаружено, что побочным эффектом таких лекарственных средств является развитие аритмии, вызываемой блокированием hERG каналов в клетках сердца. hERG-канал представляет собой канал из семейства калиевых ионных каналов, первый представитель которых был идентифицирован в конце 1980-х на мутантной плодовой мушке Drosophila melanogaster (см. Jan, L.Y. and Jan, Y.N. (1990). A Superfamily of Ion Channels. Nature, 345(6277):672). Биофизические свойства hERG калиевого ионного канала описаны Sanguinetti, M.C., Jiang, C, Curran, M.E., and Keating, M.T. (1995). A Mechanistic Link Between an Inherited and an Acquired Cardiac Arrhythmia: HERG encodes the Ikr potassium channel. Cell, 81:299-307, and Trudeau, M.C., Warmke, J. W., Ganetzky, B., and Robertson, G.A. (1995). HERG, a Human Inward Rectifier in the Voltage-Gated Potassium Channel Family. Science, 269:92-95.
Ликвидация hERG, блокирующей активности, остается важным предметом рассмотрения при разработке любого нового лекарственного средства.
Предшествующий уровень техники
В EP 0474403 (Eli Lilly) описан класс производных 4-гидроксибензамида для лечения воспалительного заболевания кишечника.
В EP 0722723 (Eli Lilly) описан класс производных 4-гидроксибензамида для лечения рассеянного склероза.
В EP 0500336 (University of Colorado Foundation) описан класс производных 4-гидроксибензамида для лечения диабета I типа.
В WO 00/59867 (Pharmacor) описаны гидроксифенильные производные для применения в качестве ингибиторов интегразы ВИЧ.
В JP 09194450 (Fujirebio) описаны производные ортогидроксибензамида в качестве фармацевтических промежуточных соединений.
В EP 0486386 описаны замещенные производные бензоилпролина.
В WO 2005/012297 (Janssen) описан пиперидинамид 4-гидрокси-3-фторбензойной кислоты в качестве промежуточного соединения при получении соединений, имеющих модулирующую активность в отношении LTA4-гидролазы.
В WO 2005/000839 (Tanabe) описан морфолинамид 4-гидрокси-3-бромбензойной кислоты в качестве промежуточного соединения при получении ациламинобензофурановых соединений.
Применение производных гидроксибензамида в качестве синтетических промежуточных соединений описано в патенте США 5310951, JP 49010506, WO 01/36351, WO 98/45255 и WO 97/35999.
В EP 0347168 (Ono Pharmaceutical Co.) описаны паразамещенные фениловые эфиры пивалиновой кислоты в качестве ингибиторов эластазы. Одно конкретное соединение, описанное в данном патенте, представляет собой 3-гидрокси-4-[(N-метил-N-фенил)карбамоилфениловый эфир пивалиновой кислоты.
В EP 0353753 (Takeda) описаны соединения амидов замещенной бензойной кислоты, обладающие ингибирующей активностью в отношении глутаматного рецептора.
В патенте США 2005/0037922 (Bayer Cropscience) описаны различные гидроксированные диметиламиды и диэтиламиды бензойной кислоты в качестве средств сохранения сельскохозяйственных культур.
В WO 2005/009940 (Leo Pharma) описаны аминобензофеноновые соединения, которые, как указано, могут быть полезны при лечении воспалительных заболеваний и раковых заболеваний.
В WO 99/29705 (Glycomed et al.) описан класс соединений-гликомиметиков, имеющих ряд возможных применений, включая лечение рака. Одно соединение, специально описанное в WO 99/29705, представляет собой 2-(2-гидроксибензоил)-1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту.
Сущность изобретения
Изобретение относится к соединениям, которые обладают Hsp90-ингибирующей или модулирующей активностью и которые, как предполагается, будут полезны при предотвращении или лечении болезненных состояний, опосредованных Hsp90. Так, например, предполагается, что соединения по изобретению могут быть полезны для облегчения или снижения случаев развития рака.
В первом аспекте, изобретение представляет соединение формулы (I):
или его соли, таутомеры, сольваты и N-оксиды;
где R1 представляет собой гидроксигруппу или водород;
R2 представляет собой гидроксигруппу; метоксигруппу или водород; при условии, что по меньшей мере один из R1 и R2 является гидроксигруппой;
R3 выбирают из атома водорода; галогена; циано; C1-5 гидрокарбила и C1-5 гидрокарбилокси; где C1-5 гидрокарбильный и C1-5 гидрокарбилокси фрагменты, каждый необязательно замещен одним или несколькими заместителями, выбранными из гидрокси, галогена, C1-2алкокси, амино, моно- и ди-C1-2алкиламино, и арильных и гетероарильных групп, имеющих 5-12 атомов в кольце;
R4 выбирают из атома водорода; группы -(Q)n-R7, где n равно 0 или 1, и R7 представляет собой ациклическую C1-5 гидрокарбильную группу или моноциклическую карбоциклическую или гетероциклическую группу, имеющую 3-7 атомов в кольце; галоген; циано; гидрокси; амино; и моно- или ди-C1-5 гидрокарбиламино, где ациклическая C1-5 гидрокарбильная группа и моно- и ди-C1-5 гидрокарбиламинные фрагменты в каждом случае необязательно замещены одним или несколькими заместителями, выбранными из гидрокси, галогена, C1-2алкокси, амино, моно- и ди-C1-2алкиламино, и арильных и гетероарильных групп, имеющих 5-12 атомов в кольце;
или R3 и R4 вместе образуют моноциклическое карбоциклическое или гетероциклическое кольцо из 5-7 атомов в кольце;
R5 и R6 вместе с атомом азота, к которому они присоединены, образуют бициклическую гетероциклическую группу, имеющую 8-12 атомов в кольце, из которых до 5 атомов в кольце представляют собой гетероатомы, выбранные из кислорода, азота и серы; где бициклическая гетероциклическая группа необязательно замещена одним или несколькими заместителями R10;
R8 выбирают из атомов водорода и фтора; и
R10 выбирают из:
галогена;
гидрокси;
трифторметила;
циано;
нитро;
карбокси;
амино;
моно- или ди-C1-4 гидрокарбиламино;
карбоциклических и гетероциклических групп, имеющих от 3 до 12 атомов в кольце; и
группы Ra-Rb,
где Ra представляет собой связь, O, CO, X1C(X2), C(X2)X1, X1C(X2)X1, S, SO, SO2, NRc, SO2NRc или NRcSO2; и
Rb выбирают из атома водорода; карбоциклических и гетероциклических групп, имеющих от 3 до 12 атомов в кольце; и C1-12 гидрокарбила (такой как C1-10 гидрокарбил), необязательно замещенного одним или несколькими заместителями, выбранными из гидрокси, оксо, галоген, циано, нитро, карбокси, амино, неароматического моно- или ди-C1-8 гидрокарбиламино (например, моно- или ди-C1-4 гидрокарбиламино), и карбоциклических и гетероциклических групп, имеющих от 3 до 12 атомов в кольце, и где один или несколько атомов углерода C1-12 гидрокарбильной группы (или C1-10 гидрокарбильной группы) могут быть необязательно заменены на O, S, SO, SO2, NRc, X1C(X2), C(X2)X1, X1C(X2)X1;
Rc выбирают из Rb, атома водорода и C1-4 гидрокарбила; и
X1 представляет собой O, S или NRc и X2 представляет собой=O,=S или=NRc;
но исключая соединение, 2-(2-гидроксибензоил)-1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту.
Изобретение, помимо прочего, также предоставляет:
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения при профилактике или лечении болезненного состояния, опосредованного Hsp90;
применение соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения болезненного состояния, опосредованного Hsp90;
способ профилактики или лечения болезненного состояния, опосредованного Hsp90, который включает введение субъекту, нуждающемуся в этом, соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения для облегчения или снижения случаев болезненного состояния, опосредованного Hsp90;
применение соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для производства лекарственного средства для облегчения или снижения случаев болезненного состояния, опосредованного Hsp90;
способ облегчения или снижения случаев болезненного состояния, опосредованного Hsp90, который включает введение субъекту, нуждающегося в этом, соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения при лечении заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего;
применение соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для производства лекарственного средства для лечения заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего;
способ лечения заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего, который включает введение млекопитающему соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, в количестве, эффективном для ингибирования аномального клеточного роста;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения для облегчения или снижения случаев заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего;
применение соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для производства лекарственного средства для облегчения или снижения случаев заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего;
способ для облегчения или снижения случаев заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего, который включает введение млекопитающему соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, в количестве, эффективном для ингибирования аномального клеточного роста;
способ лечения заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего, который включает введение млекопитающему соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb), или любых их подгрупп или примеров, как определено в настоящем описании, в количестве, эффективном для ингибирования активности Hsp90;
способ облегчения или снижения случаев заболевания или состояния, включающих или возникающих из-за аномального клеточного роста у млекопитающего, который включает введение млекопитающему соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, в количестве, эффективном для ингибирования активности Hsp90;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения в качестве ингибитора Hsp90;
способ ингибирования Hsp90, который включает контактирование Hsp90 с Hsp90-ингибирующим соединением формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения при модулировании клеточного процесса (например, деления клетки) путем ингибирования активности Hsp90;
способ модулирования клеточного процесса (например, деления клетки) путем ингибирования активности Hsp90 с использованием соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения при профилактике или лечении болезненного состояния, как описано выше;
применение соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для производства лекарственного средства, где лекарственное средство предназначено для любого одного или нескольких из применений, определенных выше;
фармацевтическая композиция, содержащая соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, и фармацевтически приемлемый носитель;
фармацевтическая композиция, содержащая соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, и фармацевтически приемлемый носитель в форме, пригодной для орального введения;
фармацевтическая композиция, содержащая соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, и фармацевтически приемлемый носитель в форме, пригодной для парентерального введения, например, путем внутривенного (i.v.) введения;
фармацевтический композиция, содержащая соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, и фармацевтически приемлемый носитель в форме, пригодной для внутривенного (i.v.) введения путем инъекции или инфузии;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения в медицине;
соединение, как описано выше, для любого из применений и способов, представленных выше, как описано в настоящем описании в других местах;
соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для применения при лечении или профилактике болезненного состояния у пациента, который был обследован и диагностирован как страдающий или находящийся в зоне риска заболевания или состояния, которое должно быть восприимчиво к лечению соединением, обладающим активностью в отношении Hsp90;
применение соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании, для производства лекарственного средства для лечения или профилактики заболевания или состояния у пациента, который был обследован и диагностирован как страдающий или находящийся в зоне риска заболевания или состояния, которое должно быть восприимчиво к лечению соединением, обладающим активностью в отношении Hsp90;
способ диагностики и лечения болезненного состояния, опосредованного Hsp90, который включает (i) обследование пациента для определения, является ли заболевание или состояние, которыми пациент страдает или может страдать, заболеванием или состоянием, которое будет восприимчивым к лечению соединением, обладающим активностью в отношении Hsp90; и (ii) где обнаружено, что заболевание или состояние, которым страдает пациент, таким образом, является восприимчивым, после введения пациенту соединения формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) или любых их подгрупп или примеров, как определено в настоящем описании.
Общие предпочтительные значения и определения
В данном разделе, как во всех других разделах данного описания, пока в контексте не указано иное, ссылки на соединение формулы (I) включают все подгруппы формулы (I), как определено в настоящем описании, включая формулы (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) и (VIIb), и термин 'подгруппы' включает все предпочтительные варианты, варианты осуществления примеры и конкретные соединения, определенные в настоящем описании.
Кроме того, ссылка на соединение формулы (I), (II), (III), (IV), (V), (VI), (VIa), (VII), (VIIa) или (VIIb) и их подгрупп включает ионные формы, соли, сольваты, изомеры, таутомеры, N-оксиды, сложные эфиры, пролекарства, изотопы и их защищенные формы, как обсуждается ниже, предпочтительно соли, или таутомеры, или изомеры, или N-оксиды, или их сольваты, и, более предпочтительно, соли, или таутомеры, или N-оксиды, или их сольваты.
Следующие общие предпочтительные значения и определения следует применять к каждому из R1-R8, R10, Ra, Rb, Rc, X1 и X2 и их различным подгруппам, подопределениям, примерам и вариантам осуществления, пока в контексте не указано иное.
Любые ссылки на формулу (I) в настоящем описании также означают любую подгруппу соединений в пределах формулы (I) и любые предпочтительные значения и их примеры, пока в контексте не указано иное.
Ссылки на "карбоциклические" и "гетероциклические" группы, используемые в настоящем описании, пока в контексте не указано иное, включают как ароматические, так и неароматические кольцевые системы. Так, например, термин "карбоциклические и гетероциклические группы" включает в пределах их объема ароматические, неароматические, ненасыщенные, частично насыщенные и полностью насыщенные карбоциклические и гетероциклические кольцевые системы. Как правило, такие группы могут быть моноциклическими или бициклическими и могут содержать, например, 3-12 атомов в кольце, более конкретно 5-10 атомов в кольце. Примерами моноциклических групп являются группы, содержащие 3, 4, 5, 6, 7, и 8 атомов в кольце, более конкретно от 3 до 7, например от 5 до 7, и предпочтительно 5 или 6 атомов в кольце. Примерами бициклических групп являются такие, которые содержат 8, 9, 10, 11 и 12 атомов в кольце, более конкретно, 9 или 10 атомов в кольце.
Используемый в настоящем описании термин "бициклический", относится к группам, которые имеют два кольца, соединенных вместе таким образом, что по меньшей мере один атом кольца задействован в обоих кольцах. Так, бициклическая группа может представлять собой конденсированное кольцо (два атома в кольце задействованы в обоих кольцах), спироциклическое (один атом кольца задействован в обоих кольцах) или мостиковое кольцо (три или более атома в кольце задействованы в обоих кольцах).
Карбоциклические или гетероциклические группы могут представлять собой арильные или гетероарильные группы, имеющие от 5 до 12 атомов в кольце, более конкретно, от 5 до 10 атомов в кольце. Термин "арил", используемый в настоящем описании, относится к карбоциклической группе, имеющей ароматический характер, и термин "гетероарил" используется в настоящем описании для обозначения гетероциклической группы, имеющей ароматический характер. Термины "арил" и "гетероарил" включают полициклические (например, бициклические) кольцевые системы, где один или несколько колец являются неароматическими, при условии, что по меньшей мере одно кольцо является ароматическим. В таких поликольцевых системах группа может быть присоединена через ароматическое кольцо или через неароматическое кольцо. Арильные или гетероарильные группы могут быть моноциклическими или бициклическими группами и могут являться незамещенными или замещены одним или несколькими заместителями, например одной или несколькими группами R10, как определено выше.
Термин "неароматическая группа" включает ненасыщенные кольцевые системы, не имеющие ароматического характера, частично насыщенные и полностью насыщенные карбоциклические и гетероциклические кольцевые системы. Термины "ненасыщенный" и "частично насыщенный" относятся к кольцам, где кольцевая структура(ы) содержит атомы, связанные более чем одной валентной связью, то есть кольцо содержит по меньшей мере одну кратную связь, например C=C, C=C или N=C связь. Термины "полностью насыщенный" и "насыщенный" относятся к кольцам, где нет кратных связей между атомами кольца. Насыщенные карбоциклические группы включают циклоалкильные группы, как определено ниже. Частично насыщенные карбоциклические группы включают циклоалкенильные группы, как определено ниже, например, циклопентенил, циклогептенил и циклооктенил. Следующим примером циклоалкенильной группы является циклогексенил.
Примерами гетероарильных групп являются моноциклические и бициклические группы, содержащие от пяти до двенадцати атомов в кольце, и, более конкретно, от пяти до десяти атомов в кольце. Гетероарильная группа может представлять собой, например, пятичленное или шестичленное моноциклическое кольцо или бициклическую структуру, образуемую из конденсированных пяти- и шестичленных колец или двух конденсированных шестичленных колец или, в качестве следующего примера, два конденсированных пятичленных кольца. Каждое кольцо может содержать приблизительно до четырех гетероатомов, обычно выбранных из азота, серы и кислорода. Обычно гетероарильное кольцо содержит до 4 гетероатомов, более конкретно до 3 гетероатомов, еще более конкретно до 2, например одиночный гетероатом. В одном варианте осуществления гетероарильное кольцо содержит по меньшей мере один атом азота кольца. Атомы азота в гетероарильных кольцах могут быть основными, как в случае имидазола или пиридина, или фактически лишенными основных свойств, как в случае индольного или пиррольного азота. Как правило, число основных атомов азота, присутствующих в гетероарильной группе, включая любые аминные заместители кольца, будет составлять менее чем пять.
Примеры пятичленных гетероарильных групп включают, но без ограничения, пиррольные, фурановые, тиофеновые, имидазольные, фуразановые, оксазольные, оксадиазольные, оксатриазольные, изоксазольные, тиазольные, изотиазольные, пиразольные, триазольные и тетразольные группы.
Примеры шестичленных гетероарильных групп включают, но без ограничения, пиридин, пиразин, пиридазин, пиримидин и триазин.
Бициклическая гетероарильная группа может представлять собой, например, группу, выбранную из:
a) бензольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце;
b) пиридинового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце;
c) пиримидинового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
d) пиррольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце;
e) пиразольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
f) пиразинового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
g) имидазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
h) оксазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
i) изоксазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
j) тиазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
k) изотиазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1 или 2 гетероатома в кольце;
l) тиофенового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце;
m) фураного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце;
n) циклогексильного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце; и
o) циклопентильного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольц