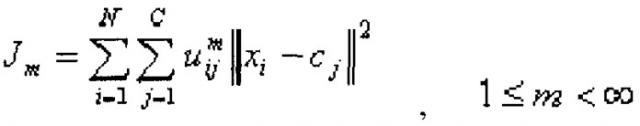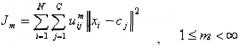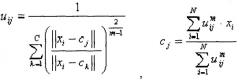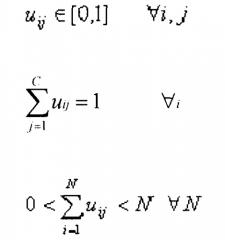Направляемая клиницистом компьютерная диагностика на базе примеров
Иллюстрации
Показать всеИзобретение относится к области компьютерной диагностики на базе примеров. Техническим результатом является оптимизация компьютерной диагностики на базе примеров. Оптимизацию компьютерной диагностики на базе примеров (CADx) обеспечивают группировкой представляющих интерес объемов (VO1) (116) в базе (120) данных в соответствующие кластеры согласно субъективной оценке сходства (S220). Затем выбирают оптимальное множество признаков представляющего интерес объема (VOI) вызова таких примеров, чтобы объективная оценка сходства, основанная на выбранных признаках, кластерах в пространстве признаков, VOI в базе данных, согласовалась с субъективной группировкой в кластеры (S230). Вызванные примеры визуально представляются вместе с подлежащим диагностированию VOI для сравнения клиницистом. В предпочтительном варианте визуально представляемый пример может быть выбран пользователем для дополнительного визуального представления прогноза, информации о лечении, вторичной информации, текущего состояния и/или клинической информации, вызываемых из электронной медицинской карты (S260). 4 н. и 17 з.п. ф-лы, 4 ил.
Реферат
Настоящее изобретение относится к компьютерной диагностике на базе примеров и, в частности, к выбору оптимального множества признаков представляющего интерес объема (VOI), по которым следует вызывать примеры из базы данных.
Радиологи должны считать много томографических изображений, полученных методами компьютерной томографии (CT), рентгеновского исследования, магнитно-резонансной визуализации (MRI), ультразвукового исследования, позитронной эмиссионной томографии (PET) и т.п. В результате этого возможна «информационная перегрузка» радиологов. Кроме того, радиологи могут пропустить, например, многие случаи раковых заболеваний во время интерпретации изображений при скрининговом обследовании на рак. Информационная перегрузка потенциально обостряет данную проблему. Даже если последующее сканирование обнаруживает рак, коэффициент выживаемости можно повысить благодаря ранней диагностике. И, наоборот, ложно-положительные результаты могут иметь следствием необязательную биопсию. В результате, как для совершенствования последовательности выполняемых действий, так и для улучшения исхода для пациента все шире применяют системы поддержки принятия решений, например схемы компьютерной диагностики (CADx).
Уровнем техники для системы CADx на базе примеров служит то, что клиницисты получают знания из опыта и рассмотрения случаев, с которыми они сталкивались прежде. Один способ, с использованием которого система поддержки принятия решений может помочь клиницисту при постановке диагноза по CT-томограмме (компьютерной томограмме) (или томограммам, полученным любым другим способом, при рентгеновском исследовании, магнитно-резонансной визуализации (MRI), ультразвуковом исследовании, позитронной эмиссионной томографии (PET) и т.п.), например рака легких, заключается в предоставлении полученных прежде изображений, которые уже послужили для постановки диагноза и сходны с новым изображением. Парадигма использования примеров состоит в том, что узлы, сходные с подлежащим диагностированию узлом, вызываются из базы данных узлов с известными диагнозами и представляются радиологу. Данная парадигма является основной предпосылкой системы CADx на базе примеров.
CADx на базе примеров или случаев заболеваний обычно предполагает вызов из базы данных информации, относящейся к опухолям или поражениям с известной патологией, т.е. злокачественным или доброкачественным. Информация обычно содержит изображение опухоли для визуального сравнения с изображением подлежащей диагностированию опухоли. Опухоль может быть, например, в легком пациента. Данные изображения опухоли могут быть собраны любым из ряда методов визуализации, некоторые из которых упомянуты выше. Затем по изображению можно измерить признаки опухоли, при этом каждый признак отражает конкретную визуальную характеристику опухоли. Подлежащие диагностированию опухоли и опухоли из базы данных можно располагать в общем пространстве признаков, т.е. N-мерном пространстве, каждое измерение которого отражает один соответствующий признак из N измеряемых признаков. Сходство любой опухоли из базы данных с подлежащей диагностированию опухолью можно ориентировочно и объективно оценивать на основе близости двух опухолей в пространстве признаков. Как правило, вызываются максимально близкие опухоли. Вызванные примеры могут отображаться вместе с подлежащей диагностированию опухолью для визуального сравнения. CADx на базе примеров может также приносить пользу при обучении медицинского персонала диагностированию по томограммам.
Метод CADx на базе примеров выделяется на фоне методов, в соответствии с которыми клиницисты получают знания из опыта и рассмотрения случаев, с которыми они сталкивались прежде. Авторы настоящего изобретения наблюдали, что разные радиологи могут иметь разные мнения о том, сходны ли и в чем сходны два случая заболевания, и из визуального сравнения подлежащей диагностированию опухоли с изображением опухоли с известной патологией трудно знать заранее, сходны ли или нет два случая заболевания.
Настоящее изобретение предлагает применять знания клиницистов, например радиолога, при определении пространства признаков и поточечной дистанционной метрики, подлежащей использованию при измерении сходства между подлежащей диагностированию опухолью и опухолями в базе данных. В настоящей заявке термин «поточечный» включает в себя точечно-многоточечный вариант. Хотя, как упоминалось выше, заранее трудно знать, есть ли сходство между двумя случаями, суждение о том, согласуются ли конкретное пространство признаков и дистанционная метрика с субъективными оценками сходства опухоли, можно надежно оценить количественно в соответствии с предлагаемым изобретением. Настоящие обстоятельства обосновывают применение генетического алгоритма (GA). GA итерационно выявляет множество возможных предлагаемых решений данной проблемы. Все возможные решения, называемые хромосомами, оценивают в зависимости от их соответствующей пригодности. Если критерий останова итераций не удовлетворяется, то на основе текущего множества хромосом создают, по меньшей мере, одну новую хромосому. Оценивают пригодность и на следующей итерации применяют критерий останова. После того как критерий останова удовлетворяется, выбирается наиболее пригодная хромосома. Настоящее изобретение предлагает учитывать субъективную оценку сходства радиологами во время составления итеративно применяемой количественной оценки.
В сущности, оптимизацию CADx на основе примеров осуществляют группировкой представляющих интерес объемов (VOI) в базе данных в соответствующие кластеры в зависимости от субъективной оценки сходства. Затем выбирают оптимальное множество признаков представляющих интерес объемов, которое содержит визуальные и клинические (не основанные на изображениях) признаки, для вызова примеров, чтобы объективные оценки сходства, основанные на выбранных признаках, кластерах в пространстве признаков, VOI в базе данных, согласовались с субъективной группировкой в кластеры.
Подробное описание нового метода CADx на базе примеров приведено ниже со ссылкой на нижеследующие чертежи:
Фиг.1 - функциональная схема, представляющая в общих чертах примерную систему CADx в соответствии с настоящим изобретением;
Фиг.2 - блок-схема последовательности операций, представляющая в общих чертах один пример способа в соответствии с настоящим изобретением;
Фиг.3 - виды таблиц, которые можно использовать при субъективной оценке сходства между опухолями в базе данных, чтобы формировать кластеры сходных опухолей, в соответствии с настоящим изобретением; и
Фиг.4 - блок-схема хромосомы, применимой в генетическом алгоритме в соответствии с настоящим изобретением.
На фиг.1 приведен пример устройства 100 для компьютерной диагностики (CADx) на базе примеров в соответствии с настоящим изобретением, содержащего процессор 104 и дисплейный экран 108. На дисплейном экране 108 показан узел, опухоль или поражение 112, подлежащие диагностированию. Представленное изображение предпочтительно содержит некоторую часть непосредственно окружающей ткани. Подлежащий отображению узел и, по желанию, непосредственно окружающая его ткань упоминаются в дальнейшем как представляющий интерес объем (VOI). Рядом с VOI 112 на дисплее показаны также три вызванных примера. Тремя примерами являются VOI 116a, содержащий злокачественную опухоль, и два VOI 116b, содержащие соответствующие доброкачественные опухоли. Три примерных VOI 116 вызваны из базы данных 120 процессора 104 модулем 124 вызова примеров. Модуль 124 вызова примеров работает на основе параметров, например визуальных признаков и метрики сходства, предоставляемых модулем вывода параметров (не показанным), при этом упомянутые параметры получены блоком 132 получения параметров. Модуль вывода параметров в показанном исполнении составляет одно целое с блоком 132 получения параметров. Стрелка 128 показывает передачу полученных параметров для использования модулем 124 вызова примеров. Средство 134 пользовательского ввода служит для представления в блок 132 получения параметров данных о субъективной оценке сходства между VOI 116. Средство 134 пользовательского ввода может содержать клавиатуру, мышь, трекбол, слайдер, бегунок, световое перо, сенсорный экран и т.п., а также накопители на дискетах, оптических дисках и проводные или беспроводные соединения с сетями, работающими в реальном времени. Аналогично, база 120 данных служит как устройство ввода для блока получения параметров. Примеры, вызванные модулем 124 вызова примеров и представленные на экране, можно селективно выбирать, например, щелчком мыши для отображения дополнительной клинической или другой информации, относящейся к выбранному примеру. Устройство 100 CADx содержит память (не показанную) для хранения данных изображения и, возможно, клинических данных о VOI 112, причем упомянутая память содержит оперативную память для использования модулем 124 вызова примеров и блоком 132 получения параметров. Устройство 100 CADx может быть специализированным или универсальным процессором и может быть аналоговым или цифровым. На дисплее одновременно показаны всего три примерных VOI 116, однако они могут быть представлены на дисплее в большем или меньшем числе и размещены на экране 108 по любой пространственной схеме расположения. Кроме того, хотя одновременно представляемое изображение содержит оба типа случаев, злокачественный и доброкачественный, в любой момент времени на дисплее вместе с VOI 112 может быть показан только один из двух типов случаев заболевания. В любом из двух случаев обозначения «Malignant» («Злокачественный») и/или «Benign» («Доброкачественный») могут первоначально комментировать отображаемые примеры 116 или могут выводиться в ответ на указание пользователя. В дополнение, функциональные возможности могут быть поделены между разным числом элементов 124, 132 и распределены иначе, чем показано. Например, блок 132 может располагаться удаленно от остальных частей устройства 100.
На фиг.2 представлен, в виде наглядного и не ограничивающего примера, процесс 200 для CADx на базе примеров в соответствии с настоящим изобретением. Во-первых, выполняют субъективную оценку сходства по парам для всех VOI 116 в базе данных 120 (этап S210). Оценки предпочтительно выполняются клиницистами, например радиологами, например путем опросов. Оценки предпочтительно содержат дополнительно субъективное ранжирование признаков в зависимости от их важности при оценке сходства. Для настоящих целей признаки VOI 112, 116 содержат выделяемые характеристики, получаемые из изображений VOI, например, эффективный диаметр, степень округлости, контраст, среднее значение по серой шкале, угловатость, граница, плотность, наличие острых выступов, среднеквадратичное отклонение в пикселях, radial показатель неоднородности и т.д. Клинические данные, характеризующие пациента и VOI, например возраст, анамнез ракового заболевания и т.п., также могут составлять признак. На основании оценок сходные VOI 116 группируют в кластер в логическом смысле (этап S220). Таким образом, формируют подмножества VOI 116. Упомянутые подмножества не обязательно должны быть взаимно исключающими. Субъективная группировка в кластеры может выполняться вручную или, в предпочтительном варианте, блоком 132 получения параметров.
Применяют генетический алгоритм (GA) для поиска оптимального пространства признаков и предпочтительно оптимального поточечного критерия сходства для применения в оптимальном пространстве признаков (этап S230). Оптимальное пространство признаков следует получать из совокупности признаков, составляющие признаки которой можно получать на основании субъективного ранжирования признаков на этапе S220. Совокупность признаков может дополнительно содержать любые выделяемые признаки изображения или соответствующие клинические данные, относящиеся к VOI 116 в базе данных. Подходящие критерии сходства могут различаться между собой только в отношении применяемой поточечной дистанционной метрики.
Каждый раз, когда создается новая хромосома воспроизведением в GA, оценивают пригодность хромосомы. Поскольку каждая хромосома представляет соответствующее множество признаков и предпочтительно соответствующую дистанционную метрику и поскольку наиболее пригодную хромосому выбирают, когда удовлетворяется критерий останова, то каждую оценку пригодности хромосомы можно рассматривать как итерацию итеративного процесса. Тогда методом итераций выбирают множество признаков и предпочтительно дистанционную метрику. Вследствие характера предлагаемой оценки пригодности итерации имеют склонность приводить к тому, что объективная группировка в кластеры VOI 116 становится подобной субъективной группировке в кластеры на этапе S220. Критерием, используемым при оценке пригодности, является степень сходства между субъективной группировкой в кластеры и объективной группировкой в кластеры, которая является группировкой в кластеры пространственных точек в пространстве признаков, заданном множеством признаков, содержащихся в текущей хромосоме, пригодность которой оценивают. В предпочтительном варианте хромосома содержит также соответствующую дистанционную метрику, которую предпочтительно применяют при объективной группировке в кластеры.
Одним примером алгоритма, используемого для объективной группировки в кластеры пространственных точек, является алгоритм нечетких c-средних (FCM). Данный критерий сходства является предпочтительным. Такой подход является способом группировки в кластеры, который позволяет одному блоку данных принадлежать, по меньшей мере, двум кластерам. Упомянутый способ часто применяют при распознавании образов. Данный способ основан на минимизации следующей целевой функции:
где m означает любое действительное число больше чем 1, u ij означает степень принадлежности x i кластеру j, при этом x i означает i-е из d-мерных измеренных данных, c j означает d-мерный центр кластера, и означает любую норму, выражающую сходство между любыми измеренными данными и центром. Для начального задания ряда центров C можно воспользоваться рядом кластеров, сформированных методом субъективной группировки в кластеры. Центры c j сначала задают соответственно средним точкам каждого из субъективных кластеров в текущем пространстве признаков, т.е. пространстве признаков, заданном хромосомой, пригодность которой оценивается в данный момент. Применяемая норма является дистанционной метрикой, содержащейся в текущей хромосоме.
В случае если метрика является обобщенным расстоянием (Махаланобиса), то тогда нормированная величина в вышеприведенном уравнении является обобщенным расстоянием между x i и остальными элементами кластера j. Аналогично, при вызове примера осуществляется поиск группы примеров с наименьшим обобщенным расстоянием до VOI 112. Генетический алгоритм для подобного поиска предлагается в заявке № WO 2005073916 на международный патент, поданной 21 января 2005 г. и принадлежащей подателю настоящей патентной заявки.
Нечеткое разделение выполняется посредством итерационной оптимизации вышеприведенной целевой функции, с коррекцией u ij степени принадлежности и центров c j кластеров следующим образом:
Данная итерация остановится, когда , где означает критерий останова, имеющий значение между 0 и 1, а k означает шаги итераций. Данная процедура сходится к локальному минимуму или седловой точке J m.
Алгоритм состоит из следующих шагов:
1. Инициализировать матрицу U=[u ij ], U (0)
2. На k-м шаге: вычислить вектора C (k) =[c j ] центров при U (k)
3. Скорректировать U (k) , U (k+1)
4. Если , то ОСТАНОВ; иначе возврат к шагу 2.
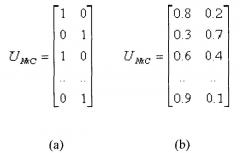
Коэффициенты матрицы U являются числами от 0 до 1, причем данные коэффициенты берут у функции принадлежности. Если все коэффициенты матрицы U равны 0 или 1, то каждый элемент данных может принадлежать только одному кластеру. К такому случаю относится приведенный ниже случай (a). В случае (b) принадлежность является нечеткой.
Число строк и столбцов зависит от того, сколько данных и кластеров рассматривается. Точнее, имеется C=2 столбца (C=2 кластера) и N строк, где C означает общее число кластеров и N означает общее число данных. Поэтому обобщенный элемент обозначен: u ij.
Другие свойства представлены ниже:
Дополнительные сведения о FCM-алгоритме изложены в работе J. C. Dunn (1973): «A Fuzzy Relative of the ISODATA Process and Its Use in Detecting Compact Well-Separated Clusters», Journal of Cybernetics 3: 32-57, и FCM-метод дополнительно разработан в работе J. C. Bezdek (1981): «Pattern Recognition with Fuzzy Objective Function Algorithms», Plenum Press, New York, причем обе упомянутые работы полностью включены в настоящее описание путем отсылки.
Функция пригодности в CADx на базе примеров в соответствии с настоящим изобретением приписывает большую степень пригодности меньшему числу несовпадений в принадлежности к подмножеству, наблюдаемых между объективным и субъективным вариантами группировки в кластеры.
Критерий останова GA может быть заданным числом циклов создания/количественной оценки или достаточно высокой степенью пригодности хромосомы. В момент останова выбирают самую пригодную хромосому, что является также выбором соответствующего множества признаков, содержащихся в хромосоме, и, по желанию, дистанционной метрики, содержащейся в хромосоме.
Окончательно выбранное множество признаков и, по желанию, окончательно выбранная дистанционная метрика вместе составляют параметры, выдаваемые блоком 132 получения параметров для использования модулем 124 вызова примеров. Упомянутое окончательно выбранное множество содержит признаки подлежащего количественной оценке VOI 112 при помещении VOI 112 в пространство признаков (этап S240). Пространство признаков является окончательно выбранным пространством, т.е. пространством признаков, заданным окончательно выбранным множеством признаков. Все VOI 116 предпочтительно также количественно оцениваются для соответствующего размещения в пространстве признаков.
В предпочтительном варианте осуществления, который содержит дистанционную метрику в хромосоме GA, окончательно выбранная дистанционная метрика предпочтительно используется оптимальным поточечным критерием сходства и модулем 124 вызова примеров в процессе вызова примеров 116 из базы данных 120 для отображения на экране (этап S250). Таким образом, вызываются примеры с минимальным расстоянием от VOI 112. Среди дистанционных метрик применимыми являются эвклидово расстояние, расстояние городских кварталов и обобщенное расстояние. В предпочтительном варианте вызванные примеры отображаются вместе с подлежащим диагностированию VOI 112 для визуального сравнения клиницистом (этап S260). Рядом с каждым примером 116 предпочтительно представляется показатель степени сходства примера с VOI 112. Представляемый численный показатель степени сходства основан на расстоянии от VOI 112. Более близкие примеры 116 считаются более сходными, и примеры, разделенные большей дистанцией, считаются менее сходными. Расстояние можно сравнивать с опорным расстоянием для образования метрики и представления ее на экране, например процентного отношения. Один пример 116 может быть сходным на 90%, тогда как другой пример имеет только 80% сходство. Порог может устанавливаться автоматически, например, на основании больничного протокола или может устанавливаться по выбору пользователя, чтобы сходство ниже порога запрещало отображение соответствующего примера 116.
В предпочтительном варианте осуществления экранные примеры могут по отдельности выбираться пользователем, например, с помощью мыши, для получения дополнительной информации. Для каждого из примеров 116 в базе данных 120 клиницист уже поставил диагноз, который предпочтительно подкреплен исходно верной информацией, относящейся к патологии. Исходно верную информацию о патологии получают, например, путем биопсии, другой хирургической процедуры или наблюдения за течением болезни. Для пациента мог быть также составлен прогноз. Кроме того, электронная медицинская карта (EMR), которую ведут в учреждении, предоставляет историю болезни, в которой обычно указаны виды проводимого лечения, например химиотерапевтического или оперативного, и получаемые результат или результаты. Желателен был бы также удобный доступ к подробным сведениям о пациенте. Например, химиотерапия могла не приводить к успешному результату для пожилого пациента; тогда как такое же лечение аналогичной опухоли могло бы быть полезным для пациента моложе возрастом. Один курс терапии мог продлить жизнь пациента, но при сравнительно сниженном качестве жизни. Соответственно, информация о прогнозе, планировании терапии и другие данные о пациенте, получаемые из EMR или другим путем, предпочтительно немедленно доставляются пользователю при осуществлении назначений из меню, с помощью гиперссылок и т.п. и сопровождают представляемый пример 116 (этап S270). В частности, в таком случае представляемый пример предпочтительно может быть выбран пользователем для дополнительного представления прогноза, информации о лечении, вторичной информации, текущего состояния и/или клинической информации, вызываемых из EMR. Если, по меньшей мере, две томограммы одного и того же пациента дают в результате несколько VOI 116 в базе данных 120, то связанная информация, которую вызывают на экран, может иметь несколько связей, где каждая связь относится к соответствующему примеру.
На фиг.3 представлены таблицы, которые можно использовать при субъективной оценке сходства между опухолями VOI 116. Например, клиницисту, собирающему анамнез, может быть представлено 11 VOI 116. Один пример из 11 служит эталоном, и другие десять сравнивают с эталоном.
Таблица 304 сравнения VOI и ранжирования их признаков содержит одну строку для каждого из десяти VOI.
Первый 308 из десяти VOI имеет, по оценке клинициста, сходство с образцом по первому признаку 312. Поэтому в элемент ввода (1, 1) записан символ «S». Сходство обычно оценивают визуально по изображениям VOI 116, хотя некоторые признаки могут быть элементами клинических данных, как упоминалось выше. Аналогично, клиницист оценивает сходство по второму признаку 316, и в элемент (1, 2) ввода вставляется соответствующий символ «S». Клиницист обозначает второй признак 316 как более важный для оценки сходства двух VOI, чем первый признак 312, и соответственно, выше ранжирует второй признак единицей. В общем, из десяти VOI упомянутый первый VOI 308 в строке 1 обозначен рангом один как более сходный с эталоном. Как видно из строки 2, клиницист не сделал вывода о сходстве. Третий VOI 320 был оценен как сходный с эталоном, но клиницист не представил информации о том, какие признаки привели к данной оценке или к общему рангу сходства. Для четвертого VOI 324 указаны три признака, но они не ранжированы по их относительной важности для получения общего ранга сходства. Те же самые исходные данные можно привести в пользу отличия. Таким образом, восьмой VOI 328 оценен как отличающийся от эталона, когда первый признак 312 более важен при проводимой оценке, чем третий признак 330. Процесс сравнения десяти VOI 116 с эталоном повторяют с разными VOI/эталонами для каждой таблицы 304.
В предпочтительном варианте оценки даются разными клиницистами. Цель заключается в получении «исходно верной информации о сходстве/отличии». Иногда клиницист может указать на признаки, которые приводят его к заключению. Однако клиницист может получать заключение без определенного знания причины. Кроме того, получают исходно верную информацию, специфическую для данного последнего случая, как составляющую общей исходно верной информации, отраженной в последующей субъективной группировке в кластеры. В предпочтительном варианте осуществления клиницисту не сообщается о патологическом, т.е. злокачественном или доброкачественном, состоянии VOI 116 или эталона. Данный подход имеет целью недопущение искажения выносимого клиницистом суждения о сходстве. Однако в качестве альтернативы можно сообщать о патологии заранее.
Для сведения к минимуму числа сравнений, на описанной стадии сбора исходных данных можно сделать допущение, что два VOI 116 сходны, если и тот и другой сходны с одним и тем же эталоном. Когда собран достаточный объем информации о сходстве/отличии, дают окончательные оценки о сходстве по парам и затем о группировке в кластеры.
Окончательные оценки о сходстве по парам вводят в таблицу 332 сходства/отличия. Таблица является симметричной матрицей, все диагональные элементы которой указывают на сходство введенным символом «S». Поскольку VOI 336, 340 в третьей и четвертой строках (столбцах) сходны с VOI 344 в первой строке (столбце), то они сходны между собой, как указано символом «S» в элементах (3, 4) и (4, 3) ввода. VOI 348 во второй строке (столбце) отличается от VOI 344, как показано символом «D», введенным в позиции (1, 2) или (2, 1) матрицы. Соответственно, VOI 336, 340, 344 в первой, третьей и четвертой строках находятся в одном кластере, и VOI 348 во второй строке не находится в данном кластере. Знак (?) вопроса в элементе ввода таблицы указывает, что оба соответствующие VOI оцениваются как отличающиеся от общего эталона и что не существует никаких дополнительных оценок, которые указывают на сходство или отличие между двумя VOI. Тщательный выбор VOI 116 для оценки на стадии таблицы 304 сравнения VOI и ранжирования признаков должен свести к минимуму число помеченных вопросами элементов ввода. Помеченные вопросами элементы ввода можно также заменить на базе дополнительно введенных данных от радиолога. В случае если две разные таблицы 304 сравнения VOI и ранжирования признаков конфликтуют в соответствующих оценках сходства/отличия конкретных пар VOI 116, то наличием или отсутствием ранжирования признаков и общим рангом, при его наличии, можно воспользоваться для разрешения конфликта тем или иным путем.
На фиг.4 представлен примерный формат текущей хромосомы 400, подлежащей количественной оценке на пригодность в GA. Хромосома 400 содержит битовую карту 410 признаков и показатель 420 дистанционной метрики. Битовая карта 410 признаков содержит по одному биту на каждый признак в совокупности признаков. Если бит установлен, т.е. равен единице, а не нулю, то признак, соответствующий установленному биту, является одним из признаков в множестве признаков, который содержится в хромосоме 400. Следовательно, если установлено 10 бит, то настоящая хромосома представляет собой 10-мерное пространство признаков, измерения которого являются, каждое, признаками, указанными соответствующим установленным битом. Показатель 420 дистанционной метрики имеет длину, равную наименьшему целому числу, больше (log2(M)) бит, где M равно числу возможных дистанционных метрик, и предельная функция дает наименьшее целое число, больше аргумента. Соответственно, если M=10, то показатель дистанционной метрики имеет длину 4 бита.
Правила GA предпочтительно содержат, в качестве метода объединения, обмен концевыми битами индекса 420 и концевыми битами карты 410. Граничный бит может быть фиксирован или может изменяться случайным образом. Мутация, в качестве другого способа создания, может применяться относительно редко по времени. Для ускорения сходимости к оптимуму ранги признаков в таблице 304 сравнения VOI и ранжирования признаков применяют при установке битов признаков в исходном семействе хромосом.
Выше показаны, описаны и выделены фундаментальные новые признаки изобретения на примере предпочтительных вариантов его осуществления, однако следует понимать, что специалистами в данной области техники могут быть сделаны различные исключения, подстановки и изменения в форме и деталях представленных устройств и их функционировании, без выхода за пределы существа изобретения. Например, пользовательский интерфейс может допускать обозначение весовых коэффициентов признаков для соответствующих дистанционных метрик. Следует понимать, что конструкции, и/или элементы, и/или этапы способа, представленные и/или описанные в связи с любыми раскрытыми формой или вариантом осуществления изобретения, можно включать в любые другие раскрытые, или описанные, или предложенные форму или вариант осуществления, вообще говоря, в зависимости от выбора схемы.
1. Устройство, которое оптимизирует компьютерную диагностику на базе примеров пациента на основе медицинского изображения пациента, содержащее:блок (132) получения параметров, выполненный с возможностью выбора оптимального множества признаков представляющего интерес объема (VOI), по которым вызывают примеры так, чтобы объективная оценка сходства группирования в кластеры представляющих интерес объемов (VOI) происходила (116) в базе данных таким образом, чтобы согласоваться с субъективной оценкой сходства группирования в кластеры VOI в базе данных (S220, S230), причем объективная оценка сходства группирования в кластеры происходит в пространстве признаков, и при этом оптимальное множество признаков специфично для медицинского изображения; имодуль вывода, выполненный с возможностью обеспечения выбранного множества в качестве выходных данных.
2. Устройство по п.1, в котором упомянутый выбор состоит в том, что выбирается оптимальный критерий сходства для применения при вызове примеров (S250).
3. Устройство по п.2, в котором упомянутый выбор состоит в том, что выбирается межточечная дистанционная метрика, которую содержит упомянутый оптимальный критерий сходства, при этом упомянутую метрику применяют при группировании в кластеры, основанном на объективной оценке, в упомянутом пространстве признаков, заданном упомянутыми выбранными признаками (S240).
4. Устройство по п.1, в котором признаки в упомянутом множестве задают упомянутое пространство признаков (S240).
5. Устройство по п.1, в котором упомянутый выбор содержит итерационный выбор множества признаков VOI для получения упомянутого оптимального множества (S230).
6. Устройство по п.5, в котором генетический алгоритм (400) выполняет итерационный выбор.
7. Устройство по п.5, в котором данная итерация выбирает соответствующее множество, которое задает пространство признаков для такой итерации (S230).
8. Устройство по п.1, в котором субъективная оценка содержит распределение VOI в базе данных по упомянутым соответствующим кластерам на основе восприятия во время попарных сравнений упомянутых модулей базы данных (S210).
9. Устройство по п.1, в котором среди упомянутых признаков содержится признак изображения VOI из упомянутых VOI (S230).
10. Устройство по п.9, в котором среди упомянутых признаков содержатся клинические данные, относящиеся к VOI из упомянутых VOI (S230).
11. Система компьютерной диагностики на базе примеров, содержащая устройство по п.1, при этом упомянутая система дополнительно содержит:базу данных (120), выполненную с возможностью содержать представляющие интерес объемы (VOI);модуль вызова (124), соединенный с возможностью обмена информацией с упомянутым модулем вывода и выполненный с возможностью количественно оценивать на основе выбранного множества представляющий интерес объем (VOI) (116), подлежащий диагностированию, и для выполнения на основе результата упомянутой количественной оценки выполненный с возможностью вызывать упомянутые примеры из упомянутой базы данных, содержащей VOI; идисплей (108), выполненный с возможностью визуального представления вызванных примеров.
12. Система компьютерной диагностики на базе примеров по п.11, дополнительно содержащая пользовательский блок (134) управления и процессор, выполненный с возможностью инициировать визуальное представление на упомянутом дисплее вызванных примеров и для одного визуально представленного примера из упомянутых вызванных примеров, выбранного с помощью упомянутого пользовательского блока управления, по меньшей мере, одного из прогноза, информации о лечении, вторичной информации, текущего состояния и клинической информации, вызываемых из электронной медицинской карты (EMR)(S260).
13. Компьютерно-читаемый носитель информации, воплощающий компьютерную программу, содержащую команды, исполняемые процессором для выполнения множества операций для компьютерной диагностики на базе примеров, при этом упомянутое множество содержит операции, при которых осуществляют:выбор оптимального множества признаков представляющего интерес объема (VOI), по которым так вызывают примеры, чтобы объективная оценка сходства, основанная на выбранных признаках, кластерах в пространстве признаков, VOI в базе данных, согласовалась с группированием в кластеры VOI в базе данных в соответствующие кластеры посредством субъективной оценки сходства (S230); иобеспечение выбранного множества в качестве выходных данных (S260).
14. Компьютерно-реализуемый способ оптимизации компьютерной диагностики на базе примеров, при этом способ содержит этапы, на которых:группируют представляющие интерес объемы (VOI) в базе данных в соответствующие кластеры согласно субъективной оценке сходства (S220); ивыбирают оптимальное множество признаков представляющего интерес объема (VOI), по которым так вызывают примеры, чтобы объективная оценка сходства, основанная на выбранных признаках, кластерах в пространстве признаков, VOI в базе данных, согласовывалась с упомянутым группированием в кластеры, причем выбор осуществляется генетическим алгоритмом, который итеративно выбирает множество признаков VOI для получения упомянутого оптимального множества (S230).
15. Способ по п.14, дополнительно содержащий этап, на котором используют при вызове примеров оптимальный критерий сходства, который выбирает упомянутый этап выбора (S250).
16. Способ по п.15, в котором упомянутый этап выбора заключается в том, что выбирают межточечную дистанционную метрику, которую содержит упомянутый оптимальный критерий сходства, при этом упомянутую метрику используют при группировании в кластеры, основанном на объективной оценке, в упомянутом пространстве признаков, заданном упомянутыми выбранными признаками (S230).
17. Способ по п.14, в котором признаки в упомянутом множестве задают упомянутое пространство признаков (S240).
18. Способ по п.14, в котором данная итерация заключается в том, что выбирают соответствующее множество, которое задает пространство признаков для такой итерации (S240).
19. Способ по п.14, в котором выполнение субъективной оценки содержит распределение VOI в базе данных по упомянутым соответствующим кластерам на основе восприятия во время попарных сравнений упомянутых модулей базы данных (S210, S220).
20. Способ по п.14, в котором среди упомянутых признаков содержится признак изображения VOI из упомянутых VOI (S230).
21. Способ по п.20, в котором среди упомянутых признаков содержатся клинические данные, относящиеся к VOI из упомянутых VOI (S230).