Защитные композиции от ишемии/реперфузии и способы применения
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к защитным композициям от ишемии/реперфузии, содержащим по меньшей мере одно кетоновое тело, выбранное из β-гидроксибутирата, ацетоацетата и их фармацевтически приемлемых солей и мелатонина. Изобретение также предоставляет способы применения таких композиций для уменьшения или предотвращения ишемического/реперфузионного нарушения в результате потери крови, апоплектического удара или кардиопульмонального шока или хирургического вмешательства. 6 н. и 37 з.п. ф-лы, 6 пр., 4 табл., 32 ил.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка заявляет приоритет патентной заявки США No 60/911460, поданной 12 апреля 2007 года, и No 61/026321, поданной 5 февраля 2008 года, раскрытия которых включены в описание в полном объеме.
ИССЛЕДОВАНИЯ ИЛИ РАЗРАБОТКИ, ПОДДЕРЖАННЫЕ НА ФЕДЕРАЛЬНОМ УРОВНЕ
Правительство США имеет определенные права на данное изобретение в соответствии с грантом No. W911NF-05-1-0432 и W911NF-06-1-0088, выделенным Управлением перспективных исследовательских проектов министерства обороны США (DARPA).
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к ишемическому повреждению и реперфузионному нарушению, а конкретнее к композициям и способам лечения или предупреждения нарушения и повреждения вследствие ишемии и/или реперфузии. Ишемия и/или реперфузионное нарушение могут возникнуть в результате, например, геморрагического шока.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Ишемия обычно представляет собой ограничение кровоснабжения, с вытекающим повреждением или нарушением функции ткани. Ишемия относиться к полному или относительному недостатку кровоснабжения органа. Относительный недостаток кровоснабжения означает рассогласование кровоснабжения (доставки кислорода) и необходимости в адекватной оксигенации ткани.
Реперфузионное нарушение относится к повреждению, причиненному ткани, когда кровоснабжение восстанавливается в ткани после периода ишемии. Отсутствие кислорода и питательных веществ из крови создает условия, при которых восстановление циркуляции приводит к воспалению и окислительному или перокислительному повреждению.
КРАТКОЕ ОПИСАНИЕ
Одно или более кетоновых тел и мелатонин можно вводить индивидууму для защиты индивидуума от ишемического повреждения и/или реперфузионного нарушения.
В одном аспекте изобретение предоставляет защитную композицию от ишемии/реперфузии. Защитная композиция от ишемии/реперфузии содержит или состоит в основном из одного или нескольких кетоновых тел и мелатонина. Одно или более кетоновых тел могут представлять собой, например, D-β-гидроксибутират или его фармацевтически приемлемую соль (напр., Na-D-β-гидроксибутират), ацетоацетат или его фармацевтически приемлемую соль, или D-β-гидроксибутират и ацетоацетат в комбинации. Мелатонин может представлять собой, например, 5-метокси-N-ацетилтриптамин. В некоторых вариантах осуществления композиция в значительной степени свободна от неорганических анионов.
В некоторых вариантах осуществления защитная композиция от ишемии/реперфузии представляет собой жидкую композицию. В случае составления в виде жидкости защитная композиция от ишемии/реперфузии может содержать от около 0,1 M до около 8 M кетоновых тел и от около 4 мкМ до около 150 мМ мелатонина. В одном конкретном варианте осуществления защитная композиция от ишемии/реперфузии может содержать около 4 M Na-D-β-гидроксибутирата и около 43 мМ мелатонина. В некоторых вариантах осуществления защитная композиция от ишемии/реперфузии в значительной степени свободна от Cl-. В определенных вариантах осуществления жидкой композиции растворитель представляет собой воду. В некоторых вариантах осуществления жидкая композиция включает солюбилизатор (например, ДМСО) и/или стабилизатор.
В других вариантах осуществления защитная композиция от ишемии/реперфузии представляет собой сухую порошковую композицию. При составлении в качестве сухого порошка защитная композиция от ишемии/реперфузии может иметь молярное соотношение кетоновых тел к мелатонину от около 100 до 1.
Такие защитные композиции от ишемии/реперфузии могут дополнительно включать один или более антибиотиков, одну или более свободных жирных кислот, одно или более анальгетических веществ, один или более гормонов, один или более метаболитов, одну или более молекул обмена веществ, и/или одно или более соединений, которые изменяют клеточный метаболизм (например, полипептиды, молекулы антисмысловых РНК или сиРНК, лекарственные средства или малые молекулы).
В одном аспекте изобретение предоставляет изделие, которое включает защитную композицию от ишемии/реперфузии. В одном варианте осуществления изделие может представлять собой IV-упаковку, содержащую защитную композицию от ишемии/реперфузии (например, жидкий состав или сухой порошковый состав). В другом варианте осуществления изделие может включать первый и второй флакон, где первый флакон может содержать защитную композицию от ишемии/реперфузии и второй флакон может содержать растворитель. В таком варианте осуществления изделие можно скомпоновать таким образом, что растворитель второго флакона можно контролируемым образом приводить в контакт с композицией первого флакона. В другом варианте осуществления изделие включает цилиндр шприца, который содержит защитную композицию от ишемии/реперфузии. В еще одном варианте осуществления изделие может включать упаковочный материал и защитную композицию от ишемии/реперфузии, где упаковочный материал может включать этикетку или вкладыш в упаковку, содержащий инструкции для лечения индивидуума, который испытывает или перенес кровопотерю, который испытывает или перенес удар или который готовится подвергнуться или подвергается медицинской процедуре (например, хирургическому вмешательству).
В другом аспекте изобретение предоставляет способы лечения индивидуума, который испытывает или перенес кровопотерю. Такие способы включают введение одного или нескольких кетоновых тел и мелатонина индивидууму. В некоторых вариантах осуществления одно или более кетоновых тел и мелатонин вводят совместно в единой композиции. В определенных вариантах осуществления индивидуум, нуждающийся в лечении, имеет уровни StO2, которые составляют менее чем 75%. Как правило, стадия введения приводит к возвращению уровней StO2 индивидуумов к величине более чем 75%, которая является характерной для индивидуума, подвергавшегося лечению. В определенных вариантах осуществления индивидуум, нуждающийся в лечении, имеет уровни лактата, которые выше чем 2,1 мг/дл. Обычно стадия введения приводит к возвращению уровней лактата индивидуумов к величине меньшей чем 2,1 мг/дл, которая является характерной для индивидуума, подвергавшегося лечению. Обычно стадия введения предотвращает достижение дефицита основания у индивидуума величины 6 мЭк/л.
В определенных вариантах осуществления индивидуум испытывает или перенес обширное геморрагическое событие (например, индивидуум потерял объем крови, по меньшей мере, около 10%, по меньшей мере, около 20%, по меньшей мере, около 30%, по меньшей мере, около 40%, по меньшей мере, около 50% или, по меньшей мере, около 60%). В некоторых вариантах осуществления кровопотеря у индивидуума приводит к систолическому давлению крови около 70 мм рт. ст. (например, 65 мм рт.ст., 60 мм рт.ст.) или менее. В определенных вариантах осуществления одно или более кетоновых тел вводят индивидууму в количестве, достаточном для достижения концентрации в крови от около 3 мМ до около 15 мМ, и мелатонин вводят индивидууму в количестве, достаточном для достижения концентрации в крови от около 20 мкМ до около 150 мкМ. В определенных вариантах осуществления одно или более кетоновых тел и мелатонин вводят в объеме от около 0,3 до около 2 миллилитров (мл) на килограмм (кг) массы индивидуума. В определенных вариантах осуществления одно или более кетоновых тел и мелатонин вводят в объеме от около 0,3 до около 2 мл на кг массы индивидуума в час. В определенных вариантах осуществления одно или более кетоновых тел и мелатонин вводят в объеме от около 0,3 до 2 мл на кг массы индивидуума, после чего следует введение одного или нескольких кетоновых тел и мелатонина в объеме от около 0,3 до 2 мл на кг массы тела индивидуума в час. Типичными способами введения одного или нескольких кетоновых тел и мелатонина являются внутривенный и внутрикостный.
В другом аспекте изобретение предоставляет способ лечения индивидуума, уровни StO2 которого находятся ниже 75%, и/или который обладает уровнем дефицита основания выше чем 6 мЭк/л, включающий выявление такого индивидуума, уровни StO2 которого находятся ниже 75% или уровень дефицита основания которого выше чем 6 мЭк/L; и введение одного или нескольких кетоновых тел и мелатонина индивидууму.
В еще одном аспекте изобретение предоставляет способы защиты индивидуума от ишемического повреждения или реперфузионного нарушения. Такие способы обычно включают введение одного или нескольких кетоновых тел и мелатонина индивидууму. Характерные индивидуумы - те, кто получил удар или рискует получить удар, те, кому предстоит подвергнуться хирургическому вмешательству (например, нейрохирургическому). В некоторых вариантах осуществления одно или более кетоновых тел и мелатонин вводят в количестве 1 мл на кг массы индивидуума. В определенных вариантах осуществления такое введение может следовать за медленной инфузией одного или нескольких кетоновых тел и мелатонина.
В еще одном аспекте изобретение предоставляет способы лечения органа перед изъятием органа у донора органа. Такие способы обычно включают введение одного или нескольких кетоновых тел и мелатонина донору органа (например, внутривенно). Посредством примера, одно или более кетоновых тел и мелатонин можно вводить донору органа в количестве, по меньшей мере, около 1 мл на кг массы донора органа. В определенных случаях донор органа находится в устойчивом вегетативном состоянии.
Если не указано особо, все используемые технические и научные термины имеют то же значение, которое обычно подразумевает любой специалист в области, к которой данное изобретение относится. Хотя способы и материалы, сходные или эквивалентные описанным способам и материалам, можно использовать на практике или при проверке настоящего изобретения, применимые способы и материалы описаны ниже. Кроме того, материалы, способы и примеры носят лишь иллюстративный характер и не являются ограничивающими. Все отмеченные в описании публикации, патентные заявки, патенты и другие ссылки или ссылочные материалы включены в качестве ссылки во всей полноте. В случае конфликта настоящую спецификацию, включая определения, следует считать регулирующей.
Подробные описания одного или нескольких вариантов осуществления изобретения изложены в прилагаемых ниже чертежах и описании. Другие характеристики, предметы и преимущества изобретения станут очевидными из чертежей и подробного описания и из пунктов формулы изобретения.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
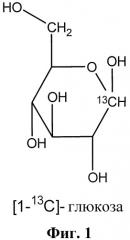
Фигура 1 демонстрирует структуру [1-13C]глюкозы.
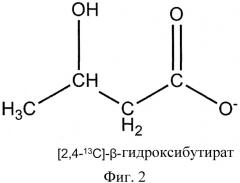
Фигура 2 демонстрирует структуру [2,4-13C]D-β-гидроксибутирата.
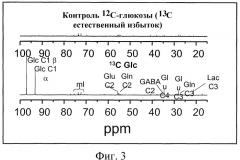
Фигура 3 представляет собой кривую, демонстрирующую базовые уровни 13C-глюкозы в мозге.
Фигура 4 представляет собой меченый спектр выбранных метаболитов земляных белок в состоянии спячки, проанализированный на спектрофотометре 14,1 Tesla UNITY INOVA (Varian; Palo Alto, CA). Панель A демонстрирует результаты после IP-инъекции 1 мл 1 M 13C BHB февральскому животному в состоянии спячки (Tb=16,8°C в момент умерщвления). Панель B демонстрирует результаты после IP-инъекции 1 мл 1 M 13C-глюкозы декабрьскому животному в состоянии спячки (Tb=35,3°C в момент умерщвления). Значения в обеих панелях были нормированы на два естественным образом меченых пика 13C-таурина, которые не менялись при инфузии метки и могли быть использованы для определения концентрации других соответствующих метаболитов. Сокращения отражают обозначенные метаболиты и специфически меченые углеродом: Tau C1, таурин C1; BHB C2, β-гидроксибутират C2; Tau C2, таурин C2; GLu C4, глутамат C4; BHB C4, β-гидроксибутират C4; Lac C3, лактат C3; Glc C1-α, глюкоза C1 α; Glc C1-β, глюкоза C1 β.
Фигура 5 демонстрирует результаты иммуноцитохимического анализа транспортера монокарбоксилата 1 (MCT1) и транспортера глюкозы (GLUT1) в мозге крысы и земляной белки (GS).
Фигура 6 демонстрирует повышенные уровни MCT1 в гемоэнцефалическом барьере находящихся в спячке земляных белок, на основании иммуноцитохимического анализа.
Фигура 7 демонстрирует повышенные уровни MCT1 в гемоэнцефалическом барьере по оптической плотности MCT1 в кровеносных сосудах во время состояния зимней спячки (HIB) и в августе (AUG), октябре (OCT) и апреле (APR).
Фигура 8 демонстрирует 2-мерные гели полипептидов из сердец от активных и находящихся в спячке земляных белок. 1, легкая цепь 1 вентрикулярного миозина (n.c, act, n=5; hib, n=4); 2, сукцинил-CoA трансфераза (6-кратное увеличение, * = p<0,005).
Фигура 9 демонстрирует временную шкалу экспериментов с сильными травмами. Кровь отбирали в помеченные буквами моменты времени (A-J).
Фигура 10 демонстрирует график уровней β-гидроксибутирата в сыворотке после введения 1 мл 4 M D-BHB или 4 M NaCl на кг массы крысы. Образцы подсчитывали в трех повторностях для минимизирования ошибки отмеривания пипеткой, и значения представлены в миллимолярных концентрациях. Планки погрешностей представляют собой стандартные погрешности среднего.
Фигура 11 демонстрирует график уровней β-гидроксибутирата в сыворотке после введения 1 мл/кг с последующей инфузией в 100 мкл/час. Образцы подсчитывали в трех повторностях для минимизирования ошибки отмеривания пипеткой, и значения представлены в миллимолярных концентрациях. Планки погрешностей представляют собой стандартные погрешности среднего.
Фигура 12 представляет собой график, демонстрирующий эффект поддержания температуры (левый столбец) против гиповолемического охлаждения (правый столбец) на выживаемость после геморрагического шока. Планки погрешностей представляют собой стандартные погрешности среднего.
Фигура 13 демонстрирует эффекты различных схем введения на выживаемость после геморрагического шока. Планки погрешностей представляют собой стандартные погрешности среднего.
Фигура 14 демонстрирует кривую выживаемости Kaplan-Meyer крысы, получившей указанное лечение в сочетании с 60%-ой потерей крови в течение одного часа. Через один час после 60%-ой потери крови пролитую кровь возвращали и контролировали выживаемость животных. Фиктивных животных анестезировали и катетизировали, но кровь не отбирали.
Фигура 15 представляет собой график, демонстрирующий эффект указанного лечения на частоту пульса.
Фигура 16 представляет собой график, демонстрирующий эффект указанного лечения на среднее артериальное давление крови.
Фигура 17 представляет собой график, демонстрирующий эффект указанного лечения на температуру тела.
Фигура 18 демонстрирует стратегию реанимации после геморрагического шока у свиней. SBP = систолическое давление крови; UO = диурез; Hgb = гемоглобин.
Фигура 19 демонстрирует кривые выживаемости Kaplan-Meyer для групп крыс, которые испытали 60%-ную потерю крови и которым вводили либо защитную композицию от ишемии/реперфузии, содержащую 4M D-BHB и 43 мМ мелатонина (4M D-BHB+M), либо контрольный раствор, содержащий 4M D-BHB, 4M NaCl, или 4M NaCl плюс 43 мМ мелатонина (4M NaCl + M). Фиктивных животных (SHAM) не подвергали потере крови, кроме как при отборе образцов крови, но с ними проводили анестезию, катетеризировали и давали возможность восстановления в течение того же количества времени, что и животным в других группах. Возвращение крови = время, через которое пролитую кровь возвращали; 18 часов, 24 часов, 48 часов, 72 часов, 96 часов и 10 дней = 18 часов, 24 часов, 48 часов, 72 часов, 96 часов и 10 дней после возвращения пролитой крови соответственно. Временные точки на оси х представлены не в масштабе.
Фигура 20 представляет собой график, изображающий средние уровни лактата, определенные в различных временных точках в сыворотке от крысы, которая испытала 60%-ную потерю крови и которой вводили либо защитную композицию от ишемии/реперфузии, содержащую D-BHB и мелатонин (4M D-BHB+M), либо контрольный раствор, содержащий 4M D-BHB, 4M NaCl, или 4M NaCl плюс мелатонин (4M NaCl + M). В каждой группе лечения было 10 животных. Фиктивных животных (SHAM) не подвергали потере крови, кроме как при отборе образцов крови, но с ними проводили анестезию, катетеризировали и давали возможность восстановления в течение того же количества времени, что и животным в других группах. До гипотензии = перед потерей крови; 35 мм рт. ст. = около 40% потери крови; Инф посл раст = инфузия после раствора; 60% BL = 60% потери крови; 1 ч после 60% BL = один час после 60%-ой потери крови; возвращение крови = время, через которое пролитую кровь возвращали.
Фигура 21 представляет собой график, изображающий уровни D-BHB (мМ), определенные в многочисленных временных точках в сыворотке от свиней, которые испытали потерю крови и которым вводили низкую, среднюю или высокую дозы защитной композиции от ишемии/реперфузии, содержащий D-BHB плюс мелатонин. Уровни D-BHB в сыворотке контрольных свиней также представлены на графике. Shk 30, 60, 90 = 30, 60 и 90 минут после шока соответственно. 1 Hr, 2Hr, 4 Hr, 6 Hr и 8 Hr = 1, 2, 4, 6 и 8 часов после начала реанимации соответственно. Левая и правая вертикальные линии показывают начало и окончание соответственно введения жидкости.
Фигура 22 представляет собой график, изображающий средние уровни лактата (ммоль/л), определенные в различных временных точках в сыворотке от свиней, которые испытали потерю крови и подвергшиеся лечению защитной композицией от ишемии/реперфузии или контрольным раствором. Shk 30, Shk 60 и Shk 90 = 30, 60 и 90 минут после шока соответственно. 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно. Левая и правая вертикальные линии показывают начало и окончание соответственно, введения жидкости.
Фигура 23 представляет собой график, изображающий значения дефицита/избытка основания (моль/л) в многочисленных временных точках у свиней, которых подвергли геморрагическому шоку и подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором. Start = момент времени, когда начался протокол геморрагического шока; Shk 30, Shk 60 и Shk 90 = 30, 60 и 90 минут после шока соответственно; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно.
Фигура 24 представляет собой график, изображающий значения pH, определенные в некоторых временных точках в сыворотке от свиней, которых подвергли геморрагическому шоку и подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором. Start = момент времени, когда начался протокол геморрагического шока; Shk 30, Shk 60 и Shk 90 = 30, 60 и 90 минут после шока соответственно; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации, соответственно.
Фигура 25 представляет собой график, изображающий перфузию периферийной ткани (StO2; %), определенную в некоторых временных точках у свиней, которых подвергли геморрагическому шоку и подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором. End Sx = стабилизация животных перед шоком; Start = начало протокола геморрагического шока; Infusion = начало инфузии защитной композиции от ишемии/реперфузии или контрольного раствора; Shock 30 = 30 минут после шока; End Shock = момент времени, при котором систолическое давление составляло около 50 мм рт. ст.; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно. Левая и правая вертикальные линии показывают начало и окончание, соответственно, инфузии защитной композиции от ишемии/реперфузии или контрольного раствора.
Фигура 26 представляет собой график, изображающий доставку кислорода (мл O2 в минуту) в некоторых временных точках у свиней, которых подвергли геморрагическому шоку и которым вводили защитную композицию от ишемии/реперфузии или контрольный раствор. Start = момент времени, когда начался протокол геморрагического шока; Shk 30, Shk 60 и Shk 90 = 30, 60 и 90 минут после шока соответственно; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно.
Фигура 27 представляет собой график, изображающий общие объемы отобранной крови и жидкостей, введенных свиньям, которых подвергли геморрагическому шоку и которых подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором.
Фигура 28 представляет собой график, изображающий жидкости, введенные (мл/кг) в многочисленных временных точках свиньям, которых подвергли геморрагическому шоку и которым вводили защитную композицию от ишемии/реперфузии или контрольный раствор. OR Fluids - операционные жидкости; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно.
Фигура 29 представляет собой график, изображающий сердечный выброс (л/минуту) в нескольких временных точках у свиней, которых подвергли геморрагическому шоку и которых подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором. Start = момент времени, когда начался протокол геморрагического шока; Shk 30, Shk 60 и Shk 90 = 30, 60 и 90 минут после шока соответственно; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно.
Фигура 30 представляет собой график, изображающий частоту пульса (ударов/минуту) в нескольких временных точках у свиней, которых подвергли геморрагическому шоку и которых подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором. Start = момент времени, когда начался протокол геморрагического шока; Болюс = время, при котором болюс был введен; Shk 30 = 30 минут после шока; Resus = реанимация; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно. Левая и правая вертикальные линии показывают начало и окончание, соответственно, инфузии защитной композиции от ишемии/реперфузии или контрольного раствора.
Фигура 31 представляет собой график, изображающий систолическое давление крови (мм рт.ст.) в многочисленных временных точках у свиней, которых подвергли геморрагическому шоку и которых подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором. End Sx = стабилизация животных перед шоком; Start = момент времени, когда начался протокол геморрагического шока; Болюс = время, при котором болюс был введен; Шок 30 = 30 минут после шока; End Shk = время окончания шока; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно. Левая и правая вертикальные линии показывают начало и окончание, соответственно, инфузии защитной композиции от ишемии/реперфузии или контрольного раствора.
Фигура 32 представляет собой график, изображающий диурез (мл/кг/час), определенный в многочисленных временных точках у свиней, которых подвергли геморрагическому шоку и которых подвергали лечению защитной композицией от ишемии/реперфузии или контрольным раствором. Start = момент времени, когда начался протокол геморрагического шока; Shk 30, Shk 60 и Shk 90 = 30, 60 и 90 минут после шока соответственно; 1 Hr, 2 Hr, 3 Hr, 4 Hr, 5 Hr, 6 Hr, 7 Hr и 8 Hr = 1, 2, 3, 4, 5, 6, 7 и 8 часов после реанимации соответственно. Левая и правая вертикальные линии показывают начало и окончание, соответственно, инфузии защитной композиции от ишемии/реперфузии или контрольного раствора.
ПОДРОБНОЕ ОПИСАНИЕ
Одно или более кетоновых тел и мелатонин можно вводить индивидууму для защиты индивидуума от ишемического повреждения и/или реперфузионного нарушения. Одно или более кетоновых тел и мелатонин можно вводить индивидууму, испытывающему или испытавшему кровопотерю, переносящему или перенесшему удар или кардиопульмональный шок или готовящемуся к или подвергаемому хирургическому вмешательству. Кроме того, одно или более кетоновых тел и мелатонин можно вводить донору органа до изъятия с тем, чтобы тщательно опрыскивать ткань или орган перед изъятием.
Защитные композиции от ишемии/реперфузии
Это раскрытие предоставляет композиции, которые включают одно или более кетоновых тел и мелатонин. Эти композиции представляют собой жидкости для защиты от ишемии/реперфузии, которые могут защищать ткани, органы и, таким образом, индивидуумов от значительных травм. Раскрытые в описании композиции могут включать одно или более кетоновых тел и мелатонин, и могут включать другие компоненты, такие как, например, терапевтические соединения, некоторые из которых описаны ниже. Раскрытые в описании композиции могут «состоять в основном из» одного или нескольких кетоновых тел и мелатонина, подразумевая, что такие композиции представляют собой преимущественно одно или более кетоновых тел и мелатонин, но могут содержать другие компоненты, присутствующие в композиции, которые по существу или фактически не ослабляют защитные характеристики композиции от ишемии/реперфузии.
«Кетоновые тела», как используют здесь, относится к β-гидроксибутирату или ацетоацетату (или физиологически приемлемым солям β-гидроксибутирата или ацетоацетата). Кетоновые тела представляют собой природные вещества, образуемые в результате распада жирных кислот и используемые тканями в качестве источника энергии. Ацетоацетат образуется из ацетил CoA, и β-гидроксибутират образуется путем обратимого восстановления ацетоацетата. Физиологически соотношение гидроксибутирата к ацетоацетату зависит от соотношения NADH/NAD+ внутри клетки. Как используют здесь в отношении защиты от ишемии/реперфузии, термин «кетоновые тела» относится к β-гидроксимасляной кислоте или ее фармацевтически приемлемой соли или ацетоуксусной кислоте или ее фармацевтически приемлемой соли или любым их комбинациям. Термин «фармацевтически приемлемая соль» относится к солям, которые обладают профилями токсичности в диапазоне, который предусматривает применение в фармацевтических заявках. Если отчетливо не указано иначе, ссылку в спецификации на β-гидроксибутират или ацетоацетат следует понимать как охватывающие солевые формы соединения, вне зависимости от четкой обозначенности этого.
Подходящие фармацевтически приемлемые кислотно-аддитивные соли можно получить при помощи неорганической кислоты или органической кислоты. Примеры неорганических кислот включают соляную, бромистоводородную, йодистоводородную, азотную, карбоновую, серную и фосфорную кислоты. Соответствующие органические кислоты можно выбрать из алифатического, циклоалифатического, ароматического, аралифатического, гетероциклического, карбонового и сульфонового классов органических кислот, примеры которых включают муравьиную, уксусную, пропионовую, янтарную, гликолиевую, глюконовую, молочную, яблочную, виннокаменную, лимонную, аскорбиновую, глюкуроновую, малеиновую, фумаровую, пировиноградную, аспарагиновую, глутаминовую, бензойную, аминобензойную, 4-гидроксибензойную, фенилуксусную, миндальную, эмбоновую (памовую), метансульфоновую, этансульфоновую, бензолсульфоновую, пантотеновую, трифторметансульфоновую, 2-гидроксиэтансульфоновую, p-толуолсульфоновую, сульфаниловую, циклогексиламиносульфоновую, стеариновую, альгиновую, β-гидроксимасляную, салициловую, галактаровую и галактуроновую кислоту.
Подходящие фармацевтически приемлемые основно-аддитивные соли включают, например, соли металлов, включая соли щелочных металлов, щелочноземельных металлов и металлов переходной валентности, такие как, например, соли кальция, магния, калия, натрия и цинка.
Фармацевтически приемлемые основно-аддитивные соли могут также включать органические соли, полученные из основных аминов, таких как, например, N,N'-дибензилэтилендиамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглюмин (N-метилглюкамин) и прокаин.
Каждую из этих солей можно получить общепринятыми способами из β-гидроксибутирата или ацетоацетата путем реакции, например, соответствующей кислоты или основания с β-гидроксибутиратом или ацетоацетатом. Предпочтительно соли находятся в кристаллическом виде и предпочтительно готовятся путем кристаллизации соли из приемлемого растворителя. Специалистам в данной области должно быть известно, как получать и выделять приемлемые солевые формы, например, как описано в Handbook of Pharmaceutical Salts: Properties, Selection, and Use By P. H. Stahl and C. G. Wermuth (Wiley- VCH 2002).
Соль β-гидроксимасляной кислоты и/или ацетоуксусной кислоты обычно является предпочтительной в защитной композиции от ишемии/реперфузии, поскольку композиция должна быть ближе к физиологически приемлемому pH, чем при использовании кислоты. Приемлемая соль β-гидроксимасляной кислоты для использования в защитной композиции от ишемии/реперфузии представляет собой натриевую соль D-β-гидроксибутирата (т.е. Na-D-β гидроксибутират). D-β-гидроксимасляную кислоту и ацетоуксусную кислоту (или их фармацевтически приемлемые соли) можно приобрести коммерчески от ряда компаний, таких как, например, Sigma Chemical Co. (St. Louis, MO). Следует отметить, что 'D'-стереоизомер β-гидроксибутирата, временами называемый 'R'-стереоизомером, является предпочтительным в описанной защитной композиции от ишемии/реперфузии, в противоположность 'L'-стереоизомеру.
Мелатонин (5-метокси-N-ацетилтриптамин) представляет собой гормон, который в природе синтезируется из аминокислоты триптофана посредством синтеза из серотонина, и хорошо известен по его вовлечению в циркодианный ритм (особенности сна-бодрствования). Мелатонин действует как антиоксидант широкого спектра и проявляет рецептор-независимую активность удалять свободные радикалы. Способность мелатонина удалять свободные радикалы распространяется на его вторичные, третичные и четвертичные метаболиты, так что взаимодействие мелатонина с реакционноспособными видами кислорода и азота является длительным процессом каскадного типа, в который вовлечены многие из его метаболитов. Таким образом, метаболиты, ближайшие предшественники или аналоги мелатонина (или их комбинации) можно использовать в защитной композиции от ишемии/реперфузии, как описано здесь. Характерные метаболиты мелатонина включают, например, 6-гидроксимелатонин (6-HMEL), 6-сульфатоксимелатонин (aMT6s), N1-ацетил-N2-формил-5-метоксикинурамин (AFMK), N1-ацетил-S-метоксикинурамин (AMK), и 3-гидроксимелатонин (3-HMEL); характерные ближайшие предшественники мелатонина включают, например, N-ацетилсеротонин, 5-гидрокситриптамин, 5-гидрокситриптофан или L-триптофан; и характерные аналоги мелатонина включают, например, 2-хлормелатонин, 6-фтормелатонин, 6-хлормелатонин, 6-гидроксимелатонин, N-изобутаноил-5-метокситриптамин, N-валероил-5-метокситриптамин, 6-метоксимелатонин, 5-метил-N-ацетилтриптамин, 5-бензоил-N-ацетилтриптамин, O-ацетил-5-метокситриптамин, N-ацетилтриптамин, N-ацетил-5-гидрокситриптамин и 5-метокситриптамин. Несмотря на отсутствие связи путем какого-либо конкретного механизма, мелатонин, метаболиты мелатонина, предшественники или аналоги или функционально сходные малые молекулы могут оказывать свои эффекты через посредство рецептор-обусловленного пути (например, через мелатониновый рецептор 1A (MTNR1A) или мелатониновый рецептор 1B (MTNR1B)), через это содействуя описанной защите от ишемии/реперфузии. Как показано здесь, ссылку в спецификации на мелатонин или метаболиты мелатонина, предшественники или аналоги следует понимать так, что включены солевые формы, если не указано особо.
В дополнение к или вместо мелатонина или метаболитов мелатонина, предшественников или аналогов защитная композиция от ишемии/реперфузии может включать один или более других антиоксидантов. Характерные антиоксиданты включают, без ограничения, ресвератрол, витамин A, аскорбиновую кислоту (витамин C), α-токоферол (витамин E), глутатион, β-каротин, ликопен и/или 4-гидрокси-2,2,6,6-тетраметилпиперидин-N-оксил (TEMPOLTM). Далее, поскольку мелатонин представляет собой антиоксидант - производное триптофана, производные других аминокислот, которые обладают антиоксидантной активностью (например, цистеин, например, (R)-2-ацетамидо-3-меркаптопропионовая кислота (N-ацетилцистеин) или синтетическое производное цистеина, 2-[(2-метил-2-сульфонилпропаноил)амино]-3-сульфонилпропионовая кислота (Bucillamine)), также могут подходить для использования в защитных композициях от ишемии/реперфузии.
Описанную защитную композицию от ишемии/реперфузии можно составить, например, в виде жидкости, которая готова к использованию, или в виде сухого порошка, который необходимо развести или ресуспендировать перед использованием. При составлении в качестве сухого порошка защитная композиция от ишемии/реперфузии может иметь любое количество в диапазоне от менее чем одного моля до 1×107 молей или более кетоновых тел на каждый моль мелатонина или метаболита мелатонина, предшественника или аналога мелатонина (например, (0,67-10000000): 1). Соотношение кетоновых тел к мелатонину от около 100 до около 1 представлено здесь в качестве примера, однако защитная композиция от ишемии/реперфузии может содержать больше или меньше кетоновых тел или больше или меньше мелатонина (или метаболита, предшественника или аналога мелатонина). Характерные молярные соотношения кетоновых тел к мелатонину или метаболиту мелатонина, предшественнику или аналогу в защитной композиции от ишемии/реперфузии могут составлять, например, соотношение около 1:1, 5:1, 10:1, 25:1, 50:1, 100:1, 200:1, 500:1, 800:1, 1000:1, 2000:1, 4000:1, 6000:1, 8000:1, 10000:1, 50000:1, 75000:1, 100000:1, 250000:1, 500000:1, 750000:1, 1×106:1, 1,13×106:1, 1,27×106:1, 1,35×106:1, 1,44×106:1, 1,5×106:1, 1,62×106:1, 1,76×106:1, 1,89×106:1, 1,97×106:1, 2,11×106:1, 2,33×106:1, 2,5×106:1, 3,5×106:1, 4,2×106:1, 5,4×106:1, 6,7×106:1, 7,3×106:1, 8,8×106:1, 9,1×106:1, или 1×107:1). Специалист должен понимать, что данные соотношения предназначены просто, чтобы быть образцовыми.
При составлении в качестве жидкости композиция может содержать от около 0,1 M до около 8 M кетоновых тел (например, от около 0,4 M до 0,5 M, от 0,4 M до 0,6 M, от 0,4 M до 0,8 M, от 0,6 M до 0,8 M, от 0,5 M до 0,9 M, от 0,5 M до 1 M, от 0,8 M до 1,3 M, от 1 M до 2 M, от 0,5 M до 8 M, от 1 M до 8 M, от 2 M до 8 M, от 3 M до 8 M, от 0,1 M до 7,5 M, от 0,1 M до 7 M, от 0,1 M до 6 M, от 0,1 M до 5 M, от 0,5 M до 7,5 M, от 1 M до 7 M, от 2 M до 6 M, от 3 M до 5 M, от 3,5 M до 4,5 M или около 3 M, 4 M или 5 M кетоновых тел) и от около 4 нМ до около 150 мМ мелатонина или метаболита мелатонина, предшественника или аналога мелатонина (например, от около 4 нМ до 50 нМ, от 4 нМ до 100 нМ, от 4 нМ до 200 нМ, от 4 нМ до 0,4 мкМ, от 50 нМ до 100 нМ, от 100 нМ до 0,4 мкМ, от 0,4 мкМ до 8 мкМ, от 0,4 мкМ до 40 мкМ, от 0,4 мкМ до 100 мкМ, от 0,4 мкМ до 500 мкМ, от 0,4 мкМ до 1 мМ, от 0,4 мкМ до 50 мМ, от 4 мкМ до 50 мкМ, от 4 мкМ до 200 мкМ, от 4 мкМ до 500 мкМ, от 4 мкМ до 1 мМ, от 4 мкМ до 50 мМ, от 4 мкМ до 100 мМ, от 8 мкМ до 50 мкМ, от 8 мкМ до 250 мкМ, от 20 мкМ до 2 мМ, от 200 мкМ до 500 мкМ, от 500 мкМ до 2 мМ, от 2 мМ до 4 мМ, от 2 мМ до 50 мМ, от 4 мМ до 6 мМ, от 4 мМ до 7 мМ, от 4 мМ до 9 мМ, от 4 мМ до 125 мМ, от 4 мМ до 100 мМ, от 4 мМ до 75 мМ, от 4 мМ до 50 мМ, от 5 мМ до 10 мМ, от 5 мМ до 11 мМ, от 6 мМ до 9 мМ, от 8 мМ до 15 мМ, от 10 мМ до 25 мМ, от 10 мМ до 150 мМ, от 20 мМ до 150 мМ, от 25 мМ до 150 мМ, от 30 мМ до 150 мМ, от 35 мМ до 150 мМ, от 40 мМ до 150 мМ, от 10 мМ до 130 мМ, от 12,5 мМ до 120 мМ, от 15 мМ до 110 мМ, от 20 мМ до 100 мМ, от 25 мМ до 80 мМ, от 30 мМ до 50 мМ, от 40 мМ до 45 мМ, от 0,5 мкМ до 125 мМ, от 1 мкМ до 100 мМ, от 150 мкМ до 150 мМ, от 200 мкМ до 2 мМ, от 500 мкМ до 100 мМ, от 800 мкМ до 150 мМ или от 750 мкМ до 125 мМ мелатонина или метаболита мелатонина, предшественника или аналога мелатонина). Концентрация каждого компонента должна быть ниже точки насыщения растворителя, такой, чтобы не происходила преципитация, хотя концентрация каждого компонента может быть относительно высокой, поскольку токсичность кетоновых тел и мелатонина является низкой. Конечная концентрация каждого компонента в защитной композиции от ишемии/реперфузии будет зависеть от нескольких факторов, включая желаемую концентрацию каждого компонента в крови и объем введения.
Любое число растворителей можно использовать в жидкой защитной композиции от ишемии/реперфузии или для растворения или повторного суспендирования сухого порошкового состава защитной композиции от ишемии/реперфузии. Поскольку кетоновые тела легко растворимы в воде, стерильную дистиллированную воду можно использовать в качестве первичного растворителя. Поскольку мелатонин является более гидрофобным, солюбилизатор (например, менее чем 50%, менее чем 40%, менее чем 30%, менее чем 25%, менее чем 24%, менее чем 23%, менее чем 22%, менее чем 21%, менее чем 15%, менее чем 10%, менее чем 8%, менее чем 6%, менее чем 5%, менее чем 4%, менее чем 3%, менее чем 2% или менее чем 1% конечного объема), такой как диметилсульфоксид (ДМСО) или другой неполярный растворитель, можно использовать для растворения мелатонина. Кроме использования в качестве солюбилизатора, ДМСО также может действовать как поглотитель радикалов гидроксила (Paller et al., 1985, J. Lab. Clin. Med., 105(4):459-63). Этанол (EtOH) также можно использовать в качестве солюбилизатора для мелатонина, одн