Способ нанесения медного покрытия на частицы порошка гидрида титана
Иллюстрации
Показать всеИзобретение относится к порошковой металлургии и может быть использовано для повышения термической стабильности порошкообразного гидрида титана. Способ заключается в создании на поверхности порошкообразных частиц гидрида титана диффузионного барьера в виде покрытия, которое наносят из раствора, содержащего, г/л: сульфат меди 15-35, сигнетова соль 60-170, гидроксид натрия 15-50, карбонат натрия 3-35, формалин 6-16, тиосульфат натрия 0,003-0,01, хлорид никеля 2-3. Порошок гидрида титана заливается свежеприготовленным раствором, перемешивается магнитной мешалкой, фильтруется, промывается и сушится. Заявляемый способ позволяет увеличить температуру термического разложения гидрида титана на 60°С при сохранении удельного содержания водорода, при этом снижается скорость выделения водорода. 3 ил., 1 табл.
Реферат
Изобретение относится к порошковой металлургии, в частности к способу нанесения покрытия на частицы порошка гидрида титана, и может быть использовано для повышения термической стабильности порошкообразного гидрида титана.
Аналогом служит способ нанесения металлического покрытия из никеля на гидрид циркония для удержания водорода в гидриде циркония, описанный в монографии /1/. Однако в ряде случаев происходит окисление такого покрытия на воздухе с последующим растрескиванием.
Известен способ создания на поверхности частиц гидрида титана оксидных пленок из ТiO2 /2/. Способ заключается в создании на образцах гидрида титана пленки ТiO2 толщиной в несколько сотен ангстрем путем анодного окисления гидрида титана в 15%-ном растворе серной кислоты при плотности тока 0,016 А/см2, что повышает термическую стабильность гидрида титана.
Недостатком данного способа является то, что при температуре 400-500°С кислород имеет высокую растворимость в титане, и поэтому оксидные пленки не обеспечивают создания эффективного барьера для проникновения водорода.
Задачей изобретения является снижение скорости выделения водорода из гидрида титана и увеличение температуры начала выделения водорода.
При использовании изобретения достигается следующий технический результат:
- температура термического разложения смещается в сторону более высоких температур на 60°С;
- снижается скорость выделения водорода;
- удельное содержание газа остается неизменным.
Для решения поставленной задачи и достижения технического результата предложен способ нанесения медного покрытия на частицы порошка гидрида титана за счет создания на поверхности порошкообразных частиц диффузионного барьера в виде покрытия, в котором согласно изобретению нанесение покрытия проводят из раствора, содержащего (г/л):
| сульфат меди | 15-35 |
| сегнетова соль | 60-170 |
| гидроксид натрия | 15-50 |
| карбонат натрия | 3-35 |
| формалин | 6-16 |
| тиосульфат натрия | 0,003-0,010 |
| хлорид никеля | 2-3 |
Частицы порошка гидрида титана покрывают слоем меди химическим методом. Процесс покрытия частиц гидрида титана саморегулирующийся:
при образовании сплошной пленки меди на поверхности частиц реакция осаждения меди прекращается. Наличие слоя меди на частицах порошка повышает термическую устойчивость гидрида титана. При этом наблюдается снижение скорости выделения водорода и увеличивается температура начала выделения водорода.
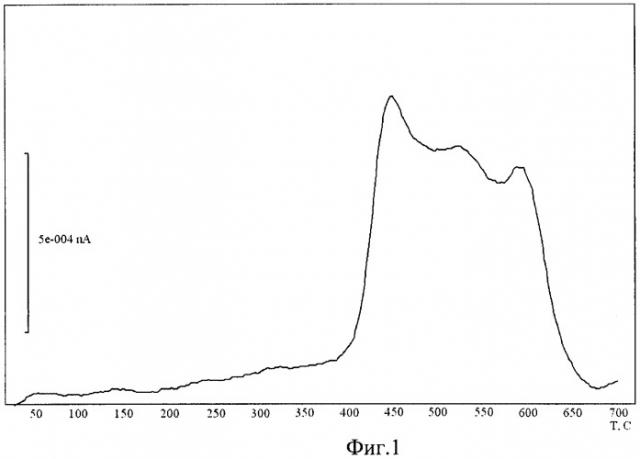
На фиг.1 представлены кривые TG, SDTA и спектр термодесорбции водорода из исходного гидрида титана.
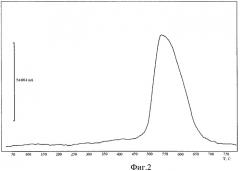
На фиг.2 представлены кривые TG, SDTA и спектр термодесорбции водорода из гидрида титана с медным покрытием.
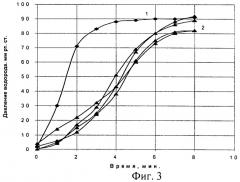
На фиг.3 приведены кинетические кривые термического разложения гидрида титана, полученного из губчатого титана (кривая 1), и гидрида титана с медным покрытием (кривая 2).
Технология процесса нанесения слоев меди на частицы гидрида титана заключается в следующем. Навеска порошка гидрида титана в количестве ≈5 г помещается в стеклянный стакан, заливается ≈50 см3 свежеприготовленного раствора, содержащего (г/л): сульфат меди 35; сегнетову соль 170; гидроксид натрия 50; карбонат натрия 35; формалин 16; тиосульфат натрия 0,003; хлорид никеля 3. С помощью магнитной мешалки производят перемешивание в течение фиксированного времени (от 5 до 60 мин). После окончания перемешивания суспензия порошка переносится на стеклянный фильтр и откачивается вместе с осадком с помощью насоса Камовского. Оставшийся на фильтре порошок гидрида титана с нанесенным слоем меди несколько раз промывается дистиллированной водой, а затем высушивается в вакуумном сушильном шкафу в течение 2 часов при температуре 105°С.
В таблице 1 приведены данные по составу раствора, используемого для нанесения слоев меди, данные по удельному содержанию газа как исходного гидрида титана, так и после нанесения слоев меди, а также толщина нанесенного на порошок гидрида титана слоя меди.
| Таблица | ||||
| Результаты опытов по нанесению меди на порошок гидрида титана | ||||
| Состав раствора, г/л | № образца | Удельное содержание газа, см3/г | Толщина медного покрытия, мкм | |
| Исходное | После выдержки | |||
| Сульфат меди - 35 | 1 | 292,5 | 297,2 | - |
| Сегнетова соль - 170 | ||||
| Гидроксид натрия - 50 | ||||
| Карбонат натрия - 35 | 2 | 425,3 | 421,5 | 0,71 |
| Формалин - 16 | ||||
| Тиосульфат натрия - 0,003 | ||||
| Хлорид никеля - 3 |
Показатели качества порошка с медным покрытием показаны на фиг.1-3.
Приведенные спектры термодесорбции водорода из образцов исходного гидрида титана (фиг.1) и гидрида титана с медным покрытием (фиг.2), снятые в процессе нагрева в интервале температур от 25 до 700°С в среде аргона, свидетельствуют о различной термической устойчивости сравниваемых образцов в интервале температур от 400 до 700°С. Для образцов характерен эндотермический эффект разложения, наблюдаемый на спектрах термодесорбции, при этом:
1) начало и окончание процесса разложения исходного гидрида титана соответствует температурам 431,0 и 540,9°С соответственно, а максимальной скорости разложения отвечает температура, равная 460,5°С (фиг.1),
2) начало и окончание процесса разложения гидрида титана с медным покрытием соответствует температурам 503,3 и 585,9°С, а максимальной скорости разложения отвечает температура 526,9°С (фиг.2).
С использованием данного способа пик термодесорбции водорода из гидрида титана с медным покрытием по сравнению с пиком термодесорбции водорода из исходного гидрида титана без медного покрытия смещен на ≈60°С в сторону более высоких температур.
С использованием данного способа кинетические кривые термического разложения гидрида титана с медным покрытием (фиг.3, кривая 2) на начальном участке расположены ниже соответствующей кривой термического разложения гидрида титана без медного покрытия (фиг.3, кривая 1), что свидетельствует о снижении скорости выделения водорода из гидрида титана с медным покрытием.
С использованием данного способа удельное содержание газа в гидриде титана с медным покрытием не изменяется по сравнению с исходным гидридом титана. Так, в первом примере таблицы в исходном гидриде титана удельное содержание газа составило 292,5 см3/г, а после нанесения медного покрытия - 297,2 см3/г.Во втором примере таблицы в исходном гидриде титана удельное содержание газа составляло 425,3 см3/г, а после нанесения медного покрытия - 421,5 см3/г.
Литература
1. Гидриды металлов. Под ред. В.Мюллера. - М.:Атомиздат.1973. С.79.
2. Schoenfelder C.W., Swisher I.H. Kinetics of thermal decomposition of TiH2 // Journal of Vacuum Science and Technology. 1973. V.10. No.5. 862-870.
Способ нанесения медного покрытия на частицы порошка гидрида титана, включающий создание на поверхности порошкообразных частиц диффузионного барьера в виде покрытия, отличающийся тем, что нанесение покрытия проводят из раствора, содержащего, г/л:
| сульфат меди | 15-35 |
| сегнетова соль | 60-170 |
| гидроксид натрия | 15-50 |
| карбонат натрия | 3-35 |
| формалин | 6-16 |
| тиосульфат натрия | 0,003-0,010 |
| хлорид никеля | 2-3 |