Иммуногенные вещества, содержащие адъювант на основе полиинозиновой кислоты-полицитидиловой кислоты
Иллюстрации
Показать всеГруппа изобретений относится к композиции полинуклеотидного адъюванта (PICKCa) и способам его применения для проявления иммунного ответа. Полинуклеотидный адъювант включает в себя полирибоинозиновую-полирибоцитидиловую кислоту (PIC), где молекулы PIC гетерогенны по молекулярному весу и имеют молекулярный вес от 66000 до 1200000 дальтон, по меньшей мере, один антибиотик и один положительный ион. Изобретение также относится к иммуногенной композиции, включающей полинуклеотидный адъювант вместе с другими иммуногенными композициями, такими как антиген, выбранный из вирусных, бактериальных, грибковых, паразитарных и/или раковых антигенов; также к способам применения таких адъювантных композиций для генерирования иммунного ответа, иммунного ответа слизистой на антигенное соединение. Группа изобретений обеспечивает выработку в организме хозяина специфического для заболевания иммунного ответа. 12 н. и 10 з.п. ф-лы, 38 ил., 28 табл., 7 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение в целом относится к иммуногенным композициям и к способам их использования. Более конкретно, настоящее изобретение относится к иммуногенной композиции, включающей полинуклеотидный адъювант в сочетании с одним или несколькими антигенными веществами, используемыми для проявления в организме хозяине специфического для заболевания иммунного ответа.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Иммунная система может проявлять как специфические, так и неспецифические иммунные ответы. Неспецифический иммунитет охватывает различные клетки и механизмы, такие как фагоцитоз (захват чужеродных частиц или антигенов) макрофагами или гранулоцитами, и активность природных клеток-киллеров (NK), в числе других. Неспецифический иммунитет связан с механизмами, эволюционно менее развитыми, и не связан с приобретенной специфичностью и памятью, которые являются особенностями специфического иммунного ответа. Ключевые различия между специфическим и неспецифическим иммунитетом определяются специфичностью В- и Т-клеток. Эти клетки преимущественно приобретают свою реактивность после активации специфическим антигеном и обладают механизмами, позволяющими проявлять эффект памяти в случае последующего воздействия указанного специфического антигена. В результате вакцинация (включающая такие параметры, как специфичность и память) является эффективной процедурой для защиты от вредных патогенов.
В основном В- и Т-лимфоциты, которые содержат специфические рецепторы на поверхности своих клеток для данного антигена, генерируют специфическую иммунную реакцию. Специфическая иммунная система может отвечать на различные антигены двумя способами: 1) путем развития гуморального иммунитета, который включает в себя стимуляцию В-клеток и продукцию антител или иммуноглобулина, антигена и хелперных Т-клеток (преимущественно Th2), и 2) путем развития клеточного иммунитета, в который в основном вовлечены Т-клетки, включая цитотоксические Т-лимфоциты (CTL), хотя в образование CTL ответа могут вовлекаться и другие клетки (например, антигенпрезентирущие клетки и Th1-клетки).
В поисках более безопасных и более эффективных вакцин были использованы новые технологии, включающие рекомбинантные методики, методики очистки и синтеза, для повышения качества и специфичности используемых антигенов. Очищенные, субъединичные и синтезированные антигены проявляют повышенную безопасность, но пониженную иммуногенность, которая рассматривалась как один из показателей для идентификации эффективного адъюванта. Таким образом, эффективный адъювант становится все более важным компонентом современных вакцин. Адъюванты в основном представляют собой соединения, которые, при их введении вместе с антигеном (либо в сочетании с ним, либо вводимые до антигена), повышают и/или модифицируют иммунный ответ на конкретный антиген.
Репрезентативные адъюванты, которые были использованы для повышения иммунного ответа, включают соединения алюминия (в целом обозначаемые как «квасцы»), эмульсии типа масло-в-воде (полный адъювант Фрейнда (CFA) представляет собой эмульсию масло-в-воде, содержащую высушенные, термически инактивированные организмы Mycobacterium tuberculosis), сапонин (выделенный из коры Quillaja Saponoria, активный компонент адъюванта, известный как Quile A), CpG ОДН (синтетический олигодезоксинуклеотид, содержащий неметилированные CpG динуклеотиды), монофосфорил-липид А (MPL), полученный из липополисахарида Salmonella minnesota Re595, липосомы (обычно получаемые из биодеградируемых материалов, таких как фосфолипиды) и биодеградируемые полимерные микросферы (получаемые из множества полимеров, таких как полифосфазен и полиангидриды). Адъювантные свойства указанных соединений, оцениваемые с каждым из адъювантов, демонстрировали как достоинства, так и недостатки.
Полинуклеотидные комплексы были исследованы применительно к различным видам использования, включая их свойства в качестве адъювантов. Двуцепочечные РНК (дцРНК) представляют собой очень мощные биологические модификаторы, которые могут оказывать выраженное влияние на клетки в наномолярных концентрациях. Модулирующие эффекты дцРНК включают широкий спектр воздействия на молекулярном и клеточном уровнях.
На молекулярном уровне дцРНК могут проявлять биологические эффекты, такие как синтез интерферона, индукцию протеинкиназы, усиление антигенной гистосовместимости и ингибирование метаболизма. На клеточном уровне дцРНК могут демонстрировать такие биологические эффекты, как пирогенность, митогенность, макрофагальная активация, активация гуморального иммунитета, активация клеточного иммунитета и индукция антивирусного статуса. Иммуномодулирующие эффекты дцРНК были описаны. В патенте США No. 4124702 указано, что двуцепочечные полинуклеотиды вызывают индукцию интерферона в живых клетках животных. В патенте США No. 3906092 описано, что образование антител в ответ на вакцину адъювантного типа повышается при включении в вакцину полинуклеотида или комплекса полинуклеотидов. Хьюстон с соавт. (Houston et al.) установили, что PICLC (комплекс полиинозиновой кислоты - полицитидиловой кислоты - поли-L-лизинкарбоксиметилцеллюлозы) представляет собой мощный адъювант, действующий по механизму повышения первичного антительного ответа, в отсутствие дополнительного адъюванта.
Полиинозиновая - полицитидиловая кислота (PIC), как один из наиболее изученных полинуклеотидных комплексов, не был эффективен при использовании на обезьянах и людях в связи с его нестабильностью в организме после введения. В этой связи, PIC подвергли модификации различными способами, с тем чтобы преодолеть свойственный им один или другой недостаток. Так, например, комплекс полирибоинозиновой-полирибоцитидиловой кислоты с гидробромидом поли-L-лизина примерно в 5-15 раз более устойчив к гидролизу панкреатической рибонуклеазой, чем исходный препарат PIC.
Лин с соавт. (Lin et al.) указывают, что противовирусное средство, включающее в себя полиинозиновую-полицитидиловую кислоту, канамицин и кальций, можно использовать в качестве адъюванта (Lin, et al., A new immunostimulatory complex (PICKCa) in experimental rabies: antiviral and adjuvant effects, Arch Virol, 131: 307-19, 1993; и патент Китая No. 93105862.7). В патенте Китая No. 93105862.7 описано применение основной композиции поли I:C, канамицина и кальция (PICKCa) в качестве адъюванта в составе вакцины для применения у человека и других млекопитающих. Однако Лин обнаружил, что первоначально идентифицированная форма PICKCa не обеспечивает оптимального профиля эффективности/безопасности для применения в качестве адъюванта и, кроме того, в определенных условиях вызывает неприемлемые неблагоприятные побочные эффекты.
Настоящее изобретение относится к новым иммуногенным композициям, которые проявляют улучшенные профили безопасности и эффективности; и к способам применения таких композиций. Целевые иммуногенные композиции включают в себя полинуклеотидный адъювант и антиген.
Цитированная литература
Могут представлять интерес следующие ссылки:
JP1093540A2;
патент США No. 4124702
патент США No. 3692899
патент США No. 3906092
патент США No. 4389395
патент США No. 4349538
патент США No. 4024241
патент США No. 3952097
Houston et al., Infection and Immunity, 14:318-9, 1976C
Wright and Adler-Moore, Biochemical and Biophysical Research Communications, 131:949-45, 1985
Lin, et al., A new immunostimulatory complex (PICKCa) in experimental rabies: antiviral and adjuvant effects, Arch Virol, 131:307-19, 1993
Патент Китая 93105862.7
Gupta R.K. et al., Adjuvants- a balance between toxicity and adjuvanticity, Vaccine 11:293-306, 1993
Arnon, R. (Ed.) Synthetic Vaccines 1:83-92, CRC Press, Inc., Boca Raton, Fla., 1987
Sela, M., Science 166:1365-1374 (1969)
патент США No. 6008200
Ellouz et al., Biochem. & Biophy. Res. Com., 59:1317, 1974
патент США No. 4094971
патент США No. 4101536
патент США No. 4153684
патент США No. 4235771
патент США No. 4323559
патент США No. 4327085
патент США No. 4185089
патент США No. 4082736
патент США No. 4369178
патент США No. 4314998
патент США No. 4082735
патент США No. 4186194
патент США No. 4468558
New Trends and Developments in Vaccines, edited by Voller et al., University Park Press, Baltimore, Md., USA, 1978
Klein, J., et al., Immunology (2nd), Blackwell Science Inc., Boston (1997)
Gupa R.K. and Siber G.R., Adjuvants for human vaccines- current status, problems and future prospects, Vaccine, 13 (14):1263-1276, 1995
Richard T Kenney et al. Meeting Report- 2nd meeting on novel adjuvants currently in/close to human clinical testing, Vaccine 20 2155-2163, 2002
Laboratory Techniques in Rabies Edited by F X Meslin, M M Kaplan, H Koprowski 4th, 1996, Edition ISBN 92 4 1544 1
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В основном настоящее изобретение относится к новым иммуногенным композициям, включающим в себя полинуклеотидную адъювантную композицию вместе с иммуногенным или антигенным веществом, а также к способам использования их для проявления иммунного ответа.
Соответственно, в настоящем изобретении предлагаются иммуногенные композиции, включающие в себя (а) полинуклеотидный адъювант, содержащий полирибоинозиновую-полирибоцитидиловую кислоту (PIC), по меньшей мере, один антибиотик и, по меньшей мере, один положительный ион; и (b), по меньшей мере, один антиген, где указанная композиция изготавливается для введения с целью достижения пролонгированного высвобождения.
Иммуногенная композиция согласно изобретению может включать в себя полинуклеотидную адъювантную композицию с молекулами, гетерогенными по молекулярной массе, где молекулярная масса составляет по меньшей мере 66000 дальтон.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
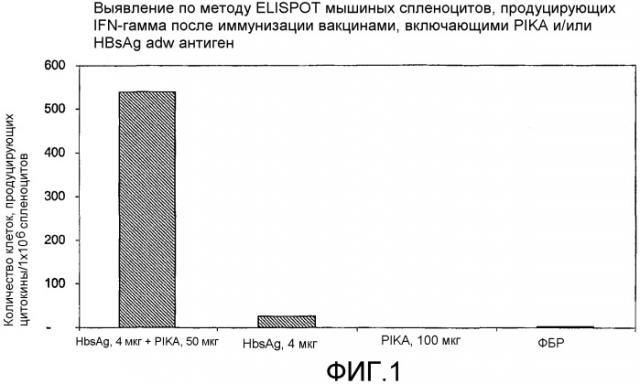
Фиг.1 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих интерферон γ после иммунизации вакцинами, включающими PIKA и/или HBsAg adw.
Фиг.2 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-2 после иммунизации вакцинами, включающими PIKA и/или HBsAg adw.
Фиг.3 - выявление по методу ELISPOT IL-4, продуцируемых мышиными спленоцитами после иммунизации вакцинами, включающими PIKA и/или HBsAg adw.
Фиг.4 - определение по методу ИФТФА титров специфических IgG в мышиной сыворотке (в 400-кратном разведении) после иммунизации вакцинами, включающими PIKA и/или HBsAg adw.
Фиг.5 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих интерферон гамма (γ) после иммунизации вакцинами, включающими PIKA и/или инактивированный субъединичный гриппозный антиген.
Фиг.6 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-2 после иммунизации вакцинами, включающими PIKA и/или инактивированный субъединичный гриппозный антиген.
Фиг.7 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-4 после иммунизации вакцинами, включающими PIKA и/или инактивированный субъединичный гриппозный антиген.
Фиг.8 - определение по методу ИФТФА титров специфических IgG в мышиной сыворотке (в 900-кратном разведении) после иммунизации вакцинами, включающими PIKA и/или инактивированный субъединичный гриппозный антиген.
Фиг.9 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих интерферон гамма (γ) после иммунизации вакцинами, включающими PIKA и/или антиген HIV gp 120.
Фиг.10 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-2 после иммунизации вакцинами, включающими PIKA и/или антиген HIV gp 120.
Фиг.11 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-4 после иммунизации вакцинами, включающими PIKA и/или антиген HIV gp 120.
Фиг.12 - анализ с использованием флуоресцентного сортировщика (FACS-анализ) мышиных спленоцитов после иммунизации вакцинами, включающими PIKA и/или антиген HIV gp 120, а также процентного содержания CD4+ клеток, экспрессирующих интерферон γ.
Фиг.13 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих интерферон γ после иммунизации вакцинами, включающими PIKA и/или rPA антиген сибирской язвы.
Фиг.14 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-2 после иммунизации вакцинами, включающими PIKA и/или rPA антиген сибирской язвы.
Фиг.15 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-4 после иммунизации вакцинами, включающими PIKA и/или rPA антиген сибирской язвы.
Фиг.16 - анализ с использованием флуоресцентного сортировщика (FACS-анализ) мышиных спленоцитов после иммунизации вакцинами, включающими PIKA и/или rPA антиген сибирской язвы, а также процентного содержания CD4+ клеток, экспрессирующих интерферон γ.
Фиг.17 - определение по методу ИФТФА титров специфических IgG в мышиной сыворотке (в 400-кратном разведении) после иммунизации вакцинами, включающими PIKA и/или rPA антиген сибирской язвы.
Фиг.18 - определение по методу ИФТФА титров специфических IgG в мышиной сыворотке через 16 недель после иммунизации вакцинами, включающими PIKA и/или rPA антиген сибирской язвы.
Фиг.19 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих интерферон γ после иммунизации вакцинами, включающими PIKA и/или антиген HSV2-gD.
Фиг.20 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-2 после иммунизации вакцинами, включающими PIKA и/или антиген HSV2-gD.
Фиг.21 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-4 после иммунизации вакцинами, включающими PIKA и/или антиген HSV2-gD.
Фиг.22 - анализ с использованием флуоресцентного сортировщика (FACS-анализ) мышиных спленоцитов после иммунизации вакцинами, включающими PIKA и/или антиген HSV2-gD, а также процентного содержания CD4+ клеток, экспрессирующих интерферон γ.
Фиг.23 - определение по методу ИФТФА титров специфических IgG в мышиной сыворотке (в разведении 2700 раз) после иммунизации вакцинами, включающими PIKA и/или антиген HSV2-gD.
Фиг.24 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих интерферон γ после иммунизации вакцинами, включающими PIKA и/или инактивированный антиген H5N1.
Фиг.25 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-2 после иммунизации вакцинами, включающими PIKA и/или инактивированный антиген H5N1.
Фиг.26 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих IL-4 после иммунизации вакцинами, включающими PIKA и/или инактивированный антиген H5N1.
Фиг.27 - анализ с использованием флуоресцентного сортировщика (FACS-анализ) мышиных спленоцитов после иммунизации вакцинами, включающими PIKA и/или инактивированный антиген H5N1, а также процентного содержания CD4+ve клеток, экспрессирующих интерферон γ.
Фиг.28 - определение по методу ИФТФА титров специфических IgG в мышиной сыворотке (в 900-кратном разведении) после иммунизации вакцинами, включающими PIKA и/или инактивированный антиген H5N1.
Фиг.29 - определение по методу ИФТФА титров специфических IgG в мышиной сыворотке (в разведении 16000 раз) после иммунизации вакцинами, включающими PIKA и/или полный инактивированный антиген SARS.
Фиг.30 - определение по методу ИФТФА титров специфических H5 антител в куриной сыворотке после иммунизации вакцинами, включающими PIKA и/или инактивированный антиген H5N1.
Фиг.31 - определение по методу ИФТФА титров специфических H9 антител в куриной сыворотке после иммунизации вакцинами, включающими PIKA и/или инактивированный антиген H9N2.
Фиг.32 - уровень выживания мышей, подвергнутых воздействию вируса бешенства дикого типа с последующей обработкой вакциной против бешенства.
Фиг.33 - определение по методу ИФТФА титров специфических антител в мышиной сыворотке после иммунизации вакцинами, включающими PIKA и/или HBsAg adw.
Фиг.34 - определение по методу ИФТФА титров специфических антител в мышиной сыворотке после иммунизации вакцинами, включающими PIKA и/или инактивированный субъединичный гриппозный антиген.
Фиг.35 - определение по методу ИФТФА титров специфических IgG1 в мышиной сыворотке после иммунизации вакцинами, включающими PIKA и/или HBsAg.
Фиг.36 - определение по методу ИФТФА титров специфических IgG2 в мышиной сыворотке после иммунизации вакцинами, включающими PIKA и/или HBsAg.
Фиг.37 - выявление по методу ELISPOT мышиных спленоцитов, продуцирующих интерферон γ после иммунизации вакцинами, включающими PIKA и/или HBsAg.
Фиг.38 - выявление по методу ELISPOT мышиных спленоцитов (после 6-дневной рестимуляции с использованием 2 мкг/мл пептида IPQ), продуцирующих интерферон γ после иммунизации вакцинами, включающими PIKA и/или HBsAg.
В Таблице 1 приводится перечень репрезентативных вирусных патогенов, которые могут служить в качестве источника антигена, а также описание заболеваний, ассоциированных с этими организмами.
В Таблице 2 приводится перечень репрезентативных бактериальных патогенов, которые могут служить в качестве источника антигена, а также описание заболеваний, ассоциированных с этими организмами.
В Таблице 3 приводится перечень репрезентативных грибковых патогенов, которые могут служить в качестве источника антигена, а также описание заболеваний, ассоциированных с этими организмами.
В Таблице 4 приводится перечень репрезентативных паразитов, которые могут служить в качестве источника антигена, а также описание заболеваний, ассоциированных с этими организмами.
В Таблице 5 приводится перечень репрезентативных видов рака (например, по типу ткани), которые могут служить в качестве источника антигена.
ПОДРОБНОЕ ОПИСАНИЕ РЕПРЕЗЕНТАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение может быть пояснено лучшим образом с помощью приведенного ниже подробного описания некоторых вариантов осуществления настоящего изобретения и со ссылкой на включенные в текст примеры.
В тексте заявки, когда приводятся ссылки на публикации, раскрытие этих публикаций приводится в данной заявке полностью, в качестве ссылки, для целей более полного описания состояния уровня техники в той области, к которой относится настоящее изобретение.
Перед описанием изобретения следует отметить, что данное изобретение не ограничивается конкретными вариантами его осуществления, поскольку они, разумеется, могут варьировать. Следует также понимать, что терминология, использованная в тексте, приводится только с целью описания конкретных вариантов, но не служит целям ограничения, поскольку область настоящего изобретения определяется лишь прилагаемой формулой изобретения.
Если особо не указано иное, все технические и научные термины, приведенные в настоящем описании, имеют общепринятые значения, используемые специалистами в той области, к которой относится настоящее изобретение. Хотя на практике осуществления или тестирования согласно настоящему изобретения могут также использоваться любые способы и материалы, аналогичные или эквивалентные приведенным в настоящем описании, описываются предпочтительные способы и материалы. Все публикации, приведенные в настоящем тексте, включены в него в качестве ссылки с тем, чтобы более полно раскрыть способы и/или материалы, применительно к которым цитируется настоящая публикация.
Следует также отметить, что несмотря на то, что в тексте и прилагаемой формуле изобретения используются артикли единственного числа, указанный текст и формула изобретения включают множественные варианты, если из контекста четко не следует иное. Так, например, ссылка на «иммуногенную композицию» включает множество таких композиций, а ссылка на «антиген» означает ссылку на один или несколько антигенов и их эквивалентов, известных специалистам в данной области и т.п. Следует также отметить, что описанный материал может быть изменен путем исключения какого-либо необязательного элемента. В этой связи в тексте используются такие ограничительные термины, как «единственно», «только» и т.п., в сочетании с цитированием описываемых элементов или соответствующие варианты сопровождаются терминами «отрицательного» ограничения.
Определение терминов
В начале подробного описания настоящего изобретения может быть полезно дать определение ряду используемых в тексте терминов.
Термин «адъювант» в контексте настоящего описания относится к любому веществу или смеси веществ, которые повышают или диверсифицируют иммунный ответ организма хозяина на антигенное соединение. Конкретно:
1. Термин “PICKCa” в целом относится к композиции, включающей поли I:C, канамицин и кальций, независимо от конкретных физических и иммуногенных свойств.
2. Термин “Av-PICKCa” относится к форме PICKCa, используемой в коммерческом варианте как противовирусное лекарственное средство.
3. Термин “PIKA” относится к композиции согласно изобретению, включающей в себя поли I:C, антибиотик (например, канамицин) и положительный ион (например, ион кальция), где PIKA характеризуется такими физическими свойствами (например, молекулярная масса, размер и т.п.), что при введении PIKA проявляют свойства адъюванта с пониженными побочными эффектами (например, со сниженной токсичностью) относительно, например, PICKCa и большей эффективностью (например, стимулирует усиленный иммунный ответ) относительно, например, Av-PICKCa.
Термин «поли I:C» или «PIC» относится к композиции, включающей в себя полирибоинозиновую и полирибоцитидиловую нуклеиновые кислоты, которые могут также называться как полиинозиновая кислота-полицитидиловая кислота соответственно.
Термин «PIC-содержащая молекула» или «PIC-содержащее соединение» относится, без ограничения, к PIC, который необязательно может образовывать комплекс или иным образом объединяться с антибиотиком (например, канамицином) и положительным ионом (например, ионом кальция), по меньшей мере, с одним из них или с обоими, в композиции, которая включает PIC-содержащую молекулу. В одном варианте осуществления настоящего изобретения PIC-содержащая молекула не включает поли-L-лизин или его производное в составе комплекса.
Термин «гетерогенные» относится в контексте настоящего описания к адъювантным композициям согласно изобретению и обозначает, что компоненты композиции, например, PIC-содержащие молекулы, неоднородны с точки зрения физических характеристик, таких как молекулярная масса, размер или обе указанные характеристики. В том случае, когда композиция указывается как гетерогенная применительно к конкретному физическому параметру и описывается диапазоном значений для данного физического параметра, говорят, что композиция состоит по существу из молекул, характеризующихся молекулами, имеющими физические показатели, которые распределены в пределах указанного диапазона и на его границах. Поскольку композиция не может содержать молекулу, которая описывается физическими параметрами, выходящими за пределы, выше или ниже указанных границ приведенного диапазона, такая композиция включает в себя, по меньшей мере, одну молекулу, обладающую физическими характеристиками на верхнем значении диапазона и на нижнем значении диапазона. Указанная композиция в некоторых вариантах осуществления настоящего изобретения может включать молекулы за пределами указанного диапазона физических характеристик, используемых для описания композиции. Молекулы, которые присутствуют в композиции за пределами указанного диапазона не оказывают заметного материального воздействия на основные и новые характеристики композиции.
Термин «индивидуум», используемый в контексте настоящего описания взаимозаменяемо с терминами «организм хозяин», «субъект» и «животное», включает человека и всех домашних животных, например, домашний скот и комнатных животных, а также диких млекопитающих и птиц, включающих, без ограничения, крупный рогатый скот, лошадей, коров, свиней, овец, коз, собак, кошек, кроликов, оленей, норок, кур, уток, гусей, индюшек, бойцовых петухов и т.п.
Термин «антитело» включает поликлональные и моноклональные антитела, а также антигенное соединение, связывающееся с фрагментами таких антител, включающими Fab, F(ab')2, Fd, Fv и их одноцепочечные производные. Дополнительно, термин «антитело» включает природные антитела, а также неприродные антитела, включающие, например, химерные, бифункциональные и гуманизированные антитела и родственные синтетические изоформы. Термин «антитело» используется взаимозаменяемо с термином «иммуноглобулин».
В контексте настоящего описания термин «антигенное соединение» относится к любому веществу, которое в соответствующих условиях может быть распознано иммунной системой (например, которое связывается с антителом или процессируется таким образом, что вызывает иммунный ответ).
Термин «антиген» в контексте настоящего описания включает, без ограничения, клетки; клеточные экстракты; белки; липопротеины; гликопротеины; нуклеопротеины; полипептиды; пептиды; полисахариды; полисахаридные конъюгаты; пептидные миметики полисахаридов; липиды; гликолипиды; углеводы; вирусы; вирусные экстракты; бактерии; бактериальные экстракты; грибы; грибковые экстракты; многоклеточные организмы, такие как паразиты; и аллергены. Антигены могут быть экзогенными (например, полученными из источника, отличного от того индивидуума, которому антиген будет вводиться, например, из другого вида животных) или эндогенными (например, происходящими из организма хозяина, например, пораженного элемента организма, ракового антигена, вирус-инфицированной клетки, продуцирующей антиген и т.п.). Антигены могут быть нативными (то есть природными); синтетическими; или рекомбинантными. Антигены включают нечищеные экстракты; целые клетки; и очищенные антигены, где термин «очищенный» указывает, что данный антиген находится в форме, которая является обогащенной, относительно того окружения, в котором антиген в норме встречается, и/или относительно неочищенного экстракта, например, в случае культивируемой формы антигена.
Термин «иммуногенная композиция» в контексте настоящего описания относится к сочетанию двух или более веществ (например, антигена и адъюванта), которые вместе вызывают иммунный ответ при введении в организм хозяина.
Термины «полипептид», «пептид», «олигопептид» и «белок» используются в настоящем тексте взаимозаменяемо и относятся к полимерной форме аминокислот любой длины, которые могут включать кодируемые и некодируемые аминокислоты, химически или биохимически модифицированные или дериватизированные аминокислоты, а также полипептиды, содержащие модифицированные пептидные скелеты.
Термин «эффективное количество антигенного соединения» относится к тому количеству антигенного соединения, которое, в случае его необязательного сочетания с адъювантом, будет вызывать у субъекта специфический иммунологический ответ на антигенное соединение.
Термин «иммунный ответ» относится к любому ответу на антигенное или иммуногенное соединение, демонстрируемому иммунной системой позвоночного субъекта. Репрезентативные иммунные ответы включают, без ограничения, местный и системный клеточный и гуморальный иммунитет, такие как ответы цитотоксических Т-лимфоцитов (CTL), включая антиген-специфическую индукцию CD8+ CTL, реакции хелперных Т-клеток, включающие Т-клеточные пролиферативные ответы и высвобождение цитокинов, а также В-клеточные ответы, включающие образование антител.
Термин «проявление иммунного ответа» используется в тексте настоящего описания для обозначения индукции и/или потенцирования иммунного ответа.
Термин «индукция иммунного ответа» относится к иммунному ответу, который стимулируется, инициируется или индуцируется.
Термин «потенцирование иммунного ответа» относится к ранее существовавшему иммунному ответу, который улучшается, продолжается, включает добавление, амплифицируется, усиливается, повышается или пролонгируется.
Выражение «усиленный иммунный ответ» или аналогичный термин означает, что иммунный ответ повышается, улучшается или усиливается для пользы организма хозяина относительно ранее существовавшего статуса иммунного ответа, например, до введения иммуногенной композиции согласно изобретению.
Термины «гуморальный иммунитет» и «гуморальный иммунный ответ» относятся к такой форме иммунитета, при которой в ответ на антигенную стимуляцию продуцируются молекулы антител.
Термины «клеточный иммунитет» и «клеточный иммунный ответ» относятся к иммунологической защите, обеспечиваемой лимфоцитами, такой как защита, обеспечиваемая Т-клеточными лимфоцитами, поступающими в область пораженных клеток. В норме клеточный иммунный ответ включает пролиферацию лимфоцитов. При измерении «пролиферации лимфоцитов» определяют способность лимфоцитов пролиферировать в ответ на специфический антиген. Пролиферация лимфоцитов в контексте настоящего описания относится к пролиферации В-клеток, Т-хелперных клеток или цитотоксических Т-лимфоцитов (CTL).
Термин «иммуногенное количество» относится к такому количеству антигенного соединения, которого достаточно для стимуляции иммунного ответа, при введении субъекту иммуногенной композиции, в сравнении с иммунным ответом, вызываемым антигеном в отсутствие полинуклеотидного адъюванта.
Термин «иммунопотенцирующее количество» относится к такому количеству адъюванта, которое необходимо для целей повышения титра антител и/или клеточного иммунитета, в случае введения антигенного соединения в композиции согласно настоящему изобретению, в сравнении с повышением уровня антител и/или клеточного иммунитета, наблюдаемых в отсутствие полинуклеотидного адъюванта.
Термины «лечение», «подвергать лечению», «лечить» и т.п. в контексте настоящего описания относятся в основном к достижению фармакологического и/или физиологического эффекта. Указанный эффект может представлять собой профилактический, с точки зрения полного или частичного предупреждения заболевания или его симптома и/или может представлять собой терапевтическое воздействие с точки зрения частичной или полной стабилизации или излечивания заболевания и/или устранения побочного эффекта, связанного с заболеванием. Термин «лечение» в контексте настоящего описания охватывает любой вариант лечения субъекта, в частности, млекопитающего, более конкретно человека, и включает: (а) предупреждение заболевания или симптома, которое может развиться у субъекта, предрасположенного к данному заболеванию или симптому, но который еще не был диагностирован как имеющий его; (b) подавление симптома заболевания, например, остановку развития заболевания; или ослабление симптома заболевания, то есть воздействие, вызывающее регрессию заболевания или его симптома; (с) снижение уровня продукта, образуемого инфицирующим агентом данного заболевания (например, уровня токсина, антигена и т.п.); и (d) снижение нежелательного физиологического ответа на инфицирующий агент данного заболевания (например, лихорадки, отека ткани и т.п.).
Термин «смешивание» в контексте настоящего описание включает любой способ, применяемый для объединения компонентов в композиции; такие способы включают, без ограничения, смешивание, диспергирование, растворение, эмульгирование, коагуляцию, суспендирование или другие способы объединения компонентов в составе композиции.
«Фармацевтически приемлемая соль» соединения обозначает соль, которая является фармацевтически приемлемой и которая обладает желательной фармакологической активностью, свойственной исходному соединению. Такие соли включают в себя (1) аддитивные соли кислоты, образуемые с использованием неорганических кислот, таких как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п.; или образуемые с использованием органических кислот, таких как уксусная кислота, пропионовая кислота, гексаноевая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфоновая кислота, глюкогептоновая кислота, 4,4'-метиленбис-(3-гидрокси-2-ен-1-карбоновая кислота), 3-фенилпропионовая кислота, триметилуксусная кислота, третичная бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глютаминовая кислота, гидроксинафтоевая кислота, салициловая кислота, стеариновая кислота, муконовая кислота и т.п.; или (2) соли, образованные в том случае, когда протон кислоты, присутствующий в исходном соединении, замещается ионом металла, например, ионом щелочного металла, ионом щелочноземельного металла или ионом алюминия, или образует координационное соединение с органическим основанием, таким как этаноламин, диэтаноламин, триэтаноламин, трометамин, N-метилглюкамин и т.п.
Термин «стандартная дозированная форма» в контексте настоящего описания относится к физически дискретным единицам, подходящим в качестве стандартных дозировок для применения в случае человека и животных, где каждая стандартная доза содержит заданное количество соединений согласно изобретению, вычисленное как количество, достаточное для продуцирования желательного ответа при сочетании с фармацевтически/физиологически приемлемым разбавителем, носителем или наполнителем.
Репрезентативные варианты осуществления настоящего изобретения
Настоящее изобретение относится к иммуногенным композициям и к способам, используемым для индукции и/или усиления иммунного ответа, который может быть гуморальным и/или клеточным, у человека, животного, отличного от человека, или в клеточной культуре. В основном, иммуногенные для субъекта композиции включают в себя антиген («антигенная композиция») и адъювант. Присутствие адъюванта усиливает или модифицирует иммунный ответ на антиген. Адъювант может менять качество иммунного ответа за счет воздействия на подклассы (изотипы) образуемых иммуноглобулинов, хемокинов и/или цитокинов. В результате, природный иммунитет, гуморальный и/или клеточный иммунный ответы становятся более эффективными при наличии адъюванта.
Особым преимуществом настоящего изобретения является эффективность адъюванта PIKA в сочетании с антигенным веществом с точки зрения индукции специфического гуморального иммунного ответа, что приводит к усилению защитного иммунитета.
Другим важным преимуществом является то, что адъювант PIKA в сочетании с антигеном может индуцировать специфический клеточный иммунный ответ, который необходим для функционирования в качестве терапевтической вакцины, направленной на ограничение и лечение внутриклеточной вирусной, бактериальной или паразитарной инфекции, а также для целей лечения хронических заболеваний, таких как лечение рака или аутоиммунного заболевания.
Соответственно, настоящее изобретение охватывает своими рамками композиции, характеризующиеся уникальными свойствами входящего в них продукта, которые делают их наиболее удобными для использования в качестве вакцин, вводимых животным и/или людям, и которые удовлетворяют потребностям в безопасном адъюванте, вызывающем благоприятный иммунный ответ.
Соответственно, настоящее изобретение относится к адъювантным и иммуногенным композициям, которые могут безопасно использоваться для введения человеку и животным.
Соответственно, настоящее изобретение относится к иммуногенной композиции, которая включает в себя (а) полинуклеотидный адъювант, содержащий полирибоинозиновую-полирибоцитидиловую кислоту (PIC), по меньшей мере, один антибиотик и, по меньшей мере, один положительный ион; и (b), по меньшей мере, один антиген, где указанная композиция изготавливается для введения в качестве композиции с пролонгированным высвобождением.
Иммуногенная композиция согласно изобретению может включать в себя композицию полинуклеотидного адъюванта, молекулы которого гетерогенны по молекулярной массе, где указанная молекулярная масса составляет, по меньшей мере, 66000 дальтон. Масса 66000 дальтон соответствует размеру примерно 6,4 единиц Сведберга. Соответственно, диапазон молекулярных масс от 66000 дальтон до 1200000 дальтон соответствует размерам в диапазоне от 6,4 до 24,0 единиц Сведберга.
В некоторых вариантах осуществления настоящего изобретения композиции на основе адъюванта PIKA включают полинуклеотид, антибиотик и положительный ион, где указанный полинуклеотид может представлять собой полирибоинозиновую-полирибоцитидиловую кислоту (PIC); антибиотик может представлять собой канамицин и указанный ион может представлять собой кальций.
В одном аспекте, представляющем особый интерес, настоящее изобретение относится к иммуногенной композиции, направленной на повышение антигенности антигенно