Диклофенаковый гель
Иллюстрации
Показать всеИзобретение относится к композиции для лечения боли, а также для лечения остеоартрита у объекта, страдающего от суставной боли. Заявленная композиция включает 0,1-10% мас. нестероидного противовоспалительного соединения - диклофенака натрия или раствора диклофенака натрия, 25-60% мас. диметилсульфоксида, этанол, пропиленгликоль, загуститель, выбранный из гидроксипропилцеллюлозы и полимеров-карбомеров, и глицерин в случае, если загустителем является карбомер, воду и имеет вязкость, равную 500-5000 сантипуаз. Изобретение также относится к лекарственному средству для лечения боли, а также для лечения остеоартрита у объекта, страдающего от суставной боли, которое содержит указанную выше композицию. Изобретение обеспечивает превосходное средство доставки диклофенака натрия через кожу, которое проявляет лучшую продолжительность высыхания, большую вязкость, большее фармакокинетическое всасывание in vivo и которое может применяться для топического лечения боли. 6 н. и 7 з.п. ф-лы, 12 ил., 18 табл., 8 пр.
Реферат
Ссылки на родственные заявки
Настоящая заявка претендует на приоритет от Предварительной заявки США от 17 октября 2006 г., положения которой включены в настоящее изобретение путем ссылки во всей полноте для всех целей.
Область техники, к которой относится изобретение
Настоящее изобретение, в общем, касается композиций и способов лечения остеоартрита.
Уровень техники
1. Остеоартрит
Остеоартрит (ОА), иначе артрозоартрит - это хроническое заболевание суставов, которое характеризуется прогрессирующей дегенерацией суставного хряща. Симптомы включают боли в суставах и нарушение движений. ОА является одной из главных причин инвалидности во всем мире и представляет большое финансовое бремя для систем здравоохранения. По оценкам им поражено свыше 15 млн взрослых в одних только США. См. Boh L.E. Osteoarthritis. In: DiPiro J.T., Talbert R.L., Yee G.C. et al., editors. Pharmacotherapy: a pathophysiological approach. 4th ed. Norwalk (CT): Appleton & Lange, p.1441-59 (1999).
Основным средством при лечении ОА являются пероральные нестероидные противовоспалительные препараты (NSAIDs). Они обладают анальгетическим, противовоспалительным и жаропонижающим действием и применяются для уменьшения боли и воспаления. Однако NSAIDs связаны с потенциально серьезными побочными эффектами, включая тошноту, рвоту, язвенную болезнь, желудочно-кишечные кровоизлияния и сердечно-сосудистые явления.
Топические препараты NSAID дают возможность достижения локальной лечебной пользы вместе с уменьшением или устранением риска системных побочных эффектов. Имеется всеобщая заинтересованность в этом подходе к лечению ОА, но данные в подтверждение эффективности местного применения NSAIDs при лечении ОА пока ограничены. Например, в исследовании с контролем на плацебо из 13 рандомизированных испытаний различных топических препаратов NSAID, протестированных конкретно на применение при лечении ОА, пришли к выводу, что они в общем неэффективны для хронического применения при ОА (Lin et al., Efficacy of topical non-steroidal anti-inflammatory drugs in the treatment of osteoarthritis: meta-analysis of randomized controlled trials, BMJ, doi: 10.1136/bmj.38159.639028.7C (2004)).
В общем для измерения эффективности лечения ОА имеется три показателя: боль, физическая функция и глобальная оценка пациента. См. Bellamy N., Kirwan J., Boers M., Brooks P., Strand V., Tugwell P. et al. Recommendations for a core set of outcome measures for future phase III clinical trials in knee, hip and hand osteoarthritis. Consensus development at OMERACT III., J Rheumatol, 24: 799-802 (1997). Чтобы быть пригодной для хронического применения, терапия в общем должна проявлять эффективность по этим трем показателям в течение длительного периода времени. В США, к примеру, Управление по контролю за продуктами и лекарствами (FDA) требует, чтобы терапия ОА превосходила действие плацебо на протяжении 12 недель. Несмотря на значительный потенциал топических препаратов NSAID при лечении ОА ко времени подачи настоящей заявки ни один не был разрешен для такого применения в США.
В патентах США №4575515 и 4652557 раскрыты топические композиции NSAID, одна из которых, содержащая 1,5% диклофенака натрия, 45,5% диметилсульфоксида, 11,79% этанола, 11,2% пропиленгликоля, 11,2% глицерина и воду, оказалась эффективной при лечении хронического ОА. См. Towheed, Journal of Rheumatology 33:3 567-573 (2006), а также публикацию Oregon Evidence Based Practice Center под названием "Comparative Safety and Effectiveness of Analgesics for Osteoarthritis", AHRQ Pub. No. 06-EHC009-EF. Эта конкретная композиция будет именоваться как "сравнительная жидкая композиция" или "сравнительная" в разделе Примеры. Однако у композиций из этих предшествующих изобретений есть недостатки в том, что они медленно сохнут и растекаются. К тому же для достижения эффективности при ОА они требуют частого применения, по 3-4 раза в день, что повышает воздействие потенциальных раздражающих кожу веществ и повышает риск раздражения кожи.
В общем смысле неспособность топических препаратов NSAID выполнять свое предназначение при ОА может быть частично обусловлена трудностями, связанными со введением молекулы через кожу в количестве, достаточном для выполнения лечебного эффекта, и таким способом, чтобы само лечение было переносимым. Обычно считается, что клиническая эффективность при ОА требует всасывания активного ингредиента и его проникновения в достаточном количестве в нижележащие воспаленные ткани, включая синовиальные оболочки и синовиальную жидкость суставов. См. Rosenstein, Topical agents in the treatment of rheumatic disorders, Rheum. Dis. Clin. North Am., 25: 899-918 (1999).
Однако кожа является существенным барьером для проникновения лекарств, поэтому, несмотря на почти четыре десятилетия широких исследований, успешность трансдермального введения лекарств в общем остается весьма ограниченной, а коммерчески доступно лишь небольшое число трансдермальных лекарственных препаратов.
В связи с нанесением топических дозовых форм на кожу может происходить целый ряд взаимодействий, в том числе типа носитель-кожа, носитель-препарат и препарат-кожа. Каждое из них может влиять на высвобождение активного агента из топической дозовой формы (Roberts M.S., Structure-permeability considerations in percutaneous absorption. In: Prediction of Percutaneous Penetration, ed. by R.C.Scott et al., vol. 2, p.210-228, IBC Technical Services, London, 1991). При этом на скорость всасывания и глубину проникновения могут повлиять различные факторы, включая активный ингредиент, носитель, рН и относительную растворимость активного агента в носителе по сравнению с кожей (Ostrenga J. et al., Significance of vehicle composition I: Relationship between topical vehicle composition, skin penetrability, and clinical efficacy. Journal of Pharmaceutical Sciences, 60: 1175-1179 (1971)). В частности, такие свойства препарата, как растворимость, размер и заряд, а также такие свойства носителя, как скорость растворения препарата, растекаемость, прилипчивость и способность к изменению мембранной проницаемости, могут оказать значительное влияние на проницаемость.
При этом наблюдается значительная вариабельность при весьма незначительных изменениях композиции. Например, в работе Naito отмечена значительная вариабельность в проникновении между топическими препаратами NSAID просто при замене гелеобразующего средства, используемого в композиции (Naito et al., Percutaneous absorption of diclofenac sodium ointment. Int. Jour. of Pharmaceutics, 24: 115-124 (1985)). Также и в работе Но отмечена значительная вариабельность в проникновении при изменении долей спирта, пропиленгликоля и воды (Но et al., The influence of cosolvents on the in-vitro percutaneous penetration of diclofenac sodium from a gel system, J. Pharm. Pharmacol., 46:636-642 (1994)). Отмечено, что эти изменения влияют на три разных параметра: (i) растворимость препарата в носителе, (ii) коэффициент распределения и (iii) эффекты на изменение структуры кожи.
Но et al. (1994) также отметили, что (i) рН носителя, (ii) растворимость препарата и (iii) вязкость матрикса геля могут влиять на проникновение из гелеобразной дозовой формы. Значение рН влияет на баланс между ионизированной и неионизированной формами препарата, которые обладают различными свойствами проникновения (Obata, International Journal of Pharmaceutics, 89: 191-198 (1993)). Вязкость может влиять на диффузию препарата из матрикса геля и его высвобождение из носителя в кожу. Растворимость препарата в носителе влияет на коэффициент распределения препарата между лекарственной формой и мембраной/тканью реципиента (Но et al. 1994).
Одним из средств обратимого понижения кожного барьера являются химические усилители проникновения. Другие методы включают ионтофорез, ультразвук, электропорацию, нагревание и микроиглы. Как минимум 250 химикатов идентифицированы как усилители, способные повысить проницаемость кожи. Базовые категории составляют пирролидоны, жирные кислоты, сложные эфиры и спирты, сульфоксиды, эфирные масла, терпены, оксазолидины, поверхностно-активные вещества, полиоли, азопроизводные и эпидермальные ферменты.
Механизмы, посредством которых усилители проникновения понижают барьерную функцию кожи, плохо изучены (см. Williams and Barry "Penetration Enhancers" Advanced Drug Delivery Reviews 56: 603-618 (2004)), однако предполагается, что эти механизмы можно классифицировать на три широкие категории: разрушение липидов, повышение проницаемости корнеоцитов и усиление распределения препарата в ткани.
Проблема с применением химических усилителей проникновения состоит в том, что лишь немногие из них могут вызвать значительное или терапевтическое усиление транспорта лекарственного вещества в удовлетворительной степени. Это происходит потому, что само разрушение кожного барьера создает возможность раздражения кожи. Чем больше разрушение, тем сильнее будет раздражение кожи. Это особенно вызывает проблемы при топических способах лечения ОА, целью которых является проникновение активного агента в ткани сустава, причем препарат нужно применять на долгосрочной основе из-за природы заболевания. Изобретатели разработали способы и композиции, доставляющие больше активного ингредиента на единицу дозы, чем ранее известные композиции, поэтому ожидается, что это приведет к снижению степени раздражения кожи.
В композициях изобретения применяется диклофенак натрия, который является широко распространенным NSAID. Диклофенак образует 4 разные соли, проявляющие значительную вариабельность в степени перехода в раствор при различных растворителях. К примеру, Minghetti полагает, что для топического применения лучше всего подходят соли диклофенака с органическими основаниями (Minghetti et al., Ex vivo study of transdermal permeation of four diclofenac salts from different vehicles. Jour. of Pharm. Sci, DOI 10.1002/jps.20770 (2007)).
Другие исследования указывают на микроэмульсии как на средство доставки диклофенака натрия (Kantarci et al., In vitro permeation of diclofenac sodium from novel microemulsion formulations through rabbit skin. Drug Development Research, 65:17-25 (2005); and Sarigullu I. et al., Transdermal delivery of diclofenac sodium through rat skin from various formulations, APS PharmSciTech, 7(4) Article 88, E1-E7 (2006)).
Другие топические композиции диклофенака раскрыты в ряде патентов, включая патенты США №4543251, 4670254, 5374661, 5738869, 6399093 и 6004566. В патентной заявке США No. 20050158348 указано, что для получения гелей широко используются различные растворители, но отмечается, что их потенциал ограничен вследствие раздражения кожи. В этой работе также отмечается, что композиции гелей связаны с быстрым прекращением действия, так как активный агент выпадает из раствора в верхних слоях кожи, что ограничивает противовоспалительное действие в более глубоких тканях. Гели настоящего изобретения предназначены для противоположного, то есть для продолжительного действия и противовоспалительного действия в более глубоких тканях.
2. Гелеобразные композиции диклофенака
Ни в одной из предшествующих работ не изложены композиции изобретения или их применение при лечении ОА. Наоборот, в этих работах подчеркивается значительная, но неудовлетворенная потребность в отношении топических способов лечения ОА для хронического применения и сложность трансдермального транспорта вообще, при этом наблюдается значительная вариабельность проницаемости при изменении элементов композиции или их относительных пропорций.
В свете вышесказанного имеется значительная потребность в усовершенствовании при разработке топических форм NSAID, пригодных для долгосрочного применения при лечении ОА. Проблема состоит в том, чтобы разработать оптимальную композицию, которая должна доставлять активное вещество в нижележащие ткани в достаточной концентрации для лечения ОА на долгосрочной основе, и в то же время уменьшить или свести к минимуму степень недопустимого раздражения кожи, вызванного разрушением кожного барьера, и при этом получить такую лекарственную форму и дозировку, которые будут способствовать содействию пациентов. Настоящее изобретение удовлетворяет эти и другие потребности.
Сущность изобретения
Настоящее изобретение преодолевает недостатки предшествующего уровня техники, предоставляя гелеобразные лекарственные формы (композиции) диклофенака натрия для лечения остеоартрита, которые проявляют лучшую продолжительность высыхания, большую вязкость, повышенный трансдермальный перенос и большее фармакокинетическое всасывание in vivo по сравнению с ранее описанными композициями. Более того, предпочтительные гелеобразные композиции диклофенака натрия по настоящему изобретению обеспечивают и другие преимущества, включая подходящую стабильность в течение 6 месяцев, судя по отсутствию каких-либо существенных изменений вязкости, отсутствию разделения фаз и кристаллизации при низких температурах и низкому уровню примесей. Кроме того, данные гелеобразные композиции хорошо пристают к коже, легко размазываются, быстрее сохнут и проявляют большее всасывание in vivo по сравнению с ранее описанными композициями. Таким образом, гелеобразные композиции по настоящему изобретению обеспечивают превосходное средство доставки диклофенака натрия через кожу для лечения остеоартрита по сравнению с ранее описанными композициями.
Итак, в одном воплощении настоящего изобретения представлена гелеобразная композиция, содержащая, состоящая в основном из или состоящая из:
(i) диклофенака натрия;
(ii) DMSO;
(iii) этанола;
(iv) пропиленгликоля;
(v) загустителя;
(vi) необязательно глицерина; и
(vii) воды.
В другом воплощении настоящего изобретения представлен способ лечения остеоартрита у субъекта, страдающего болью в суставах, который включает топическое нанесение на пораженную область сустава у субъекта терапевтически эффективного количества гелеобразной композиции, содержащей, состоящей в основном из или состоящей из:
(i) диклофенака натрия;
(ii) DMSO;
(iii) этанола;
(iv) пропиленгликоля;
(v) загустителя;
(vi) необязательно глицерина; и
(vii) воды;
при этом происходит лечение остеоартрита.
В следующем воплощении предусматривается применение диклофенака натрия при получении медикамента для лечения боли, причем медикамент включает гелеобразную композицию, содержащую, состоящую в основном из или состоящую из:
(i) диклофенака натрия;
(ii) DMSO;
(iii) этанола;
(iv) пропиленгликоля;
(v) загустителя;
(vi) необязательно глицерина; и
(vii) воды.
В следующем воплощении настоящего изобретения представлена гелеобразная композиция, содержащая, состоящая в основном из или состоящая из раствора диклофенака натрия и по меньшей мере одного загустителя, который может быть выбран из полимеров целлюлозы, полимеров карбомеров, производных карбомеров, производных целлюлозы, поливинилового спирта, полиоксамеров, полисахаридов и их смесей.
В одном аспекте этого воплощения раствор диклофенака натрия содержит, состоит в основном из или состоит из:
(i) диклофенака натрия;
(ii) DMSO;
(iii) этанола;
(iv) пропиленгликоля;
(v) необязательно глицерина; и
(vi) воды.
В одном аспекте вышеприведенных воплощений загуститель может быть выбран из полимеров целлюлозы, полимеров карбомеров, производных карбомеров, производных целлюлозы, поливинилового спирта, полиоксамеров, полисахаридов и их смесей.
В одном аспекте вышеприведенных воплощений геля диклофенак натрия составляет 1-5% массы, как то 1, 2, 3, 4 или 5% массы; DMSO составляет 30-60% массы; этанол составляет 1-50% массы; пропиленгликоль составляет 1-15% массы; глицерин составляет 0-15% массы; загуститель находится в таком количестве, что конечная вязкость геля составляет от 10 до 50000 сантипуаз; а вода добавляется до 100% массы. В других аспектах глицерин составляет 0-4% массы. В следующих аспектах глицерин отсутствует.
В другом аспекте вышеприведенных воплощений диклофенак натрия составляет 2%; DMSO составляет 45,5% массы; этанол составляет 23-29% массы; пропиленгликоль составляет 10-12% массы; гидроксипропилцеллюлоза (HY119) составляет 0-6% массы; глицерин составляет 0-4%; а вода добавляется до 100% массы. В других аспектах глицерин в гелеобразной композиции отсутствует. В следующих аспектах конечная вязкость геля составляет 500-5000 сантипуаз.
Особенность вышеприведенных гелеобразных композиций состоит в том, что при нанесении их на кожу скорость высыхания и трансдермальный перенос будут выше, чем у ранее описанных композиций, таких как приведенные в патентах США №4575515 и 4652557. Другие особенности предпочтительных композиций включают снижение деградации диклофенака натрия, который разлагается меньше, чем на 0,04% за 6 месяцев при рН 6,0-10,0, например при рН 9,0.
В некоторых воплощениях гелеобразные композиции по изобретению содержат 1-5% глицерина, а при нанесении их на кожу скорость высыхания и трансдермальный перенос будут выше, чем у сравнительной жидкой композиции. В некоторых аспектах скорость высыхания приводит к образованию остатка не более 50% от исходного количества через 24 часа, а трансдермальный перенос в 1,5 или более раз выше, чем у сравнительной жидкой композиции при определении по методике с использованием ячейки Франца при ограниченном или неограниченном дозировании или том и другом.
В других воплощениях гелеобразные композиции и способы их применения обеспечивают уменьшение боли за 12 недель при топическом их применении. В различных аспектах гелеобразные композиции применяются по два раза в день, а боль может быть вызвана остеоартритом.
Эти и другие цели, воплощения и преимущества станут более понятными после прочтения вместе с фигурами подробного описания, которое следует ниже.
Краткое описание фигур
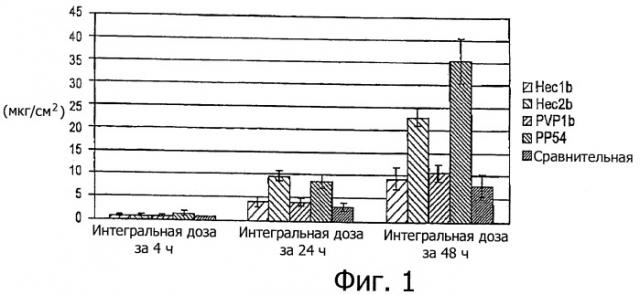
На фиг.1 представлена гистограмма скорости переноса у гелей, полученных с помощью НЕС и PVP. В диффузионные ячейки Франца вносили по 15 мг на ячейку.
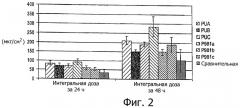
На фиг.2 представлена гистограмма скорости переноса у гелей, полученных с помощью Carbopol 981 и Ultrez 10. В диффузионные ячейки Франца вносили по 200 мкл на ячейку.
На фиг.3 представлена гистограмма скорости переноса у гелей, полученных с помощью Carbopol 971 и Carbopol 981. В диффузионные ячейки Франца вносили по 50 мкл на ячейку.
На фиг.4 представлена гистограмма скорости переноса у различных гелей и сравнительной жидкой композиции. В ячейки Франца вносили по 10 мг на ячейку.
На фиг.5 представлена гистограмма, иллюстрирующая влияние рН на скорость переноса у различных гелей и сравнительной жидкой композиции. В диффузионные ячейки Франца вносили по 7 мг на ячейку.
На фиг.6 представлена гистограмма скорости переноса у различных гелей. В ячейки Франца вносили по 7 мг на ячейку.
На фиг.7 представлена гистограмма скорости переноса у различных композиций диклофенака. Сравнительную жидкую композицию (1,5% диклофенака натрия) вносили по 20 мг на ячейку Франца, препарат Solaraze® (коммерчески доступный гель с 3% диклофенака натрия) вносили по 10 мг на ячейку Франца, а композицию по изобретению, F14/2, вносили по 15 мг на диффузионную ячейку Франца. При таком дозировании во все ячейки попадало одинаковое количество диклофенака натрия.
На фиг.8 представлена гистограмма скорости переноса в мультидозовых экспериментах. Сравнительную жидкую композицию вносили по 0,9 мг на ячейку Франца через 0, 4, 8 и 12 ч. Композицию по изобретению, F14/2, вносили по 1,5 мг на ячейку Франца через 0 и 6 ч.
На фиг.9 представлена гистограмма скорости переноса у различных композиций диклофенака. В ячейки Франца вносили по 20 мг на ячейку.
На фиг.10 представлена гистограмма данных по скорости переноса диклофенака из гелей, приведенных в Baboota et al., и гелей настоящего изобретения. В ячейки Франца вносили по 4 мг на ячейку.
На фиг.11 представлен профиль высыхания по времени у трех гелеобразных и одной жидкой композиции диклофенака натрия.
На фиг.12 представлены стационарные концентрации диклофенака натрия в плазме in vivo после применения жидкой либо гелеобразной композиции.
Раскрытие сущности изобретения
I. Определения
Термин "трансдермальный" в настоящем изобретении обычно применяется для обозначения процессов, совершающихся через кожу. Термины "трансдермальный" и "чрескожный" применяются взаимозаменяемым образом по всему описанию.
Термин "топическая лекарственная форма (композиция)" в настоящем изобретении обычно применяется для обозначения таких композиций, которые можно наносить на кожу или слизистые. Топические композиции, к примеру, могут применяться для оказания терапевтической пользы пациенту или косметической пользы клиенту. Топические формы могут использоваться как для топического, так и трансдермального введения субстанций.
Термин "топическое введение" в настоящем изобретении обычно применяется для обозначения доставки субстанций, как то терапевтически активных веществ, на кожу или в локализованную область организма.
Термин "трансдермальное введение" в настоящем изобретении обычно применяется для обозначения введения через кожу. Трансдермальное введение часто применяется тогда, когда требуется системное введение активного вещества, хотя оно может использоваться и для доставки активного вещества в лежащие под кожей ткани при минимальном системном всасывании.
Термин "усилитель проникновения" в настоящем изобретении обычно применяется для обозначения веществ, улучшающих транспорт таких молекул, как активные вещества (напр., лекарства), в или через кожу. Различные заболевания могут возникать в разных местах организма либо на коже, либо под кожей, что вызывает потребность в прицельной доставке соединений. Например, при лечении остеоартрита может потребоваться доставка активного вещества в лежащие относительно глубоко ткани суставов для достижения терапевтической пользы. Таким образом, "усилитель проникновения" может применяться для усиления доставки активного вещества непосредственно в кожу или нижележащую ткань либо косвенным образом в пораженное заболеванием место через системное распределение. Усилитель проникновения может представлять собой чистое вещество или может содержать смесь различных химических образований.
Термин "ограниченное дозирование" в настоящем изобретении обычно применяется для обозначения применения ограниченного резервуара активного вещества. Резервуар активного вещества со временем истощается, что ведет к плавному снижению скорости всасывания активного вещества после достижения максимальной скорости всасывания.
Термин "неограниченное дозирование" в настоящем изобретении обычно применяется для обозначения применения большого резервуара активного вещества. Резервуар существенно не истощается со временем, что обеспечивает долгосрочный непрерывный стационарный уровень всасывания активного вещества.
В настоящем изобретении термин "сравнительная жидкая композиция" или "сравнительная" относится к такой композиции, которая описана в патентах США №4575515 и 4652557 и состоит из 1,5% диклофенака натрия, 45,5% диметилсульфоксида, 11,79% этанола, 11,2% пропиленгликоля, 11,2% глицерина и воды.
II. Гелеобразные композиции
1. Компоненты гелеобразных композиций
В стремлении получить гелеобразную композицию диклофенака натрия с улучшенными параметрами продолжительности высыхания, повышенным трансдермальным переносом и большим фармакокинетическим всасыванием in vivo, большей вязкостью, хорошим прилипанием к коже и способностью легко размазываться при сохранении стабильности во времени авторы изобретения открыли, что для получения гелеобразных композиций настоящего изобретения можно использовать неожиданно выгодную комбинацию из следующих компонентов.
Настоящим изобретением предусмотрены гелеобразные композиции, содержащие активное вещество, предпочтительно нестероидный противовоспалительный препарат или его фармацевтически приемлемую соль. Более предпочтительно нестероидное противовоспалительное средство представляет собой диклофенак, который может существовать в виде различных солей, включая соли натрия, калия и диэтиламина. В предпочтительном воплощении используется натриевая соль диклофенака. Диклофенак натрия может составлять приблизительно от 0,1% до 10%, как то 1, 2, 3, 4 или 5% массы. Как известно, при использовании натриевой соли возникают проблемы со стабильностью водного геля, состоящие в том, что высокие концентрации соли могут вызвать разрушение матрикса геля при взаимодействии с некоторыми загустителями.
В другом воплощении настоящего изобретения содержится усилитель проникновения. Усилителем проникновения может быть диметилсульфоксид ("DMSO") или его производные. DMSO может содержаться в количестве от 1% до 70% массы, более предпочтительно от 25% до 60%, как то 25, 30, 40, 45, 50, 55 или 60% массы. Предпочтительно в настоящем изобретении DMSO используется в концентрации от 40 до 50% массы, как то 41, 42, 43, 44, 45, 46, 47,48, 49 и 50% и все дробные части между ними, как то 44, 44,5, 45, 45,5, 46, 46,5% и т.д.
В некоторых воплощениях настоящего изобретения содержится низший спирт-алканол, как то метанол, этанол, пропанол, бутанол или их смеси. В некоторых воплощениях алканол составляет от 1 до 50% массы. Предпочтительно используется этанол в количестве 1-50% массы, как то 1, 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50% массы и все дробные части между ними.
В некоторых воплощениях настоящего изобретения содержится многоатомный спирт, как то гликоль. К подходящим гликолям относятся этиленгликоль, пропилен-гликоль, бутиленгликоль, дипропиленгликоль, гексантриол и их комбинации. Предпочтительно используется пропиленгликоль в количестве 1-15% массы, как то 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15% массы и все дробные части между ними.
В некоторых воплощениях настоящего изобретения содержится глицерин (также именуется глицеролом) в концентрации 0-12% массы. Предпочтительно глицерин используется в количестве 0-4% массы, как то 0, 1, 2, 3 или 4% массы и все дробные части между ними. В некоторых воплощениях глицерин в композициях не содержится.
В предпочтительном воплощении настоящего изобретения представлена композиция, включающая раствор диклофенака и по меньшей мере один загуститель для образования геля. Этот по меньшей мере один загуститель настоящего изобретения может представлять собой акриловый полимер (например, полимер Carbopol, поликарбофил Noveon или полимерный эмульгатор Pemulen, которые коммерчески доступны из фирмы Noveon Inc. of Cleveland, Ohio), производное акрилового полимера, полимер целлюлозы, производное полимера целлюлозы, поливиниловый спирт, полиоксамер, полисахарид или их смесь. Предпочтительно этим по меньшей мере одним загустителем является гидроксипропилцеллюлоза (НРС), которая используется таким образом, чтобы конечная вязкость составляла от 10 до 50000 сантипуаз. Более предпочтительно конечная вязкость составляет от 500 до 20000 сантипуаз.
Настоящая гелеобразная композиция может необязательно включать по меньшей мере один антиоксидант и/или одно хелатирующее вещество.
Предпочтительные антиоксиданты для использования в настоящем изобретении могут быть выбраны из группы, состоящей из бутилированного гидрокситолуола (ВНТ), бутилированного гидроксианизола (ВНА), аскорбиллинолеата, аскорбилдипальмитата, аскорбилтокоферолмалеата, аскорбата кальция, каротеноидов, койевой кислоты, тиогликолевой кислоты, токоферола, токоферола ацетата, токоферета-5, токоферета-12, токоферета-18, токоферета-80 и их смесей.
Предпочтительные хелатирующие вещества могут быть выбраны из группы, состоящей из этилендиаминтетрауксусной кислоты (EDTA), двуаммониевой соли EDTA, двукалиевой соли EDTA, кальций-двунатриевой соли EDTA, HEDTA, TEA-EDTA, четырехнатриевой соли EDTA, трикалиевой соли EDTA, тринатрийфосфата, диаммоний-цитрата, галактаровой кислоты, галактуроновой кислоты, глюконовой кислоты, глюкуроновой кислоты, гуминовой кислоты, циклодекстрина, цитрата калия, калиевой соли EDTMP, цитрата натрия, натриевой соли EDTMP и их смесей.
Кроме того, топические композиции настоящего изобретения также могут содержать рН-регулирующие вещества. В одном конкретном воплощении рН-регулирующим веществом является основание. К подходящим рН-регулирующим веществам относятся бикарбонаты, карбонаты и гидроксиды, как то гидроксиды щелочных и щелочноземельных металлов, а также гидроксиды переходных металлов. С другой стороны, рН-регулирующим веществом может быть и кислота, соль кислоты или их смеси. Кроме того, рН-регулирующим веществом может быть и буфер. К подходящим буферам относятся буферы на основе цитрата/лимонной кислоты, ацетата/уксусной кислоты, фосфата/фосфорной кислоты, формиата/муравьиной кислоты, пропионата/пропионовой кислоты, лактата/молочной кислоты, карбоната/угольной кислоты, аммония/аммиака и т.п. рН-регулирующее вещество содержится в количестве, достаточном для доведения значения рН композиции в интервале от рН 4,0 до 10,0, более предпочтительно от рН 7,0 до 9,5. В некоторых воплощениях незарегулированное значение рН смешанных компонентов составляет от 8 до 10, как то 9, без необходимости добавления каких-либо рН-регулирующих веществ.
2. Характеристики гелеобразных композиций
а) Трансдермальный перенос
Как представлено ниже в Примерах, настоящим изобретением предусмотрена гелеобразная лекарственная форма диклофенака натрия, которая проявляет неожиданно эффективную скорость трансдермального переноса в сравнении с ранее описанными композициями.
Соответственно, в одном воплощении данная гелеобразная лекарственная форма, содержащая нестероидное противовоспалительное средство и по меньшей мере один загуститель, имеет скорость переноса, при определении методом ограниченного дозирования в ячейке Франца, равную или большую, чем скорость переноса у сравнительной жидкой композиции. Предпочтительно скорость переноса превышает скорость переноса у сравнительной жидкой композиции. Более предпочтительно скорость переноса по меньшей мере в 1,5 раза больше, чем у сравнительной жидкой композиции. Иными словами, соотношение между: (i) скоростью переноса у гелеобразной композиции, содержащей нестероидное противовоспалительное средство и по меньшей мере один загуститель, и (ii) скоростью переноса у сравнительной жидкой композиции предпочтительно превышает 1,0, более предпочтительно составляет по меньшей мере 1,5.
В другом воплощении настоящего изобретения еще предусмотрена гелеобразная композиция диклофенака натрия, содержащая раствор диклофенака и по меньшей мере один загуститель, у которой скорость переноса, при определении методом ограниченного дозирования в ячейке Франца, по меньшей мере равна скорости переноса у самого раствора диклофенака. Предпочтительно скорость переноса у гелеобразной композиции диклофенака натрия по меньшей мере в 2,0 раза больше, чем скорость переноса у самого раствора диклофенака натрия. Более предпочтительно предусмотренная настоящим изобретением гелеобразная композиция диклофенака натрия имеет скорость переноса, по меньшей мере в 4,0 раза большую, чем у самого раствора диклофенака натрия. Иными словами, соотношение между: (i) скоростью переноса у гелеобразной композиции диклофенака натрия и (ii) скоростью переноса у раствора диклофенака натрия составляет по меньшей мере 1,0, предпочтительно по меньшей мере 2,0, более предпочтительно по меньшей мере 4,0.
В следующем воплощении настоящего изобретения предусмотрена гелеобразная композиция диклофенака натрия, содержащая диклофенак натрия и по меньшей мере один загуститель, у которой скорость переноса, при определении методом множественного ограниченного дозирования в ячейке Франца (дозирование при 2,5 мг/см2 через 0 и 6 часов), составляет по меньшей мере 0,1 мкг/ч/см2 через 24 часа, предпочтительно по меньшей мере 0,2 мкг/ч/см2 через 24 часа.
b) Вязкость
В следующем воплощении настоящего изобретения предусмотрена гелеобразная композиция, содержащая нестероидное противовоспалительное средство (NSAID) и по меньшей мере один загуститель, у которой вязкость составляет по меньшей мере 100 сП. Предпочтительно вязкость гелеобразной композиции составляет по меньшей мере 500 сП. Более предпочтительно вязкость гелеобразной композиции составляет по меньшей мере 1000 сП. В других воплощениях вязкость составляет 5000-10000, 10000-15000 или 15000-20000 сП.
В следующем воплощении настоящего изобретения предусмотрена гелеобразная композиция диклофенака, содержащая раствор диклофенака и по меньшей мере один загуститель, у которой вязкость составляет около 1000 сП, а скорость переноса - по меньшей мере 0,2 мкг/см2/ч при определении методом множественного ограниченного дозирования (2,5 мг/см2 через 0 и 6 часов) в ячейке Франца через 24 часа.
c) Стабильность
Стабильность композиции лекарственного препарата может иметь значительное влияние на продолжительность и стоимость разработки препарата, характер исследований, необходимых для подтверждения заявок в регулятивных органах, безопасность и окончательное одобрение.
Важно, к примеру, свести к минимуму количество примесей или продуктов деградации, образующихся со временем вследствие взаимодействий между различными ингредиентами в композиции. Это может быть особенно важным для композиций, предназначенных для повышения проницаемости кожи.
Так, в некоторых воплощениях настоящего изобретения предусмотрена гелеобразная композиция диклофенака натрия, которая разлагается менее чем на 1% за 6 месяцев при комнатной температуре. Более предпочтительно скорость разложения составляет менее 0,9, 0,8, 0,7, 0,6, 0,5, 0,4, 0,3, 0,2 или менее 0,1% и все дробные части между ними за 6 месяцев при комнатной температуре.
d) Продолжительность высыхания
В сравнении с ранее раскрытыми композициями, такими как в патентах США №4575515 и 4652557 (которые в настоящем изобретении именуются как "сравнительные жидкие композиции" или "сравнительные"), композиции по изобретению высыхают быстрее и в то же время достигают большего трансдермального переноса препарата. Удивительно, что можно одновременно достичь большей скорости переноса и большей скорости высыхания, поскольку известно, что увлажнение кожи вызывает повышение трансдермального переноса или проникновения. Подсыхание кожи, вызванное быстрым испарением, должно уменьшить трансдермальный транспорт препарата, остающегося на коже. Различия в продолжительности высыхания проявляются при нанесении равного количества двух препаратов на противоположные конечности. За тридцать (30) минут композиции по изобретению почти полностью высыхают, тогда как еще остается значительное количество ранее описанной жидкой композиции.
Для более количественного сравнения продолжительности высыхания проводили параллельные определения. С этой целью авторы изобретения измеряли остаточный вес композиций, помещая равные количества (100 мг) композиции предшествующего уровня техники и композиций по изобретению на чашки весов площадью 10 см2 и взвешивая остающееся количество по времени. По этой методике сразу же отмечаются различия, которые становятся очень сильными через 4 часа (табл.11 и фиг.10).
е) Фармакокинетика
Проводили сравнение всасывания диклофенака натрия из композиций по изобретению и сравнительных композиций из патентов США №4575515 и 4652557 на животных. Гели по изобретению проявляли лучшее всасывание в пересчете на дозу, чем сравнительные жидкие композиции из этих патентов. В абсолютных величинах клиническая доза гелей по изобретению давала максимальную наблюдавшуюся в плазме концентрацию (Cmax) в стационарном состоянии 81 нг/мл и площадь под кривой (AUC) 584 нг/мл по сравнению с 12 нг/мл и 106 нг/мл у сравнительных композиций.
Эти результаты подчеркивают свойства носителя при доставке активного вещества. Большие цифры у геля наблюдались даже при том, что композицию раствора наносили четыре (4) раза в день (в сумме 5,2 мл) в сравнении с двумя (2) разами в день (в сумме 4,0 мл) для гелей.
III. Получение гелеобразных композиций
В следующем воплощении настоящего изобретения предусмотрен способ получения гелеобразных композиций диклофенака натрия. Гелеобразные композиции по настоящему изобретению предпочтительно получают путем выполнения следующих операций: (i) диспергирования загустителя, его производного и/или смеси в диметилсульфоксиде и перемешивания в течение 1 часа; (ii) растворения диклофенака натрия в водно-спиртовой смеси (напр., смеси этанол/вода); (iii) диспергирования пропиленгликоля и глицерина в растворе NSAID по п. (ii); и (iv) внесения полученного раствора NSAID в смесь загуститель/диметилсульфоксид и перемешивания в течение 1 часа при комнатной температуре. С другой стороны, гелеобразные композиции по настоящему изобретению можно получить путем выполнения следующих операций: (i) растворения NSAID (напр., диклофенака натрия) в спиртовом растворе DMSO (напр., смеси этанол/ диметилсульфоксид); (ii) диспергирования загустителя, его производного и/или смеси в растворе вода/пропиленгликоль/глицерин и перемешивания в течение 1 часа; (iii) внесения раствора NSAID по п. (i) в смесь загустителя по п. (ii) и перемешивания в течение 1 часа при комнатной температуре. Также при этих процессах смешивания можно использо