Циклические противомикробные пептиды
Иллюстрации
Показать всеНастоящее изобретение относится к циклическим катионным пептидам и их применению в лечении грибковых инфекций. 13 з.п. ф-лы, 4 табл., 1 пр.
Реферат
Область изобретения
Настоящее изобретение относится к циклическим катионным пептидам и их применению в лечении микробных инфекций.
Предшествующий уровень техники
Противомикробные пептиды (AMP) образуют основу эукариотического иммунитета и обеспечивают первую линию защиты против повреждения поверхностей кожи и слизистых оболочек микроорганизмами. Примеры природных AMP включают семейства дефензиновых и кателицидиновых пептидов. Эти AMP являются гетерогенными по длине, последовательности и структуре, но для большинства характерны их небольшой размер, суммарный катионный заряд и амфипатическая структура. Небольшие, катионные, противомикробные пептиды были выделены также из многих бактерий, грибов, растений, беспозвоночных и позвоночных и, по-видимому, также играют роль в защите прокариотических клеток.
Природные AMP демонстрируют активность широкого спектра против грамположительных и грамотрицательных бактерий, дрожжей, грибов и оболочечных вирусов. Микробные патогены, по-видимому, не приобретают устойчивости к этим катионным пептидам, и поэтому AMP были сохранены в качестве жизненно важных естественных молекул иммунной защиты хозяина на протяжении тысячелетий эволюции. Поэтому неудивительно, что AMP были вовлечены в качестве потенциальных мишеней для терапевтических средств против широкого диапазона инфекций. Однако тот факт, что они являются технически сложными и дорогостоящими для производства в рекомбинантных системах и обладают мощными хемотаксическими и биологическими функциями, исключает применение природных форм AMP в качестве терапевтических средств.
В находящейся на совместном рассмотрении заявке авторы изобретения показали, что линейные пептиды, обогащенные определенными основными остатками, такими как лизин или аргинин, обладают противомикробной активностью и, в частности, противогрибковой активностью. Однако существует необходимость в дополнительных агентах, которые могут быть использованы в лечении или предупреждении микробных инфекций.
Изложение сущности изобретения
Согласно первому аспекту изобретения предложен пептид, содержащий от 2 до примерно 200 D- и/или L-аминокислот, которые могут быть одинаковыми или разными, где указанные аминокислоты выбраны из группы, состоящей из гидрофобных аминокислот и/или катионных аминокислот, и где указанный пептид является циклическим. Циклический пептид может содержать от 3 до примерно 100 D- и/или L-аминокислот, например, от 3 до 50 D- и/или L-аминокислот, включающих от 4 до примерно 50 D- и/или L-аминокислот.
Пептиды по изобретению полезны в лечении или предупреждении микробных инфекций.
Циклические пептиды по изобретению являются желательными в качестве терапевтических средств, поскольку они являются высокоэффективными, протеолитически стабильными, по существу нечувствительными к солям, негепатотоксичными, негемолитичными и легкими для синтеза.
Катионный заряд пептидов по изобретению, как полагают, облегчает ассоциацию пептида с полярными концевыми группами микробных мембран. Стабилизация заряженных групп в более плотной конформации путем циклизации, как полагают, усиливает это притяжение, увеличивая таким образом противомикробный потенциал пептидов.
В другом аспекте изобретения предложен пептид, содержащий аминокислоты в соответствии с формулой I:
где l и m представляют собой целые числа от 0 до 10, такие, что и l, и m не равны 0, n представляет собой целое число от 1 до 10, Х и Y, которые могут быть одинаковыми или разными, представляют собой аминокислоту, выбранную из группы, состоящей из гидрофобных аминокислот и/или катионных аминокислот, и где пептид является циклическим, для применения в качестве лекарственного средства.
Пептид может содержать от 2 до 50 аминокислот, например 3, 4, 5, 6 или от 7 до 50 аминокислот, включая 3, 4, 5, 6 или от 7 до 10, 15, 20, 25, 30, 35, 40, 45 или 50 аминокислот.
В предпочтительном аспекте изобретения пептид содержит от 2 до 15 аминокислот, например от 3 до 15 аминокислот. Более предпочтительно, пептид содержит от 5 до 13 аминокислот. Еще более предпочтительными являются пептиды, содержащие от 3 до 7 аминокислот, например 7 аминокислот.
Как известно специалисту, аминокислоты могут быть разделены на разные классы, в основном в зависимости от химических и физических свойств аминокислотной боковой цепи. Например, некоторые аминокислоты обычно считаются гидрофильными или полярными аминокислотами, а другие считаются гидрофобными или неполярными аминокислотами. Гидрофобная аминокислота может быть выбрана из группы гидрофобных аминокислот, состоящей из глицина, лейцина, фенилаланина, пролина, аланина, триптофана, валина, изолейцина, метионина, тирозина и треонина; катионные аминокислоты могут быть выбраны из группы, состоящей из орнитина, гистидина, аргинина и лизина. Как использовано в данном описании, термины "гидрофобный" и "катионный" могут относиться к аминокислотам, обладающим гидрофобностью, которая больше или равна -1,10, и/или чистым зарядом, который больше или равен 0, как описано в Fauchere and Pliska Eur. J. Med Chem. 10:39 (1983). Гидрофобная или неполярная аминокислота может относиться также к аминокислоте, имеющей боковую цепь, которая не заряжена при физиологическом рН, не полярна и которая обычно отталкивается водным раствором. Аминокислоты могут встречаться в природе или могут быть синтетическими.
В предпочтительном аспекте изобретения Х и/или Y представляют собой катионные аминокислоты, выбранные из группы, состоящей из гистидина, орнитина, аргинина и лизина. Более предпочтительно, Х и/или Y представляют собой аргинин или лизин.
Х и/или Y могут представлять собой оптические изомеры гидрофобной или катионной аминокислоты, как определено в данном описании, например D-или L-аминокислоты. Предпочтительно, Х и/или Y представляют собой D-аминокислоты.
В предпочтительном аспекте изобретения пептид формулы (I) состоит из по меньшей мере 90%, например по меньшей мере 95%, например 97-99% или даже 100% D-аминокислот.
В предпочтительном аспекте изобретения пептид формулы (I) состоит из по меньшей мере 90%, например по меньшей мере 95%, например 97-99% или даже 100% L-аминокислот.
Изобретение также включает известные изомеры (структурные, стерео-, конформационные и конфигурационные), пептидомиметики, структурные аналоги вышеупомянутых аминокислот и аминокислоты, модифицированные либо в природе (например, посттрансляционная модификация), либо химически, включая, но не ограничиваясь этим, фосфорилирование, гликозилирование, сульфонилирование и/или гидроксилирование.
В общих чертах пептид по изобретению не включает аминокислоты: аспаргиновую кислоту, глутаминовую кислоту, аспарагин, глутамин или серин, но некоторые пептиды по изобретению могут обладать активностью даже тогда, когда эти аминокислоты присутствуют.
В другом предпочтительном аспекте Х и Y являются одинаковыми. Более предпочтительно, Х и Y являются одинаковыми и представляют собой лизин или аргинин.
В пептиде формулы (I) l и m могут быть равны 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 и n может быть равен 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
В пептиде формулы (I) l может быть равен 1, n может быть равен 1 и m может составлять от 4 до 9, например, m может быть равен 3, 4, 5, 6, 7, 8 или 9.
В пептиде формулы (I) l, n и/или m могут составлять от 1 до 5, например, 1, 2, 3, 4 или 5.
В пептиде формулы (I) l и m могут представлять собой целое число от 0 до 7 и n может представлять собой целое число от 1 до 10.
В пептиде формулы (I) l и m могут представлять собой 0, 1 или 2 и n может представлять собой целое число от 1 до 10.
В пептиде формулы (I) Х и Y могут быть одинаковыми, l может быть равен 0, m может быть равен 1 и n может быть равен 3, 4, 5, 6, 7, 8, 9 или 10.
В пептиде формулы (I) X и Y могут быть одинаковыми, l и m могут быть равны 1 и n может быть равен 2, 3, 4 или 5.
В пептиде формулы (I) Х и Y могут быть одинаковыми, l может быть равен 1, m может быть равен 2 и n может быть равен 1, 2, 3 или 4.
В пептиде формулы (I) Х и Y могут быть одинаковыми, l и m могут быть равны 2 и n может быть равен 1, 2, 3 или 4.
В другом аспекте изобретения предложен циклический пептид, содержащий аминокислоты в соответствии с формулой II:
где Х и n являются такими, как определено в данном описании. Предпочтительно, Х представляет собой лизин, аргинин или орнитин. Предпочтительно, n представляет собой целое число от 3 до 15.
В одном воплощении изобретения Х представляет собой аргинин.
В альтернативном воплощении изобретения Х представляет собой лизин.
В еще одном альтернативном воплощении изобретения Х представляет собой орнитин.
Пептиды по изобретению могут включать один или более цистеиновых остатков, например, вплоть до 6 цистеиновых остатков, например, 1, 2, 3, 4, 5 или 6 цистеиновых остатков.
Кроме того, аминокислотная последовательность пептида может быть модифицирована таким образом, чтобы дать вариант пептида, который включает замену по меньшей мере одного аминокислотного остатка в пептиде другим аминокислотным остатком, включая замены, в которых используется D-, а не L-форма.
Один или более чем один остаток пептида может быть заменен другим для того, чтобы изменить, усилить или сохранить биологическую активность пептида. Такой вариант может иметь, например, по меньшей мере примерно 10% биологической активности соответствующего невариантного пептида. Часто используют консервативные аминокислоты, т.е. замены аминокислот со сходными химическими и физическими свойствами, как описано выше. Поэтому, например, замены консервативных аминокислот могут включать замену лизина на аргинин, орнитин или гистидин; или замену аргинина на лизин или изолейцин, орнитина на гистидин; или замену одной гидрофобной аминокислоты на другую. После введения замен варианты подвергают скринингу на биологическую активность.
Термин "пептид", как использовано в данном описании, означает, в общих чертах, множество аминокислотных остатков, соединенных вместе пептидной связью. Он используется взаимозаменяемо и означает то же самое, что полипептид и протеин.
В одном воплощении изобретения циклический пептид выбран из группы, состоящей из:
К-К-К-К-К-К-К
R-R-R-R-R-R-R.
Пептиды по изобретению обычно представляют собой синтетические пептиды. Пептиды могут представлять собой выделенные, очищенные пептиды или их варианты, которые могут быть синтезированы in vitro, например, с использованием способа твердофазного синтеза пептидов, синтеза пептидов, катализируемого ферментами, или с помощью технологии рекомбинантной ДНК.
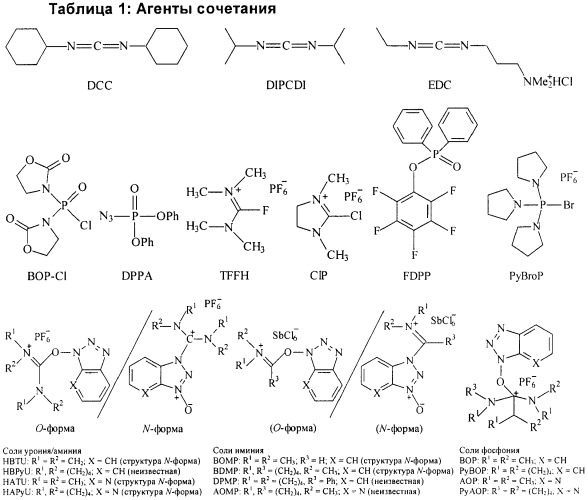
В другом аспекте изобретения предложен способ получения пептида по изобретению, включающий циклизацию пептида формулы (I) или (II) путем взаимодействия пептида с агентом сочетания.
Агент сочетания может представлять собой любой агент, способный образовывать пептидную связь между двумя концевыми (С- и N-концевыми) аминокислотными остатками пептида, когда он находится в линейной форме, например, между двумя аминокислотными скелетами или боковыми цепями. Выбор агента сочетания может влиять на эффективность сочетания и, следовательно, на выход циклического пептида. Примеры агентов сочетания, полезных в способе по изобретению, представлены в Таблице 1, хотя специалисту будут известны и другие известные агенты сочетания, которые также полезны в изобретении. Предпочтительно, агент сочетания представляет собой HATU - O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат.
Предпочтительно, реакция между пептидом и агентом сочетания происходит в присутствии основания. Основание может включать, но не ограничивается этим, н-метилморфолин (NMM) или диизопропилэтиламин (DIEA). Предпочтительно, реакция происходит при щелочном рН, например, при рН 8,5-9. Пептид может быть модифицирован для включения защитной группы перед его взаимодействием с агентом сочетания. Защитные группы могут включать Pbf (2,2,4,6,7-пентаметилдигидробензофуран-5-сульфонил), tBu (тpeт-бутиловый эфир), Mtr (метокситриметилбензолсульфонил), Рmc (2,2,5,7,8-пентаметилхроман-6-сульфонилхлорид), Mbh (4,4-диметилоксибензилгидрид), Tmob (2,4,6-триметоксибензил), Aloc (аллилоксикарбонил), Fmoc (9-флуоренилметоксикарбонил) и Воc {трет-бутилоксикарбонил). После взаимодействия с агентом сочетания защитная группа может быть удалена путем отщепления в мягких кислотных условиях, например, в присутствии раствора трифторуксусной кислоты (TFA).
Во время скелетной циклизации пептида, пептид на С-конце линейного пептида подвергают воздействию активирующей группы агента сочетания, и в ходе реакции образуется кето-енольное промежуточное соединение на альфа-атоме углерода этой аминокислоты. Поэтому енольное (или алкенольное) промежуточное соединение может приводить к получению двух энантиомеров при удалении активирующей группы с соседнего атома углерода и образовании пептидной связи. Эта рацемизация, т.е. образование соответствующих энантиомеров индивидуальной аминокислоты (например, правовращающей и левовращающей форм (т.е. d- и l-изомеров соответственно)) и получение диастереомеров пептида в целом может происходить в участке циклизации при активации используемым агентом сочетания. Поскольку желательно, чтобы пептиды по изобретению были энантиомерно чистыми, получение нежелательных диастереомеров должно быть уменьшено или предотвращено. Для того чтобы уменьшить или предотвратить это получение диастереомеров и получить диастереомерно чистый пептид, пептид по изобретению может быть модифицирован для включения ахиральной группировки, которая предотвращает рацемизацию пептида во время циклизации.
Таким образом, в другом предпочтительном аспекте изобретения пептид по изобретению или пептид, определенный в способе по изобретению, модифицируют для включения группировки, которая предотвращает образование пептидных диастереомеров во время циклизации. Как использовано в данном описании, "рацемический пептид" представляет собой пептид, который содержит количества (обычно равные количества) соответствующих оптических изомеров, например, правовращающих и левовращающих форм (т.е. d- и l-изомеров соответственно) аминокислоты на С-конце пептида перед циклизацией данного пептида. Группировка, вводимая в пептид, обычно представляет собой ахиральную аминокислоту, которая может представлять собой встречающуюся в природе аминокислоту или аминокислотный аналог. Ахиральная аминокислота может быть выбрана из группы, состоящей из глицина, β-аланина, 3-аминопропановой кислоты, 4-аминомасляной кислоты, 5-аминопентановой кислоты и 6-аминогексановой кислоты. В одном воплощении изобретения пептид модифицирован на С-конце для включения ахиральной аминокислоты, например глицина.
Так же как модификация пептида по изобретению для включения группировки, как определено в данном описании, на С-конце, соотношение двух энантиомеров, образующихся во время циклизации пептида, зависит от нескольких факторов, таких как используемый растворитель, время инкубации и температура во время циклизации (т.е. реакции с агентом сочетания) и активирующей группы, используемой для облегчения циклизации.
Настоящее изобретение дополнительно относится к циклизованным пептидам, получаемым способом по изобретению.
В одном воплощении изобретения циклический пептид содержит аминокислотную последовательность, выбранную из группы, состоящей из:
К-К-К-К-К-К-К
R-R-R-R-R-R-R
O-O-O-O-O-O-O
dR-dR-dR-dR-dR-dR-dR
dO-dO-dO-dO-dO-dO-dO
dK-dK-dK-dK-dK-dK-dK.
Для идентификации активных пептидов, которые обладают незначительной токсичностью или не обладают нежелательной токсичностью в отношении клеток млекопитающих, могут быть получены индивидуальные пептиды или библиотеки пептидов, и индивидуальные пептиды или пептиды из этих библиотек могут быть подвергнуты скринингу на противомикробную активность и токсичность, включая, но не ограничиваясь этим, противогрибковую, антибактериальную, противовирусную, противопротозойную, противопаразитарную активность и токсичность.
Пептиды по изобретению могут существовать в различных формах, таких как свободные кислоты, свободные основания, сложные эфиры и другие пролекарства, соли и таутомеры, например, и данное изобретение включает все вариантные формы данных соединений.
Таким образом, изобретение охватывает соль или пролекарство пептида или пептидного варианта по изобретению.
Пептид по изобретению может быть введен в форме фармацевтически приемлемой соли. Фармацевтически приемлемые соли по настоящему изобретению могут быть синтезированы из родительского пептида, который содержит основную или кислотную группировку, традиционными химическими способами. Обычно такие соли могут быть получены путем взаимодействия свободных кислотных или основных форм пептида со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе, или в смеси их обоих; обычно предпочтительными являются неводные среды, такие как простой эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечни подходящих солей можно найти в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., US, 1985, p.1418, описание которого таким образом включено посредством ссылки; см. также Stahl et al, Eds, "Handbook of Pharmaceutical Salts Properties Selection and Use" Verlag Helvetica Chimica Acta and Wiley-VCH, 2002.
Таким образом, изобретение включает фармацевтически приемлемые соли пептида по изобретению, где родительское соединение модифицируют путем получения его кислотных или основных солей, например, традиционных нетоксичных солей или четвертичных аммониевых солей, которые образуются, например, из неорганических или органических кислот или оснований. Примеры таких солей присоединения кислот включают в себя ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфарат, камфаросульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, лактат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, пальмоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат и ундеканоат. Основные соли включают соли аммония, соли щелочных металлов, такие как соли натрия и калия, соли щелочноземельных металлов, такие как соли кальция и магния, соли с органическими основаниями, такие как соли дициклогексиламина, N-метил-D-глютамин, и соли аминокислот, таких как аргинин, лизин и т.д. Кроме того, основные азотсодержащие группы могут быть кватернизированы такими агентами, как низшие алкилгалогениды, такие как метил-, этил-, пропил- и бутилхлориды, бромиды и йодиды; диалкилсульфаты, такие как диметил-, диэтил-, дибутил- и диамилсульфаты, длинноцепочечные галогениды, такие как децил-, лаурил-, миристил- и стеарилхлориды, бромиды и йодиды, аралкильные галогениды, как бензил- и фенилэтилбромиды и другие.
Соли карбоксильных групп пептида или пептидного варианта по изобретению могут быть получены обычным способом путем приведения пептида в контакт с одним или более эквивалентами желаемого основания, такого как, например, гидроксид металла, например, гидроксид натрия; карбонат или бикарбонат металла, такой как, например, карбонат или бикарбонат натрия; или аминное основание, такое как, например, триэтиламин, триэтаноламин и тому подобное.
Изобретение включает пролекарства активного фармацевтического вида описанного пептида, например, в котором одна или более функциональных групп защищены или дериватизированы, но могут превращаться in vivo в функциональную группу, как в случае сложных эфиров карбоновых кислот, превращающихся in vivo в свободные кислоты, или в случае защищенных аминов, в свободную аминогруппу. Термин "пролекарство", как использовано в данном описании, представлен в конкретных структурах, которые быстро превращаются in vivo в родительскую структуру, например, путем гидролиза в крови.
В другом аспекте изобретения предложена фармацевтическая композиция, содержащая фармацевтически эффективное количество пептида по изобретению, или два или более различных пептидов по изобретению.
Композиция также содержит фармацевтически приемлемый носитель, эксципиент или разбавитель. Фраза "фармацевтически приемлемый" используется в данном описании в отношении тех соединений, веществ, композиций и/или лекарственных форм, которые в пределах обоснованного медицинского заключения подходят для применения в контакте с тканями человека или, в зависимости от обстоятельств, животного без чрезмерных токсичности, раздражения, аллергического ответа или другой проблемы или осложнения, соразмерных с разумным соотношением выгода/риск.
Пептид по изобретению полезен, в частности, в качестве противомикробного пептида, например, против бактерий, грибков, дрожжей, паразитов, простейших и вирусов. Термин "противомикробный пептид" может быть использован в данном описании для определения любого пептида, который обладает микробицидной и/или микробостатической активностью и охватывает, не исключительно, любой пептид, который, как описано, обладает антибактериальными, противогрибковыми, антимикозными, противопаразитарными, противопротозойными, противовирусными, противоинфекционными, антисептическими и/или гермицидными, альгицидными, амебицидными, микробицидными, бактерицидными, фунгицидными, паразитицидными, протозоацидными, протозоицидными свойствами.
В предпочтительном аспекте в изобретении предложено применение пептида по изобретению в изготовлении лекарственного средства для лечения микробной инфекции.
Под "микробной инфекцией" подразумевают инфекцию, вызванную бактерией, паразитом, простейшими, вирусом или грибком, включая дрожжи. "Патоген" обычно определяют как любой организм, вызывающий заболевание.
Бактериальный патоген может быть производным бактериального вида, выбранного из группы, но не ограниченного данной группой, состоящей из: Staphylococcus spp., например, Staphylococcus aureus (например, Staphylococcus aureus NCTC 10442), Staphylococcus epidermidis; Chlamydia spp., например, Chlamydia trachomatis, Chlamydia pneumoniae, Chlamydia psittaci; Enterococcus spp., например, Enterococcus faecalis; Streptococcus pyogenes; Listeria spp.; Pseudomonas spp.; Mycobacterium spp., например, Mycobacterium tuberculosis; Enterobacter spp.; Campylobacter spp.; Salmonella spp.; Streptococcus spp., например, Streptococcus группы А или В, Streptoccocus pneumoniae; Helicobacter spp., например, Helicobacter pylori; Neisseria spp., например, Neisseria gonorrhea, Neisseria meningitidis; Borrelia burgdorferi; Shigella spp., например, Shigella flexneri; Escherichia coli (E.coli O157:H7 NCTC 12900); Haemophilus spp., например, Haemophilus influenzae; Francisella tularensis; Bacillus spp., например, Bacillus anthracis; Clostridia spp., например, Clostridium botulinum; Yersinia spp., например, Yersinia pestis; Treponema spp.; Burkholderia spp.; например, Burkholderia cepacia, B. mallei и B. pseudomallei.
В предпочтительном применении по изобретению бактериальный патоген представляет собой Staphyloccus aureus или E.coli.
Вирусный патоген может быть производным вируса, выбранного, но не ограниченного этим, из группы, состоящей из: вируса иммунодефицита человека (ВИЧ 1 и 2); вируса Т-клеточного лейкоза человека (HTLV 1 и 2); вируса Эбола; вируса папилломы человека (например, HPV-2, HPV-5, HPV-8, HPV-16, HPV-18, HPV-31, HPV-33, HPV-52, HPV-54 и HPV-56); паповавируса; риновируса; полиовируса; вируса герпеса; аденовируса; вируса Эпштейна-Барра; вируса гриппа, вирусов гепатита В и С, вируса оспы, ротавируса или коронавируса SARS (атипичной пневмонии).
Паразитарный патоген может быть производным паразита, выбранного, но не ограниченого этим, из группы, состоящей из Trypanosoma spp. (Trypanosoma cruzi, Trypanosoma brucei), Leishmania spp., Giardia spp., Trichomonas spp., Entamoeba spp., Naegleria spp., Acanthamoeba spp., Schistosoma spp., Plasmodium spp., Crytosporidium spp., Isospora spp., Balantidium spp., Loa Loa, Ascaris lumbricoides, Dirofilaria immitis, Toxoplasma ssp., например, Toxoplasma gondii.
В предпочтительном применении по изобретению микробная инфекция представляет собой грибковую инфекцию.
Грибковый патоген может быть производным грибка (включая дрожжи) выбранного, но не ограниченного этим, из родов Candida spp., (например, C.albicans), Epidermophyton spp., Exophiala spp., Microsporum spp., Trichophyton spp., (например, T.rubrum и T.interdigitale), Tinea spp., Aspergillus spp., Blastomyces spp., Blastoschizomyces spp., Coccidioides spp., Cryptococcus spp. (например, Cryptococcus neoformans), Histoplasma spp., Paracoccidiomyces spp., Sporotrix spp., Absidia spp., Cladophialophora spp., Fonsecaea spp., Phialophora spp., Lacazia spp., Arthrographis spp., Acremonium spp., Actinomadura spp., Apophysomyces spp., Emmonsia spp., Basidiobolus spp., Beauveria spp., Chrysosporium spp., Conidiobolus spp., Cunninghamella spp., Fusarium spp., Geotrichum spp., Graphium spp., Leptosphaeria spp., Malassezia spp. (например, Malassezia Furfur), Mucor spp., Neotestudina spp., Nocardia spp., Nocardiopsis spp., Paecilomyces spp., Phoma spp., Piedraia spp., Pneumocystis spp., Pseudallescheria spp., Pyrenochaeta spp., Rhizomucor spp., Rhizopus spp., Rhodotorula spp., Saccharomyces spp., Scedosporium spp., Scopulariopsis spp., Sporobolomyces spp., Syncephalastrum spp., Trichoderma spp., Trichosporon spp., Ulocladium spp., Ustilago spp., Verticillium spp., Wangiella spp.
В предпочтительном применении по изобретению грибковым патогеном является представитель рода Trichophyton spp. или Cryptococcus spp. Например, грибковый патоген может представлять собой Trichophyton rubrum, Trichophyton interdigitale или Cryptococcus neoformans.
Грибковая инфекция может быть системной, местной, подкожной, кожной инфекцией или инфекцией слизистой оболочки.
Местные грибковые инфекции ногтей и кожи обычно вызываются дерматофитами, хотя некоторые недерматофиты, такие как дрожжи, также могут вызывать кожные инфекции. Дерматофитная инфекция может включать лишайную инфекцию, например, Tinea barbae (борода, усы), Tinea capitis (голова), Tinea corporis (тело), Tinea cruris (пах), Tinea faciei (лицо), Tinea manuum (рука), Tinea pedis (стопа), Tinea unguium (ноготь), Tinea (Pityriasis) versicolor, Tinea incognito или Tinea nigra. Инфекция может быть вызвана грибками родов Epidermophyton, Microsporum и Trichophyton spp. (например, Т. rubrum и Т. inter digitale).
Дерматофитная инфекция может представлять собой инфекцию кожи, ламины, рогового слоя, ногтей (ногтей рук и ногтей ног) или волос. Особого упоминания заслуживают дерматофитные инфекции, вызванные дерматофитами родов Trichophyton, Epidermophyton или Microsporum. Типичные дерматофиты включают Epidermophyton floccosum, Microsporum canis, Microsporum audouinii, Microsporum gypseum, Microsporum nanum, Microsporum ferrugineum, Microsporum distortum, Microsporum fulvum, Trichophyton rubrum, Trichophyton mentagrophytes var. interdigitale, Trichophyton mentagrophytes var. nodulare, Trichophyton tonsurans, Trichophyton soudanese, Trichophyton violaceum, Trichophyton megnini, Trichophyton schoenlenii, Trichophyton gallinae, Trichophyton krajdenii, Trichophyton yaoundei, Trichophyton equinum, Trichophyton erinacei и Trichophyton verrucosum.
В конкретном воплощении изобретения дерматофитная инфекция представляет собой онихомикоз. Термин "онихомикоз" включает, но не ограничивается этим, дистально-латеральный подногтевой, поверхностный белый, проксимальный белый подногтевой, вторичный дистрофический, первичный дистрофический, концевой ногтевой (endonyx), кандидазный (например, онихолизис и хроническое слизисто-кожное заболевание) типы онихомикоза и Tinea ungium.
Недерматофитные грибки, ассоциированные с онихомикозом, включают Aspergillus spp., Cephalosporum spp., Fusahum oxysporum, Scopularis brevicaulis, Scytalidium spp.
Пептиды по изобретению являются эффективыми противомикробными пептидами в отношении широкого спектра патогенных организмов. Однако пептиды по изобретению могут быть также полезными в лечении других состояний, включающих, но не ограничивающихся этим, состояния, ассоциированные с инфекциями слизистых оболочек, например кистозный фиброз, желудочно-кишечные инфекции, инфекции мочеполовых, мочевых путей (например, почечная инфекция или цистит) или инфекции дыхательных путей.
Пептиды по изобретению могут быть также полезными в лечении или предупреждении инфекций, ассоцированных типично с кожей, включая, в частности, раны, язвы и поражения, например кожные раны, такие как порезы или ожоги, и состояний, ассоциированных с ними.
В предпочтительном аспекте изобретения пептиды являются полезными в лечении бактериальных кожных инфекций или "пиодермий".
Термин "лечение" относится к эффектам пептидов, раскрытых в данном описании, которые состоят в обеспечении пользы для пациентов, страдающих (инфекционным) заболеванием, включая улучшение в состоянии пациента или замедление развития заболевания.
Как использовано в данном описании, "лечение раны" может включать заживление раны и ассоциированных состояний и терапию, которая стимулирует, усиливает и ускоряет заживление тканей и включает послеоперационное рубцевание, ожоги, язвы, псориаз, ускорение тканевого ремодулирования, например, после косметической операции и трансплантации органов.
Таким образом, в другом аспекте изобретения предложен субстрат, на который наносят или к которому прикрепляют пептид по изобретению. Предпочтительно, субстрат является подходящим для нанесения на раны или для доставки к раневым участкам. Предпочтительно, субстрат делает возможным перенос пептидов по изобретению с субстрата на поверхность раны для достижения их антибиотического эффекта. Субстрат может представлять собой повязку, например раневую повязку. Повязка может включать тканевой материал или она может представлять собой коллагеноподобный материал.
Пептиды по изобретению могут также найти применение в качестве/в составе дезинфицирующего средства. В этом контексте пептид или фармацевтические композиции по изобретению могут быть нанесены либо отдельно, либо в комбинации с другими дезинфицирующими агентами на поверхность, подлежащую обработке. Как использовано в данном описании, "поверхность, подлежащая обработке" может представлять собой субстрат, как определено в данном описании, или медицинское устройство.
В другом аспекте в изобретении предложен способ лечения или предупреждения микробной инфекции у субъекта, включающий введение указанному субъекту терапевтически эффективного количества пептида по изобретению.
В предпочтительном способе по изобретению микробная инфекция представляет собой грибковую инфекцию. В способе по изобретению пептид наносят местно на кожу или ногти указанного субъекта.
Млекопитающих, птиц и других животных можно лечить пептидами, композициями или способами, раскрытыми в данном описании. Такие млекопитающие и птицы включают людей, собак, кошек и скот, такой как лошади, крупный рогатый скот, овцы, козы, куры и индейки и тому подобное. Кроме того, растения также можно обрабатывать пептидами, композициями или способами по изобретению.
Когда субъектом является животное, тогда способ по изобретению можно использовать к похожим на ногти частям тела, включая, но не ограничиваясь этим, копыта, когти и ноги.
Способ по изобретению может включать, в дополнение к пептидной обработке, обработки, которые могут усиливать проникание пептида в ноготь. Это можно облегчить химическими или физическими способами. Физические обработки, такие как травление ногтей или подпиливание дорсального слоя ногтя, могут усиливать проникание пептидов по изобретению. Химическое усиление проницаемости ногтя для пептидов по изобретению может быть достигнуто путем разрушения физических или химических связей в кератине ногтевой пластинки. Агенты, размягчающие ноготь, включая, но не ограничиваясь этим, мочевину и салициловую кислоту, увеличивают гидратацию ногтя с уменьшением плотности ногтя и, следовательно, могут увеличивать проницаемость для пептидов по изобретению. Соединения, содержащие сульфгидрильные группы, расщепляют дисульфидные связи в ногтевом кератине и могут приводить к дестабилизации и повышенному прониканию лекарственных средств.
В другом аспекте в изобретении предложен способ лечения раны у субъекта, включающий нанесение на рану терапевтически эффективного количества пептида или субстрата по изобретению.
Для достижения желаемого(ых) эффекта(ов) пептид, его вариант или их комбинацию можно вводить в виде однократной или разделенной доз, например, по меньшей мере от примерно 0,01 мг/кг до примерно 500-750 мг/кг, по меньшей мере от примерно 0,01 мг/кг до примерно 300-500 мг/кг, по меньшей мере от примерно 0,1 мг/кг до примерно 100-300 мг/кг или по меньшей мере от примерно 1 мг/кг до примерно 50-100 мг/кг массы тела или по меньшей мере от примерно 1 мг/кг до примерно 20 мг/кг массы тела, хотя другие дозировки могут обеспечивать полезные результаты. Вводимое количество будет варьировать в зависимости от различных факторов, включающих, но не ограничивающихся этим, выбранный пептид и его клинические эффекты, заболевание, массу, физическое состояние, здоровье, возраст млекопитающего, должно ли быть достигнуто предупреждение или лечение, и является ли пептид химически модифицированным.
Введение терапевтических агентов в соответствии с настоящим изобретением может осуществляться в однократной дозе, в многократных дозах, непрерывным или прерывистым образом, в зависимости, например, от физиологического состояния реципиента, от того, является ли цель введения терапевтической или профилактической, и от других факторов, известных специалистам. Введение пептидов по изобретению может быть по существу непрерывным в течение предварительно выбранного периода времени или может представлять собой серию разнесенных во времени доз. Рассматривается как местное, так и системное введение.
Для приготовления композиции пептиды синтезируют или иным образом получают, очищают при необходимости или желании и затем лиофилизируют и стабилизируют. Пептид может быть затем доведен до подходящей концентрации и возможно объединен с другими агентами. Абсолютная масса данного пептида, включенного в стандартную дозу, может широко варьироваться. Например, может быть введено от примерно 0,01 до примерно 2 г или от примерно 0,01 до примерно 500 мг по меньшей мере одного пептида по изобретению или множества пептидов, специфичных для конкретного типа клеток. Альтернативно, стандартная дозировка может варьироваться от примерно 0,01 г до примерно 50 г, от примерно 0,01 г до примерно 35 г, от примерно 0,1 г до примерно 25 г, от примерно 0,5 г до примерно 12 г, от примерно 0,5 г до примерно 8 г, от примерно 0,5 г до примерно 4 г или от примерно 0,5 г до примерно 2 г.
Таким образом, одну или более подходящих стандартных лекарственных форм, содержащих терапевтические пептиды по изобретению, можно вводить разными путями, включая пероральный, парентеральный (включая подкожный, внутривенный, внутримышечный и интраперитонеальный), ректальный, дермальный, трансдермальный, интраторакальный, внутрилегочный и интраназальный (дыхательный) пути. Терапевтические пептиды могут быть также приготовлены в виде липидного препарата или для замедленного высвобождения (например, с использованием микроинкапсуляции, см. WO 94/07529, и патент США №4962091). Препараты могут быть, где это целесообразно, удобно представлены в дискретных стандартных лекарственных формах и могут быть приготовлены любым способом, хорошо известным в фармацевтической области. Такие способы могут включать стадию смешивания терапевтического агента с жидкими носителями, твердыми матрицами, полутвердыми носителями, тонкодиспергированными твердыми носителями или их комбинациями, и затем, при необходимости, введение или формование продукта в желаемую систему доставки.
Когда терапевтические пептиды по изобретению приготавливают для перорального введения, тогда их обычно объединяют с фармацевтически приемлемым носителем, разбавителем или эксципиентом с образованием фармацевтического препарата или стандартной лекарственной формы. Для перорального введения пептиды могут быть представлены в виде порошка, гранулированного препарата, раствора, суспензии, эмульсии или в природном или искусственном полимере или смоле для всасывания активных ингредиентов из жевательной резинки. Активные пептиды могут быть также представлены в виде болюса, электуария или пасты. Перорально вводимые терапевтические пептиды по изобретению могут быть также приготовлены в виде препаратов для замедленного высвобождения, например, пептиды могут быть покрыты оболочкой, микроинкапсулированы или иным образом помещены в устройство для замедленной доставки. Общие активные ингредиенты в таких препаратах включают от 0,1 до 99,9% от массы препарата.
Фармацевтические препараты, содержащие терапевтические пептиды по изобретению, могут быть приготовлены методами, известными в данной области с использованием хорошо известных и легкодоступных ингредиентов. Например, пептид может быть приготовлен в виде препарата со стандартными эксципиентами, разбавителями или носителями и сформован в таблетки, капсулы, растворы, суспензии, порошки, аэрозоли и тому подобное. Примеры эксципиентов, разбавителей и носителей, которые подходят для таких препаратов, включают буферы, а также наполнители и разбавители, такие как крахмал, целлюлоза, сахара, маннит и производные кремния. Также могут быть