Способ количественной оценки усвоенного лекарственного средства в организме
Иллюстрации
Показать всеИзобретение относится к области медицины и описывает способ количественной оценки усвоенного лекарственного средства в организме, включающий сопутствующее потребление визуализирующего вещества, и проведение исследований через определенное время, где в качестве визуализирующего вещества используют флюоресцирующую пищевую добавку, смешанную с основным лекарственным средством в постоянной весовой пропорции F:X=φ:(1-φ), где F - доза флюоресцирующей добавки мг/кг веса в сутки, Х - доза лекарственного средства мг/кг веса в сутки, выписанная врачом, φ - весовая доля флюоресцирующей добавки, а исследование проводят с помощью спектрофотометрического метода до приема смеси и после ее приема через 12-72 часа, при этом выбранные участки эпителия пациента освещают лазером с длиной волны 532 нм, непрерывной мощностью 5÷10 мВт, регистрируют интенсивности флюоресценции в диапазоне длин волн 650-690 нм - J0(λ) и J1(λ) соответственно, а количество лекарственного средства определяют по формуле:
где CJ(S) - функционал зависимости интеграла сигнала флюоресценции используемой визуализирующей добавки в ее характеристическом диапазоне длин волн, находимый по калибровочному графику для хлорофилла в качестве флюоресцирующей пищевой добавки, где значение SJ рассчитывается по формуле:
,
где λ - длина волны в нанометрах, a J0(λ) и J1(λ) - значения мощности флюоресценции (в одинаковых условных оптических единицах), измеренные соответственно до начала исследования и в контрольное время t (час). Данный способ прост, доступен, обеспечивает неинвазивный экспресс-контроль in vivo за дозировкой усвоенного фармакологического препарата. 1 пр., 4 ил.
Реферат
Изобретение относится к области медицины и фармакопии и может быть использовано для определения количества лекарственного препарата, накопленного в организме животного. Данные экспериментальные исследования позволят в дальнейшем осуществлять непрямой контроль за приемом лекарственных препаратов и их усвояемости в организме человека, что необходимо в тех случаях, когда неадекватный прием препарата может иметь серьезные последствия для организма.
Известно устройство для определения концентрации органического вещества в органической ткани, содержащее подкожную иглу с нагнетательно-отсасывающим средством, многоходовым клапаном с резервуаром для перфузионной жидкости, соединенную каналом с анализатором (патент РФ №2016540, кл A61B 5/00, 1994).
Недостатком данного способа является инвазивность и необходимость в дополнительных расходных материалах для изготовления перфузионных жидкостей и аналитических растворов для последующего исследования.
Известен способ определения концентрации адреналина, норадреналина, дофамина и диоксифенилаланина в биологическом материале, где выделяют катехоламины из биологического материала путем адсорбции на окиси алюминия, элюирования и окисления с последующим определением концентрации этих веществ по интенсивностям флюоресценции (патент РФ №2174231, кл. G01N 33/52, 1994).
Его недостатком является трудоемкость, необходимость использования большого количества расходных материалов при исследовании и ограниченные возможности, связанные со специфичностью способа для обязательного выявления катехоламинов.
Наиболее близким к предлагаемому является способ определения количества лекарственного средства в организме, включающий введение лекарственного средства в организм, выдерживание его в течение определенного времени и проведение исследований (патент РФ №2268638, A61B 5/00, 2006).
Недостатком данного способа является инвазивность, требовательность к точности соблюдения методики квалифицированным персоналом, а также необходимость в дополнительных расходных материалах по анализу аспирированной жидкости.
В соответствии с этим поставлена задача, направленная на создание простого, доступного способа, обеспечивающего неинвазивный экспресс-контроль in vivo за дозировкой усвоенного фармакологического препарата.
Для решения этой задачи в способе количественной оценки усвоенного лекарственного средства в организме, включающем сопутствующее потребление визуализирующего вещества, и проведение исследований через определенное время, предложено в качестве визуализирующего вещества использовать флюоресцирующую пищевую добавку, смешанную с основным лекарственным средством в постоянной весовой пропорции F:X=φ:(1-φ), где F - доза флюоресцирующей добавки мг/кг веса в сутки, Х - доза лекарственного средства мг/кг веса в сутки, выписанная врачом, φ - весовая доля флюоресцирующей добавки, а исследование проводить с помощью спектрофотометрического метода до приема смеси и после ее приема через 12-72 часа, при этом выбранные участки эпителия пациента освещать лазером с длиной волны 532 нм непрерывной мощностью 5÷10 мВт, при этом регистрировать интенсивности флюоресценции в диапазоне длин волн 650-690 нм - J0(λ) и J1(λ) соответственно, а количество лекарственного средства определять по формуле:
где CJ(S) - функционал зависимости интеграла сигнала флюоресценции используемой визуализирующей добавки в ее характеристическом диапазоне длин волн, находимый по калибровочному графику (для хлорофилла в качестве флюоресцирующей пищевой добавки), где значение SJ рассчитывается по формуле:
,
где λ - длина волны в нанометрах, a J0(λ) и J1(λ) - значения мощности флюоресценции (в одинаковых условных оптических единицах), измеренные соответственно до начала исследования и в контрольное время t (час).
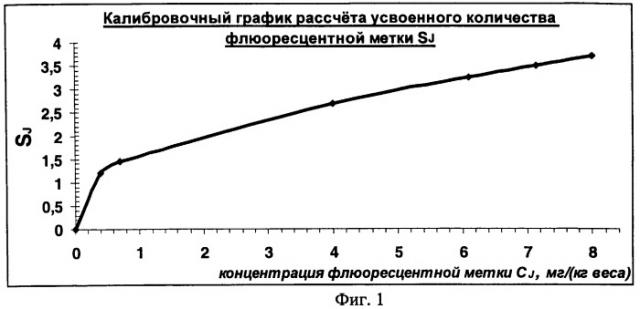
На фиг.1 изображен калибровочный график расчета усвоенного количества флюоресцентной метки Sj.
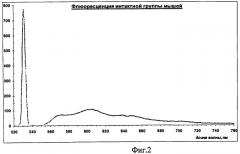
На фиг.2 изображен график флюоресценции интактной группы мышей.
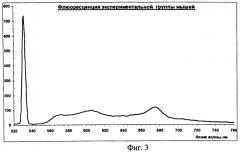
На фиг.3 изображен график флюоресценции экспериментальной группы мышей.
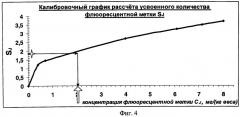
На фиг.4 изображен калибровочный график расчета усвоенного количества флюоресцентной метки с примером расчета.
Способ осуществляется следующим образом.
Для регистрации спектров пригоден любой сканирующий спектроанализатор, например ЛАКК-М. По относительной интегральной интенсивности флюоресценции в характеристическом диапазоне оценивают количество усвоенного фармопрепарата. При этом в качестве пищевой добавки используют хлорофилл.
1. Снимается in vivo изначальный спектр флюоресценции с контрольных участков тела J0(λ).
2. Флюоресцентную метку, являющуюся разрешенной к применению флюоресцирующей пищевой добавкой, например хлорофиллом, смешивают с основным лекарственным средством в постоянной весовой пропорции: φ:(1-φ), где φ - весовая доля флюоресцирующей добавки, из диапазона значений [0,0001; 0,9].
Более точно расчет φ осуществляется, исходя из соотношения дневных дозировок показанного фармопрепарата и используемой флюоресцентной метки. Например, по показаниям пациент обязан принимать в сутки Х мг/(кг веса) фармопрепарата, а для визуализации метки удобно использовать дозировку F мг/(кг веса·сутки), тогда легко получить пропорцию:
,
откуда легко получить значение для φ
3. Спустя интересующее контрольное время t=12-72 час после приема лекарственного препарата, смешанного с флюоресцирующей добавкой, с тех же самых участков тела снимается in vivo спектр флюоресценции флюоресценции J1(λ).
4. Рассчитывается значение функционала на участке [650; 690] нм по формуле:
,
где λ - длина волны в нанометрах.
Значение усвоенной дозы CJ флюоресцирующей метки - хлорофилла находится по данным калибровочного графика CJ(S):
5. Значение усвоенной дозы CJ флюоресцирующей метки - хлорофилла находится по данным калибровочного графика CJ(S) (Фиг.1).
6. Концентрация принимаемого препарата в миллиграммах на килограмм веса тела находится по формуле:
,
Во время приема лекарственного средства должен быть исключен прием алкоголя в дозировке выше 1 г/(кг веса тела·сутки).
Участки тела, с которых снимаются показания флюоресценции, предварительно должны быть очищены и обезжирены.
При использовании иного визуализирующего флюоресцентного агента необходимо предварительно построить калибровочный график на основании предварительных испытаний с известными регулярными дозировками приема в различных вариациях концентрационных значений.
Исследования проводят через 12-72 часа с момента первого приема лекарственного средства, а интервал приема лекарственной смеси не должен быть более 24 часов, что обеспечивает необходимое и стабильное количество накопленной смеси в организме.
Конкретный пример выполнения способа
При проведения эксперимента в качестве лекарственного средства использовали аскорбиновую кислоту. Контроль за потреблением аскорбиновой кислоты (витамина C) проводился на мышах.
Известно, что нормальное потребление витамина C по нормативам ВОЗ определяется как 5-7,5 мг/(кг веса·сут). Рекомендуемое потребление хлорофилла для мышей - 0,2÷0,4 г/(кг веса·сут). Это дает рекомендации к смешению витамина С и хлорофилла 1:25÷1:70. Для контроля за приемом витамина С используем среднее смешение 1:40, то есть на 1 мг аскорбиновой кислоты возьмем 40 мг хлорофилла. Таким образом, доля флюоресцентной метки хлорофилла будет определяться как φ=1/(40/1+1)≈0,024.
Калибровочный график для контроля за дозировкой регулярного приема хлорофилла был получен следующим образом. Экстракт хлорофилла добавлялся в питьевую воду мышам в различных концентрациях от 7 до 75 мг/л, с расчетом, что мышь выпивает с сутки в среднем от 2 до 8 мл воды, получая таким образом от 0,014 до 0,6 мг хлорофилла ежедневно, что соответствует дозировке 0,56-20 мг/(кг веса·сут). Для каждой использованной дозировки снимались начальные графики флюоресценции интактных животных и затем животных, получавших регулярную дозировку хлорофилла из указанного спектра концентраций. По результатам расчета значений функционала отношения полученных спектральных функций интенсивности:
- для каждой потребляемой концентрации СФ флюоресцентной метки хлорофилла и был построен калибровочный график зависимости значений функционала SJ спектральных данных от потребляемой концентрации (Фиг.1).
Таким образом, оценка количества усвояемой концентрации витамина С мышами проводилась следующим образом. Изначально измерялась флюоресценция интактных животных. Спектр флюоресценции кожи нижней части спины интактной мыши имеет вид: (Фиг.2).
Смешение экстракта хлорофилла в пропорции 1:40 с аскорбиновой кислотой и прием их мышами на протяжении 5 дней приводит к получению следующих спектров флюоресценции тех же участков кожного эпителия: (Фиг.3).
Это приводит к получению значения функционала
,
что по данным калибровочного графика (Фиг.4) соответствует усвоенной концентрации флюоресцирующей метки 1,8 мг/(кг веса·сут). По этим данным сопутствующее потребление витамина С, смешанного с хлорофиллом в пропорции 1:40, где φ=0,024, может быть рассчитано как:
С=1,8·(40/1)=72 мг/(кг веса·сут) или 0,72 г/(кг веса),
что равносильно 0,02 г/(мышь·сут). Это приблизительно соответствует количеству аскорбиновой кислоты, потребляемой мышью в день.
Способ отличается быстротой и простотой получения данных, неинвазивен и не требует каких-либо дополнительных расходных материалов, помимо включенной в лекарственное средство флюоресцентной метки.
Преимуществом настоящего изобретения является неинвазивность, малое количество затрат, связанное только с затратой на флюоресцентную пищевую добавку и ее смешением с основным лекарственным средством, отсутствие требований специальных медицинских навыков у исполняющего персонала, а также малое время самого процесса снятия контрольных данных, причем данных in vivo.
Способ количественной оценки усвоенного лекарственного средства в организме, включающий сопутствующее потребление визуализирующего вещества и проведение исследований через определенное время, отличающийся тем, что в качестве визуализирующего вещества используют флюоресцирующую пищевую добавку, смешанную с основным лекарственным средством в постоянной весовой пропорции F:X=φ:(1-φ), где F - доза флюоресцирующей добавки, мг/кг веса в сутки; Х - доза лекарственного средства, мг/кг веса в сутки, выписанная врачом; φ - весовая доля флюоресцирующей добавки, а исследование проводят с помощью спектрофотометрического метода до приема смеси и после ее приема через 12-72 ч, при этом выбранные участки эпителия пациента освещают лазером с длиной волны 532 нм, непрерывной мощностью 5÷10 мВт, регистрируют интенсивности флюоресценции в диапазоне длин волн 650-690 нм - J0(λ) и J1(λ) соответственно, а количество лекарственного средства определяют по формуле: где CJ(S) - функционал зависимости интеграла сигнала флюоресценции используемой визуализирующей добавки в ее характеристическом диапазоне длин волн, находимый по калибровочному графику для хлорофилла в качестве флюоресцирующей пищевой добавки, где значение SJ рассчитывается по формуле: где λ - длина волны в нанометрах, a J0(λ) и J1(λ) - значения мощности флюоресценции (в одинаковых условных оптических единицах), измеренные соответственно до начала исследования и в контрольное время t (ч).