Гетероциклические низкомолекулярные sapp-миметики, фармацевтическая композиция, способы получения и применения
Иллюстрации
Показать всеНастоящее изобретение относится к новым гетероциклическим соединениям формулы I, в которой: n и m могут принимать значения 0, 1, 2 и 3; знак (#) здесь и далее обозначает возможность наличия хирального центра; R представляет необязательно замещенный С5-С10арил или 5-6-членный гетарил, содержащий 1-2 гетероатома, выбранных из азота, кислорода и серы, возможно конденсированный с бензольным кольцом, причем, заместители выбираются из С1-С8алкила, С1-С8алкокси, галогена, ОН, CF3, NO2, CF3O, СООН, незамещенной амино-группы или моно-С1-6алкил- или ди(С1-6алкил)замещенной амино-группы, С1-8алкилсульфанила, С1-8алкоксикарбонил; A1 и А2 независимо представляют необязательно замещенный 5-6 членный насыщенный, или ароматический азагетероцикл, содержащий от 1 до 2 атомов азота в цикле и возможно конденсированный с бензольным кольцом; или к их фармацевтически приемлемым солям, или сложным алкиловым эфирам, в виде отдельных оптических изомеров, или к их смесям. Также изобретение относится к фармацевтической композиции на основе соединения формулы I, к лекарственному средству на основе соединения формулы I, a также к способу получения соединения формулы I. Технический результат: получены новые непептидные гетероциклические низкомолекулярные пептидомиметики секреторного предшественника амилоидного пептида sAPP (sAPP-миметиков), обладающих способностью эффективно воздействовать на процессы формирования, хранения и воспроизведения памяти, утраченной в норме и патологии. 4 н. и 6 з.п. ф-лы, 4 ил., 22 пр.
Реферат
Изобретение относится к новым соединениям непептидной природы, которые являются пептидомиметиками секреторного предшественника амилоидного пептида sAPP (sAPP-миметиками). Соединения могут быть использованы для восстановления памяти, утраченной в норме и патологии.
В настоящее время серьезной медицинской проблемой является деменция (слабоумие) у людей пожилого возраста, которая проявляется у 4% населения в возрасте 65 лет и по крайней мере у 35% населения в возрасте 85 лет. Число больных, страдающих от деменции, в связи с увеличением продолжительности жизни, стремительно растет и, предполагается, что достигнет 80 миллионов в 2040 году. Наиболее распространенной формой деменции является болезнь Альцгеймера (БА, около 60% всех случаев), представляющая собой прогрессирующее необратимое нейродегенеративное заболевание с недостаточно изученным патогенезом и практически не имеющая эффективных средств лечения. Разработка таких средств интенсивно ведется на протяжении многих лет, однако до сих пор основным направлением поиска остается попытка фармакологической коррекции холинергического дефицита, приведшая к созданию ряда известных препаратов на основе ингибиторов ацетилхолинэстеразы (Такрин, Амиридин, Арисепт и т.п.), имеющих, однако, весьма ограниченную клиническую применимость. Широко применяется сейчас также антагонист NMDA рецепторов Мемантин, который приводит к кратковременному улучшению когнитивных функций, однако практически не предотвращает прогрессию БА.
Из литературы известно, что один из синаптических гликопротеинов, sAPP, играет ключевую роль в регуляции нейрональной активности, пластичности и формирования памяти. Необычной особенностью АРР является то, что этот белок является предшественником как нейротоксического амилоида β-А, играющего ключевую роль в патогенезе, так и нейпротекторного и нейротрофического секреторного нейропептида sAPP. Гликопротеин АРР подвергается расщеплению под действием трех ферментов: α-, β- и γ-секретаз. Амилоид β-А, состоящий из 40-42 аминокислот, образуется амилоидогенным процессингом АРР последовательным действием β- и γ-секретаз. Растворимые формы Р-А проявляют нейротоксические свойства и вызывают нарушения памяти у экспериментальных животных. Аггрегированные β-А пептиды являются основным компонентом сенильных бляшек, образующихся в мозгу у больных БА. Однако в норме основным направлением протеолиза АРР является неамилоидогенный процессинг под действием α-секретазы. Основным результатом действия α-секретазы на АРР является высвобождение растворимого секретируемого пептида sAPP, обладающего нейропротекторными и нейротрофическими свойствами. Особую роль пептид sAPP играет в процессах обучения, формировании и консолидации памяти.
Нейпротекторные, нейротрофические и промнестические свойства секретируемого пептида sAPP позволяют рассматривать активацию неамилоидогенного процессинга белка-предшественника АРР как новую и исключительно перспективную стратегию создания новых болезнь-модифицирующих средств лечения БА. Эта стратегия включает два направления, а именно: 1) создание нейрофармакологических средств, активирующих α-секретазу; и 2) создание пептидомиметических нейротропных средств, проявляющих эффекты, подобные нейпротекторным, нейротрофическим и промнестическим свойствам секретируемого пептида sAPP. В рамках первого направления были найдены и в настоящее время проходят всесторонние испытания активаторы α-секретазы различной природы. Поиск sAPP-миметиков в рамках второго направления оказался менее успешным. В настоящее время обнаружены только небольшие пептиды, в основном фрагменты белка АРР, (в частности, пентапептиды), которые проявляют нейропротекторные и промнестические свойства. Учитывая крайне низкую биодоступность и легкую протеолитическую деградацию пептидных sAPP-миметиков, клиническое применение найденных небольших пептидных sAPP-миметиков представляется маловероятным.
Необходимо отметить, что до настоящего времени не было найдено ни одного sAPP-миметика непептидной природы.
Среди непептидных структурных аналогов, которые могут быть использованы при лечении нейродегенеративных, неврологических и психотических заболеваний, можно упомянуть, например, соединения, описанные в документах, указанных ниже.
В патентах US 6943149 B2 и 6858577 В1 описываются индольные и имидазольные пептидомиметики, которые могут быть использованы для лечения нейродегенеративных заболеваний. В заявках US 2010/0048656 A1 и 2009/0325993 А1 описываются циклические амидные производные аминоуксусной кислоты для лечения неврологических расстройств и психотических заболеваний, таких как психозы, деменция или синдром дефицита внимания. Известны производные арилглицинамида, описанные, например, в патенте RU 2167866, которые проявляют свойства антагонистов нейрокинина и могут быть использованы при лечении заболеваний ЦНС, таких как деменция (слабоумие), БА, шизофрении, психозы и т.д.
Задачей настоящего изобретения является поиск новых высокоэффективных средств для лечения и ранней диагностики БА с принципиально новым механизмом действия, в особенности соединений, блокирующих или тормозящих развитие нейродегенеративных процессов.
Соединения настоящего изобретения относятся к соединениям нового класса sAPP-миметиков непептидной природы, которые обладают уникальным сочетанием двух основных подходов в лечении, например, БА. При этом мишенью действия соединений является метаболический каскад АРР и, кроме того, соединения обладают способностью стимулировать долговременную память.
Соединения настоящего изобретения представляют собой новые (азагетероциклил)алкильные производные амидов 2-(гет)арилглицинов, соответствующие общей формуле (I)
в которой:
n и m могут принимать значения 0, 1, 2 и 3;
знак (#) здесь и далее обозначает возможность наличия хирального центра;
R представляет необязательно замещенный С5-С10арил или 5-7-членный гетарил, содержащий 1-3 гетероатома, выбранных из азота, кислорода и серы, возможно конденсированный с бензольным кольцом;
A1 и А2 независимо представляют необязательно замещенный 3-7-членный насыщенный, частично насыщенный или ароматический азагетероцикл, содержащий от 1 до 3 атомов азота в цикле и возможно конденсированный с бензольным кольцом;
или их фармацевтически приемлемые соли, или сложные алкиловые эфиры, в виде отдельных оптических изомеров, или их смесей.
Предпочтительные соединения представляют собой (азагетероциклил)алкильные производные амидов арилглицинов общей формулы I.1,
в которой:
k и l могут принимать значения 0 и 1;
X представляет Н, необязательно замещенный алкил, необязательно замещенный С1-С8алкокси, галоген, ОН, CF3, CN, CF3O, необязательно замещенную амино-группу, С1-С6ацильную группу, необязательно замещенный С6арил или 5-6-членный гетарил, содержащий 1-3 гетероатома, С2-С4алкенил, С2-С4алкинил, С6арС1-С6алкил, С1-С6алкоксикарбонил, 5-6-членный гетарил, содержащий 1-2 гетероатома, выбранных из азота, кислорода и серы, С6арилсульфонил или С1-С6алкилсульфонил, необязательно N-замещенный аминосульфонил; либо группа X означает бензольное кольцо, аннелированное с фенилом или 5-7-членным гетероциклилом, содержащим 1-3 гетероатома, выбранных из атомов азота, кислорода, серы,
R1 и R2 независимо представляют необязательно замещенный 6-членный азагетероцикл, такой как пиридин, пиперидин, пиримидин, триазин, хинолин, изохинолин, хиназолин, хиноксалин.
При этом особенно предпочтительны соединения I.1 в виде отдельных изомеров или в виде смеси R-(-)- и S-(+)-изомеров, соответственно представленных общими формулами I.1.1 и I.1.2:
в которых:
k и l могут принимать значения 0 и 1;
X представляет Н, необязательно замещенный С1-С8алкил, необязательно замещенный С1-С4алкокси, галоген, ОН, CF3, CN, CF3O, необязательно замещенную аминогруппу, С1-С6ацильную группу, необязательно замещенный С6арил или 5-6-членный гетарил, содержащий 1-3 гетероатома, выбранных из азота, кислорода или серы, С2-С4алкенил, С2-С4алкинил, С6арС1-С6алкил, С1-С8алкоксикарбонил, карбоксигруппу, С6арилсульфонил или С1-С8алкилсульфонил, необязательно N-замещенный аминосульфонил; либо группа X означает бензольное кольцо, аннелированное с фенилом или 5-7-членным гетероциклилом, содержащим 1-3 гетероатома, выбранных из атомов азота, кислорода, серы,
R1 и R2 независимо представляют необязательно замещенный 6-членный азагетероцикл, преимущественно пиридин, пиперидин, пиримидин, триазин, хинолин, изохинолин, хиназолин, хиноксалин.
Соединения формулы 1 потенцируют токи АМРА рецепторов и тем самым могут быть полезны для улучшения когнитивных функций, таких как обучение, формирование, консолидация и извлечение памяти.
При этом неожиданно было обнаружено, что соединения формулы 1, кроме того, обладают также способностью влиять и на другие звенья памяти: а именно, - улучшать процессы извлечения памяти, что делает их уникальными и особо ценными среди всех известных препаратов, которые влияют на память.
Способность восстанавливать память с помощью соединений формулы 1, благодаря обнаружению у них новых неожиданных свойств, не является очевидной и не вытекает из химической структуры этих соединений. Указанные свойства позволяют использовать соединения в качестве средства для восстановления утраченной памяти в норме и патологии у пациентов всех возрастных групп. Соединения могут быть использованы для восстановления памяти, утраченной, например, в результате нейродегенеративного заболевания или других заболеваний ЦНС. Такими заболеваниями могут быть болезнь Альцгеймера, болезнь Паркинсона; болезни (хореи) Хантингтона; рассеянный склероз; мозжечковая дегенерация; амиотрофический латеральный склероз; деменция с тельцами Леви; спинальная мускульная атрофия; периферическая нейропатия; губчатый энцефалит; СПИД-ассоциированная деменция; мультиинфарктная деменция; лобно-височная деменция; лейкоэнцефалопатия; хронические нейродегенеративные заболевания; инсульт; ишемическое, реперфузионное и гипоксическое повреждение мозга; эпилепсия; церебральная ишемия; глаукома; синдром Дауна; энцефаломиелит; менингит; энцефалит; нейробластома; шизофрения; депрессия; и нейродегенеративные процессы.
В соединениях настоящего изобретения в группах А1, А2, R
С1-С8алкил представляет собой линейный или разветвленный алкил, возможно циклический, в котором одна или несколько СН2групп могут быть заменены атомами кислорода, азота или серы. Примерами таких заместителей могут быть метил, этил, изопропил, н-пропил, изобутил, s-бутил, трет бутил, гексил, нонил циклопропил, циклогексил, циклобутил, циклопентил, циклооктил и др.
Заместители алкила могут быть выбраны из атомов галогена, таких как атомы хлора, брома, иода, С1-С8, предпочтительно С1-С4алкокси, галогенированного С1-С4алкокси, гидрокси, арилокси, амино, моно- или С1-С4алкиламина, циано, нитро, алкилтио и др.
Заместители амино-группы выбираются прежде всего из С1-С8алкила, преимущественно С1-С4алкила, который может быть разветвленным, или С1-С4валкила, замещенного гидрокси, С1-С4алкокси или амино, моно- или С1-С4алкиламингруппами.
Заместители арила или гетарила выбираются из Н, необязательно замещенного алкила, где заместители указаны выше, необязательно замещенного С1-С4алкокси, например, галогенированного алкокси, такого как CF3O, галогена, ОН, CN, необязательно замещенной, как указано выше, амино-группы, C1-С6ацильной группы, необязательно замещенного С6арила или 5-6-членного гетарила, содержащего 1-3 гетероатома, где в каждом ариле и гетариле заместители могут быть выбраны из галогена, С1-С4алкила, С2-С4алкенила; С2-С4алкенила, С2-С4алкинила, С6арС1-С6алкила, С1-С8алкоксикарбонила, карбоксигруппы, 5-6-членного гетарила, содержащего 1-2 гетероатома выбранных из азота, кислорода и серы, С6арилсульфонила или С1-С8алкилсульфонила, необязательно N-замещенного, как указано выше, аминосульфонила.
Бензольное кольцо, аннелированное с фенилом или 5-7-членным гетероциклилом, содержащим 1-3 гетероатома, выбранных из атомов азота,кислорода, серы, как правило, представляет собой бициклическую или трициклическую группу, выбранную, например, из нафталина, хинолила, индолила, бензопиразолила, бензотиофенила, бензофуранила, бензоизофуранила, бензодиоксалила, бензодиоксина, бензазепина, бензодиазепина, бензимидазола, бензизоксазолила, бензоксазолила, бензтиазолила, бензоизотиазолила, пиридопиримидина, пиридоимидазолила, пиридотриазолила и др. Аннелированные группы также могут быть замещены, например, атомами галогена, С1-С4алкилом, С1-С4алкокси.
В качестве фармацевтически приемлемых солей могут быть использованы соли галоидводородных солей, особенно хлоргидраты, соли серной и сульфоновой кислоты, такие как мезилат, тозилат, фосфорной, малеиновой, фумаровой, лимонной, винной, уксусной кислоты, карбоновой кислоты, например, бикарбонаты, соли щелочных или щелочноземельных металлов.
Изобретение также относится к использованию соединений общих формул I, I.1, I.1.1 и I.1.2 в качестве физиологически активных агентов, способных эффективно воздействовать на процессы формирования, хранения и воспроизведения памяти, а также к использованию физиологически активных агентов для потенциации ранних стадий формирования памяти с целью формирования более устойчивой, длительно хранящейся памяти, в особенности потенциации процессов, происходящих на поздних сроках формирования памяти, с целью усиления памяти о ранее приобретенном опыте (о событиях, произошедших в прошлом).
Как это обычно принято в медицине, соединения формулы 1 согласно настоящему изобретению рекомендуется применять в виде лекарственного средства, которое также является объектом изобретения.
При этом соединения общей формулы I, I.I, I.1.1 и I.1.2, их фармацевтически приемлемые соли или сложные алкиловые эфиры, в виде отдельных оптических изомеров, или их смесей, обладающие способностью эффективно воздействовать на процессы формирования, хранения и воспроизведения памяти, могут быть использованы в качестве активного компонента для производства фармацевтических композиций и лекарственных препаратов.
Изобретение также относится к фармацевтической композиции, обладающей свойством эффективно воздействовать на процессы формирования, хранения и воспроизведения памяти, содержащей вышеуказанный активный компонент в эффективном количестве.
Изобретение относится также к лекарственному средству в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для лечения и предупреждения заболеваний, связанных с нарушением процессов формирования, хранения и воспроизведения памяти, включающему вышеуказанный активный компонент или фармацевтическую композицию на их основе. Фармацевтическая композиция и лекарственное средство могут быть получены традиционными для фармацевтической промышленности методами.
Фармацевтическую композицию можно получить смешением с фармацевтически приемлемыми носителями, растворителями или разбавителями.
Возможно также добавление в композицию добавок, таких как вспомогательные, распределяющие и воспринимающие средства, средства доставки;
консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки. Выбор и соотношение указанных компонентов зависит от природы и способа назначения и дозировки.
Понятие «эффективное количество», используемое в данной заявке, подразумевает использование того количества соединения формулы 1, которое в соединении с его показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной фармацевтической композиции или лекарственной форме.
Содержание активного ингредиента(компонента) обычно составляет от 1 до 20 вес.%, в сочетании с одной или более фармацевтически приемлемыми вспомогательными добавками, такими как разбавители, связующие, разрыхляющие агенты, адсорбенты, ароматизирующие вещества, вкусовые агенты.
Лекарственное средство может находиться в виде жидкой или твердой формы. Примерами твердых лекарственных форм являются, например, таблетки, пилюли, желатиновые капсулы и др. Примерами жидких лекарственных форм для инъекций и парентерального введения являются растворы, эмульсии, суспензии и др.
Изобретение также относится к использованию соединения общей формулы I,I.1, I.1.1 и I.1.2 в качестве молекулярных фармакологических инструментов для исследований (in vitro и in vivo) биохимических сигнальных, нейротрофических и нейропротекторных процессов, связанных с секреторным белком sAPP, а также механизмов формирования, хранения и воспроизведения памяти.
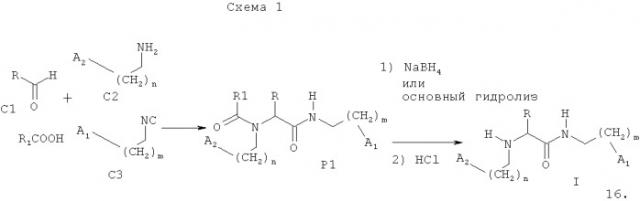
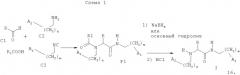
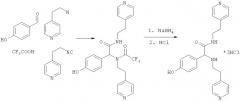
Соединения настоящего изобретения могут быть получены мультикомпонентной реакцией альдегида, амина, изонитрила и карбоновой кислоты с последующим удалением N-ацильной группы в соответствии со схемой 1:
Более подробно способ осуществляют следующим образом.
В мультикомпонентную реакцию в соответствии со схемой I вводят эквивалентные количества альдегида С1, амина С2, изонитрила С3 и карбоновой кислоты, и процесс проводят при температуре 10-25°С в инертном протонном растворителе (метанол, этанол, трифторэтанол и подобных) или апротонном растворителе (гексан, циклогексан, этиленкарбонат, нитрометан и подобных) без катализатора или в его присутствии. При этом соединения формулы I получают, удаляя карбоксильную группу из полупродукта Р1 действием восстановительного агента, например, такого как борогидрид щелочного металла (NaBH4, LiBH4, KBH4) или действием основания, такого как гидроксиды или карбонаты щелочных металлов, или подобного (основной гидролиз).
Приведенные ниже примеры иллюстрируют получение представителей предлагаемых соединений согласно изобретению, но не ограничивают последнее.
Все соединения, указанные ниже, как и соединения, перечисленные выше, но не упоминаемые в примерах, получены в соответствии со схемой 1.
Для синтеза были использованы следующие исходные реагенты и физико-химические методы доказательства строения синтезированных веществ и их чистоты:
Все растворители и реагенты были получены из коммерческих источников, таких как Sigma-Aldrich (США), Fluka (Германия), Acros (Бельгия) и Lancaster (Англия). Точки плавления (т.пл.) были получены на приборе фирмы Buchi модель В-520. 1Н и 13С ЯМР спектры были получены на спектрометрах фирмы Varian (300 MHz) в CDCl3, D2O и DMSO-d6, химические сдвиги приведены в шкале δ (м.д.). Внутренний стандарт тетраметилсилан.
Содержание основного вещества контролировали с помощью LC-MS на приборе Applied Biosystems (Shimadzu 10-AV LC, Gilson-215 автоматическая подача образца, масс-спектрометр API 150EX, детекторы UV (215 и 254 нм) и ELS, колонка Luna-C18, Phenomenex, 5 см × 2 мм). В соответствии с данными LC/MS все синтезированные соединения в спектрах MS имели молекулярный пик М+1, при этом содержание основного вещества во всех случаях было выше 95%.
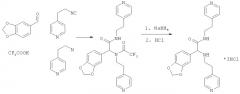
Пример 1. 2-(1,3-бензодиоксол-5-ил)-Н-(2-пиридин-4-илэтил)-2-[(2-пиридин-4-илэтил)-амино]ацетамид (вещество 271)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 48%, 250 мг. Здесь и далее, если не указано иначе, приведены спектры оснований заявляемых соединений. Спектр 1Н-ЯМР: 2.64-2.75 (м, 5Н), 2.85-2.93 (м, 1H), 3.27-3.39 (м, 1H), 3.43-3.54 (м, 1H), 3.99 (с, 1H), 5.87 (с, 2Н), 6.52-6.55 (м, 4Н), 6.97 (д, J=5.8 Гц, 2Н), 7.10 (д, J=5.8 Гц, 2Н), 8.43-8.50 (м, 4Н).
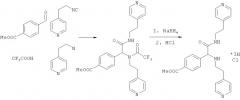
Пример 2. Метил 4-{2-оксо-1,2-бис[(2-пиридин-4-илэтил)амино]этил}бензоат (вещество 661)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 19% (100 мг). Спектр 1Н-ЯМР: 2.65-2.75 (м, 5Н), 2.85-2.93 (м, 1H), 3.28-3.40 (м, 1H), 3.44-3.54 (м, 1H), 3.88 (с, 3Н), 4.15 (с, 1Н), 6.85 (t, J=6.1 Гц, 1H), 6.95 (д, J=5.8 Гц, 2Н), 7.06 (д, J=5.8 Гц, 2Н), 7.27 (д, J=8.1 Гц, 2Н), 7.95 (д, J=8.1 Гц, 2Н), 8.41 (д, J=6.41 Гц, 2Н), 8.46 (д, J=8.46 Гц, 2Н).
Пример 3. 2-(4-гидроксифенил)-N-(2-пиридин-4-илэтил)-2-[(2-пиридин-4-илэтил)амино]-ацетамид (вещество 581)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:МеОН 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 25% (120 мг). Спектр 1Н-ЯМР: 2.60-2.93 (м, 6Н), 3.27-3.37 (м, 1H), 3.45-3.57 (м, 1H), 4.01 (с, 1H), 6.67 (д, J=8.6 Гц, 2Н), 6.92 (t, J=6.1 Гц, 1H), 6.90-6.97 (м, 4Н), 7.07 (д, J=5.6 Гц, 2Н), 8.37 (д, J 5.8 Гц, 2Н), 9.45 (д, J=5.8 Гц, 2Н).
Пример 4. 2-(1,3-бензодиоксол-5-ил)-N-(пиридин-4-илметил)-2-[(пиридин-4-илметил)-амино]ацетамид (вещество 272)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:МеОН 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 29% (140 мг). Спектр 1Н-ЯМР: 3.11 (д, J=14.2 Гц, 2Н), 3.16 (д, J=6.8 Гц), 3.38 (д, J=6.8 Гц, 2Н), 3.77 (д, J=14.2 Гц, 2Н), 5.98 (с, 2Н), 6.69 (АВ-система, J=7.8 Гц, 2Н), 6.98 (с, 1H), 7.13 (д, J=4.8 Гц), 7.23 (д, J=4.8 Гц), 8.49 (д, J=4.1 Гц, 2Н), 8.51 (д, J=4.1 Гц, 2Н).
Пример 5. 2-(1,3-бензодиоксол-5-ил)-2-[(2-пиперидин-4-илэтил)амино]-N-(2-пиридин-4-илэтил)ацетамид (вещество 273)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии СН2Сl2:МеOН 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 29% (150 мг). Спектр 1Н-ЯМР: 1.25-1.40 (м, 2Н), 1.55-1.70 (м, 3Н), 1.78-1.86 (м, 2Н), 2.75-2.95 (м, 4Н), 2.95-3.13 (м, 2Н), 3.25-3.33 (м, 2Н), 3.44-3.52 (м, 1H), 3.69-3.80 (м, 1Н), 5.98 (д, J=21.5 Гц, 2Н), 6.76-6.85 (м, 2Н), 6.91-6.97 (м, 1H), 7.78 (д, J=6.3 Гц, 2Н), 8.58 (д, J=6.3 Гц, 2Н).
Пример 6. 2-(1,3-бензодиоксол-5-ил)-2-[(2-пиперидин-4-илэтил)амино]-N-(пиридин-4-ил-метил)ацетамид (вещество 274)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 20% (100 мг). Спектр 1Н-ЯМР: 1.07-1.24 (м, 2Н), 1.50-1.70 (м, 5Н), 2.57-2.76 (м, 3Н), 2.80-2.90 (м, 1H), 3.00-3.17 (м, 3Н), 5.14 (д, J=8.6 Гц, 1H), 5.52 (д, J=8.6 Гц, 1H), 5.68 (с, 2Н), 6.50 (д, J 7.6 Гц, 1H), 6.75-6.79 (м, 1H), 6.93 (с, 1H), 8.04 (д, J=5.6 Гц, 2Н), 8.63 (д, J=5.6 Гц, 2Н).
Пример 7. 2-(4-гидроксифенил)-2-[(2-пиперидин-4-илэтил)амино]-N-(2-пиридин-4-ил-этил)ацетамид (вещество 583)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:МеОН 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:МеОН 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 21% (100 мг). Спектр 1Н-ЯМР: 1.29-1.60 (м, 6Н), 1.75-2.00 (м, 2Н), 2.85-3.10 (м, 4Н), 3.33-3.40 (м, 2Н), 3.45-3.60 (м, 1Н), 3.90-4.10 (м, 2Н), 5.47 (с, 2Н), 6.84 (д, J=8.1 Гц, 2Н), 7.01 (д, J=8.1 Гц, 2Н), 8.04 (д, J=6.1 Гц, 2Н), 8.74 (д, 1=6.1 Гц, 2Н).
Пример 8. Метил 4-{2-оксо-1-[(2-пиридин-3-илэтил)амино]-2-[(2-пиридин-4-илэтил)амино]этил}бензоат (вещество 669)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 38% (200 мг). Спектр 1Н-ЯМР: 2.65-2.75 (м, 5Н), 2.81-2.90 (м, 1H), 3.31-3.40 (м, 1H), 3.44-3.55 (м, 1H), 3.87 (с, 3Н), 4.15 (с, 1H), 6.85-7.05 (м, 3Н), 7.2 (уш.с, 1H), 7.26 (д, J=8.1 Гц, 2Н), 7.43 (д, J=7.6 Гц, 1H), 7.93 (д, J=8.1 Гц, 2Н), 8.4 (уш.с, 4Н).
Пример 9. Метил 4-{2-оксо-1,2-бис[(2-пиридин-3-илэтил)амино]этил}бензоат (вещество 668)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 38% (200 мг). Спектр 1Н-ЯМР: 2.65-2.75 (м, 5Н), 2.80-2.90 (м, 1H), 3.30-3.40 (м, 1H), 3.44-3.50 (м, 1Н), 3.87 (с, 3Н), 4.15 (с, 1Н), 6.03 (t, J=5.8 Гц), 7.13 (дд, J=4.8, 2.8 Гц, 1H), 7.18 (дд, J=4.8, 2.8 Гц, 1Н), 7.27 (д, J=8.3 Гц, 2Н), 7.35 (д, J=7.8 Гц, 1H), 7.44 (д, J=7.8 Гц, 1H), 7.93 (д, J=8.3 Гц, 2Н), 8.34 (с, 1H), 8.39-8.47 (м, 3Н).
Пример 10. Метил 4-{2-оксо-2-[(2-пиридин-3-илэтил)амино]-1-[(2-пиридин-4-илэтил)амино]этил}бензоат (вещество 670)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:МеОН 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 38% (200 мг). Спектр 1Н-ЯМР: 2.65-2.75 (м, 5Н), 2.80-2.90 (м, 1H), 3.30-3.40 (м, 1H), 3.44-3.50 (м, 1Н), 3.88 (с, 3Н), 4.15 (с, 1Н), 6.03 (t, J=5.8 Гц), 7.06 (д, J=5.6 Гц, 2Н), 7.10-7.20 (м, 1Н), 7.27 (д, J=8.3 Гц, 2Н), 7.35 (д, J=7.8 Гц, 1H), 7.94 (д, J=8.3 Гц, 2Н), 8.34 (с, 1H), 8.42 (д, J=3.8 Гц, 1H), 8.47 (д, J=5.6 Гц, 2Н).
Пример 11. Метил 3-{2-оксо-1,2-бис[(2-пиридин-4-илэтил)амино]этил}бензоат (вещество 651)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 30% (160 мг). Спектр 1Н-ЯМР: 2.60-2.77 (м, 5Н), 2.81-2.93 (м, 1H), 3.32-3.55 (м, 2Н), 3.88 (с, 3Н), 4.15 (с, 1Н), 7.00 (с, 1H), 7.10-7.20 (м, 2Н), 7.30-7.55 (м, 4Н), 7.86-8.00 (м, 2Н), 8.30-8.57 (м, 4Н).
Пример 12. Метил 3-{2-оксо-1-[(2-пиридин-3-илэтил)амино]-2-[(2-пиридин-4-илэтил)-амино]этил}бензоат (вещество 659)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 30% (160 мг). Спектр 1Н-ЯМР: 2.64-2.77 (м, 5Н), 2.81-2.93 (м, 1H), 3.32-3.40 (м, 1H), 3.44-3.53 (м, 1Н), 3.88 (с, 3Н), 4.15 (с, 1H), 6.91-7.00 (м, 3Н), 7.17-7.20 (м, 1H), 7.32-7.44 (м, 3Н), 7.90-7.95 (м, 2Н), 8.35-8.50 (м, 4Н).
Пример 13. Метил 3-{2-оксо-1,2-бис[(2-пиридин-3-илэтил)амино]этил}бензоат (вещество 658)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 23% (120 мг). Спектр 1Н-ЯМР: 2.60-2.77 (м, 5Н), 2.81-2.93 (м, 1H), 3.32-3.55 (м, 2Н), 3.88 (с, 3Н), 4.15 (с, 1H), 7.00 (с, 1Н), 7.10-7.20 (м, 2Н), 7.30-7.55 (м, 4Н), 7.86-8.00 (м, 2Н), 8.30-8.57 (м, 4Н).
Пример 14. 2-(1,3-бензодиоксол-5-ил)-N-(пиридин-3-илметил)-2-[(пиридин-4-илметил)-амино]ацетамид (вещество 277)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают НСl (газ) и упаривают в вакууме. Выход 23% (110 мг). Спектр 1Н-ЯМР: 3.66-3.75 (м, 2Н), 4.13 (с, 1H), 4.35-4.45 (м, 2Н), 5.92 (с, 2Н), 6.72-6.78 (м, 2Н), 6.92 (с, 1Н), 7.15 (д, J=5.3 Гц, 2Н), 7.15-7.20 (м, 1Н), 7.25-7.30 (м, 1Н), 7.48 (д, J=8.1 Гц, 1H), 8.41 (с, 1H), 8.45 (д, J=5.3 Гц).
Пример 15. 2-(1,3-бензодиоксол-5-ил)-N-(пиридин-3-илметил)-2-[(пиридин-3-илметил)-амино]ацетамид (вещество 275)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают НС1 (газ) и упаривают в вакууме. Выход 23% (110 мг). Спектр 1Н-ЯМР: 3.66 (АВ-система, J=8.6 Гц, 2Н), 4.16 (с, 1H), 4.41 (д, J=6.1 Гц, 2Н), 5.93 (с, 2Н), 6.73-6.79 (м, 2Н), 6.83 (с, 1H), 7.18-7.23)м, 2Н), 7.51 (д, J=7.8 Гц, 1H), 7.56 (д, J=7.8 Гц, 1H), 8.41-8.49 (м, 4Н).
Пример 16. 2-(2,3-дигидро-1,4-бензодиоксин-6-ил)-N-(пиридин-4-илметил)-2-[(пиридин-4-илметил)амино]ацетамид (вещество 612)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:МеОН 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 20% (100 мг). Спектр 1Н-ЯМР: 3.10-3.16 (м, 1H), 3.37 (д, J=7.1 Гц), 3.73 (д, J=14.2 Гц), 4.17 (д, J=7.1 Гц), 4.20-4.30 (м, 5Н), 6.70-6.85 (м, 2Н), 6.93 (д, J=1.8 Гц, 1Н), 7.14 (д, J=5.8 Гц, 2Н), 7.23 (д, J=5.8 Гц, 2Н), 8.47 (д, J=5.8 Гц, 2Н), 8.50 (д, J=5.8 Гц, 2Н).
Пример 17. 2-(2,3-дигидро-1,4-бензодиоксин-6-ил)-N-(пиридин-3-илметил)-2-[(пиридин-4-илметил)амино1ацетамид (вещество 617)
К раствору 1 ммоль альдегида и 1 ммоль амина в 10 мл метанола добавляют CF3COOH (1 ммоль) и 1 ммоль изонитрила. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Полученный трифторацетамид растворяют в метаноле (10 мл), охлаждают до 0°С и добавляют 0.2 г NaBH4. Смесь перемешивают 12 часов при комнатной температуре, растворитель упаривают в вакууме, а остаток очищают методом колоночной хроматографии CH2Cl2:MeOH 20:1. Чистый продукт растворяют в метаноле, насыщают HCl (газ) и упаривают в вакууме. Выход 32% (160 мг). Спектр 1Н-ЯМР: 3.65-3.74 (м, 2Н), 4.10 (с, 1H), 4.19 (с, 4Н), 4.33-4.43 (м, 2Н), 6.78 (с, 2Н), 6.84 (с, 1Н), 7.10-7.20 (м, 3Н), 7.33 (t, J=5.6 Гц, 1H), 7.47 (д, J=7.8 Гц), 8.39 (с,