Способ очистки рекомбинантных аденовирусов млекопитающих и человека
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, а именно к способу очистки рекомбинантных аденовирусов млекопитающих и человека. Способ включает накопление аденовируса в пермиссивной культуре клеток линии НЕК-293, сбор этих клеток, высвобождениие рекомбинантных аденовирусов за счет разрушения клеток путем перемораживания и их очистку. Используют рекомбинантный капсид-модифицированный аденовирус с модифицированным капсидным белком рlХ, несущим полисахарид-связывающий домен, который выбирают из группы, включающей целлюлозо-связывающий домен, декстран-связывающий домен. Производят посадку рекомбинантных капсид-модифицированных аденовирусов на полисахаридный носитель, который выбирают из группы, включающей целлюлозный носитель для связывания с целлюлозо-связывающим доменом, декстрановый носитель - для связывания с декстран-связывающим доменом. Инкубируют полученную смесь. Осуществляют процесс очистки, для чего полисахаридный носитель с аденовирусами осаждают центрифугированием, а полученный супернатант удаляют. Промывают осажденный полисахаридный носитель с аденовирусами промывочными буферами, после этого производят элюирование аденовирусов с полисахаридного носителя. Производят разделение полученной суспензии центрифугированием. Отбирают вируссодержащий супернатант и стабилизируют его. Предложенное изобретение позволяет получить биологически активный, хроматографически чистый и концентрированный аденовирусный препарат и сократить время его очистки. 14 з.п. ф-лы, 4 ил., 2 табл., 4 пр.
Реферат
Изобретение относится к молекулярной биотехнологии и нанотехнологии, конкретно к процессам, связанным с очисткой рекомбинантных аденовирусов человека и млекопитающих от клеточного дебриса и других компонентов вируссодержащей среды. Изобретение может быть использовано в прикладной вирусологии, производстве псевдоаденовирусных нановакцин, нанобиотехнологии, молекулярной биологии и других областях науки и техники, где существует необходимость очистки препаративных количеств аденовирусного материала.
Традиционные способы очистки аденовирусов включают следующие основные операции: разрушение зараженных аденовирусом клеток путем 3-кратного перемораживания; осаждение клеточного дебриса низкоскоростным центрифугированием; концентрирование вирионов путем осаждения вируса на поверхность раствора CsCl плотностью 1,375 г/см3 ультрацентрифугированием; очистка вируса двукратным ультрацентрифугированием в равновесном градиенте плотности CsCI (p=1,365 г/см3) в течение суток [Green K.Y., Wold W.S.M. Human adenoviruses: growth, purification and transfection assay. // Methods Enzymology 1980 v.-80, pp.425-431]. В результате этой последовательности операций получают вирусный материал, имеющий тот или иной титр, зависящий от эффективности процесса размножения вируса. Однако существенным недостатком данного способа является содержание вирусного препарата в высокомолярном растворе хлористого цезия, являющемся токсичным продуктом, несовместимым для применения человеку и другим биологическим объектам.
В определенной степени преодолеть этот недостаток позволяет использование ионообменной хроматографии, эксклюзионной хроматографии и/или ультрафильтрации [Патент US 6537793 В2; Патент US 6261823 В1]. Однако такой способ очистки имеет несколько недостатков. Во-первых, данный метод очистки является многоступенчатым и, как следствие, трудоемким. Во-вторых, исходный клеточный лизат, содержащий аденовирус, не может быть непосредственно нанесен на хроматографическую колонку по причине потери ею функциональности вследствие «забивки» большим количеством клеточных балластных белков. В-третьих, процесс ультрафильтрации, сам по себе, также не может быть отдельно использован для очистки аденовирусного препарата из клеточного лизата, так как процесс ультрафильтрации не является абсолютным и не позволяет полностью освободиться от массы балластных белков. И, наконец, в-четвертых, в связи с многостадийностью такого способа очистки, возможны существенные потери аденовирусного материала на выходе.
В этой связи, наиболее простым в отношении процесса очистки вируса из клеточного лизата является способ, позволяющий непосредственно использовать клеточный лизат, содержащий аденовирус, для очистки аденовирионов и получать чистый препарат аденовируса на выходе. В частности, известен способ очистки капсид-модифицированных аденовирусов методом аффинной хроматографии на сорбенте, где в качестве активной фазы выступает мономерный авидин с сорбированным на нем биотином. В этом случае, в качестве очищаемого аденовируса может выступать капсид-модифицированный аденовирус, к капсидным белкам которого генетически привязаны биотин-связывающие пептиды, способные специфически взаимодействовать с биотин-авидиновым носителем. Капсидные белки аденовируса, которые могут подвергаться такой модификации, - это фиберы, пентоны, гексоны или белок pIX. Наибольшую эффективность при таком способе очистки показали pIX-модифицированные аденовирусы, которые представляют собой рекомбинантные аденовирусы, в которых к С-концу капсидного белка pIX через альфа-спиральный спейсер (длиной 45 Ангстрем) генетически привязан биотин-связывающий пептид. Таким образом, принцип очистки таких аденовирусов основан на физико-химическом специфическом взаимодействии биотин-связывающего пептида, расположенного на поверхности капсида аденовируса, и биотин-авидинового носителя. [Campos S.K., Parrott M.B., Barry M.A., 2004. Avidin-based targeting and purification of a protein IX-modified, metabolically biotinylated adenoviral vector. Mol. Ther. 9 (6), 942-954]. Такая модификация капсида аденовируса, как показали исследования, не приводит к снижению трансдуцирующей способности вируса, что может, без ущерба для биофизических свойств вируса, быть использовано в качестве платформы для очистки аденовирусов [Campos S.K., M.B., Barry 2006. Comparison of adenovirus fiber, protein IX, and hexon capsomeres as scaffolds for vector purification and cell targeting. Virology 349, 453-462].
Схема такой очистки включает следующие этапы.
1. Подготовка вирус-содержащего материала.
а) Накопление аденовируса в клетках.
Для наращивания капсид-модифицированного аденовируса с биотин-связывающими пептидами, клетки линии 293А высевают на 150-мм культуральные чашки и выращиваются на питательной среде, содержащей биотин, до достижения ими конфлюэнтности, равной 95%. После этого отработанную среду удаляют, а клетки инфицируют вирусом с множественностью инфекции 20 вирусных частиц на клетку. Инфицирование проводят в 7 мл ростовой среды DMEM с добавлением 30 мкМ биотина в течение 3 ч при 37°C. Затем к клеткам добавляли 18 мл полной питательной среды и выращивали в течение 72 ч.
б) Сбор зараженных клеток и их отмывка от культуральной среды.
После того, как у всех зараженных аденовирусом клеток регистрировали цитопатическое действие вируса, они были собраны в 50-мл конические пробирки и центрифугированы при 300 g в течение 10 минут, а супернатант удален. Осадок клеток дважды промывают 15 мл стабилизирующего буфера (50 мМ Трис, рН=8; 150 мМ NaCl; 5% глицерин) для удаления белковых и нуклеиновых примесей и переносят в 15-мл конические пробирки. Снова центрифугируют при 300 g 10 минут, супернатант удаляют, а клеточный осадок ресуспендируют в 1 мл стабилизирующего буфера (СБ).
в) Лизис клеток для высвобождения аденовируса.
Суспензию отмытых от культуральной среды клеток переносят в микроцентрифужные пробирки и лизируют клетки путем трехкратного замораживания-оттаивания для высвобождения вируса из клеток.
г) Освобождение от клеточного дебриса.
Клеточные лизаты после трехкратного перемораживания центрифугируют при 10000 g для осаждения клеточного дебриса и отбирают супернатант, содержащий аденовирус, для последующей очистки аденовируса.
Описанный выше этап 1 (подэтапы а, б, в, г) подготовки вирус-содержащего материала является общеизвестным и используется в качестве подготовительного этапа при всех известных способах очистки аденовирусов (в плотности хлористого цезия, в ионообменной и эксклюзионной хроматографии, в ультрафильтрации).
2. Непосредственная очистка аденовируса на носителе с мономерным авидином, которая состоит из следующих стадий.
а) Предварительная подготовка носителя для очистки аденовируса.
Для очистки капсид-модифицированного аденовируса из клеточного лизата, носитель с мономерным авидином (2,5 мл, «SoftLink») активировали путем адсорбции на нем биотина и регенерировали в соответствии с инструкциями производителя. Затем активированный носитель промывали один раз в 10 мл СБ и ресуспендировали в конечном объеме СБ 2,5 мл.
б) Посадка аденовируса на биотиновый носитель. 500 мкл вируссодержащего лизата добавляли к 500 мкл ресуспендированного активированного носителя и инкубировали в течение 4 ч при медленном встряхивании при +4°С.
в) Осаждение носителя с аденовирусом.
Для осаждения носителя, связавшегося с аденовирусом, смесь вируса и носителя центрифугируют.
г) Промывка носителя с аденовирусом.
Носитель с аденовирусом для освобождения от нуклеиновых и белковых примесей промывали путем добавления 12 мл СБ и последующего осаждения носителя с аденовирусом и удаления супернатанта (как в п.5.4). Такую процедуру проводили 5 раз.
д) Элюирование аденовируса с носителя.
Аденовирус элюировали добавлением 500 мкл СБ и 5 мМ биотина при аккуратном встряхивании в течение ночи при +4°С.
е) Отбор вирус-содержащего раствора.
Элюированный с носителя капсид-модифицированный аденовирус отбирали в супернатанте после осаждения (путем центрифугирования) носителя.
Для этого способа очистки капсид-модифицированного аденовируса характерны достаточная чистота получаемого препарата аденовируса, а также технологичность процесса очистки аденовирусного препарата.
Данное техническое решение, как наиболее близкое к заявляемому по использованию капсид-модифицированных аденовирусов для очистки с помощью аффинной хроматографии на носителе, выбрано за прототип.
Недостатками прототипа являются:
- Невозможность непосредственного использования носителя для сорбции на нем капсид-модифицированного аденовируса. Данный недостаток связан с тем, что носитель, используемый для очистки капсид-модифицированных аденовирусов и представляющий собой сорбент с активной фазой в виде мономерного авидина, нуждается в предварительной подготовке: активировании и регенерации, суть которой сводится к сорбированию на поверхности носителя молекул биотина и отмывке активированного носителя в стабилизирующем буфере. Эта подготовка представляет собой дополнительный этап очистки, который существенно увеличивает трудоемкость процесса в целом и требует затрат на дополнительные расходные материалы (биотин, компоненты буфера).
- Высокое соотношение объема вирус-содержащего лизата клеток и объема ресуспендированного носителя, которое в данном способе составляет 1:1. Такое соотношение является невыгодным как с экономической точки зрения, так и с точки зрения возможности концентрирования аденовирусного препарата. В связи с большим объемом носителя, для элюирования капсид-модифицированного аденовируса необходимы большие объемы элюирующего буфера, что приводит к неизбежному разбавлению конечного продукта.
Длительная подготовка клеточного вирус-содержащего материала (первичное центрифугирование, 2-кратное отмывание, центрифугирование, ресуспендирование), что может приводить к потерям аденовирусного урожая на этом этапе очистки в связи с механическим разрушением клеток при многократных процедурах промывания и центрифугирования клеток. Кроме того, длительная подготовка клеточного материала усложняет технологию очистки и увеличивает ее время.
- В прототипе используется более дорогостоящий носитель (авидин-биотиновый), чем предлагамый в заявленном изобретении - полисахаридный (например, целлюлозный или декстрановый), для очистки аденовируса, что существенно увеличивает себестоимость целевого продукта.
- Кроме того, в прототипе после цикла очистки аденовирусный препарат оказывается связанным с биотином через модифицированный белок pIX, что препятствует дальнейшей модификации аденовектора путем физико-химического привязывания к модифицированному белку pIX различных целевых лигандов (бактериальные антигены, антитела против маркерных клеточных рецепторов) для использования векторов как наноносителей антигенов для вакцинации или для направленной трансдукции капсид-модифицированными аденовирусами определенных типов клеток человека и животных.
Задачей предлагаемого изобретения является разработка способа очистки рекомбинантных аденовирусов млекопитающих и человека, позволяющего получать биологически активный, хроматографически чистый и концентрированный аденовирусный препарат и сократить время его очистки, при этом удешевить способ за счет использования более дешевого носителя.
Указанная задача решается за счет того, что в предлагаемом способе, включающем накопление аденовируса в пермиссивной культуре клеток, сбор этих клеток, высвобождение рекомбинантных аденовирусов за счет разрушения клеток путем перемораживания, и их очистку, в качестве очищаемого рекомбинантного аденовируса выбирают рекомбинантный капсид-модифицированный аденовирус с модифицированным капсидным белком pIX, несущим полисахарид-связывающий домен, а в процессе очистки производят посадку рекомбинантных капсид-модифицированных аденовирусов на полисахаридный носитель путем смешивания полисахаридного носителя с вируссодержащим лизатом и инкубируют, при этом рекомбинантные капсид-модифицированные аденовирусы аффинно связываются с полисахаридным носителем за счет полисахарид-связывающих доменов. Затем осуществляют процесс очистки, для чего полисахаридный носитель с адсорбированными на нем рекомбинантными капсид-модифицированными аденовирусами путем осаждения его центрифугированием освобождают от клеточных растворимых продуктов, разрушенных клеток и других балластных веществ, оставшихся от питательной среды, в которой выращивались клетки, а полученный супернатант удаляют, после чего осажденный полисахаридный носитель с адсорбированными на нем рекомбинантными капсид-модифицированными аденовирусами промывают промывочными буферами для окончательного удаления балластных веществ и опять осаждают, а полученный супернатант удаляют. После этого производят элюирование рекомбинантных капсид-модифицированных аденовирусов с полисахаридного носителя, для чего добавляют элюирующий буфер и инкубируют раствор, при этом происходит диссоциация и рекомбинантные капсид-модифицированные аденовирусы переходят в раствор, а для дальнейшего разделения полисахаридного носителя и рекомбинантных капсид-модифицированных аденовирусов производят разделение полученной суспензии центрифугированием. Затем отбирают вируссодержащий супернатант и стабилизируют его путем нейтрализации за счет добавления нейтрализующего буфера. В качестве полисахаридного носителя используют нерастворимый в водных средах субстрат, полностью состоящий из целлюлозы, а в качестве целлюлозы используют аморфную целлюлозу, либо модифицированные формы целлюлозы, например метилцеллюлозу, карбоксиметилцеллюлозу. В качестве полисахаридного носителя могут быть использованы целлюлозные остатки, привитые к субстрату другой, не полисахаридной химической природы. В качестве полисахаридного носителя может быть использован декстрановый носитель, например, сефадексы, либо сефакрилы. В качестве полисахаридного носителя могут быть использованы декстрановые остатки, привитые к субстрату другой, не полисахаридной химической природы. В заявленном способе смешивание полисахаридного носителя с вируссодержащим лизатом производят в соотношении по массе от 1:1 до 1:100, а инкубирование осуществляют в течение 2-24 часов в динамическом режиме. В способе осажденный полисахаридный носитель с адсорбированными на нем рекомбинантными капсид-модифицированными аденовирусами промывают в два этапа, при этом сначала промывают нейтральным промывочным буфером с рН от 6,0 до 7,8 в соотношении от 1:5 до 1:100 по объему, причем промывку осуществляют многократно, затем промывают кислым отмывочным буфером рН от 3,7 до 6,0 однократно. Элюирование рекомбинантных капсид-модифицированных аденовирусов с полисахаридного носителя производят, с добавлением элюирующего буфера с рН от 2,9 до 3,5 а инкубирование производят продолжительностью от 20 до 90 минут. Вируссодержащий супернатант, содержащий рекомбинантные капсид-модифицированные аденовирусы, нейтрализуют до значения рН от 6,5 до 7,4.
Выбор путей и режимов реализации, а также характеристик используемых материалов заявляемого способа обусловлен следующими факторами.
Предлагаемое техническое решение предусматривает использование для аффинной очистки лизата зараженных капсид-модифицированным аденовирусом клеток, полученного при непосредственном перемораживании клеточного материала без предварительной отмывки зараженных клеток в отмывочных буферах. Это, с одной стороны, позволяет избавиться от дополнительных этапов технологии очистки аденовируса, а с другой стороны, предохраняет от возможных потерь аденовирусного урожая вследствие механического разрушения клеток в процессе отмывки и центрифугирования. В отношении аффинной очистки аденовируса на полисахаридных носителях, предлагаемое техническое решение ранее не было известно.
В качестве носителя для очистки капсид-модифицированного аденовируса в заявляемом способе используют дешевые полисахаридные носители как целлюлозные, так и декстрановые. Такие носители не нуждаются в предварительной подготовке (активировании, регенерации), что существенно упрощает технологию и делает ее более дешевой, в связи с низкой себестоимостью самого носителя и отсутствием необходимости использовать дополнительные реагенты для активирования и регенерации носителя.
Соотношение объема ресуспендированного полисахаридного носителя и объема вируссодержащего лизата клеток может составлять от 1:1 до 1:100, соответственно, в зависимости от концентрации аденовируса в лизате. Такое соотношение является наиболее выгодным как с экономической точки зрения, так и с точки зрения возможности концентрирования аденовирусного препарата, так как в связи с малым объемом носителя для элюирования аденовируса требуются небольшие объемы элюирующего буфера, а значит конечный продукт (аденовирусный препарат) будет более концентрированным, что существенно для использования его в медицине и ветеринарии.
В качестве материала для очистки выбирают рекомбинантные капсид-модифицированные аденовирусы, к капсиду которых, посредством генетической модификации капсидных белков, привязаны полисахарид-связывающие домены. Благодаря наличию и экспонированию полисахарид-связывающих доменов на поверхности капсида таких рекомбинантных аденовирусов, вирусные частицы приобретают способность взаимодействовать с соответствующим полисахаридным носителем. Как показали проведенные эксперименты (в данной заявке результаты не приводятся), взаимодействие капсид-модифицированного аденовируса с носителем является достаточно прочным для того, чтобы иметь возможность многократно промывать адсорбированный на носителе аденовирус от неспецифических клеточных и культуральных компонентов различной химической природы (белки, нуклеиновые кислоты, липиды, гликопротеиды и т.д.), что позволяет получать достаточно чистый аденовирусный препарат на выходе. Адсорбированный на полисахаридном носителе аденовирус после серии промывок элюируют буферами различной ионной силы и кислотности. Так, например, аденовирус с целлюлозо-связывающим доменом в составе белка pIX способен взаимодействовать с аморфной нерастворимой целлюлозой и элюироваться путем добавления трис-фосфатного буфера с рН=3,0 в течение 30 минут. По данным исследования элюированного аденовируса, такой способ элюирования вируса с носителя позволяет получать аденовирусный препарат с выходом не менее 60%, не повреждая структуру аденовирионов, и последние способны сохраняться в буфере более суток при температуре +4°C.
Предлагаемое техническое решение предполагает использование полисахаридного носителя и полисахарид-связывающего домена в составе рекомбинантного аденовируса. Поскольку для каждого из полисахаридных носителей те или иные полисахарид-связывающие домены в структуре аденовируса могут быть подходящими или неподходящими для их физико-химического взаимодействия осуществляют подбор на соответствие полисахарид-связывающего домена и полисахаридного носителя, к которому конкретные капсид-модифицированные аденовирусы будут проявлять сродство для эффективного прикрепления. Это связано с тем, что предсказать, что какая-либо модификация аденовируса путем генетического привязывания к его капсидным белкам полисахарид-связывающего домена будет совместима с жизнью такого модифицированного аденовируса, невозможно. Это объясняется тем, что не всякая модификация капсидных белков аденовируса способна давать стабильное вирусное потомство в связи с возможными конформационными помехами при ассемблировании вирусных частиц, вызванными встраиванием в капсид конкретного полисахарид-связывающего домена. Подбор основан на химическом сродстве данного полисахарид-связывающего домена и полисахаридного носителя. В этой связи, предлагаемым изобретением предусматривается, что нерастворимый полисахаридный носитель содержит химические группировки углеводной природы или целые молекулы поли- или олигосахаров, обеспечивающие аффинное прикрепление соответствующих полисахарид-связывающих доменов, экспонированных на поверхности капсида аденовируса, к поверхности полисахаридного носителя. При этом носитель может представлять собой полностью углеводный субстрат, с которым способны взаимодействовать определенные полисахарид-связывающие домены. Кроме того, сам носитель может быть приготовлен на основе как природных, так и синтетических полимеров, не способных специфически взаимодействовать с аденовирусами, а вышеуказанные углеводные группировки или молекулы могут быть введены в структуру носителя после его формирования, что достигается известными способами, например химической прививкой. Подбор полисахаридных носителей не является предметом данного заявляемого изобретения.
Такое сочетание признаков, как совокупность используемых в заявляемом техническом решении операций процесса очистки рекомбинантных капсид-модифицированных аденовирусов и применяемых для этого нерастворимых полисахаридных носителей, ранее известно не было.
Примеры для очистки.
Пример 1.
1. Подготовка вируссодержащего материала.
1) Накопление рекомбинантного капсид-модифицированного аденовируса в клетках.
Для накопления рекомбинантного капсид-модифицированного аденовируса с целлюлозо-связывающими доменами в структуре капсидного белка pIX, этим вирусом заражали клетки линии НЕК-293, высеянные на тридцать 150-мм культуральных чашек с конфлюэнтностью монослоя 90% в дозе 15 инфекционных вирусных частиц на клетку. На вторые сутки после заражения наблюдали цитопатическое действие (далее ЦПД) вируса у 100% клеток.
2) Сбор зараженных клеток.
После наступления ЦПД клетки собирали в центрифужные банки (V=200 мл) и центрифугировали для осаждения клеток при 1500 об/мин, в течение 10 минут, а супернатант удаляли. Осадок клеток ресуспендировали в 10 мл фосфатного солевого буфера (далее PBS).
3) Лизис клеток для высвобождения рекомбинантного капсид-модифицированного аденовируса.
Клетки в полученной суспензии лизировали путем трехкратного перемораживания для высвобождения рекомбинантного капсид-модифицированного аденовируса из клеток.
4) Освобождение от клеточного дебриса.
Клеточные лизаты после трехкратного перемораживания центрифугировали при 5000 об/мин в течение 10 минут для осаждения клеточного дебриса, а супернатант, содержащий рекомбинантный капсид-модифицированный аденовирус, отбирали для его последующей очистки.
На этой стадии, после получения суспензии рекомбинантного капсид-модифицированного аденовируса, освобожденной от клеточного дебриса, из этой суспензии отбирали 200 мкл в отдельную пробирку для определения исходного титра рекомбинантного капсид-модифицированного аденовируса для последующего сравнения с титром этого аденовируса после очистки и определения его выхода (данные в таблице 1, где приведена концентрация аденовирусов до и после очистки).
Перечисленные этапы подготовки вируссодержащего материала, а также отбор аликвоты исходного материала для определения титра рекомбинантного капсид-модифицированного аденовируса, являются общими для всех примеров, поэтому в примерах 2 и 3 будут упоминаться кратко.
2. Непосредственная очистка рекомбинантного капсид-модифицированного аденовируса на целлюлозном носителе.
2.1. Посадка рекомбинантного капсид-модифицированного аденовируса на целлюлозный носитель. В качестве носителя для очистки рекомбинантного капсид-модифицированного аденовируса использовали целлюлозные носители: аморфную целлюлозу; носители, содержащие остатки целлюлозы, привитые к субстрату другой (не полисахаридной) химической природы; модифицированные формы целлюлозы (метилцеллюлоза, карбоксиметилцеллюлоза). Эти носители смешивали с приготовленной вируссодержащей суспензией в соотношении: 1 г целлюлозного носителя +9 мл вируссодержащей суспензии. Смесь инкубировали в течение 16 часов при постоянном покачивании при температуре +4°C.
2.2. Осаждение целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом.
Затем целлюлозный носитель с адсорбированным на нем рекомбинантным капсид-модифицированным аденовирусом осаждали центрифугированием при 4000 об/мин в течение 5 минут. Супернатант удаляли.
2.3. Промывка.
а) Сначала осадок целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом промывали нейтральным трис-фосфатным буфером рН=7,2 в объеме 10 мл, а затем снова осаждали центрифугированием 4000 об/мин в течение 5 минут с последующим удалением супернатанта, как описано в этапе 2.2. Промывку повторяли 2 раза.
б) Для окончательной отмывки целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом от связавшихся с ним балластных веществ (белки, нуклеиновые кислоты, липиды, гликопротеиды и т.д.) целлюлозный носитель с рекомбинантным капсид-модифицированным аденовирусом промывали кислым трис-фосфатным буфером рН 4,5 в объеме 8 мл. Целлюлозный носитель с рекомбинантным капсид-модифицированным аденовирусом затем осаждали и удаляли супернатант, как в этапе 2.2.
2.4. Элюирование рекомбинантного капсид-модифицированного аденовируса.
Для элюирования рекомбинантного капсид-модифицированного аденовируса с целлюлозного носителя добавляли кислый элюирующий трис-фосфатный буфер (рН 3,0) в объеме 3,5 мл и инкубировали в течение 30 минут при постоянном покачивании.
2.5. Отбор вируссодержащего раствора.
Для разделения целлюлозного носителя и рекомбинантного капсид-модифицированного аденовируса суспензию центрифугировали, как описано в этапе 2.2, а затем отбирали вируссодержащий супернатант.
2.6. Нейтрализация.
Так как в отобранном вируссодержащем супернатанте рН=3,0, рекомбинантный капсид-модифицированный аденовирус не может сохраняться длительное время, раствор нейтрализовали путем добавления карбонатного буфера (рН=9,2) в объеме 3,5 мл для выравнивания рН до значения 7,2.
Аликвоты полученного очищенного рекомбинантного капсид-модифицированного аденовируса отбирали для определения его концентрации и титра, а также для определения чистоты рекомбинантного капсид-модифицированного аденовируса методом высокоэффективной жидкостной хроматографии.
Пример 2.
1. Подготовка вируссодержащего материала. Как в примере 1.
2. Непосредственная очистка рекомбинантного капсид-модифицированного аденовируса на целлюлозном носителе.
2.1. Посадка аденовируса на целлюлозный носитель.
Как и в примере 1, носителями для очистки рекомбинантного капсид-модифицированного аденовируса являлись: аморфная целлюлоза; носители, содержащие остатки целлюлозы, привитые к субстрату другой (не полисахаридной) химической природы; модифицированные формы целлюлозы (метилцеллюлоза, карбоксиметилцеллюлоза). Эти носители смешивали с приготовленной вируссодержащей суспензией в соотношении: 0,5 г целлюлозного носителя + 9 мл вируссодержащей суспензии. Смесь инкубировали в течение 2 часов при постоянном покачивании при температуре +4°C.
2.2. Осаждение целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом.
Затем целлюлозный носитель с адсорбированным на нем рекомбинантным капсид-модифицированным аденовирусом осаждали центрифугированием при 4000 об/мин в течение 5 минут. Супернатант удаляли.
2.3. Промывка.
а) Сначала осадок целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом промывали нейтральным трис-фосфатным буфером рН=6,0 в объеме 10 мл, а затем снова осаждали центрифугированием 4000 об/мин в течение 5 минут с последующим удалением супернатанта, как описано в этапе 2.2. Промывку повторяли 4 раза.
б) Для окончательной отмывки целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом от связавшихся с ним балластных веществ (белки, нуклеиновые кислоты, липиды, гликопротеиды и т.д.) целлюлозный носитель с рекомбинантным капсид-модифицированным аденовирусом промывали кислым трис-фосфатным буфером рН=6,0 в объеме 8 мл. Целлюлозный носитель с рекомбинантным капсид-модифицированным аденовирусом вирусом затем осаждали и удаляли супернатант, как в этапе 2.2.
2.4. Элюирование рекомбинантного капсид-модифицированного аденовируса.
Для элюирования рекомбинантного капсид-модифицированного аденовируса с целлюлозного носителя добавляли кислый элюирующий трис-фосфатный буфер (рН 3,5) в объеме 3,5 мл и инкубировали в течение 40 минут при постоянном покачивании.
2.5. Отбор вируссодержащего раствора.
Для разделения целлюлозного носителя и рекомбинантного капсид-модифицированного аденовируса суспензию центрифугировали, как описано в этапе 2.2, а затем отбирали вируссодержащий супернатант.
2.6. Нейтрализация.
Так как в отобранном вируссодержащем супернатанте рН=3,5 рекомбинантный капсид-модифицированный аденовирус не может сохраняться длительное время, раствор нейтрализовали путем добавления карбонатного буфера (рН=9,2) в объеме 3,1 мл для выравнивания рН до значения 7,2.
Аликвоты полученного очищенного рекомбинантного капсид-модифицированного аденовируса отбирали для анализа, как в примере 1.
Пример 3.
1. Подготовка вируссодержащего материала.
Как в примере 1.
2. Непосредственная очистка рекомбинантного капсид-модифицированного аденовируса на целлюлозном носителе.
2.1. Посадка рекомбинантного капсид-модифицированного аденовируса на целлюлозный носитель.
Как и в примере 1, носителями для очистки рекомбинантного капсид-модифицированного аденовируса являлись: аморфная целлюлоза; носители, содержащие остатки целлюлозы, привитые к субстрату другой (не полисахаридной) химической природы; модифицированные формы целлюлозы (метилцеллюлоза, карбоксиметилцеллюлоза). Эти носители смешивали с приготовленной вируссодержащей суспензией в соотношении: 5 г целлюлозного носителя + 5 мл вируссодержащей суспензии. Смесь инкубировали в течение 24 часов при постоянном покачивании при температуре +4°C.
2.2. Осаждение целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом.
Затем целлюлозный носитель с адсорбированным на нем рекомбинантным капсид-модифицированным аденовирусом осаждали центрифугированием при 4000 об/мин в течение 5 минут. Супернатант удаляли.
2.3. Промывка.
а) Сначала осадок целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом промывали трис-фосфатным буфером рН=7,8 в объеме 30 мл, а затем снова осаждали центрифугированием 4000 об/мин в течение 5 минут с последующим удалением супернатанта, как описано в этапе 2.2. Промывку повторяли 7 раз.
б) Для окончательной отмывки целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом от связавшихся с ним балластных веществ (белки, нуклеиновые кислоты, липиды, гликопротеиды и т.д.) целлюлозный носитель с рекомбинантным капсид-модифицированным аденовирусом промывали кислым трис-фосфатным буфером рН 3,7 в объеме 15 мл. Целлюлозный носитель с рекомбинантным капсид-модифицированным аденовирусом затем осаждали и удаляли супернатант, как в этапе 2.2.
2.4. Элюирование рекомбинантного капсид-модифицированного аденовируса.
Для элюирования рекомбинантного капсид-модифицированного аденовируса с целлюлозного носителя добавляли кислый элюирующий трис-фосфатный буфер (рН=2,9) в объеме 3 мл и инкубировали в течение 20 минут при постоянном покачивании.
2.5. Отбор вируссодержащего раствора.
Для разделения целлюлозного носителя и рекомбинантного капсид-модифицированного аденовируса суспензию центрифугировали, как описано в этапе 2.2, а затем отбирали вируссодержащий супернатант.
2.6. Нейтрализация.
Так как в отобранном вируссодержащем супернатанте рН=2,9 рекомбинантный капсид-модифицированный аденовирус не может сохраняться длительное время, раствор нейтрализовали путем добавления карбонатного буфера (рН=9,2) в объеме 4 мл для выравнивания рН до значения 7,2.
Аликвоты полученного очищенного рекомбинантного капсид-модифицированного аденовируса отбирали для анализа, как в примере 1.
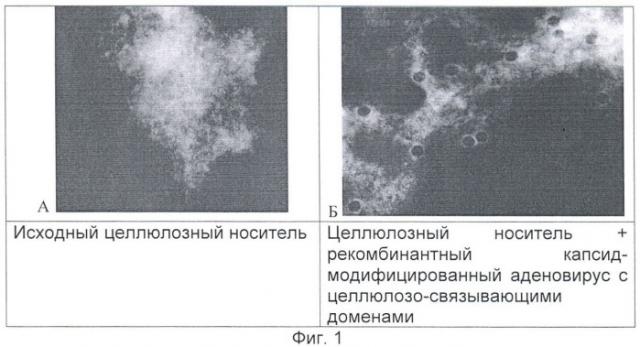
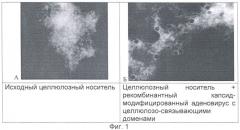
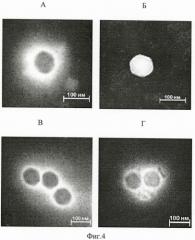
Во всех примерах после этапа 2.3 (отмывка целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом) осуществлялся отбор 100 мкл суспензии целлюлозного носителя с рекомбинантным капсид-модифицированным аденовирусом для исследования наличия специфически связанных рекомбинантных капсид-модифицированных аденовирусных частиц на поверхности целлюлозного носителя методом трансмиссионной электронной микроскопии. Во всех трех примерах на поверхности целлюлозного носителя регистрировали наличие связанных с ним рекомбинантных капсид-модифицированных аденовирусных частиц (фиг.1). На фиг.1 представлена трансмиссионная электронная микроскопия образцов целлюлозного носителя и носителя с адсорбированными на нем рекомбинантными капсид-модифицированными аденовирусными частицами, где А - исходный целлюлозный носитель, Б - Целлюлозный носитель + рекомбинантный капсид-модифицированный аденовирус с целлюлозо-связывающими доменами.
В очищенных на целлюлозном носителе образцах рекомбинантных капсид-модифицированных аденовирусов с целлюлозо-связывающими доменами, а также контрольного аденовируса (без целлюлозо-связывающих доменов) определялись концентрация аденовируса на выходе (спектрофотометрически по максимуму поглощения при λ=260 нм) и титр аденовируса (методом бляшкообразования). Концентрацию аденовирусов выражали в вирусных частицах в 1 мл вирусной, суспензии (вч/мл), титр аденовирусов выражали в бляшкообразующих единицах в 1 мл (БОЕ/мл) В таблице 1 представлена концентрация аденовирусов до и после очистки.
| Таблица 1 | |||
| Всего вирусных частиц | Выход по вирусным частицам, % | ||
| До очистки | После очистки | ||
| Ad5 (к-) | 6,3×1012 | 6×1010 | 0,952% |
| Ad5-CBD (с целлюлозо-связывающими доменами) | 3,1×1012 | 2×1012 | 64,51% |
В таблице 2 представлен титр аденовирусов до и после очистки на аморфной целлюлозе.
| Таблица 2 | |||
| Всего БОЕ | Выход по БОЕ, % | ||
| До очистки | После очистки | ||
| Ad5 (к-) | 6×1010 | 5,25×108 | 0,875 |
| Ad5-CBD (с целлюлозо-связывающими доменами) | 2×1010 | 1,19×1010 | 59,5 |
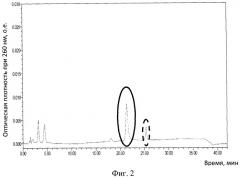
Также полученные после очистки образцы рекомбинантных капсид-модифицированных аденовирусов исследовались на чистоту методом высокоэффективной жидкостной хроматографии (фиг.2). На фиг.2. представлена хроматограмма рекомбинантного капсид-модифицированного аденовируса с целлюлозо-связывающими доменами, очищенного на целлюлозном носителе. Сплошным маркером отмечен пик рекомбинантного капсид-модифицированного аденовируса (22,5 мин), пунктирным - сателлитный пик (дефектные рекомбинантные капсид-модифицированные аденовирусные частицы).
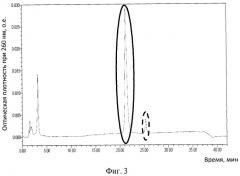
В качестве стандарта чистоты для сравнения в хроматографию брали рекомбинантный капсид-модифицированный аденовирус, очищенный в градиенте плотности хлористого цезия (фиг.3). На фиг.3 представлена хроматограмма рекомбинантного капсид-модифицированного аденовируса с целлюлозо-связывающими доменами, очищенного в плотности хлористого цезия. Сплошным маркером отмечен пик рекомбинантного капсид-модифицированного аденовируса (22,5 мин), пунктирным - сателлитный пик (дефектные рекомбинантные капсид-модифицированные аденовирусные частицы).
По результатам хроматографии можно видеть, что очистка рекомбинантных капсид-модифицированных аденовирусов на целлюлозном носителе позволяет получать рекомбинантные капсид-модифицированные аденовирусы, по чистоте сравнимые с образцами рекомбинантных капсид-модифицированных аденовирусов, очищенными в плотности хлористого цезия.
Пример 4.
Очистка рекомбинантного капсид-модифицированного аденовируса с декстран-связывающими доменами на декстрановых носителях.
1. Подготовка вируссодержащего материала.
1) Накопление рекомбинантного капсид-модифицированного
аденовируса в клетках.
Для накопления рекомбинантного капсид-модифицированного а