Способ моделирования условий протезирующей герниопластики брюшной стенки
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к экспериментальной медицине, и может быть использовано для моделирования условий протезирующей герниопластики передней брюшной стенки. Осуществляют послойное восстановление раневого дефекта, включающее формирование фрагментов из композиционного герниопротеза, покрытого полимерным композитом, с последующей имплантацией данных фрагментов в любой из слоев раны подкожно или внутрибрюшинно. Герниопротез представляет собой сетку основовязаной структуры из синтетических полимерных полиэфирных некрученых пневмосоединенных нетермофиксированных комплексных нитей. Полимерный композит состоит из субстанции повиаргола и поливинилпирролидона медицинского. Молекулярный вес поливинилпирролидона медицинского составляет 13000-90000D при соотношении компонентов, мас.%: 45-55 : 45-55. Способ обеспечивает возможность изучения тканевых реакций при моделировании условий протезирующей герниопластики с использованием предложенного герниопротеза, обладающего выраженным противовоспалительным, противоспаечным и репаративным действием. 9 ил., 2 пр.
Реферат
Изобретение относится к экспериментальной медицине и может использоваться при моделировании условий протезирующей герниопластики передней брюшной стенки для изучения течения воспалительных и репаративных реакций в ране и в брюшной полости в зависимости от места расположения герниопротеза.
В экспериментальной хирургии известны способы изучения тканевых реакций на герниопротезы, изготовленные из различных полимерных материалов (В.Н.Егиев, Д.В.Чижов, Н.В.Филаткина. Взаимодействие полипропиленовых эндопротезов с тканями передней брюшной стенки. Герниология. - 2. - 6. - 2005. - 41-49).
Данные способы характеризуют тканевые реакции, непосредственно связанные с раздражающим действием различных полимерных материалов на перипротезные ткани, в том числе, в зависимости от места расположения герниопротеза, над апоневрозом или под париетальной брюшиной вентральной стенки. Все изучаемые таким образом герниопротезы не обладали противовоспалительными свойствами, что резко увеличивало интенсивность воспалительных реакций в послеоперационной ране и продлевало экссудативную фазу имплантации герниопротеза до двух недель и более.
Известен способ моделирования спайкообразования в брюшной полости при размещении в ней герниопротеза из полипропилена, отступя в сторону от лапаротомного разреза на 1 см, при этом репаративные процессы в ране передней брюшной стенке не изучались (В.А.Липатов, Е.С.Романова, А.А.Нетяга, А.А.Мартынцев, В.А.Синьков. Роль хронического асептического гранулематозного перитонита http//medinfa.ru/article/36/117797).
По собственным данным, при использовании герниопротеза, не обладающего противоспалительными и противоспаечными свойствами, наблюдается генерализованная воспалительная инфильтрация, не позволяющая произвести дифференцированную послойную оценку воспалительных реакций в хирургической ране передней брюшной стенки.
Известен способ моделирования условий протезирующей герниопластики передней брюшной стенки с использованием герниопротеза, изготовленного из синтетического материала РЕПЕРЕН с оценкой тканевых реакций в зависимости от расположения герниопротеза, над апоневрозам или внутрибрюшинно, в сроки имплантации до 90 дней (httpHYPERLINK
"http://surqeon.my1/ru/publ/1-1-1"://HYPERLINK
"http://surgeon.my1/ru/publ/1-1-1"surgeonHYPERLINK
"http.//surgeon.my1/ru/publ/1-1-1".HYPERLINK
"http://surgeon.my1/ru/publ/1-1-1"myHYPERLINK
"http://surgeon.my1/ru/publ/1-1-1"1/HYPERLINK
"http://surgeon.my1/ru/publ/1-1-1"ruHYPERLINK
"http://surgeon.my1/ru/publ/1-1-1"HYPERLINK
"http://surgeon.my1/ru/publ/1-1-1"publHYPERLINK
"http://surgeon. my1/ru/publ/1-1-1"/1-1-0-1).
Способ заключается в размещении герниопротеза из синтетического материала (реперена) в брюшной полости или подкожно. При этом изучалась только тканевая реакция на герниопротез в месте его имплантации.
В качестве прототипа по наиболее близкой технической сущности нами выбран способ моделирования условий протезирующей герниопластики передней брюшной стенки с использованием герниопротеза, представляющего собой сетку основовязаной структуры из синтетических полимерных полиэфирных комплексных нитей. (Пострелов Н.А., Афиногенов Г.Е., Басин Б.Я., Афиногенова А.Г., Кольцов А.И., Клюев А.Н. Обоснование клинического применения при герниопластике сетчатого протеза с антимикробными свойствами // Вестник хирургии. - 2009. - №6. - С.21-24).
Недостатком прототипа является то, что способ, выбранный нами в качестве прототипа, не позволял изучать репаративные реакции во всех слоях раны передней брюшной стенки, так как используемый в способе-прототипе герниопротез не обладал противовоспалительными и противоспаечными свойствами.
Из доступной литературы не известен способ моделирования условий протезирующей герниопластики передней брюшной стенки, позволяющий изучать репаративные ракции не только в зоне подкожного или внутрибрюшинного расположения герниопротеза, но и во всех слоях раны передней брюшной стенки.
Техническим результатом изобретения является возможность изучения репаративных реакций при моделировании условий протезирующей герниопластики передней брюшной стенки с использованием герниопротеза не только в зоне подкожного или внутрибрюшинного расположения герниопротеза, но и во всех слоях раны передней брюшной стенки.
Технический результат изобретения достигается тем, что способ моделирования условий протезирующей герниопластики передней брюшной стенки заключается в послойном зашивании проникающего в брюшную полость раневого дефекта и формировании фрагментов имплантатов из герниопротеза с последующей имплантацией данных фрагментов в любой из слоев раны подкожно или внутрибрюшинно. Имплантируют фрагменты из композиционного герниопротеза, обладающего противовоспалительными и противоспаечными свойствами и представляющего собой сетку основовязаной структуры из синтетических полимерных полиэфирных комплексных нитей, покрытую полимерным композитом, состоящим из субстанции повиаргола, представляющего собой металлополимерную композицию высокодисперсного металлического серебра, стабилизированного синтетическим полимером коллидоном, и поливинилпирролидона медицинского. Комплексная нить сетки основовязаной структуры выполнена из некрученых пневмосоединенных нетермофиксированных комплексных нитей. Молекулярный вес поливинилпирролидона медицинского составляет 13000-90000 D при соотношении компонентов, мас.%:
Субстанция повиаргола 45-55
Поливинилпирролидон медицинский 45-55.
Способ осуществляется следующим образом.
Для осуществления способа используют композиционный герниопротез, обладающий противовоспалительными и противоспаечными свойствами и представляющий собой сетку основовязаной структуры из синтетических полимерных полиэфирных комплексных нитей, покрытую полимерным композитом, состоящим из субстанции повиаргола, представляющего собой металлополимерную композицию высокодисперсного металлического серебра, стабилизированного синтетическим полимером коллидоном, и поливинилпирролидона медицинского, причем комплексная нить сетки основовязаной структуры выполнена из некрученых пневмосоединенных нетермофиксированных комплексных нитей, а молекулярный вес поливинилпирролидона медицинского составляет 13000-90000 D при соотношении компонентов, мас.%:
Субстанция повиаргола 45-55
Поливинилпирролидон медицинский 45-55.
Из данного протеза формируют фрагменты круглой формы диаметром 15 мм, которые имплантируют через срединную лапаротомную рану передней брюшной стенки длиной 20 мм. Имплантат фиксируют проленовой нитью 5/0 к париетальной брюшине вентральной стенки в области раны или герниопротез располагают подкожно над зашитым раневым дефектом брюшинно-мышечного слоя передней брюшной стенки. Во всех наблюдениях кожу зашивают наглухо. Способ осуществляют на подопытных животных (морские свинки, половозрелые самцы весом 250-300 г). Операции выполняют в условиях контаминации, связанной с несоблюдением асептического режима операционной.
Отличительными существенными признаками заявляемого способа являются следующие:
- в зону герниопластики передней брюшной стенки имплантируют фрагменты, сформированные из композиционного герниопротеза, обладающего противовоспалительными и противоспаечными свойствами и представляющего собой металлополимерную композицию высокодисперсного металлического серебра, стабилизированного синтетическим полимером коллидоном, и поливинилпирролидона медицинского, причем комплексная нить сетки основовязаной структуры выполнена из некрученых пневмосоединенных нетермофиксированных комплексных нитей, а молекулярный вес поливинилпирролидона медицинского составляет 13000-90000 D при соотношении компонентов, мас.%:
Субстанция повиаргола 45-55
Поливинилпирролидон медицинский 45-55.
(Оформлена заявка на полезную модель №2010132048/15 (045321), заявл. 29.07.2010. Протез для герниопластики/Басин Б.Я., Пострелов Н.А., Басин А.Б., Платонов С.М.
Решение о выдаче патента на ПМ от 19.10.2010).
Причинно-следственная связь между существенными отличительными признаками и достигаемым результатом заключается в следующем:
- Высокодисперсное серебро, входящее в состав полимерного композита, в виде нанокластеров, придает герниопротезу антимикробные свойства широкого спектра действия, а высокомолекулярный полимер обеспечивает их пролонгацию до 3 суток. Благодаря антимикробным свойствам в области хирургического вмешательства не возникает воспалительных реакций с присоединением инфекций, а также не происходит отторжения герниопротеза через нагноение с течением времени. В присутствии нанокластеров серебра предупреждается формирование микробной биопленки и развитие инфекционного осложнения вокруг герниопротеза, что создает условия для изучения репаративных реакций не только в зоне подкожного или внутрибрюшинного расположения герниопротеза, но и во всех слоях раны передней брюшной стенки.
Антимикробный эффект связан не только с противомикробным действием высокодисперсного серебра, входящего в состав полимерного композита в виде нанокластеров, но и с присутствием в антимикробном композите поливинилпирролидона медицинского.
- Выполнение комплексной нити из некрученых пневмосоединенных нетермофиксированных комплексных нитей способствует увеличению порозности комплексных нитей, что улучшает их диффузное пропитывание полимерным композитом, тем самым увеличивая содержание нанокластеров серебра в сетчатом герниопротезе, а также блокируя межтканевые пространства нити, превращая ее в псевдомононить толщиной 350 мкм вместе с полимерным покрытием, предупреждая тем самым проникновение инфекта в поры сетчатого герниопротеза, что, в свою очередь, усиливает его противовоспалительные свойства.
- Молекулярный вес поливинилпирролидона 13000-90000 D закрепляет монолитность некрученых комплексных нитей и каркасность псевдомоноконструкции основовязаной структуры сетки герниопротеза, обеспечивая высокую концентрацию нанокластеров серебра в полимерном композите, покрывающим сетку, тем самым обеспечивая противовоспалительные свойства герниопротеза.
- При соотношении компонентов, мас.%: субстанция повиаргола 45-55, поливинилпирролидон медицинский 45-55, количество металлического серебра на грамм сетки составляет 10-11 мг, что обеспечивает четко выраженный противовоспалительный эффект, проявляющийся в резком угнетении образования спаек в свободной брюшной полости при интраабдоминальном расположении герниопротеза.
- Постепенное размягчение и растворение композита в тканевой жидкости со временем, сохраняя пролонгацию антимикробных и противовоспалительных свойств, освобождает элементарные нити сетчатого протеза, создавая благоприятные условия для более раннего и эффективного прорастания пористой матрицы сетки соединительной тканью.
Использование герниопротеза, не обладающего противовоспалительными и противоспаечными свойствами, при несоблюдении асептического режима операционной, сопровождается генерализованным воспалением всех слоев лапаротомной раны и прилегающих к ране органов брюшной полости.
Имплантация герниопротеза с противовоспалительными и противоспаечными свойствами в аналогичных условиях резко снижает воспалительные реакции в лапаротомной ране и в брюшной полости и позволяет определить их преимущественную локализацию, а также характер репаративного процесса относительно расположения герниопротеза.
Противовоспалительное действие герниопротеза не зависит от его месторасположения внутри брюшной полости. Отмечено противоспаечное действие. В подкожно-мышечном слое лапаротомной раны воспалительные реакции ткани выражены в большей степени, чем в брюшной полости. Благоприятному течению репаративных процессов имплантации способствовало также использование лавсановой пористой сетки, превращенной пропитыванием высокомолекулярным поливинилпирролидоном в псевдомоноткань.
Совокупность существенных отличительных признаков является новой и позволяет изучать репаративные реакции при моделировании условий протезирующей герниопластики передней брюшной стенки не только в зоне подкожного или внутрибрюшинного расположения герниопротеза, но и во всех слоях раны передней брюшной стенки.
Примеры конкретного выполнения способа
Пример 1 (заявляемый способ).
Исследование №10. Морская свинка, самец, вес 240 г. Наркоз нембуталовый внутрибрюшинно. Разрез через все слои передней брюшной стенки длиной 20 мм. Фрагмент герниопротеза диаметром 15 мм, представляющий собой сетку основовязаной структуры из синтетических полимерных полиэфирных комплексных нитей, покрытую полимерным композитом, состоящим из субстанции повиаргола, представляющего собой металлополимерную композицию высокодисперсного металлического серебра, стабилизированного синтетическим полимером коллидоном, и поливинилпирролидона медицинского, причем комплексная нить сетки основовязаной структуры выполнена из некрученых пневмосоединенных нетермофиксированных комплексных нитей, а молекулярный вес поливинилпирролидона медицинского составляет 13000-90000 D при соотношении компонентов, мас.%:
Субстанция повиаргола 55
Поливинилпирролидон медицинский 45.
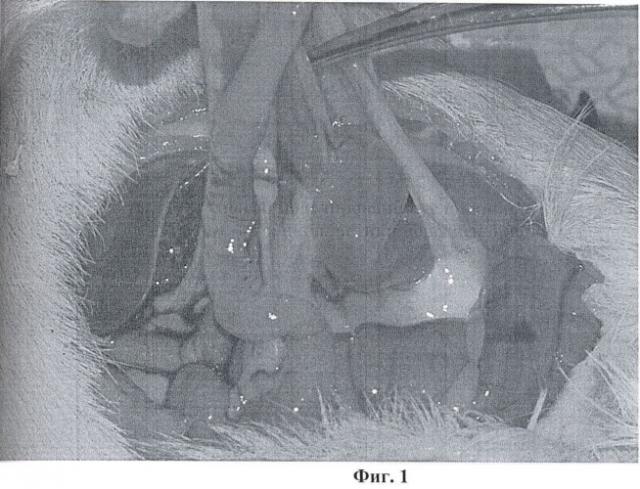
Фрагмент герниопротеза вводили внутрибрюшинно. Затем фиксировали его, последовательно прошивая проленовой нитью края раны в середине разреза брюшной стенки через ячейки герниопротеза в его центре. Швы на кожу. Послеоперационный период протекал гладко. Животное активное, с хорошим аппетитом. Рана зажила первичным натяжением. Через 14 дней животное выведено из опыта. При аутопсии воспалительных изменений в брюшной полости не выявлено. Герниопротез фиксирован в области раны без видимых воспалительных изменений. Фиг.1, иллюстрирующая данный пример, подтверждает отсутствие воспалительных реакций в области раны.
Гистологические данные также подтверждают отсутствие воспалительных реакций в области раны, что дает возможность проводить дифференцированную оценку во всех слоях передней брюшной стенки в связи с протезирующей герниопластикой с расположением герниопротеза подкожно или внутрибрюшинно.
Пример 2 (прототип).
Исследование №5. Морская свинка, самец, вес 240 г. Наркоз нембуталовый внутрибрюшинно. Разрез через все слои передней брюшной стенки длиной 20 мм. Фрагмент герниопротеза диаметром 15 мм, представляющий собой сетку основовязаной структуры из синтетических полимерных полиэфирных комплексных нитей, без покрытия полимерным композитом, вводили внутрибрюшинно. Затем фиксировали его, последовательно прошивая проленовой нитью края раны в середине разреза брюшной стенки через ячейки герниопротеза в его центре. Швы на кожу. Животное неактивное, отмечена потеря веса по сравнению с исходным, вялость, снижение аппетита. Клинически были выражены признаки клинической интоксикации. Кожная рана заживала вторичным натяжением. Через 14 дней животное выведено из опыта. При аутопсии интраабдоминально в области раны передней брюшной стенки определялся воспалительный инфильтрат вокруг лавсановой сетки с включением сальника, стенок кишки и печени (Фиг.2).
При гистологическом исследовании тканей передней брюшной стенки, включающих герниопротез, отсутствует возможность дифференцированной оценки выраженности воспалительных реакций анатомических структур во всех слоях раны передней брюшной стенки лабораторного животного, независимо от места расположения герниопротеза - подкожно или внутрибрюшинно.
Всего прооперировано 15 морских свинок. Через 14 суток после имплантации герниопротеза испытуемых выводили из опыта передозировкой эфира. Контрольную серию составили 5 испытуемых, которым была имплантирована сетка основовязаной структуры из синтетических полимерных полиэфирных комплексных нитей (лавсановая сетка без пропитки) противовоспалительной противоспаечной композицией интраабдоминально.
Основную группу исследованных представляли 10 животных, которым был имплантирован герниопротез по заявляемому способу, обладающий противовоспалительными противоспаечными свойствами (5 - интраабдоминально, 5 - подкожно). Гистологические данные подтверждают отсутствие выраженной воспалительной реакции во всех слоях раны.
Общие и местные реакции на интраабдоминальную имплантацию герниопротеза в контрольной группе были однозначными. Они характеризовались осложненным течением послеоперационного периода. У всех животных контрольной группы отмечалась потеря веса по сравнению с исходным, вялость, снижение аппетита. Клинически были выражены признаки хронической интоксикации. Кожная рана заживала вторичным натяжением, у 3 - под струпом. При аутопсии интраабдоминально в области раны передней брюшной стенки определялся воспалительный инфильтрат вокруг лавсановой сетки с включением сальника, стенок кишечника и печени. В лапаротомной ране также была выражена воспалительная инфильтрация (Фиг.2).
У всех 10 животных, которым был имплантирован герниопротез с противовоспалительными и противоспаечными свойствами по заявляемому способу, послеоперационный период протекал гладко.
Животные были активными, с хорошим аппетитом. Кожная рана передней брюшной стенки заживала без значительных воспалительных изменений, у 4 - первичным натяжением. При аутопсии воспалительных изменений в брюшной полости не выявлено. Фиксация герниопротеза как в брюшной полости, так и подкожно, в области раны со стороны париетальной брюшины, спайкообразованием не сопровождалась (Фиг.1).
Произведена сравнительная гистологическая оценка тканевых реакций на имплантацию герниопротеза без противовоспалительной пропитки и с противовоспалительными противоспаечными свойствами (по заявляемому способу).
При использовании герниопротеза, не обладающего противовоспалительным действием, в лапаротомной ране со стороны брюшины выявлялась выраженная воспалительная реакция. Экссудат носил гнойный характер и был представлен значительным количеством полиморфноядерных лейкоцитов. Также обнаруживались участки некрозов, кровоизлияния, формирующаяся грануляционная ткань. Гистологическая картина в лапаротомной ране представлена на Фиг.3 (а - лейкоциты, б - участки некрозов, в - очаговые кровоизлияния, г - грануляции; окр. гематоксилин-эозин, ув. ×100).
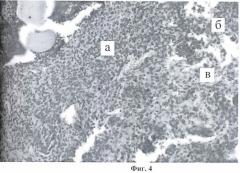
Аналогичная гистологическая картина имела место и в тканях, расположенных более поверхностно. В дерме, жировой клетчатке и между поперечнополосатыми мышцами также обнаруживался массивный нейтрофильный инфильтрат, выявлялись кровоизлияния и незрелые грануляции. Гистологическая картина в жировой ткани и между волокнами поперечнополосатой мышцы представлена на Фиг.4 (а - гнойный экссудат, б - очаговые кровоизлияния, в - незрелые грануляции; окр. гематоксилин-эозин, ув. ×100).
Вокруг самого герниопротеза экссудативная реакция также была значительно выражена. В тканях, прилегающих непосредственно к инородному телу, обнаруживались незрелая грануляционная ткань и массивная инфильтрация полиморфноядерными лейкоцитами. Экссудативная реакция вокруг герниопротеза представлена на Фиг.5. (а - герниопротез, б - грануляционная ткань, в - лейкоцитарная инфильтрация; окр. гематоксилин-эозин, ув. ×100).
При имплантации протеза с противовоспалительным и противоспаечным действием в аналогичных условиях в прилежащей к герниопротезу ткани выявлялась минимальная инфильтрация полиморфноядерными лейкоцитами, с примесью лимфоцитов, плазмоцитов и макрофагов. Также обнаруживалась грануляционная ткань разных степеней зрелости. Клеточная реакция в лапаротомной ране представлена на Фиг.6 (а - многослойный плоский эпителий, б - лимфоплазмоцитарная и нейтрофильная инфильтрация, в - грануляции; окр. гематоксилин-эозин, ув. ×400).
В дерме и в подлежащей жировой ткани клеточная реакция была выражена менее. Обнаруживались очаговая умеренная лимфоплазмоцитарная инфильтрация, единичные макрофаги и мелкоочаговые кровоизлияния (а - очаговая лимфоплазмоцитарная инфильтрация, б - мелкоочаговые кровоизлияния; окр. гематоксилин-эозин, ув.×100). (Фиг.7).
Вокруг герниопротеза выявлялось формирование тонких прослоек соединительной ткани, минимальная очаговая лимфоплазмоцитарная инфильтрация, единичные гигантские клетки типа клеток инородных тел. Подобная гистологическая картина наблюдалась при разных локализациях герниопротеза, как при расположении его в брюшной полости, так и при внедрении в брюшную стенку. Клеточная реакция вокруг герниопротеза при расположении его в брюшной полости представлена на Фиг.8 (а -герниопротез, б - лимфоплазмоцитарная инфильтрация, в - гигантская клетка инородных тел, г - прослойка соединительной ткани; окр. гематоксилин-эозин, ув. ×100).
Клеточная реакция вокруг герниопротеза при расположении его в брюшной полости представлена также на Фиг.9 (а - герниопротез, б - лимфоплазмоцитарная инфильтрация; окр. гематоксилин-эозин, ув. ×400).
Таким образом, заявляемый способ, в отличие от способа-прототипа, позволяет изучать репаративные реакции при моделировании условий протезирующей герниопластики передней брюшной стенки не только в зоне подкожного или внутрибрюшинного расположения герниопротеза, но и во всех слоях раны передней брюшной стенки.
Способ моделирования условий протезирующей герниопластики передней брюшной стенки, заключающийся в послойном восстановлении раневого дефекта, включающем формирование фрагментов из герниопротеза, представляющего собой сетку основовязаной структуры из синтетических полимерных полиэфирных комплексных нитей, с последующей имплантацией данных фрагментов в любой из слоев раны подкожно или внутрибрюшинно, отличающийся тем, что имплантируют фрагменты из композиционного герниопротеза, обладающего противовоспалительными и противоспаечными свойствами и покрытого полимерным композитом, состоящим из субстанции повиаргола, представляющего собой металлополимерную композицию высокодисперсного металлического серебра, стабилизированного синтетическим полимером коллидоном, и поливинилпирролидона медицинского, причем комплексная нить сетки основовязаной структуры выполнена из некрученых пневмосоединенных нетермофиксированных комплексных нитей, а молекулярный вес поливинилпирролидона медицинского составляет 13000-90000D при соотношении компонентов, мас.%:
| Субстанция повиаргола | 45-55 |
| Поливинилпирролидон медицинский | 45-55 |