Распадающиеся в полости рта твердые дозированные формы, содержащие прогестин, и способы получения и применение указанных дозированных форм
Иллюстрации
Показать всеНешипучая распадающаяся в полости рта фармацевтическая твердая дозированная форма содержит прогестин в количестве, эквивалентном от 0,5 до 2 мг левоноргестрела, ионный дезинтегрант в количестве от 8% до 60% от массы дозированной формы и гидрофильный нерастворимый в воде неионный наполнитель в количестве от 1% до 20% от массы дозированной формы. Также описан терапевтический набор, включающий дозированную форму, и способы ее использования. Твердая дозированная форма по изобретению характеризуется быстрым распадением в ротовой полости, не требует запивания ее водой, обеспечивает эффективную абсорбцию (всасывание) и высокую биодоступность прогестина. Фармацевтическая дозированная форма по изобретению подходит для лечения женщин, нуждающихся в экстренной контрацепции. 5 н. и 24 з.п. ф-лы, 10 ил., 23 табл., 8 пр.
Реферат
Область техники
[0001] Настоящее изобретение направлено на разработку нешипучих распадающихся в полости рта фармацевтических твердых дозированных форм, содержащих прогестин, а также способов получения и применения указанных дозированных форм для лечения состояний у женщин, которые в этом нуждаются.
Уровень техники
[0002] Под экстренной контрацепцией в общем случае понимают применение контрацептивных мер к женщине после сексуального контакта (посткоитально) или нежелательного оплодотворения, в частности, после незащищенного сексуального контакта. В настоящий момент доступными формами экстренной контрацепции являются таблетки для экстренной контрацепции (emergency contraceptive pills, ECP) и внутриматочные средства (ВМС). Указанные способы обеспечивают как предотвращение овуляции или оплодотворения, так и возможную имплантацию бластоцисты (эмбриона) после оплодотворения.
[0003] Имеющиеся в настоящее время ECP, также известные как экстренные контрацептивы (ЭК), содержат более высокие дозы тех же стероидных соединений (эстрогенов и прогестинов, или одних лишь прогестинов), которые содержатся в обычных, или традиционных, противозачаточных таблетках для ежедневного перорального приема. Способ, основанный на применении одних лишь прогестинов, предусматривает прием левоноргестрела (синтетического прогестагена) в виде двух доз по 0,75 мг с 12-часовым интервалом (например, Plan В®) или в виде однократной дозы в 1,5 мг в течение 72 часов после коитуса. Согласно комбинированной схеме, или схеме Юзпе, применяют совместно этинилэстрадиол (0,1 мг) и левоноргестрел (0,5 мг) в виде двух доз с 12-часовым интервалом в течение 72 часов после коитуса. Способ, основанный на применении мифепристона, предусматривает прием большой дозы мифепристона, представляющего собой антипрогестин, либо в качестве ЕСР, либо в качестве абортивного средства, в зависимости от того, применяется ли он до или после имплантации. Способы экстренной контрацепции описаны в работах Von Hertzen, H. et al., Lancet, 352:428-432 (1988); Но, Р.С. et al., Human Reproduction, 8(3):389-392 (1993); публикации патента США 2005/0032755; публикации WO 2007/000056 и работе Von Hertzen, H. et al., Lancet, 360: 1803-1810 (2002). Кроме того, в целях экстренной контрацепции также возможно недокументированное применение высокой дозы (высоких доз) традиционных комбинированных или только прогестиновых противозачаточных таблеток для перорального приема.
[0004] Левоноргестрел, представляющий собой синтетический прогестаген, обычно используют в сочетании с эстрогеном в качестве противозачаточного средства; его также можно использовать в отдельности в качестве экстренного противозачаточного средства. Левоноргестрел также применяют для лечения менструальных нарушений, эндометриоза, а также при заместительной терапии прогестероном.
[0005] Фармацевтические препараты, содержащие Левоноргестрел в отдельности, и способы применения левоноргестрела в отдельности для экстренной контрацепции описаны в заявке на патент США 2005/0032755. Фармацевтические препараты, содержащие Левоноргестрел в отдельности, также описаны в CN 1634077.
[0006] Применение традиционных твердых дозированных форм может быть нежелательным при лечении взрослых, испытывающих затруднения, связанные с проглатыванием таких дозированных форм. Кроме того, большое количество взрослых пациентов страдает от дисфагии и испытывает затруднения, связанные с проглатыванием таких дозированных форм. Кроме того, желательно, в частности, для целей экстренной контрацепции, чтобы вводимая дозированная форма обеспечивала быстрое и стабильное наступление действия, обладала высокой биодоступностью и была активна в течение длительного времени. Быстрое наступление действия можно обеспечить путем парентеральной инъекции, однако такой способ неприемлем для многих пациентов и может быть связан с риском при осуществлении вне медицинского учреждения. Хотя для указанной цели также могут подходить жидкие сиропы, с ними трудно обращаться и вводить в точной дозировке. Кроме того, многие активные средства нестабильны в жидкостях при хранении на протяжении длительного времени. Поэтому предпочтительной является дозированная форма, которая распадается во рту в отсутствие воды, поскольку она подходит для широкого круга пациентов и обеспечивает простоту введения.
Краткое описание изобретения
[0007] В настоящем изобретении предложена нешипучая фармацевтическая твердая дозированная форма, распадающаяся в полости рта, содержащая (а) прогестин в количестве, эквивалентном примерно от 0,5 мг до 2,0 мг левоноргестрела; (б) ионный дезинтегрант и (в) гидрофильный нерастворимый в воде неионный наполнитель; причем ионный дезинтегрант содержится в количестве выше чем от примерно 8% до примерно 60% от массы дозированной формы, а гидрофильный нерастворимый в воде неионный наполнитель содержится в количестве примерно от 1% до 20% от массы дозированной формы.
[0008] Согласно некоторым из вариантов реализации ионный дезинтегрант выбирают из группы, включающей кроскармеллозу натрия, натрия крахмала гликолят, полакрилин калия, кальцийкарбоксиметилцеллюлозу и комбинации указанных веществ. Согласно некоторым из вариантов реализации ионный дезинтегрант содержится в количестве примерно от 10% до 50% от массы дозированной формы.
[0009] Согласно некоторым из вариантов реализации гидрофильный нерастворимый в воде неионный наполнитель выбирают из группы, включающей микрокристаллическую целлюлозу, прежелатинизированный крахмал, соединения целлюлозы, кросповидон, крахмалы и комбинации указанных веществ. Согласно некоторым из вариантов реализации гидрофильный нерастворимый в воде неионный наполнитель содержится в количестве примерно от 2% до 15,0% от массы дозированной формы.
[0010] Согласно некоторым из вариантов реализации более 40% мас. прогестина переходит в раствор менее чем примерно за 7 минут при помещении дозированной формы в среду, содержащую поверхностно-активное вещество, в соответствии со способом II, описанным в Фармакопее США (USP) при 75 об/мин.
[0011] Согласно некоторым из вариантов реализации по меньшей мере 75% мас. прогестина переходит в раствор менее чем примерно за 15 минут при помещении дозированной формы в среду, содержащую поверхностно-активное вещество, в соответствии со способом II USP при 75 об/мин.
[0012] Согласно некоторым из вариантов реализации по меньшей мере 75% мас. от содержания прогестина, эквивалентного примерно 0,75 мг левоноргестрела, переходит в раствор менее чем примерно за 15 минут при помещении дозированной формы в среду, содержащую 5 миллионных долей (мд) Твин 80 в 900 мл воды, в соответствии со способом II USP при 75 об/мин.
[0013] Согласно некоторым из вариантов реализации по меньшей мере 75% мас. от содержания прогестина, эквивалентного примерно 1,5 мг левоноргестрела, переходит в раствор менее чем примерно за 15 минут при помещении дозированной формы в среду, содержащую 0,1% додецилсульфата натрия (ДСН) в 0,1 N HCl, в соответствии со способом USP II при 75 об/мин.
[0014] В настоящем изобретении также предложен способ лечения женщины, нуждающейся в экстренной контрацепции, включающий посткоитальное введение указанной женщине первой фармацевтической твердой дозированной формы, распадающейся в полости рта; и введение женщине в течение примерно 12 часов после введения первой дозированной формы второй фармацевтической твердой дозированной формы, распадающейся в полости рта, причем каждая из указанных первой и второй дозированных форм содержит (а) прогестин в количестве, эквивалентном примерно 0,75 мг левоноргестрела; (б) ионный дезинтегрант и (в) гидрофильный нерастворимый в воде неионный наполнитель; причем ионный дезинтегрант содержится в количестве выше чем от примерно 8% до 60% от массы дозированной формы, а гидрофильный нерастворимый в воде неионный наполнитель содержится в количестве примерно от 1% до 20% от массы дозированной формы.
[0015] В настоящем изобретении также предложен способ лечения женщины, нуждающейся в экстренной контрацепции, включающий посткоитальное введение указанной женщине твердой фармацевтической дозированной формы, распадающейся в полости рта, содержащей: (а) прогестин в количестве, эквивалентном примерно 1,5 мг левоноргестрела; (б) ионный дезинтегрант и (в) гидрофильный нерастворимый в воде неионный наполнитель; причем ионный дезинтегрант содержится в количестве выше чем примерно от 8% до примерно 60% от массы дозированной формы, а гидрофильный нерастворимый в воде неионный наполнитель содержится в количестве примерно от 1% до 20% от массы дозированной формы.
[0016] В настоящем изобретении также предложен терапевтический набор для лечения женщины, нуждающейся в экстренной контрацепции, содержащий: (а) одну или более нешипучих твердых фармацевтических дозированных форм, распадающихся в полости рта, согласно настоящему изобретению; (б) подходящий контейнер и (в) этикетку, содержащую указания по введению твердой фармацевтической дозированной формы нуждающейся в этом женщине.
[0017] В настоящем изобретении также предложен способ получения нешипучей твердой фармацевтической дозированной формы, распадающейся в полости рта, включающий смешивание ионного дезинтегранта и количества прогестина, эквивалентного примерно от 0,5 мг до 2 мг левоноргестрела, с получением исходной смеси; добавление к указанной исходной смеси гидрофильного нерастворимого в воде неионного наполнителя с получением конечной смесим и прессование конечной смеси с получением фармацевтической дозированной формы; причем указанный ионный дезинтегрант содержится в количестве выше чем от 8% до примерно 60% от массы дозированной формы, а указанный гидрофильный нерастворимый в воде неионный наполнитель содержится в количестве примерно от 1% до 20% от массы дозированной формы.
[0018] Согласно некоторым из вариантов реализации указанный способ обеспечивает переход в раствор по меньшей мере 75% мас. прогестина менее чем за 15 минут при помещении дозированной формы в среду, содержащую поверхностно-активное вещество, в соответствии со способом USP II при 75 об/мин. Согласно некоторым из вариантов реализации по меньшей мере 75% мас. от содержания прогестина, эквивалентного примерно 0,75 мг левоноргестрела, переходит в раствор менее чем за 15 минут при помещении дозированной формы в среду, содержащую 5 мд Твин 80 в 900 мл воды, в соответствии со способом USP II при 75 об/мин. Согласно некоторым из вариантов реализации по меньшей мере 75% мас. от содержания прогестина, эквивалентного примерно 1,5 мг левоноргестрела, переходит в раствор менее чем за 15 минут при помещении дозированной формы в среду, содержащую 0,1% ДСН в 0,1 N HCl, в соответствии со способом USP II при 75 об/мин. Согласно некоторым из вариантов реализации указанный способ обеспечивает переход в раствор более 40% мас. прогестина менее чем за 7 минут при помещении дозированной формы в среду, содержащую поверхностно-активное вещество, в соответствии со способом USP II при 75 об/мин. Согласно другим вариантам реализации указанный способ может включать добавление к исходной смеси неполимерного водорастворимого носителя. Согласно другим вариантам реализации указанный способ может включать добавление к конечной смеси ароматизатора, подсластителя или вещества, способствующего скольжению. Согласно некоторым из вариантов реализации указанный способ может включать добавление к конечной смеси смазывающего вещества.
Краткое описание чертежей
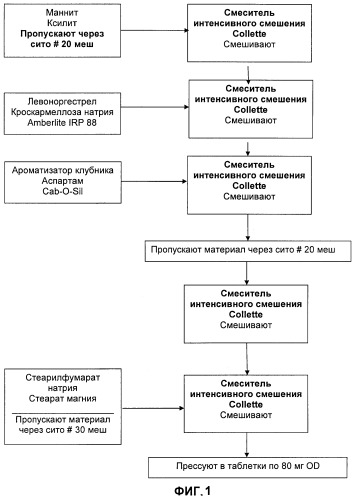
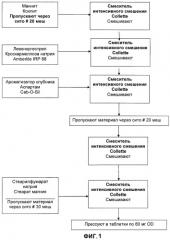
[0019] На ФИГ.1 представлена технологическая схема способа получения нешипучей твердой фармацевтической дозированной формы, распадающейся в полости рта, согласно настоящему изобретению.
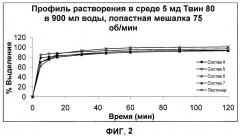
[0020] На ФИГ.2 представлены графики сравнения профилей растворения Состава 4 (закрашенные кружки), Состава 5 (пустые кружки), Состава 6 (пустые треугольники), Состава 7 (закрашенные треугольники) и POSTINOR®-2 (X). Профили растворения получены в среде, содержавшей 5 мд Твин 80 в 900 мл воды, при скорости вращения лопастной мешалки 75 об/мин.
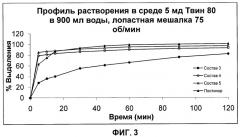
[0021] На ФИГ.3 представлены графики сравнения профиля растворения Состава 3 (сплошные кружки) и Состава 4 (закрашенные кружки), Состава 5 (пустые треугольники) и POSTINOR®-2 (закрашенные треугольники). Профили растворения получены в среде, содержавшей 5 мд Твин 80 в 900 мл воды, при скорости вращения лопастной мешалки 75 об/мин. На ФИГ.3 приведено сравнение воздействия на скорость растворения левоноргестрела неионного дезинтегранта, представляющего собой кросповидон, NF, с ионными дезинтегрантами - полакрилином калия и кроскармеллозой натрия.
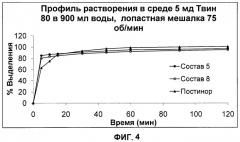
[0022] На ФИГ. 4 представлены графики сравнения профиля растворения Состава 5 (закрашенные кружки), Состава 8 (пустые кружки) и POSTINOR®-2 (закрашенные треугольники). Профили растворения получены в среде, содержавшей 5 мд Твин 80 в 900 мл воды, при скорости вращения лопастной мешалки 75 об/мин.
[0023] На ФИГ.5 представлены графики сравнения профиля растворения Состава 1 (закрашенные кружки), Состава 9 (пустые кружки), Состава 10 (пустые треугольники) и POSTINOR®-2 (закрашенные треугольники). Профили растворения получены в среде, содержащей 5 мд Твин 80 в 900 мл воды, при скорости вращения лопастной мешалки 75 об/мин.
[0024] На ФИГ.6 представлены графики сравнения профиля растворения Состава 8 (пустые кружки), Состава 11 (пустые треугольники) и POSTINOR®-2 (закрашенные треугольники). Профили растворения получены в среде, содержавшей 5 мд Твин 80 в 900 мл, воды при скорости вращения лопастной мешалки 75 об/мин.
[0025] На ФИГ.7 представлены графики сравнения профиля растворения Состава 6 (пустые кружки), Состава 12 (пустые треугольники) и POSTINOR®-2 (закрашенные треугольники). Профили растворения получены в среде, содержавшей 5 мд Твин 80 в 900 мл воды, при скорости вращения лопастной мешалки 75 об/мин.
[0026] На ФИГ.8 представлены графики сравнения профиля растворения Состава 5 (пустые кружки), Состава 8 (пустые треугольники), Состава 11 (закрашенные треугольники) и POSTINOR®-2 (звездочки). Профили растворения получены в среде, содержавшей 5 мд Твин 80 в 900 мл воды, при скорости вращения лопастной мешалки 75 об/мин.
[0027] На ФИГ.9 представлены графики сравнения профиля растворения Состава 7 (закрашенные кружки), Состава 14 (пустые кружки) и POSTINOR®-2 (закрашенные треугольники). Профили растворения получены в среде, содержавшей 5 мд Твин 80 в 900 мл воды, при скорости вращения лопастной мешалки 75 об/мин. На ФИГ.9 показано воздействие отсутствия одновалентных катионов на высвобождение лекарства.
[0028] На ФИГ.10 представлены графики сравнения профиля растворения Состава 16 (пустые кружки), Состава 17 (ромбы), Состава 18 (звездочки), образца сравнения (пустые треугольники) и образца сравнения (сплошные треугольники). Профили растворения получены в среде, содержавшей 0,1% ДСН в 0,1 N HCl, при скорости вращения лопастной мешалки 75 об/мин.
Подробное описание изобретения
[0029] В настоящем изобретении предложены нешипучие фармацевтические твердые дозированные формы, распадающиеся в полости рта, содержащие прогестин и комбинацию наполнителей, обеспечивающих быстрый распад твердых дозированных форм во рту без необходимости заливания водой, при этом обеспечивается легкость проглатывания указанных дозированных форм субъектом, который в этом нуждается. Фармацевтические дозированные формы согласно настоящему изобретению обеспечивают эффективную абсорбцию и высокую биодоступность прогестина и, в частности, подходят для лечения женщин, нуждающихся в экстренной контрацепции.
Нешипучие фармацевтические твердые дозированные формы, распадающиеся в полости рта
[0030] В настоящем изобретении предложена нешипучая твердая фармацевтическая дозированная форма, распадающаяся в полости рта, содержащая (а) прогестин в количестве, эквивалентном примерно от 0,5 мг до 2,0 мг левоноргестрела; (б) ионный дезинтегрант и (в) гидрофильный нерастворимый в воде неионный наполнитель; причем ионный дезинтегрант содержится в количестве выше чем от 8% до примерно 60% от массы дозированной формы, а гидрофильный нерастворимый в воде неионный наполнитель содержится в количестве примерно от 1% до 20% от массы дозированной формы.
[0031] Используемый в настоящем описании термин «распадающаяся в полости рта» дозированная форма относится к твердой дозированной форме, которая «быстро распадается, обычно за несколько секунд, при помещении на язык». Кроме того, термин «распадающийся в полости рта» может относиться к потере структурной целостности дозированной формы при ее помещении в ротовую полость субъекта с образованием мелкодисперсной вязкой или жидкой композиции, которую можно легко проглотить без воды. «Распадающийся» также относится к потере целостности дозированной формы согласно настоящему изобретению с образованием гранул, агрегатов или частиц, как описано в общем случае в работе Remington: The Science and Practice of Pharmacy, 21st Ed., Lippincott Williams & Wilkins, Baltimore, MD (2003), содержание которой полностью включено в настоящее описание посредством ссылки.
[0032] Согласно некоторым из вариантов реализации дозированные формы согласно настоящему изобретению распадаются в ротовой полости субъекта, представляющего собой человека, без приема воды примерно за 60 секунд или менее, примерно за 45 секунд или менее, примерно за 30 секунд или менее, примерно за 15 секунд или менее, примерно за 10 секунд или менее, или примерно за 5 секунд или менее. Согласно некоторым из вариантов реализации фармацевтические дозированные формы согласно настоящему изобретению распадаются в ротовой полости субъекта, представляющего собой человека, без приема воды в течение примерно от 5 секунд до 60 секунд, примерно от 5 секунд до 45 секунд, примерно от 5 секунд до 30 секунд, примерно от 5 секунд до 15 секунд, примерно от 5 секунд до 10 секунд, или примерно от 5 секунд до 8 секунд.
[0033] Используемый в настоящем описании термин «фармацевтическая твердая дозированная форма» относится к таблетке, облатке, пленке, порошку, драже или твердой или мягкой желатиновой капсуле. Согласно некоторым из вариантов реализации дозированные формы согласно настоящему изобретению представляют собой таблетки. Используемый в настоящем описании термин «таблетка» относится к прессованным фармацевтическим дозированным формам любых форм и размеров, с покрытием или без покрытия. Указанные дозированные формы представляют собой таблетки, распадающиеся в полости рта. Твердые дозированные формы согласно настоящему изобретению могут обладать по существу жесткой структурой, являющейся механически устойчивой и прочной. Единичная дозировка представляет собой вводимое в отдельности количество фармацевтической композиции.
[0034] Вес нетто фармацевтической дозированной формы согласно настоящему изобретению может составлять примерно от 20 мг до 1000 мг, примерно от 20 мг до 500 мг, примерно от 30 мг до 480 мг, примерно от 30 мг до 360 мг, примерно от 30 мг до 240 мг, примерно от 30 мг до 180 мг, примерно от 30 мг до 150 мг. Согласно некоторым из вариантов реализации фармацевтические дозированные формы согласно настоящему изобретению весят примерно 30 мг, примерно 60 мг, примерно 80 мг, примерно 100 мг, примерно 120 мг, примерно 180 мг, примерно 240 мг, примерно 360 мг или примерно 480 мг.
[0035] При изменении единичного дозированного количества прогестина вес фармацевтических дозированных форм может увеличиваться или уменьшаться пропорциональным образом (т.е. дозированные формы представляют собой дозированные формы с пропорциональным изменением веса (dose-proportional dosage forms)). Согласно некоторым из вариантов реализации вес фармацевтической дозированной формы является постоянным, тогда как единичное дозированное количество прогестина изменяется (т.е. дозированные формы представляют собой дозированные формы со сходным весом (dose-similar dosage forms)). Таблетки, относящиеся к дозированным формам со сходным весом, могут быть особенно подходящими, поскольку в этом случае более высокие дозы прогестина можно доставлять при помощи таблеток небольшого размера. Используемый в настоящем документе термин «дозированная форма в виде таблетки небольшого размера» относится к дозированной форме, которая весит примерно 100 мг или менее, примерно 80 мг или менее, примерно 40 мг или менее, или примерно 30 мг или менее.
[0036] Фармацевтические дозированные формы согласно настоящему изобретению могут содержать прогестин в количестве, эквивалентном содержанию левоноргестрела примерно от 0,05% до 10%, примерно от 0,05% до 7,5%, примерно от 0,05% до 3,0%, примерно от 0,05% до 2,0%, примерно 0,07% или примерно 1,7% от массы дозированных форм.
[0037] На всем протяжении настоящего описания все приводимые процентные содержания, соотношения, общие количества и др. являются «весовыми», если не указано иное. Используемый в настоящем описании термин «весовой» является синонимом термина «массовый» и указывает на то, что выраженное таким образом процентное содержание или соотношение рассчитано на основании веса, а не объема, вязкости или каких-либо других характеристик.
[0038] Используемый в настоящем описании термин «примерно» при использовании совместно с процентным содержанием или другими численными величинами означает плюс или минус 10% от указанного процентного содержания или другой численной величины. Например, термин «примерно 80%» включает 80% плюс или минус 8%.
[0039] Используемый в настоящем описании термин «прогестин» включает гидраты, сольваты, пролекарства и соли, включая, но не ограничиваясь ими, соли присоединения кислот, таких как, например, соляная, бромоводородная, лимонная, винная, фосфорная, фумаровая, яблочная или янтарная кислоты, натриевые и калиевые соли и сочетания указанных кислот. Соответственно, используемый в настоящем описании термин «левоноргестрел» включает каждую из таких форм.
[0040] Химическим наименованием левоноргестрела, представляющего собой синтетический прогестаген, является [18,19-динорпрегн-4-ен-20-ин-3-он-13-этил-17-гидрокси, (17α)-(-)-]. Левоноргестрел имеет следующую химическую структуру:
[0041] Согласно некоторым из вариантов реализации левоноргестрел, применяемый в дозированных формах согласно настоящему изобретению, может быть микронизированным. Используемый в настоящем документе термин «микронизированный» означает, что частицы композиции измельчены до частиц, диаметр которых составляет лишь несколько микрон или менее. Например, микронизированный левоноргестрел означает, что частицы левоноргестрела измельчены настолько, что их диаметр составляет лишь несколько микрон или менее.
[0042] Согласно некоторым из вариантов реализации пероральные дозированные формы согласно настоящему изобретению содержат дозу прогестина, эквивалентную примерно от 0,5 мг до 2 мг левоноргестрела. Согласно некоторым из вариантов реализации пероральные дозированные формы согласно настоящему изобретению содержат дозу прогестина, эквивалентную примерно от 0,5 мг до 1,5 мг, примерно 0,5 мг, примерно 0,75 мг или примерно 1,5 мг левоноргестрела.
[0043] Указанные выше диапазоны дозировок приведены для левоноргестрела, при этом в случае применения другого прогестина можно осуществить корректировку используемого количества на основании относительной эффективности или активности соединения. Известны соотношения активностей различных прогестинов; см., например, ЕР 0253607, содержание которого включено в настоящее описание во всей полноте посредством ссылки. Например, согласно контрацептивной схеме 0,050 мг левоноргестрела примерно эквивалентны примерно 0,175 мг норэтиндрона ацетата, примерно 0,050 мг дезогестрела, примерно 0,050 мг 3-кетодезогестрела, примерно 0,035 мг гестодена, или примерно 0,100 мг норгестрела. Следует понимать, что если норгестрел используют вместо левоноргестрела, его концентрация в два раза выше концентрации левоноргестрела. Норгестрел (dl-норгестрел) представляет собой рацемическую смесь оптически активных изомеров, тогда как левоноргестрел представляет собой один из оптически активных изомеров, присутствующих в норгестреле.
[0044] Эквивалентные концентрации прогестинов можно определить при помощи способов исследований in vitro или in vivo. См., например, Kuhl, H., Drugs 51(2):188-215 (1996); Philibert, D., et al., Gynecol. Endocrinol. 13:316-326 (1999); и Lundeen, S., et a., J. Steroid Biochem. Molec. Biol. 78:137-143 (2001), в которых сравнивают относительные мощности различных прогестинов с использованием исследований как in vitro, так и in vivo. См. также, например, Dickey, R.Р., "Contraceptive Therapy," OBG Management Supplement (October 2000), стр.2-6. Каждый из указанных документов включен в настоящее описание посредством ссылок во всей своей полноте.
[0045] Например, эквиваленты прогестинов приведены в Таблице 1.
| Таблица 1 | ||
| Таблица эквивалентов прогестинов | ||
| Прогестин | Доза (мг) | Эквивалентная* доза норетиндрона (мг) |
| Норетинодрел | 9,85 | 9,85 |
| 5,00 | 5,00 | |
| 2,50 | 2,50 | |
| 2,50 | 2,50 | |
| Норетиндрон | 10,00 | 10,00 |
| 2,00 | 2,00 | |
| 1,00 | 1,00 | |
| 1,00 | 1,00 | |
| Норетиндрона | 1,00 | 1,00 |
| ацетат | 1,00 | 1,00 |
| 0,50 | 0,50 | |
| 0,40 | 0,40 | |
| Норетиндрона | 2,50 | 2,50 |
| ацетат | 1,00 | 1,00 |
| 0,60 | 0,60 | |
| 1,50 | 1,50 | |
| 1,00 | 1,00 | |
| Этинодиола диацетат | 1,00 | 1,00 |
| Этинодиола диацетат | 1,00 | 1,00 |
| 1,00 | 1,00 | |
| dl-Норгестрел | 0,50 | 0,75 |
| 0,30 | 0,45 | |
| Левоноргестрел | 0,10 | 0,35 |
| 0,15 | 0,52 | |
| * Эквивалентности: 0,10 мг dl-Норгестрела=приблизительно 0,15 мг Норетиндрона |
[0046] Подходящие прогестины для использования в настоящем изобретении включают, но не ограничены этим, природные и синтетические соединения, обладающие прогестационной активностью, такие как, например, прогестерон, хлормадинона ацетат, норетиндрон, ципротерона ацетат, норетиндрона ацетат, дезогестрел, левоноргестрел, дрозпиренон, тримегестон, норгестрел, норгестимат, норелгестромин, этоногестрел, гестоден, и другие природные и/или синтетические гестагены. Пролекарства подходящих прогестинов также можно использовать в схемах согласно настоящему изобретению.
[0047] Выражение «пролекарство» обозначает производное известного непосредственно действующего лекарства, причем указанное производное обладает улучшенными характеристиками доставки и терапевтическим индексом по сравнению с лекарством и превращается в активное лекарство при помощи ферментного или химического способа. Этинодиола диацетат, который превращается in vivo в норетиндрон, представляет собой пример прогестинового Пролекарства, которое можно использовать в настоящем изобретении. Дополнительные примеры прогестиновых пролекарств включают, но не ограничены этим, норгестимат (который превращается in vivo в 17-дезацетилноргестимат, также известный как норелгестромин), дезогестрел (который превращается in vivo в 3-кетодезогестрел, также известный как этоногестрел) и норетиндрона ацетат (который превращается in vivo в норетиндрон).
[0048] Фармацевтические дозированные формы согласно настоящему изобретению не требуют шипучести для распада в воде, но вместо этого полагаются на ионные дизинтегранты для облегчения их распада в ротовой полости.
[0049] Согласно некоторым из вариантов реализации ионные дизинтегранты являются гидрофильными и не растворимыми в воде. Гидрофильные, не растворимые в воде ионные дизинтегранты, подходящие для использования согласно настоящему изобретению, включают, но не ограничены этим, сшитые полимеры карбоксиметилцеллюлозы натрия (например, кроскармеллоза натрия, имеющаяся в продаже под названиями Solutab®, Blanver Farmoquimica, Ltda., Cotia, Brazil; Ac-Di-Sol®, FMC Corp., Philadelphia, PA; и Vivasol®, J.Rettenmaier & Sohne GmbH+Co. KG Ltd., Rosenberg, Germany); сшитые производные крахмала (например, натрия крахмала гликолат, имеющийся в продаже под названиями Primojel®, Campina Nederland Holding B.V., Zaltbommel, Netherland Antilles; и Explotab®, Edward Mendell Co., Inc., Carmel, NY); сополимеры метакриловой кислоты и дивинилбензола (например, смола полакрилекс, имеющаяся в продаже под названием Amberlite® IRP64, и полакрилин калия, имеющийся в продаже под названием Amberlite® IRP88, Rohm and Haas, Philadelphia, PA); сульфонированные сополимеры стирола и дивинилбензола (например, натрия полистирол сульфонат, имеющийся в продаже под названием Amberlite®IRP69, и холестираминовая смола, имеющаяся в продаже под названием DUOLITE® AP143, Rohm and Haas, Philadelphia, PA); и их сочетания.
[0050] Было обнаружено, что благодаря использованию гидрофильного не растворимого в воде ионного дизинтегранта (например, кроскармеллозы натрия, натрия крахмала гликолата, полакрилина калия) в дозированной форме согласно настоящему изобретению прогестин обладает более быстрым и более полным высвобождением лекарства, чем при использовании неионного дизинтегранта (например, кросповидона), который приводит к более медленному и неполному высвобождению лекарства.
[0051] Согласно некоторым из вариантов реализации ионный дизинтегрант находится в фармацевтических дозированных формах согласно настоящему изобретению в концентрации выше 8% и до примерно 60%, примерно от 9% до 60%, примерно от 9% до 50%, примерно от 9% до 40%, примерно от 9% до 35%, примерно от 9% до 30%, примерно от 9% до 25%, примерно от 15% до 50%, примерно от 15% до 40%, примерно от 15% до 35%, примерно от 15% до 30%, примерно от 20% до 50%, примерно от 20% до 45%, примерно от 20% до 40%, примерно от 20% до 35%, примерно от 20% до 30%, примерно 10%, примерно 15%, примерно 19%, примерно 20%, примерно 25%, примерно 27%, или примерно 30% от массы дозированных форм.
[0052] Фармацевтические дозированные формы согласно настоящему изобретению, кроме того, содержат гидрофильный не растворимый в воде неионный наполнитель. Согласно некоторым из вариантов реализации гидрофильный не растворимый в воде неионный наполнитель включает разбавитель и/или связующее вещество. Согласно некоторым из вариантов реализации гидрофильный не растворимый в воде разбавитель и/или связующее может способствовать, по меньшей мере, одному из способов прессования и/или распада дозированных форм согласно настоящему изобретению. Не ограничиваясь никакой конкретной теорией, многие наполнители подвергаются уплотнению при прессовании, что может часто уменьшить свободный объем, который обычно связан со смесью, приводя в результате к спрессованному составу, обладающему высокой плотностью и низким свободным объемом. Снижение свободного объема и/или пористости спрессованной дозированной формы обычно снижает скорость распада, например, в ротовой полости. Таким образом, выбор разбавителя и/или связующего, сохраняющего высокую пористость и/или свободный объем при прессовании, может помочь добиться того, чтобы дозированные формы согласно настоящему изобретению были эффективно проницаемы для воды и быстро распадались при введении. Свободный объем и/или пористость могут быть связаны с плотностью наполнителя, и разбавители и/или связующие, подходящие для использования согласно настоящему изобретению, можно, таким образом, выбирать, основываясь на их плотности. Согласно некоторым из вариантов реализации разбавители и связующие, подходящие для использования согласно настоящему изобретению, имеют плотность примерно 0,7 г/см3 или менее, примерно 0,6 г/см3 или менее, или примерно 0,5 г/см3 или менее.
[0053] Разбавители и связующие, подходящие для использования согласно настоящему изобретению, также включают наполнители, обладающие волокнистой и/или пористой структурой. В частности, разбавители и связующие, являющиеся как волокнистыми, так и пористыми, можно использовать согласно настоящему изобретению для добавления к структурной целостности твердых дозированных форм, таким образом, придавая дозированным формам пористую структуру.
[0054] Согласно некоторым из вариантов реализации гидрофильные не растворимые в воде неионные разбавители и связующие, подходящие для использования согласно настоящему изобретению, могут быть гигроскопичными. Это может помочь добиться того, чтобы вода впитывалась внутрь дозированных форм для способствования распаду. Разбавители и связующие, подходящие для использования согласно настоящему изобретению, включают, но не ограничены этим, нерастворимые в воде целлюлозы и их производные (например, микрокристаллическая целлюлоза и порошкообразная целлюлоза), диспергируемые в воде целлюлозы и их производные (например, метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза и метилгидроксиэтилцеллюлоза), диспергируемые в воде полимеры (например, гомополимеры N-винилпирролидона и полиэтиленгликоль), крахмал, лактозу, сахарозу, глюкозу, декстрозу, диоксид кремния, неорганические наполнители и их сочетания.
[0055] Согласно некоторым из вариантов реализации фармацевтические дозированные формы согласно настоящему изобретению включают гидрофильный не растворимый в воде неионный разбавитель и/или связующее в концентрации примерно от 1% до 20%, примерно от 1% до 15%, примерно от 1% до 10%, примерно от 1% до 7%, примерно от 3% до 20%, примерно от 3% до 15%, примерно от 3% до 10%, примерно от 3% до 8%, примерно от 3% до 7%, примерно от 5,% до 20%, примерно от 5% до 15%, примерно от 5% до 10%, примерно 3%, примерно 4%, примерно 5%, примерно 6% или примерно 10% от массы дозированных форм.
[0056] Согласно некоторым из вариантов реализации гидрофильный не растворимый в воде неионный разбавитель или связующее, используемый согласно настоящему изобретению, представляет собой микрокристаллическую целлюлозу. Микрокристаллическая целлюлоза представляет собой гидрофильный, не растворимый в воде наполнитель, обладающий впитывающей способностью, способствуя, таким образом, проникновению воды в дозированные формы при контакте, и он имеется в продаже нескольких сортов, с размерами частиц в диапазоне примерно от 20 µм до примерно 200 µм (например, Emcocel®, Penwest Pharmaceuticals Co., Pafterson, NJ; и Avicel®, FMC Corp., Philadelphia, PA). Микрокристаллическая целлюлоза, подходящая для использования согласно настоящему изобретению, может иметь насыпную плотность примерно от 0,28 г/см3 до 0,34 г/см3 и плотность утряски примерно от 0,35 г/см3 до 0,48 г/см3. Согласно некоторым из вариантов реализации фармацевтические дозированные формы согласно настоящему изобретению включают микрокристаллическую целлюлозу в концентрации примерно от 1% до 20%, примерно от 1% до 15%, примерно от 1% до 10%, примерно от 1% до 7%, примерно от 3% до 20%, примерно от 3% до 15%, примерно от 3% до 10%, примерно от 3% до 8%, примерно от 3% до 7%, примерно от 5% до 20%, примерно от 5% до 15%, примерно от 5% до 10%, примерно 3%, примерно 4%, примерно 5%, примерно 6% или примерно 10% от массы дозированных форм.
[0057] Было обнаружено, что большие количества микрокристаллической целлюлозы в дозированных формах согласно настоящему изобретению, по-видимому, снижают скорость и степень высвобождения прогестина из дозированных форм в раствор.
[0058] Дозированные формы согласно настоящему изобретению также могут содержать один или более фармацевтически приемлемых наполнителей. Используемый в настоящем описании термин «фармацевтически приемлемый» относится к таким наполнителям, соединениям, материалам и/или композициям, которые являются, в рамках обоснованного медицинского суждения, подходящими для контакта с тканями людей и животных без избыточной токсичности, раздражения, аллергической реакции, или других возможных осложнений, соизмеримых с разумным соотношением риск/польза. Согласно некоторым из вариантов реализации термин «наполнитель» относится к веществам, применяемым для сочетания с левоноргестрелом для получения твердой дозированной формы, подходящей для введения нуждающемуся в этом субъекту. Кроме того, специалистам понятно, что в настоящем изобретении можно использовать фармацевтически приемлемые наполнители, включая те, которые перечислены в The Handbook of Pharmaceutical Excipients, 5th Ed., The Pharmaceutical Press and American Pharmacists Association, London, UK and Washington, DC (2006) и Remington: The Science and Practice of Pharmacy, Lippincott Williams & Wilkins, 21st Ed. (2005), включенных в настоящий документ посредством ссылок во всей своей полноте.
[0059] Применимые фармацевтически приемлемые наполнители включают такие, которые придают сухой композиции, которую затем спрессовывают, хорошие реологические и компрессионные характеристики. Фармацевтически приемлемые наполнители и добавки, подходящие для и