Фосфониевые соли на основе производных пиридоксина
Иллюстрации
Показать всеНастоящее изобретение относится к фосфониевым солям производных пиридоксина общей формулы (I), которое может быть использовано в медицине и ветеринарии
где при R1=СН3; R2=СН3; Х=Н; n=1; R1=CH3; R2=H; Х-Н; n=1;
R1=СН3; R2=СН3; Х=CН2Р+Ph3; n=2; R1=CH3; R2=H; X=CH2P+Ph3; n=2; R1=СН3; R2=С(СН3)2; X=CH2P+Ph3; n=2.
Предложены новые соединения с антибактериальной активностью по отношению к Staphylococcus aureus, включая мультирезистентные штаммы, а также низкой токсичностью. 1 пр., 1 табл.
Реферат
Изобретение относится к новым производным пиридоксина формулы
где при R1=СН3; R2=СН3; Х=Н; n=1
R1=СН3; R2=H; X=H; n=1
R1=СН3; R2=СН3; Х=CH2P+Ph3; n=2
R1=CH3; R2=Н; Х=CH2P+Ph3; n=2
R1=СН3; R2=С(СН3)2; Х=CH2P+Ph3; n=2
Соединения формулы (I) обладают высокой антибактериальной активностью по отношению к Staphylococcus aureus и могут найти применение в медицине и ветеринарии.
Функционализация природных биологически активных соединений является одним из важнейших подходов к созданию новых лекарственных средств. Ярким представителем таких соединений является витамин В6 - один из ключевых витаминов, вовлеченный в метаболизм с более чем 100 ферментами и участвующий в процессах биосинтеза аминокислот, метаболизме углеводов, жирных кислот и липидов. Среди более тысячи синтезированных производных пиридоксина обнаружены вещества, проявляющие кардиопротекторную, антихолинэстеразную, ноотропную, радиопротекторную, антидепрессантную и другие виды активности.
Широкое применение в медицине нашел пиридитол (бис-(2-метил-3-гидрокси-4-гидроксиксиметил-5-метил-пиридил)дисульфид), использующийся в качестве эффективного ноотропного препарата [Pat. GB 927666, IPC C07D. Process for the manufacture of a sulphur-containing derivative of vitamin B6 / Mewburn Ellis & Co. - Опубл. - 29.05.1961].
Общеприняты способы внутриклеточной доставки активных веществ, основанные на преодолении защитных барьеров организма, к числу которых относятся, в частности, кожные покровы, оболочки органов и клеточные мембраны. Многие активные вещества плохо преодолевают эти барьеры вследствие высокой гидрофильности, которая ограничивает их транспорт через липидные барьеры (например, межклеточный жировой слой кожи и липидные мембраны клеток). Накоплению активных веществ в устойчивых к ним клетках, таких как опухолевые клетки и патогенные микроорганизмы, также препятствует высокая активность в этих клетках мембранных транспортных белков, которые осуществляют выброс веществ из цитоплазмы. Особую угрозу для больных представляют мультирезистентные (MDR) штаммы, устойчивые одновременно к нескольким лекарственным препаратам.
Для достижения нужной терапевтической концентрации активного вещества в клетке или органе-мишени традиционным подходом является увеличение используемой дозы вещества в организме. В результате увеличиваются побочные эффекты активного вещества, которые часто превосходят по последствиям положительный терапевтический эффект от его применения.
В связи с этим перспективным подходом к увеличению проницаемости биологических барьеров для активных веществ является создание эффективных и безопасных систем их внутриклеточного транспорта. Создание подобных транспортных систем позволит значительно уменьшить терапевтическую дозу активных веществ и, как следствие, их побочные эффекты и тем самым совершить качественный прорыв в фармакологии и медицине.
Известно, что 4-дезоксипиридоксин и его сложные эфиры обладают антибактериальным действием против Eimeria acervulina [Morisawa Y., Kataoka M., Watanabe Т., Kitano N., Matsuzawa T. Studies on anticoccidial agents. 2. Synthesis and anticoccidial activity of pyridoxol analogs // J. Med. Chem. - 1974. V.17, N.11. - P.1235-1237]. Несмотря на низкую токсичность, антибактериальная активность вышеуказанных соединений оказалась невысокой.
Ряд соединений обладающих антибактериальной активностью известен и среди четвертичных фосфониевых солей. В частности, японскими авторами сообщается о замещенных фосфониевых солях с длинноцепочечными алкильными радикалами, обладающими высокой антибактериальной активностью против Staphylococcus aureus [Kanazava A., Ikeda Т., Endo T. Synthesis and antimicrobial activity of dimethyl - and trimethil-substituted phosphonium salts with alkyl chains of various lengths // Antimicrobal agents and chemotherapy - 1994. - V.38. - №5. - P.945-952].
Румынские ученые получили четвертичные фосфониевые соли на полимерном носителе, которые обладали высокой антибактериальной активностью против Staphylococcus aureus, Escherichia coli и Pseudomonas aeruginosa [Popa A., Davidescu C., Trif R., Ilia G. Study of quaternary onium salts grafted on polymers: antibacterial activity of quaternary phosphonium salts grafted on gel-type styrene-divinylbenzene copolymers. Reactive & functional polymers - 2003. - V.55. - P.151-158].
Ряд дифосфониевых солей на основе производных ксилола с высокими антибактериальными свойствами были получены и запатентованы японскими авторами [Pat. JP 2005060332. Phosphonium salt compound effective as antibacterial agents / Shibata Sh. - Опубл. - 03.10.2005].
Известные из уровня техники фосфониевые соединения обладают высокой антибактериальной активностью, однако достаточно токсичны, что может приводить к побочным эффектам, значительно снижающим положительный результат от воздействия этих лекарственных средств.
Одной из важнейших проблем, стоящих перед здравоохранением, является высокая резистентность бактерий к известным лекарственным препаратам, поэтому поиск новых антибактериальных агентов является актуальным.
Следует отметить, что описанные выше соединения по мнению заявителя не могут рассматриваться в качестве аналогов к заявленному техническому решению вследствие того, что они не совпадают с заявляемыми соединениями по химической структуре.
Задачей предлагаемого изобретения является создание принципиально новых малотоксичных соединений, обладающих высокой антибактериальной активностью по отношению к Staphylococcus aureus, в т.ч. к его мультирезистентным штаммам, расширяющие арсенал известных препаратов указанного назначения.
Техническим результатом заявленного изобретения является получение новых соединений общей формулы (I), содержащих в своем составе как трифенилфосфониевые, так и пиридоксиновые или 6-гидроксиметилпиридоксиновые фрагменты.
В заявленном техническом решении предлагаются фосфониевые соли на основе производных пиридоксина общей формулы (I),
где при R1=СН3; R2=СН3; Х=Н; n=1
R1=CH3; R2=H; X=H; n=1
R1=СН3; R2=СН3; Х=CH2P+Ph3; n=2
R1=СН3; R2=Н; Х=CH2P+Ph3; n=2
R1=СН3; R2=С(СН3)2; Х=CH2P+Ph3; n=2
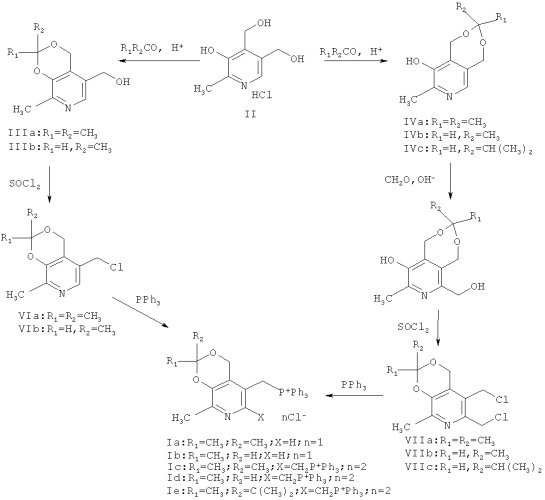
Предлагаемые в данном изобретении соединения формулы (I) получали согласно нижеприведенной схеме:
Характеристики новых соединений приведены в примерах конкретного выполнения. Структуры полученных соединений подтверждены методами масс-спектрометрии, 1Н, 13С и 31Р-ЯМР спектроскопии, элементного анализа. Спектры ЯМР регистрировали на приборе Bruker AVANCE-400. Химический сдвиг определялся относительно сигналов остаточных протонов дейтерорастворителя (1Н и 13С) или внешнего стандарта - H3PO4 (31Р). Данные элементного анализа получены на приборе Perkin Elmer 2400 Series II. Контроль за ходом реакций и чистотой соединений проводили методом ТСХ на пластинах Silufol UV-254 и Sorbfil Plates.
Масс-спектры MALDI регистрировались на приборе Ultraflex III компании Bruker, оборудованном твердотельным лазером и время - пролетным анализатором масс. Ускоряющее напряжение 25 кВ. Образцы наносили на мишень Anchor Chip. Запись спектров производили в режиме положительных ионов. Результирующий спектр представлял собой сумму 300 спектров, полученных в разных точках образца. В качестве матриц применяли 2,5-дигидроксибензойную кислоту (DHB) (Acros, 99%) и n-нитроанилин (PNA). Для приготовления матриц использовали хлороформ. Нанесение образцов на мишень проводили методом «высушенных капель».
Примеры конкретного выполнения заявленного технического решения Синтез циклических ацеталей и кеталей из пиридоксина и карбонильных соединений
5-Гидроксиметил-2,2,8-триметил-4H-[1,3]диоксино[4,5-с]пиридин (IIIa)
Через суспензию 20 г (97.3 ммоль) пиридоксингидрохлорида в 300 мл ацетона, при охлаждении до 3-5°С и перемешивании пропускают 50 г (603 ммоль) хлористого водорода. Полученную реакционную смесь перемешивают в течение 20 ч. Осадок отфильтровывают, промывают эфиром и нейтрализуют водным раствором поташа. Продукт отфильтровывают и перекристаллизовывают из этилового спирта. Выход 56%, бесцветные кристаллы. Т.пл. 108-109°С (лит. 113-115°С [Cohen A., Huges E.G. Synthetical Experiments in the В Group of Vitamins. Part V. Novel Derivatives of Pyridoxine. // J. Chem. Soc. - 1952. - P.4384-4386]).
5-Гидроксиметил-2,8-диметил-4H-[1,3]диоксино[4,5-c]пиридин (IIIb)
Синтезируют и разрабатывают аналогично соединению (IIIa) из 12 г (0,059 моль) пиридоксингидрохлорида в 150 мл ацетальдегида и 39 г (1.07 моль) хлороводорода. Выход 5.65 г (50%), бесцветные кристаллы. Т.пл. 125°С. Спектр ЯМР 1Н (400 МГц, CDCl3): δ, м.д.: 1.54 д (3Н, 3JHH=5.2 Гц, СН3), 2.32 с (3Н, СН3), 4.45 с (2Н, СН2), 4,90 уш (1Н, ОН), 4.91, 4.94 (АВ, 2JHH=-16 Гц, CH2), 5.11 к (1Н, 3JHH=5.2 Гц, СН), 7.70 с (1Н, СН). ЯМР 13С {Н} (100 МГц, COCl3) δ, м.д.: 17.93, 20.51 (СН3); 59.65, 63.99 (СН3); 97.05 (СН(СН3)); 127.45, 130.12, 138.85, 146.86, 147.72 (CAr). [Арустамова И.С. Некоторые превращения 5-оксиметил-8-метил-1,3-диоксинопиридинов. / И.С.Арустамова, В.Г.Кульневич // Журн. орг.химии. - 1985. - Т.21, Вып.11. - С.2433-2438].
3,3,8-Триметил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-ол (IVa)
Синтезируют и разрабатывают аналогично соединению (IIIa) из 20 г (97.3 ммоль) пиридоксингидрохлорида в 300 мл ацетона и 22 г (603 ммоль) хлороводорода. Выход 19.1 г (94%), бесцветные кристаллы. Т.пл. 184.5-186°С (184-185°С [Korytnyk W. A seven-membered cyclic ketal of pyridoxol // J. Org. Chem. - 1962. - V.27, N.10. - P.3724-3726]).
3,8-Диметил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-ол (IVb)
Синтезируют и разрабатывают аналогично соединению (IIIa) из 20 г (0.096 моль) пиридоксингидрохлорида, 300 мл ацетальдегида и 22 г (603 ммоль) хлороводорода. Выход 65%, бесцветные кристаллы. Т.пл. 186-186.5°С (лит. 186-186.5°С [Fedorenko V.Yu., Lodochnikova O.A., Petukhov A.S., Kataeva O.N., Litvinov I.A., Shtyrlin Yu.G., Klimovitskii, E.N. Crystal structure of seven-membered acetals withfuran and pyridine planar fragments // J. Mol. Struct. - 2003. - V.644, N 1-3 - P.89-96].
3-Изопропил-8-метил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-ол (IVc)
К раствору хлористого водорода (полученного из 10.5 г (0.095 моль) хлористого кальция и избытка конц. серной кислоты в 50 мл абсолютного диметилсульфоксида добавляют 5 г (0.024 моль) пиридоксингидрохлорида и 3.5 г (0.048 моль) изомасляного альдегида. Реакционную массу нагревают 2 часа при 50-60°С. Затем выливают в 30 мл водного раствора 14.5 г (0,136 моль) карбоната натрия при перемешивании и нейтрализуют разбавленным раствором хлористого водорода до рН 7. Выпавший осадок отфильтровывают, маточный раствор высушивают в вакууме и получившуюся маслообразную смесь промывают водой. Не растворившуюся в воде массу объединяют с осадком, полученным после нейтрализации реакционной массы, и перекристаллизовывают из этилового спирта. Выход 62%, бесцветные кристаллы. Т.пл. 163.5-164°С (лит. 164-164.5°С [Pat. FR1384099, C07D 491/04. Precede pour la preparation de derives de pyridine / Hoffmann La Roche. - Опубл. - 04.01.1965]).
Гидроксиметилирование семичленных ацеталей и кеталей пиридоксина
6-Гидроксиметил-3,3,8-триметил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-ол (Va)
Смесь 7 г (33.5 ммоль) соединения (IVa), 1.6 г (40 ммоль) NaOH и 3.9 г (48 ммоль) 37%-ного водного раствора формальдегида в 50 мл воды нагревают 60 ч при температуре 70°С. После охлаждения реакционную смесь нейтрализуют конц. НСl, выпавшую смолу отделяют, а фильтрат отгоняют в вакууме. Сухой остаток экстрагируют ацетоном, нерастворившуюся часть отфильтровывают, а растворитель отгоняют в вакууме. Остаток промывают ацетоном. Выход 6.4 г (80%), бесцветные кристаллы, Т.пл. 161-163°С (лит 161-163°С [Штырлин Н.В. Стрельник А.Д., Сысоева Л.П., Лодочникова О.А., Климовицкий Е.Н., Штырлин Ю.Г. Новый метод синтеза 6-метил-2,3,4-трис(гидроксиметил)пиридин-5-ола // Журн. орг.химии. - 2009. - Т.45, Вып.8. - С.1266-1268]).
6-Гидроксиметил-3,8-диметил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-ол (Vb)
Синтезируют и разрабатывают аналогично соединению (Va) из 7 г (31.1 ммоль) соединения (IVb), 2 г (49.8 ммоль) NaOH и 3.77 г (46.5 ммоль) 37%-ного водного раствора формальдегида. Выход 60%, бесцветные кристаллы, Т.пл. 167-168°С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6): δ, м.д.: 1.28 д (3Н, 3JHH=5.2 Гц, СН3), 2.33 с (3Н, СН3), 4.42, 4.44 (АВ, 2JHH=-12.2 Гц, СН3), 4.67, 5.00 (АВ, 2JHH=-15.8 Гц, CH2), 4.72, 5.04 (АВ, 2JHH=-15.4 Гц, СН2),5.12 к (1Н, 3JHH=5.2 Гц, СН), 8.47 с (1Н,ОН). Найдено, %: С 57.93; Н 6.75; N 6.11. C11H15NO4. Вычислено, %: С 58.66; Н 6.71; N 6.22.
6-Гидроксиметил-3-изопропил-8-метил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-ол (Vc)
Синтезируют и разрабатывают аналогично соединению (Va) из 7 г (26.2 ммоль) соединения (IVc), 1.26 г (31.5 ммоль) NaOH и 3.49 г (43.0 ммоль) 37%-ного водного раствора формальдегида. Выход 37%, белые кристаллы, т.пл. 138°С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6): δ, м.д.: 0.91 д (6Н, 3JHH=6.8 Гц, 2СН3), 1.90 м (1Н, СН), 2.34 с (3Н, СН3), 4.44, 4.45 (АВ, 3JHH=-12.4 Гц, CH2), 4.53 д (3Н, 3JHH-6.8 Гц, СН3), 4.68, 5.05 (АВ, 2JHH=-15.2 Гц, СН2), 4.74, 5.02 (АВ, 2JHH=-14.8 Гц, СН2), Найдено, %: С 61.64; Н 7.56; N 5.53. C14H21NO4. Вычислено, %: С 62.60; Н 8.19; N 5.77.
Получение хлорпроизводных на основе шестичленных кеталей и ацеталей пиридоксина
5-Хлорметил-2,2,8-диметил-4H-[1,3]диоксино[4,5-с]пиридин (VIa)
К раствору 2 г (9,6 ммоль) соединения (IIIa) в 15 мл хлороформа добавляют 7 мл (96 ммоль) хлористого тионила и перемешивают в течение 7 часов. Затем растворитель удаляют в вакууме. Твердый остаток промывают диэтиловым эфиром. Выход продукта в виде гидрохлорида 2,27 г (90%), белое кристаллическое вещество, т.пл. 190-191°С (лит. 191-192°С [Tomita I., Brooks H.G., Metzler D.E. Synthesis of vitamin В6 derivatives. II. 3-Hydroxy-4-hydroxymethyl-2-methyl-5-pyridine acetic acid and related substances // J. Heterocycl. Chem. - 1966 - V.3., N.2. - P.178-183]).
Далее полученный гидрохлорид нейтрализуют водно-спиртовым раствором поташа. Растворитель отгоняют в вакууме. Сухой остаток растворяют в хлороформе, осадок отфильтровывают и очищают с помощью колоночной хроматографии (элюент - хлороформ). Выход 1.48 г (68%). Полученное соединение используют in situ в синтезе фосфониевой соли (Ia).
5-Хлорметил-2,8-диметил-4H-[1,3]диоксино[4,5-с]пиридин (VIb)
К раствору 1.5 г (7,7 ммоль) соединения (IIIb) в 15 мл хлороформа добавляют 5.6 мл (77 ммоль) хлористого тионила и перемешивают в течение 7 часов. Затем растворитель удаляют в вакууме. Твердый остаток промывают диэтиловым эфиром. Выход продукта в виде гидрохлорида 1.76 г (91%), белое кристаллическое вещество. Т.пл. 186-190°С (разл.). Спектр ЯМР 1Н (400 МГц, CDCl3) δ, м.д.: 1.24 с (1Н, N+-H), 1.67 с (3Н, СН3), 2.80 с (3Н, СН3), 4.58 с (2Н, CH2), 5.16 с (2Н, CH2), 5.35 с (1Н, СН(СН3)), 8.27 с (1Н, СН). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 14.06, 20.18 (СН3); 38.41, 63.69 (СН2); 99.08 (СН(СН3)); 130.74, 131.42, 135.89, 144.10, 150.39 (CAr). Найдено, %: С 48.02; Н 5.24; N 5.60. C10H13Cl2NO2 Вычислено, %: С 47.99; Н 5.18; N 5.60.
Далее полученный гидрохлорид нейтрализуют водно-спиртовым раствором поташа. Растворитель отгоняют в вакууме. Сухой остаток растворяют в хлороформе, осадок отфильтровывают и очищают с помощью колоночной хроматографии (элюент - хлороформ). Выход 1.50 г (91%). Полученное соединение используют in situ в синтезе фосфониевой соли (Ib).
5,6-Бис(хлорметил)-2,2,8-триметил-4H-[1,3]диоксино[4,5-с]пиридин (VIIa)
Растворяют 0.5 г (2,09 ммоль) соединения (Va) в 10 мл хлористого тионила (137,5 ммоль) и перемешивают в течение 7 часов. Затем растворитель удаляют в вакууме, а твердый остаток нейтрализуют водно-спиртовым раствором поташа. Растворитель отгоняют в вакууме. Далее сухой остаток растворяют в хлороформе, осадок отфильтровывают и очищают с помощью колоночной хроматографии (элюент - хлороформ). Выход 0.37 г (65%), белое кристаллическое вещество, Т.пл. 162-164°С. Спектр ЯМР 1Н (300 МГц, COCl3) δ, м.д.: 1.55 с (6Н, 2СН3), 2.40 с (3Н, СН3), 4.58 с (2Н, CH2), 4.72 с (2Н, СН2), 4.94 с (2Н, СН2). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 18.47, 24.61 (СН3); 37.56, 44.60, 58.22 (СН2); 99.92 (С(СН3)2); 125.36, 126.25, 144.92, 146.25, 148.31 (CAr). Найдено, %: С 51.72; Н 5.35; N 5.03. C12H15Cl2NO2. Вычислено, %: С 52.19; Н 5.47; N 5.07. 5,6-Бис(хлорметил)-2,8-диметил-4H-[1,3]диоксино[4,5-с]пиридин (VIIb)
Синтезируют и разрабатывают аналогично соединению (VIIa) из 0.91 г (4,04 ммоль) соединения (VIb) и 10 мл (137,5 ммоль) хлористого тионила. Выход 25%, белое кристаллическое вещество. Т.пл. 120-121°С. Спектр ЯМР 1Н (400 МГц, COCl3) δ, м.д.: 1.59 д (3Н, 3JHH=5,1 Гц, СН3), 2.42 с (3Н, СН3), 4.54, 4.57 (АВ, 2JHH=-12.4 Гц, СН2), 4.71, 4.73 (АВ, 2JHH=-11.4 Гц, СН2), 5.01 с (2Н, СН2), 5.14 кв (1H, 3JHH=5,1 Гц, СН). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 18.42, 20.44 (СН3); 37.54, 44.55, 63.67 (СН2); 97.12 (СН); 125.65, 127.81, 145.70, 147.95, 147.98 (CAr). Найдено, %: С 50.74; Н 4.50; N 5.45. C11H13Cl2NO2. Вычислено, %: С 50.40; Н 5.00; N 5.34.
5,6-Бис(хлорметил)-2-изопропил-8-метил-4H-[1,3]диоксино[4,5-с]пиридин (VIIc)
Синтезируют и разрабатывают аналогично соединению (VIIa) из 1.2 г (4,7 ммоль) соединения (VIc) и 10 мл (137,5 ммоль) хлористого тионила. Выход 26%, белое кристаллическое вещество. Т.пл. 68-69°С. Спектр ЯМР 1Н (400 МГц, ацетон-d6) 5, м.д.: 1.07 д (6Н, 3JHH=5 Гц, 2СН3), 2.05 м (1H, СН(СН3)2), 2.37 с (3Н, СН3), 4.78, 4.82 (АВ, 2JHH=-11,2 Гц, СН2), 4.76, 4,80 (АВ, 2JHH=12,4 Гц, СН2), 4.93 д (1H, 3JHH=5 Гц, СН), 5.13, 5,16 (АВ, 2JHH=16 Гц, СН2). ЯМР 13С {Н} (100 МГц, ацетон-d6) δ, м.д.: 17.68, 17.80, 19.47 (СН3); 33.99 (СН(СН3)2); 39.75, 46.45, 65.58 (СН2); 104.81(СН); 128.05, 130.46, 147.36, 149.02, 149.77 (CAr).
Получение четвертичных фосфониевых солей на основе производных пиридоксина
5-Метилентрифенилфосфоний-2,2,8-триметил-4H-[1,3]диоксино[4,5-с] пиридин хлорид (Ia)
К раствору 0.76 г (2.75 ммоль) соединения (VIa) в 20 мл ацетонитрила приливают 2.16 г (8.26 ммоль) трифенилфосфина. Реакционную смесь перемешивают при кипячении в течение 24 часов. Затем растворитель удаляют в вакууме, сухой остаток растворяют в хлороформе. Раствор промывают водой, водную часть отделяют, промывают хлороформом и сушат досуха. Продукт перекристаллизовывают из ацетона. Выход 0.80 г (60%), белое кристаллическое вещество, Т.пл. 217-218°С (разл). Спектр ЯМР 1Н (400 МГц, CDCl3) δ, м.д.: 1.24 с (6Н, 2СН3), 2.24 с (3Н, СН3), 4.34 с (2Н, СН2), 5.32 д (2Н, 1JHP=14,4 Гц, СН2), 7.55-7.75 (16Н, PPh3+СН). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 18.44, 24.56 (СН3); 24.74 д (1JCP=49 Гц); 58.77 (СН2); 99.74 (С); 116.99, 117.31, 117.39, 117.84, 127.30, 127.36, 130.21, 130.34, 133.98, 134.08, 135.15, 135.18, 141.05, 141.10, 146.09, 146.11, 147.95, 147.99 (CAr). ЯМР 31P {Н} (161 МГц, CDCl3) δ, м.д.: 24.86. Масс-спектр (MALDI TOF): Найдено [M-2Cl]+ 454. C29H29NO2PCl2. Вычислено M525.4.
5-Метилентрифенилфосфоний-2,8-диметил-4H-[1,3]диоксино[4,5-с] пиридин хлорид (Ib)
Синтезируют и разрабатывают аналогично соединению (Ia) из 1.3 г (6.16 ммоль) соединения (VIb), 20 мл ацетонитрила и 4.84 г (18.4 ммоль) трифенилфосфина. Выход 41%, белое кристаллическое вещество, Т.пл. 230°С (разл). Спектр ЯМР 1Н (400 МГц, CDCl3) δ, м.д.: 1.29 д (3Н, 3JHH=4.9 Гц, СН3), 2.22, 2.23 с (3Н, СН3), 4.14, 4.34 (АВ, 2JHH=-16,4 Гц, СН2), 4.61 кв (1H, 3JHH=4.9 Гц, СН), 5.35, 5.57 (АВ - часть от АВХ системы, 2JHH=- 15,3 Гц, Гц, СН2), 7.51-7.76 (16Н, PPh3+СН). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 17.73, 20.08 (СН3); 24.37 д (1JCP=47,8 Гц); 64.46 (СН2); 96.86 (С); 116.72, 117.58, 118.21, 118.30, 129.89, 130.04, 130.17, 134.02, 134.12, 134.21, 134.95, 135.02, 135.05, 140.97, 141.03, 146.73, 146.77, 147.56, 147.59. (CAr). ЯМР 31Р {Н} (161 МГц, CDCl3) δ, м.д.: 25.39. Масс-спектр (MALDI TOF): Найдено [M-2Cl]+ 440. C28H27NO2PCl2. Вычислено М 511.4.
5,6-Бис(метилентрифенилфосфоний)-2,2,8-триметил-4H-1,3]диоксино[4,5-с]пиридин дихлорид (Ic)
Синтезируют и разрабатывают аналогично соединению (Ia) из 0.6 г (2.17 ммоль) соединения (VIIa), 20 мл ацетонитрила и 3.41 г (13.0 ммоль) трифенилфосфина. Выход 77%, белое кристаллическое вещество, Т.пл. 230°С (разл). Спектр ЯМР 1Н (400 МГц, CDCl3) δ, м.д.: 1.16 с (6Н, 2СН3), 1.85 с (3Н, СН3), 3.99 с (2Н, СН2), 5.05 с (уш., 2Н, СН2), 5.62 с (уш, 2Н, CH2), 7.62-7.73 м (30Н, 2PPh3). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 16.68, 24.21 (СН3); 25.51 д (1JCP=47 Гц), 32.53 д (1JCP=62 Гц), 58,57 (CH2); 99.87 (С(СН3)2); 116.53, 117.37, 119.36, 120.25, 129.59, 129.72, 130.59, 130.72, 133.34, 133.44, 134.07, 134.15, 134.17, 135.59, 135.62, 139.73, 139.67, 145.36, 145.39, 146.54, 146.58 (CAr). ЯМР 31P {Н} (161 МГц, CDCl3) δ, м.д.: 18.34, 24.56. Масс-спектр (MALDI TOF): Найдено [M-2HCl]+ 728. C48H45N2O2P2Cl2. Вычислено М 800.7.
5,6-Бис(метилентрифенилфосфоний)-2,8-диметил-4H-[1,3]диоксино[4,5-с]пиридин дихлорид (Id)
Синтезируют и разрабатывают аналогично соединению (Ia) из 0.41 г (1.56 ммоль) соединения (VIIb), 20 мл ацетонитрила и 2.46 г (9.38 ммоль) трифенилфосфина. Выход 89%, белое кристаллическое вещество, Т.пл. 197-198°С (разл). Спектр ЯМР 1Н (400 МГц, CDCl3) δ, м.д.: 1.35 д (3Н, 3JHH=5.2 Гц, СН3), 1.87, 1.87 с (3Н, СН3), 3.65, 4.20 (АВ, 2JHH=15,4 Гц, СН2), 4.41, 5.74 (АВ - часть от АВХ системы, 2JHH=-16,4 Гц, , СН2), 4.53 кв (1H, 3JHH=5,2 Гц, СН), 4.89, 6.35 (АВ - часть от АВХ системы, 2JHH=-15,4 , СН2), 7.60-7.86 (30Н, 2PPh3). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 16.66, 19.89 (СН3); 25.57 д (1JCP=47 Гц), 32.49 д (1JCP=62 Гц), 63.96 (СН2); 96.67 (СН); 116.30, 117.14, 118.24, 118.33, 118.41, 119.24, 120.13, 129.48, 129.58, 129.71, 129.82, 129.86, 130.61, 130.73, 133.35, 133.45, 134.10, 134.13, 134.16, 134.20, 135.68, 135.70, 140.51, 140.57, 140.63, 146.39, 146.43, 146.88, 146,91 (CAr). ЯМР 31Р {Н} (161 МГц, CDCl3) δ, м.д.: 20.98, 26.62. Масс-спектр (MALDI TOF): Найдено [М-2HCl]+ 714. C47H43N2O2P2Cl2. Вычислено М 786.7.
5,6-Бис(метилентрифенилфосфоний)-2-изопропил-8-метил-4H-[1,3]диоксино[4,5-с] пиридин дихлорид (Ie)
Синтезируют и разрабатывают аналогично соединению (Ia) из 0.26 г (0.89 ммоль) соединения (VIIc), 20 мл ацетонитрила и 1.39 г (5.3 ммоль) трифенилфосфина. Выход 48%, белое кристаллическое вещество, Т.пл. 222-224°С (разл). Спектр ЯМР 1Н (400 МГц, CDCl3)) δ, м.д.: 0.86, 0.88 д (6Н, 3JHH=4.4 Гц, 2СН3), 1.83 м (1Н, СН(СН3)2), 1.86, 1.87 с (3Н, СН3), 3.67, 4.23 (АВ, 2JHH=-15,2 Гц, CH2), 4.23 д (1Н, 3JHH=4.4 Гц, СН), 4.53, 5.60 (АВ - часть от АВХ системы, 2JHH=-16,4 Гц, , СН2), 5.05, 6.19 (АВ - часть от АВХ системы, 2JHH=-15,2 Гц, , CH2), 7.60-7.84 (30Н, 2PPh3). ЯМР 13С {Н} (100 МГц, CDCl3) δ, м.д.: 15.98, 16.02, 16.56 (СН3); 25.46 д (1JCP=47,3 Гц); 31.59(СН); 32.50 д (1JCP=61,4 Гц); 64.19 (СН2); 102.61 (СН); 116.36, 117.20, 118.23, 118.32, 118.41, 119.27, 120.16, 129.60, 129.73, 130.08, 130.12, 130.57, 130.64, 130.70, 133.34, 133.45, 134.04, 134.14, 134.14, 134.23, 134.31, 135.57, 135.60, 140.30, 140.36, 140.43, 146.34, 146.38, 147.03, 147.06 (CAr). ЯМР 31Р {Н} (161 МГц, CDCl3) δ, м.д.: 19.69, 25.57. Масс-спектр (MALDI TOF): Найдено [M-2HCl]+ 742. C49H47N2O2P2Cl2. Вычислено М 814.8.
Биологическая активность
Результаты исследования антибактериальной активности заявляемых соединений приведены в таблице.
Изучение бактерицидной активности полученных соединений общей формулы (I) проводилось в отношении Staphylococcus aureus.
Все штаммы микроорганизмов, используемые в эксперименте, выделены от больных гнойно-воспалительными заболеваниями:
1. Staphylococcus aureus 1
2. Staphylococcus aureus 2
3. Staphylococcus aureus 3
4. Staphylococcus aureus 4
5. Staphylococcus aureus 5, резистентный к оксациллину (MRSA)
В качестве питательной среды для культивирования микроорганизмов использовались:
1. Мюллер-Хинтон агар, BioRad, Франция
2. Мюллер-Хинтон бульон, BioRad, Франция
В опытах использовалась 24 часовая культура всех перечисленных опытных культур. Микробная взвесь готовилась на основе стерильного бульона Мюллер-Хинтон. Титрование культур до требуемого количества микробных тел в мл проводилось с использованием физиологического раствора. Для стандартизации суспензии использовался iEMS-MF ридер, Labsystems, Финляндия.
Определение бактерицидной активности соединений проводили с использованием кривых роста микроорганизмов. Измерение проводилось с использованием программы Микроб-Автомат, Аналитика, Москва, на ридере iEMS-MF. В стерильные плоскодонные планшеты вносилось стандартное количество микробных тел каждой испытуемой культуры 10×4 кое в объеме 150 мкл. В контрольные лунки добавлялось 50 мкл стерильного бульона Мюллер-Хинтон, в опытные с испытуемой культурой вносилось по 50 мкл исследуемых соединений в 5 концентрациях и 50 мкл ванкомицина (препарат ванкорус).
Концентрации веществ, используемые в эксперименте:
I. Ванкорус - 0,03 мг/мл - количество активного соединения, используемое в диск-диффузном методе, применяемом в клинической микробиологии для определения антибиотикочувствительности микробов.
II. Исследуемые соединения - 10 мг/мл, 1 мг/мл, 0,1 мг/мл, 0,01 мг/мл, 0,001 мг/мл.
Контроля:
I. Контроль роста культур - микробная взвесь 104 кое в стерильном бульоне Мюллер-Хинтон 150 мл+50 мл стерильного бульона Мюллер-Хинтон.
II. Контроль бульона Мюллер-Хинтон - 200 мкл стерильного бульона.
III. Контроль физиологического раствора - 50 мкл стерильного физиологического раствора + 150 мкл бульона Мюллер-Хинтон.
IV. Контроль всех концентраций испытуемых соединений: 50 мкл соединения в исследуемой концентрации + 150 мкл бульона Мюллер-Хинтон. Измерение проводилось в течение 18 часов. Параметры измерения:
t° инкубации: 36,5°
Количество измерений: 220
Интервал между измерениями (мин): 5
Длительность встряхивания перед измерениями (сек): 3
Фильтр для измерения: 620
| ТаблицаДанные по ингибированию роста Staphylococcus aureus растворами тестируемых соединений после 18 часов культивирования | ||||||
| СОЕДИНЕНИЕ КОНЦЕНТРАЦИЯ | Staphylococcus aureus | |||||
| №1 | №2 | №3 | №4 | №5 | ||
| Ie | 10 мг/мл | 0 | 0 | 0 | 0 | 0 |
| 1 мг/мл | 4 | 3 | 3 | 2 | 2 | |
| 0,1 мг/мл | 1 | 2 | 1 | 1 | 1 | |
| 0,01 мг/мл | 21 | 5 | 2 | 23 | 2 | |
| Id | 10 мг/мл | 3 | 2 | 2 | 2 | 2 |
| 1 мг/мл | 3 | 3 | 3 | 2 | 2 | |
| 0,1 мг/мл | 1 | 1 | 2 | 1 | 1 | |
| 0,01 мг/мл | 75 | 74 | 68 | 48 | 78 | |
| Ib | 10 мг/мл | 2 | 5 | 4 | 8 | 5 |
| 1 мг/мл | 2 | 2 | 1 | 1 | 1 | |
| 0,1 мг/мл | 83 | 80 | 79 | 79 | 78 | |
| 0,01 мг/мл | 82 | 82 | 82 | 80 | 84 | |
| 0,001 мг/мл | 83 | 82 | 81 | 80 | 81 | |
| Ia | 10 мг/ил | 3 | 3 | 3 | 8 | 5 |
| 1 мг/мл | 63 | 12 | 1 | 28 | 58 | |
| 0,1 мг/мл | 85 | 83 | 82 | 84 | 83 | |
| 0,01 мг/мл | 85 | 84 | 84 | 84 | 89 | |
| 0,001 мг/мл | 84 | 83 | 80 | 81 | 89 | |
| Ванкорус | 0,03 мг/мл | 2 | 1 | 1 | 1 | 1 |
Как видно из представленных данных, соединения (Ie) и (Id) обладают высокой бактерицидной активностью по отношению ко всем штаммам Staphylococcus aureus в концентрациях 10 мг/мл, 1 мг/мл и 0,1 мг/мл (рост по отношению к контролю от 0 до 3%) и при концентрациях от 10 до 0,1 мг/мл обладают бактерицидной активностью, сравнимой с бактерицидностью препарата Ванкорус (действующим началом является ванкомицин).
Соединения (Ia) и (Ib) менее активны.
Изучение общетоксического действия соединений проводили согласно «Методическим указаниям по изучению общетоксического действия фармакологических веществ» [Методические указания по изучению общетоксического действия фармакологических веществ. - М.: Медицина. 2005. Под ред. Р.У.Хабриева].
Максимально возможные дозы для введения при изучении острой токсичности на аутбредных мышах линии CD-I составили для соединения (Ic) - 800 мг/кг, а для соединения (Id) - 850 мг/кг, соответственно, что позволяет отнести эти соединения согласно ГОСТ 12.1.007.76 к 3 классу опасности - умеренно опасные вещества. Таким образом, заявляются новые фосфониевые соли на основе производных пиридоксина, обладающие высокой антибактериальной активностью по отношению к Staphylococcus aureus, в т.ч. его мультирезистентным штаммам, а также низкой токсичностью.
Заявленное техническое решение соответствует критерию «новизна», предъявляемому к изобретениям, т.к. из исследованного уровня техники не выявлены технические решения, обладающие сходной химической структурой и идентичными свойствами.
Заявленное техническое решение соответствует критерию «изобретательский уровень», предъявляемому к изобретениям, т.к. заявленное техническое решения не является очевидным для специалиста в данной области техники.
Заявленное техническое решение соответствует критерию «промышленная применимость», предъявляемому к изобретениям, т.к в лабораторных условиях Казанского (Приволжского) федерального университета синтезированы принципиально новые соединения, исследованы и получены практические подтверждения заявленных целей.
Фосфониевые соли на основе производных пиридоксина формулы (I), где при R1=CH3; R2=СН3; Х=Н; n=1; R1=СН3; R2=H; X=H; n=1;R1=СН3; R2=СН3; X=CH2P+Ph3; n=2; R1=CH3; R2=H; X=CH2P+Ph3; n=2; R1=СН3; R2=С(СН3)2; X=CH2P+Ph3; n=2, обладающие антибактериальной активностью по отношению к Staphylococcus aureus.