Способ преобразования хлоридов щелочноземельных металлов в вольфраматы и молибдаты и его применение
Иллюстрации
Показать всеИзобретение относится к способу, который позволяет преобразовывать хлориды щелочноземельных металлов в вольфраматы и молибдаты, а также к его применению. Способ включает реакцию хлорида щелочноземельного металла по меньшей мере с одним предшественником вольфрама или молибдена, выбранным из числа оксидов вольфрама, оксидов молибдена, вольфраматов и молибдатов. Реакция проводится в растворителе, состоящем из КСl или из смеси LiCl-KCl при температуре, по меньшей мере равной температуре плавления этого растворителя. Техническим результатом изобретения является обеспечение синтеза вольфраматов и молибдатов щелочноземельных металлов, извлечения щелочноземельных металлов из сред, в которых они находятся в виде хлоридов, извлечения продуктов расщепления в форме соединений щелочноземельных металлов из солевого флюса в рамках переработки облученного ядерного топлива в среде расплавленных хлоридов. 4 н. и 13 з.п. ф-лы, 4 ил., 4 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу, который позволяет преобразовывать хлориды щелочноземельных металлов в вольфраматы и молибдаты, а также к его применению.
Этот способ можно использовать для синтеза вольфраматов и молибдатов щелочноземельных металлов, применяемых в исследовательской работе и в промышленности, например вольфраматов и молибдатов кальция, магния, бария и стронция, на базе соответствующих хлоридов.
Это способ можно также использовать для извлечения щелочноземельных металлов из сред, в которых они находятся в виде хлоридов.
Так, в частности, способ по изобретению можно применять при переработке облученного ядерного топлива для извлечения продуктов распада в виде соединений щелочноземельных металлов, присутствующих в среде расплавленных хлоридов.
Его можно также использовать для контроля загрязненности стоков с высоким содержанием хлоридов, например бытовых и промышленных сточных вод.
Уровень техники
Известны, главным образом, два типа пирохимических способов переработки облученного ядерного топлива: способы в среде расплавленных фторидов и способы в среде расплавленных хлоридов.
Способы в среде расплавленных хлоридов, которые изучаются в настоящее время, приводят к образованию двух флюсов конечных отходов:
- солевой флюс, состоящий из продуктов распада в виде хлоридов, которые растворены в эвтектической смеси хлорид лития-хлорид калия (LiCl-KCl), при том что этими продуктами распада являются щелочные металлы (цезий и рубидий), щелочноземельные металлы (стронций и барий) и лантаноиды (иттрий, церий, лантан, празеодим, гадолиний, неодим, самарий, европий, тербий, диспрозий); и
- несолевой флюс, состоящий из продуктов распада и продуктов активации в металлическом состоянии (молибден, технеций, родий, палладий, рутений, ниобий, цирконий и железо).
Солевой флюс представляет собой высокоактивные отходы, полностью растворимые в воде; в связи с чем возникает необходимость его переработки в форму, обладающую химической стабильностью в течение продолжительного времени. Его переработка путем остекловывания по типу, который был разработан для переработки высокоактивных конечных отходов, образовавшихся при реализации гидрометаллургических способов переработки облученного ядерного топлива, в частности способа PUREX (извлечения плутония и урана из ОЯТ путем экстракции), не рассматривается, принимая во внимание высокое содержание хлора (≈60% отходов по массе).
Действительно, хлор можно включить в стекловидную силикатную основу только из расчета 1-2% по массе, поэтому для остекловывания такого флюса потребуется разбавить его по меньшей мере в 30 раз, что приведет к образованию совершенно неприемлемого объема высокоактивных отходов.
Решением этой проблемы может стать предварительная обработка этого солевого флюса с целью удаления хлора и селективного извлечения содержащихся в нем продуктов распада.
Касательно продуктов распада в виде соединений щелочноземельных металлов, более конкретно стронция и бария, было показано, что их можно извлекать, когда они находятся в виде расплавленных хлоридов, путем осаждения двойных фосфатов (V.A.Volkovich et al., Journal of Nuclear Materials, 323 (2003), 49-56 [1]).
При этом образование двойных фосфатов щелочноземельных металлов зависит от природы используемого растворителя.
Так, осаждение двойных фосфатов эффективно в эвтектической смеси хлорид натрия - хлорид калия (NaCl-KCl) или в чистом хлориде лития (LiCl) при 750°С, тогда как оно малоэффективно в смеси LiCl-KCl при 550°С.
В то же время синтез вольфрамата и молибдата бария был выполнен в среде расплавленных нитратов (NaNO3 или KNO3) (Р.Afanasiev, Materials Letters (2007), статья находится в печати [2]).
И, наконец, вольфраматы щелочноземельных металлов были получены в средах расплавленных хлоридов путем испарения при высокой температуре. Эти работы были выполнены в рамках синтеза монокристаллов. Так, A.R.Patel et al. (Journal of Crystal Growth 23 (1974), 95-100 [3]) использовали флюс NaCl-LiCl при 950°C, a A.Packter et al. (Journal of Crystal Growth 18 (1973), 86-93 [4]) и S.К.Arora et al. (Crystal Research and Technology 41 (2006), 1089-1095 [5]) работали с флюсом LiCl при 900°С.
Поскольку растворителем, который используется в пирохимических способах в среде расплавленных хлоридов, является эвтектическая смесь LiCl-KCl, было бы желательно располагать способом, позволяющим эффективно извлекать, по возможности селективно, стронций и барий, если они находятся в форме хлоридов, в эвтектическую смесь LiCl-KCl.
Кроме того, обнаружилось, что в рамках своих работ изобретатели неожиданно отметили, что реакция между хлоридами щелочноземельных металлов и подобранными надлежащим образом предшественниками вольфрама и молибдена в растворителе, состоящем из смеси LiCl-KCl или из чистого хлорида калия, приводит к полному или почти полному преобразованию этих хлоридов в вольфраматы и молибдаты, которые выпадают в осадок и, таким образом, образуют твердую фазу, которую затем можно будет легко отделить от остальной части реакционной среды.
Помимо этого, они констатировали, что еще более удивительным образом это преобразование не происходит с хлоридами щелочных металлов, присутствующими в реакционной среде, и, по-видимому, является специфическим для хлоридов щелочноземельных металлов.
На этих результатах и основано настоящее изобретение.
Краткое раскрытие изобретения
Объектом настоящего изобретения является в первую очередь способ преобразования хлорида щелочноземельного металла по меньшей мере в одну соль, выбранную из числа вольфраматов и молибдатов этого металла, при этом упомянутый способ включает:
реакцию хлорида щелочноземельного металла по меньшей мере с одним предшественником вольфрама или молибдена, выбранным из числа оксидов вольфрама, оксидов молибдена, вольфраматов и молибдатов, и эта реакция проводится в растворителе, состоящем из KCl или из смеси LiCl-KCl, при температуре по меньшей мере равной температуре плавления этого растворителя.
В тексте выше и ниже термины «вольфрамат» и «молибдат» используются в своем обычном значении, а именно они означают соли, содержащие либо двухвалентный анион WO4 -2 в случае вольфрамата, либо двухвалентный анион MoO4 -2 в случае молибдата.
По изобретению, предшественника вольфрама или молибдена предпочтительно выбирают из оксида вольфрама (VI) или триоксида вольфрама (WO3), оксида молибдена (VI) или триоксида молибдена (МоО3), вольфраматов и молибдатов щелочных металлов, более конкретно натрия, калия и лития.
Разумеется, можно использовать несколько предшественников вольфрама или молибдена, в частности смеси вольфраматов щелочных металлов, такие как, например, смеси Na2WO4-K2WO4 или Li2WO4-K2WO4, или смеси молибдатов щелочных металлов, такие как, например, смеси Na2MoO4-K2MoO4 или Li2MoO4-K2MoO4.
Растворитель предпочтительно выбирают в зависимости от предшественника вольфрама или молибдена.
Так, если таким предшественником является оксид вольфрама, и в частности WO3, в качестве растворителя следует использовать хлорид калия; в этом случае, поскольку температура плавления KCl составляет 771°С, реакцию предпочтительно проводят при температуре от 800 до 900°С.
Напротив, если таким предшественником является оксид молибдена, вольфрамат или молибдат, и в частности МоО3, вольфрамат или молибдат щелочного металла, в качестве растворителя можно также использовать как смесь LiCl-KCl, так и хлорид калия.
Ввиду этого в этом случае предпочтительно использовать смесь LiCl-KCl и, более конкретно, смесь, имеющую композицию, близкую или идентичную эвтектической композиции, то есть смесь с массовым отношением хлорида лития к хлориду калия от 40/60 до 50/50 и в идеале 45,5/55,5 (эвтектическая), таким образом, чтобы ее температура плавления составляла 350°С или близкую к указанной величину. Поэтому реакцию предпочтительно проводят при температуре от 400 до 600°С и более предпочтительно при температуре порядка 500°С.
В любом случае хлорид щелочноземельного металла (AM) и предшественник вольфрама или молибдена предпочтительно присутствуют в растворителе в стехиометрическом соотношении (молярное отношение AM/W или АМ/Мо=1), и время, в течение которого их оставляют реагировать друг с другом, составляет один или несколько часов, предпочтительно порядка от 1 до 10 часов.
Описанный способ преобразования предпочтительно может использоваться для извлечения одного или нескольких щелочноземельных металлов из среды, в которой они находятся в виде хлоридов, и более конкретно из среды, в которой этот щелочноземельный металл или эти щелочноземельные металлы уже растворены в расплавленном KCl или в расплавленной смеси LiCl-KCl, например, применительно к продуктам распада соединений щелочноземельных металлов, присутствующим в солевых отходах, которые образуются при переработке облученного ядерного топлива в среде расплавленных хлоридов.
Таким образом, объектом изобретения является также способ извлечения по меньшей мере одного щелочноземельного металла из среды, содержащей этот металл в виде хлорида, который включает
a1) преобразование хлорида щелочноземельного металла по меньшей мере в одну соль, выбранную из вольфраматов и молибдатов этого металла, способом преобразования, как это определено выше; затем
b1) извлечение соли, полученной в результате такого преобразования.
В том случае, если хлорид щелочноземельного металла уже растворен в расплавленном KCl, этап a1) способа извлечения предпочтительно включает:
- добавление к среде вольфрамата или молибдата калия; и
- выдерживание среды при температуре, по меньшей мере равной температуре плавления KCl в течение периода, достаточного для прохождения преобразования хлорида щелочноземельного металла в вольфрамат или молибдат.
Аналогичным образом, если хлорид щелочноземельного металла уже растворен в расплавленной смеси LiCl-KCl, этап a1) способа извлечения предпочтительно включает:
- добавление к среде смеси вольфраматов или молибдатов лития и калия таким образом, чтобы эти два металла по возможности присутствовали в смеси в массовом соотношении, идентичном тому, в котором они присутствуют в смеси LiCl-KCl; и
- выдерживание среды при температуре, по меньшей мере равной температуре плавления смеси LiCl-KCl, в течение периода, достаточного для прохождения преобразования хлорида щелочноземельного металла в вольфрамат или молибдат.
Можно также извлекать щелочноземельный металл из среды, в которой он находится, не изменяя при этом, как качественно, так и количественно, состав растворителя этой среды, что особенно ценно при переработке облученного ядерного топлива, при которой в высшей степени желательно иметь возможность повторно использовать растворитель, принимая во внимание очень большие объемы использованного растворителя.
В том случае, если хлорид щелочноземельного металла не растворен в расплавленном KCl или в расплавленной смеси LiCl-KCl, этап a1) способа извлечения включает:
- смешивание хлорида щелочноземельного металла и растворителя, состоящего из KCl или из смеси LiCl-KCl;
- добавление к полученной таким образом смеси по меньшей мере одного предшественника вольфрама или молибдена, выбранного из числа оксидов вольфрама, оксидов молибдена, вольфраматов и молибдатов; и
- нагрев всего комплекса до температуры, по меньшей мере равной температуре плавления растворителя, в течение периода, достаточного для прохождения преобразования хлорида щелочноземельного металла в вольфрамат или молибдат.
В любом случае этап b1) можно осуществлять любым методом, который традиционно используется для разделения твердой фазы (которая в этом случае представлена вольфраматом, молибдатом или смесью вольфраматов или молибдатов щелочноземельного металла) и жидкой фазы (которая в этом случае представлена остатком реакционной среды).
Предпочтительно среда представляет собой солевой флюс, полученный в результате переработки облученного ядерного топлива в среде расплавленных хлоридов, и щелочноземельный металл, извлеченный таким образом, является продуктом расщепления, а именно стронцием или барием.
Обнаружилось, что применение способа извлечения по изобретению в рамках переработки облученного ядерного топлива в среде расплавленных хлоридов обладает рядом преимуществ.
Действительно, этот способ извлечения позволяет извлекать продукты расщепления в виде соединений щелочноземельных металлов, присутствующие в солевом флюсе, полностью или почти полностью (выход от 98 до 100%), селективно (поскольку извлечения продуктов расщепления в виде соединений щелочных металлов не происходит) и, кроме того, в форме вольфраматов или молибдатов, которые обладают очень низкой растворимостью в воде и, следовательно, малой склонностью к выщелачиванию и которые в этой связи можно использовать в качестве матрицы для удерживания в течение длительного времени этих продуктов расщепления.
Таким образом, объектом изобретения является также способ переработки облученного ядерного топлива в среде расплавленных хлоридов, который включает извлечение по меньшей мере одного продукта расщепления в форме соединения щелочноземельного металла в виде вольфрамата или молибдата из солевого флюса способом извлечения, описанным выше.
Альтернативно, этот способ переработки предпочтительно включает преобразование вольфрамата или молибдата щелочноземельного метала, являющегося продуктом расщепления, в керамический материал для удерживания в течение длительного времени этого продукта расщепления.
Это преобразование может быть проведено с помощью методов, которые традиционно используются при изготовлении керамических материалов, то есть обычно путем превращения вольфрамата или молибдата в порошок, уплотнения этого порошка и спекания порошка, уплотненного таким образом.
Способ преобразования по изобретению может также использоваться для синтеза вольфраматов и молибдатов щелочноземельных металлов на базе соответствующих хлоридов, например вольфраматов и молибдатов кальция, магния, бария или стронция.
Так, объектом изобретения является, кроме того, способ синтеза по меньшей мере одной соли, выбранной из числа вольфраматов и молибдатов щелочноземельных металлов, и этот способ включает:
а2) преобразование хлорида щелочноземельного металла по меньшей мере в одну соль, выбранную из числа вольфраматов и молибдатов этого металла описанным выше способом преобразования; затем
b2) извлечение соли, полученной в результате этого преобразования.
Изобретение станет более понятным в свете дополнения к описанию, приведенного ниже, в котором даны примеры реализации способа по изобретению для преобразования расплавленных хлоридов стронция и бария в вольфраматы.
Очевидно, что эти примеры приведены только для иллюстрации объекта изобретения и ни в коей мере не являются ограничивающими для этого объекта.
Краткое описание фигур
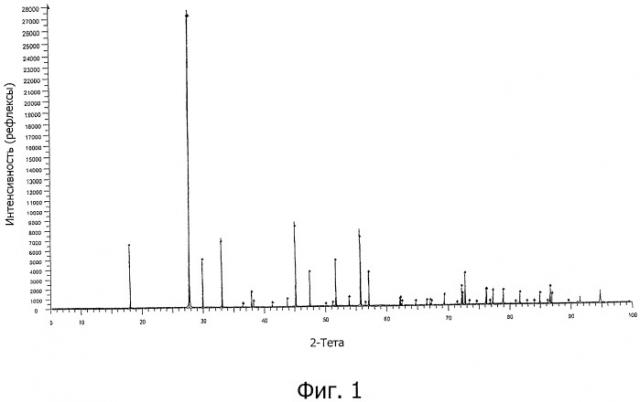
Фигура 1 представляет собой рентгеновскую дифрактограмму, зарегистрированную при анализе порошка, который был получен в результате преобразования хлорида стронция в вольфрамат стронция способом по изобретению в отсутствие какого-либо другого хлорида.
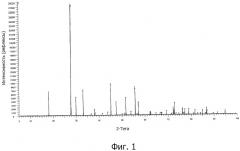
Фигура 2 представляет собой рентгеновскую дифрактограмму, зарегистрированную при анализе порошка, который был получен в результате преобразования хлорида бария в вольфрамат бария способом по изобретению в отсутствие какого-либо другого хлорида.
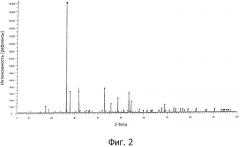
Фигура 3 представляет собой рентгеновскую дифрактограмму, зарегистрированную при анализе порошка, который был получен в результате преобразования хлорида стронция в вольфрамат стронция способом по изобретению в присутствии хлоридов рубидия и цезия.
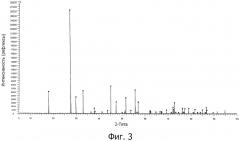
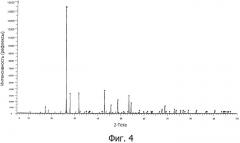
Фигура 4 представляет собой рентгеновскую дифрактограмму, зарегистрированную при анализе порошка, который был получен в результате преобразования хлорида бария в вольфрамат бария способом по изобретению в присутствии хлоридов рубидия и цезия.
Примеры
Пример 1: Преобразование SrCl2 в SrWO4 в отсутствие какого-либо другого хлорида
В алюминиевом тигле смешивают при температуре окружающей среды (20-25°С) 1 г SrCl2, имеющего чистоту выше 99%, и 9 г эвтектической смеси LiCl/KCl, составленной из 4,005 г LiCl и 4,995 г KCl, затем добавляют к полученной таким образом смеси при температуре окружающей среды 2,0567 г K2WO4.
Тигель помещают в кварцевую трубку, которую закрывают и нагревают до 500°С со скоростью порядка 5°С в минуту. Трубку выдерживают при 500°С в течение 5 часов, после этого охлаждают со скоростью порядка 2°С в минуту до температуры 300°С. После этого содержимое тигля закаливают на воздухе.
Полученный таким образом твердый материал помещают в нагретую воду сверхвысокой чистоты (25°С или 100°С) для перевода в раствор непрореагировавшего SrCl2, затем отфильтровывают с помощью воронки Бюхнера через фильтр с порогом отсечения 0,45 мкм. Осадок на фильтре промывают водой, затем высушивают при 120°С.
Полученный таким образом порошок подвергают дифракционному рентгеновскому анализу. Рентгеновская дифрактограмма этого порошка представлена на фигуре 1. Эта дифрактограмма показывает хорошее соответствие зарегистрированных пиков и пиков на расчетной карточке SrWO4 (01-085-0587 (С)), доказывающее, что SrCl2, первоначально присутствовавший в смеси с эвтектической смесью, успешно преобразовался в SrWO4.
Выход реакции определяют путем взвешивания SrWO4 и сравнения результата взвешивания с теоретической массой, соответствующей 100% реакции. Этот выход реакции превышает 90%.
Пример 2: Преобразование BaCl2 в BaWO4 в отсутствие какого-либо другого хлорида
Выполняют ту же последовательность операций, которая была описана в примере 1 выше, за исключением того, что в эвтектической смеси растворяют 1 г BaCl2 (вместо грамма SrCl2) и используют 1,5657 г K2WO4.
Рентгеновская дифрактограмма этого порошка представлена на фигуре 2. Эта дифрактограмма показывает хорошее соответствие зарегистрированных пиков и пиков на расчетной карточке BaWO4 (00-043-0646 (*)), доказывающее, что BaCl2, первоначально присутствовавший в смеси с эвтектической смесью, успешно преобразовался в BaWO4.
Выход реакции определяют путем взвешивания BaWO4 и сравнения результата взвешивания с теоретической массой, соответствующей 100% реакции. Этот выход реакции превышает 90%.
Пример 3: Преобразование SrCl2 в SrWO4 в присутствии RbCl и CsCl
Выполняют ту же последовательность операций, которая была описана в примере 1 выше, за исключением того, что в эвтектической смеси растворяют 1 г смеси SrCl2, RbCl и CsCl (1/0,5/0,5 по массе) вместо грамма SrCl2.
Рентгеновская дифрактограмма этого порошка представлена на фигуре 3.
Эта дифрактограмма практически идентична дифрактограмме, представленной на фигуре 1, что подтверждает, с одной стороны, что только SrCl2 был преобразован в вольфрамат и, с другой стороны, что присутствие двух хлоридов щелочных металлов в реакционной среде не повлияло на это преобразование.
Выход реакции (определяемый согласно описанию в примере 1) превышает 90%.
Пример 4: Преобразование BaCl2 в BaWO4 в присутствии RbCl и CsCl
Выполняют ту же последовательность операций, которая была описана в примере 2 выше, за исключением того, что в эвтектической смеси растворяют 1 г смеси BaCl2, RbCl и CsCl (1/0,5/0,5 по массе) вместо грамма BaCl2.
Рентгеновская дифрактограмма этого порошка представлена на фигуре 4.
Эта дифрактограмма практически идентична дифрактограмме, представленной на фигуре 2, что подтверждает, что и здесь тоже только BaCl2 был преобразован в вольфрамат, и присутствие двух хлоридов щелочных металлов в реакционной среде не повлияло на это преобразование.
Выход реакции (определяемый как в примере 2) превышает 90%.
Цитируемая литература
[1] V.A.Volkovich et al., Journal of Nuclear Materials, 323 (2003), 49-56.
[2] P.Afanasiev, Materials Letters (2007), статья находится в печати.
[3] A.R.Patel et al., Journal of Crystal Growth 23 (1974), 95-100.
[4] A.Packter et al.. Journal of Crystal Growth 18 (1973), 86-93.
[5] S.К.Аrоrа et al., Crystal Research and Technology 41 (2006), 1089-1095.
1. Способ преобразования хлорида щелочноземельного металла по меньшей мере в одну соль, выбранную из вольфраматов и молибдатов этого металла, который включает:реакцию хлорида щелочноземельного металла по меньшей мере с одним предшественником вольфрама или молибдена, выбранным из оксидов вольфрама, оксидов молибдена, вольфраматов и молибдатов, и эта реакция проводится в растворителе, состоящем из хлорида калия (КСl) или из смеси хлорид лития - хлорид калия (LiCl-KCl), при температуре, по меньшей мере равной температуре плавления этого растворителя.
2. Способ преобразования по п.1, в котором предшественника вольфрама или молибдена выбирают из оксида вольфрама (VI), оксида молибдена (VI), вольфраматов и молибдатов щелочных металлов.
3. Способ преобразования по п.2, в котором щелочными металлами являются натрий, калий и литий.
4. Способ преобразования по п.2, в котором предшественником вольфрама или молибдена является оксид вольфрама (VI), и растворителем является хлорид калия.
5. Способ преобразования по п.4, в котором реакцию проводят при температуре от 800 до 900°С.
6. Способ преобразования по п.2, в котором предшественником вольфрама или молибдена является оксид молибдена (VI), вольфрамат или молибдат щелочного металла, и растворителем является смесь LiCl-KCl с массовым соотношением хлорида лития к хлориду калия от 40/60 до 50/50, и предпочтительно 45,5/55,5.
7. Способ преобразования по п.6, в котором реакцию проводят при температуре от 400 до 600°С, более предпочтительно при температуре порядка 500°С.
8. Способ преобразования по любому из предшествующих пунктов, в котором хлорид щелочноземельного металла и предшественник вольфрама или молибдена присутствуют в растворителе в стехиометрическом соотношении.
9. Способ извлечения по меньшей мере одного щелочноземельного металла из среды, содержащей этот металл в виде хлорида, который включает:a1) преобразование хлорида щелочноземельного металла по меньшей мере в одну соль, выбранную из вольфраматов и молибдатов этого металла, способом преобразования по любому из пп.1-8; затемb1) извлечение соли, полученной в результате такого преобразования.
10. Способ извлечения по п.9, в котором среда содержит хлорид щелочноземельного металла в расплавленном растворителе LiCl-KCl и этап a1) способа извлечения включает:добавление к среде смеси вольфраматов или молибдатов лития и калия; ивыдерживание среды при температуре, по меньшей мере равной температуре плавления растворителя в течение времени, достаточного для прохождения преобразования хлорида щелочноземельного металла в вольфрамат или молибдат.
11. Способ извлечения по п.10, в котором смесь вольфраматов или молибдатов лития и калия характеризуется массовым соотношением лития к калию, идентичным тому, в котором они присутствуют в растворителе.
12. Способ извлечения по любому из пп.9-11, в котором среда представляет собой солевой флюс, полученный в результате переработки облученного ядерного топлива в среде расплавленных хлоридов.
13. Способ извлечения по любому из пп.9-11, в котором щелочноземельный металл является стронцием или барием.
14. Способ переработки облученного ядерного топлива в среде расплавленных хлоридов, который включает извлечение по меньшей мере одного продукта расщепления в форме соединения щелочноземельного металла в виде по меньшей мере одного вольфрамата или молибдата из солевого флюса способом извлечения по любому из пп.9-13.
15. Способ переработки по п.14, который дополнительно включает преобразование вольфрамата или молибдата щелочноземельного продукта расщепления в керамический материал для удерживания в течение длительного времени этого продукта расщепления.
16. Способ синтеза по меньшей мере одной соли, выбранной из вольфраматов и молибдатов щелочноземельных металлов, который включает:а2) преобразование хлорида щелочноземельного металла по меньшей мере в одну соль, выбранную из вольфраматов и молибдатов этого металла способом преобразования по любому из пп.1-8; затемb2) извлечение соли, полученной в результате этого преобразования.
17. Способ синтеза по п.16, в котором щелочноземельный металл является кальцием, магнием, барием или стронцием.