Способ отделения фторолефинов от фтороводорода путем азеотропной дистилляции
Иллюстрации
Показать всеНастоящее раскрытие относится к способу отделения фторолефина от смеси, содержащей фтороводород и фторолефин, предусматривающему азеотропную дистилляцию в присутствии или в отсутствие азеотропообразователя. В частности, раскрываются способы отделения любого из HFC-1225ye, HFC-1234ze, HFC-1234yf или HFC-1243zf от HF. Один способ предусматривает разделение смеси, содержащей HF и фторолефин, где указанный способ включает а) подачу композиции, содержащей HF и фторолефин, в первую дистилляционную колонну; b) отведение азеотропной композиции, содержащей HF и фторолефин, в качестве первого дистиллята и либо i) HF, либо ii) фторолефина в качестве композиции кубового остатка первой колонны; с) конденсацию первого дистиллята с образованием двух жидких фаз: i) HF-обогащенной фазы и ii) фторолефин-обогащенной фазы; и d) рециркуляцию первой жидкой фазы, обогащенной тем же самым соединением, которое удаляется в качестве кубового остатка первой колонны, где указанной первой жидкой фазой является либо i) HF-обогащенная фаза, либо ii) фторолефин-обогащенная фаза, обратно в первую дистилляционную колонну. Настоящего изобретения представляет собой более эффективный способ отделения HF от олефинов. 11 н. и 22 з.п. ф-лы, 8 ил, 13 пр., 14 табл.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
В настоящей заявке испрашивается приоритет по предварительной заявке № 60/839737, зарегистрированной 24 августа 2006 года.
УРОВЕНЬ ТЕХНИКИ
Область техники, к которой относится изобретение
Данное изобретение в целом относится к способу отделения HF от фторолефинов.
Описание предшествующего уровня техники
При химическом производстве фторолефинов могут получаться смеси желаемых фторолефинов и фтороводорода (HF). Разделение фторолефинов и HF не всегда является легко достигаемым. Существующие методы дистилляции и декантации очень часто являются неэффективными для разделения данных соединений. Промывка водой может быть эффективна, но требует использования большого количества промывных растворов и приводит к получению чрезмерного количества отходов, а также влажного продукта, который затем необходимо сушить. Поэтому необходимы новые способы отделения HF от фторолефинов.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее раскрытие относится к способу разделения смеси, содержащей HF и фторолефин, где указанный способ включает a) подачу композиции, содержащей HF и фторолефин, в первую дистилляционную колонну; b) отведение азеотропной композиции, содержащей HF и фторолефин, в качестве первого дистиллята и либо i) HF, либо ii) фторолефина в качестве композиции кубового остатка первой колонны; c) конденсацию первого дистиллята с образованием двух жидких фаз: i) HF-обогащенной фазы и ii) фторолефин-обогащенной фазы; и d) рециркуляцию первой жидкой фазы, обогащенной тем же самым соединением, которое удаляется в качестве кубового остатка первой колонны, где указанной первой жидкой фазой является либо i) HF-обогащенная фаза, либо ii) фторолефин-обогащенная фаза, обратно в первую дистилляционную колонну.
Также раскрытым является способ отделения фторолефина от смеси, содержащей фтороводород и указанный фторолефин, где указанный фторолефин присутствует в концентрации, большей, чем концентрация в азеотропной смеси фтороводорода и указанного фторолефина, где указанный способ включает a) подачу указанной смеси, содержащей фтороводород и указанный фторолефин, в первую дистилляционную колонну; b) отведение азеотропной композиции, содержащей фтороводород и фторолефин, в качестве первого дистиллята из первой дистилляционной колонны; c) извлечение фторолефина, по существу свободного от фтороводорода, в качестве композиции первого кубового остатка из первой дистилляционной колонны; d) конденсацию первого дистиллята с образованием двух жидких фаз: i) фтороводород-обогащенной фазы и ii) фторолефин-обогащенной фазы; и е) рециркуляцию фторолефин-обогащенной фазы в первую дистилляционную колонну.
Также раскрытым является способ отделения фтороводорода от смеси, содержащей фтороводород и фторолефин, где фтороводород присутствует в концентрации, большей, чем концентрация в азеотропной смеси указанного фтороводорода и фторолефина, где указанный способ включает a) подачу указанной смеси, содержащей фтороводород и фторолефин, в первую дистилляционную колонну; b) отведение азеотропной или азеотропоподобной композиции, содержащей фторолефин и HF, в качестве первого дистиллята из первой дистилляционной колонны; c) извлечение фтороводорода, по существу свободного от фторолефина, в качестве композиции первого кубового остатка из первой дистилляционной колонны; d) конденсацию первого дистиллята с образованием двух жидких фаз: фторолефин-обогащенной фазы и фтороводород-обогащенной фазы; и е) рециркуляцию HF-обогащенной фазы в первую дистилляционную колонну.
Также предлагается способ очистки фторолефина от смеси, содержащей фторолефин и HF, где указанный фторолефин присутствует в указанной смеси в концентрации, большей, чем концентрация в азеотропной смеси указанного фторолефина и HF, где указанный способ включает a) добавление азеотропообразователя к смеси, содержащей фторолефин и HF, таким образом формируя вторую смесь; b) дистилляцию указанной второй смеси на первом этапе дистилляции с образованием композиции первого дистиллята, содержащей HF, фторолефин и азеотропообразователь, и композиции первого кубового остатка, содержащей фторолефин; с) конденсацию указанной композиции первого дистиллята с образованием двух жидких фаз: i) HF-обогащенной фазы и ii) обогащенной азеотропообразователем фазы, и d) необязательно рециркуляцию фторолефин-обогащенной фазы обратно на первый этап дистилляции.
Также предлагается способ очистки HF от смеси, содержащей фторолефин и HF, где указанный HF присутствует в концентрации, большей, чем концентрация в азеотропной смеси HF и указанного фторолефина, где указанный способ включает a) добавление азеотропообразователя к смеси, содержащей фторолефин и HF, таким образом формируя вторую смесь; b) дистилляцию указанной второй смеси на первом этапе дистилляции с образованием композиции первого дистиллята, содержащей HF, азеотропообразователь и фторолефин, и композиции первого кубового остатка, содержащей HF; с) конденсацию указанной композиции первого дистиллята с образованием двух жидких фаз: i) обогащенной азеотропообразователем фазы и ii) HF-обогащенной фазы; и d) необязательно рециркуляцию HF-обогащенной фазы обратно на первый этап дистилляции.
Предшествующее общее описание и последующее детальное описание являются только иллюстративными и поясняющими и не ограничивают изобретение, как определено в прилагаемой формуле.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Примеры осуществления изобретения иллюстрируются в сопровождении фигур для лучшего понимания представленных в настоящем описании идей.
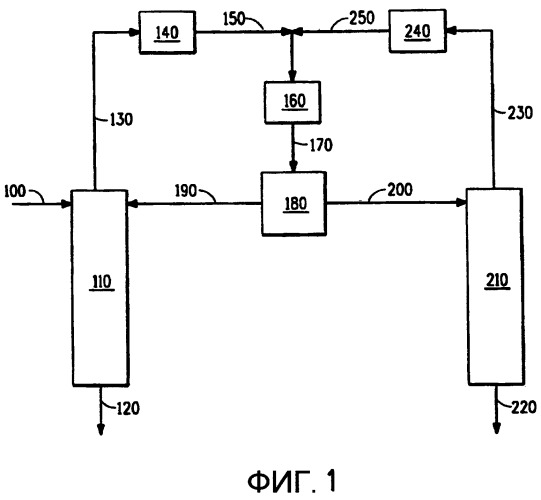
Фиг.1 является иллюстрацией одного примера осуществления азеотропной дистилляции для разделения HF и фторолефина без добавления азеотропообразователя.
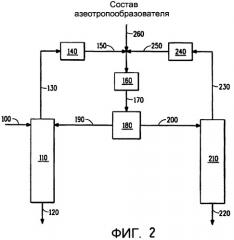
Фиг.2 является иллюстрацией одного примера осуществления азеотропной дистилляции для разделения HF и фторолефина с добавлением азеотропообразователя.
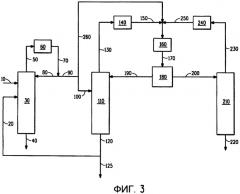
Фиг.3 является иллюстрацией одного примера осуществления процесса отделения по меньшей мере одного из HFC-236ea и HFC-236cb от смеси, содержащей HFC-1225ye, HF и по меньшей мере один из указанных HFC-236ea и HFC-236cb, посредством азеотропной дистилляции, где HFC-1225ye действует в качестве азеотропообразователя, за которым следует процесс, в котором HFC-1225ye и HF отделяются от смеси, содержащей HFC-1225ye и HF, но по существу свободной от HFC-236ea и/или HFC-236cb, с помощью азеотропной дистилляции без добавления другого химического соединения, действующего как азеотропообразователь.
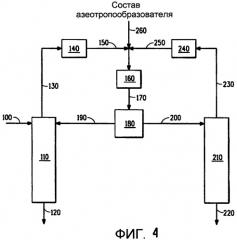
Фиг.4 является иллюстрацией одного примера осуществления процесса отделения HFC-1225ye и по меньшей мере одного из HFC-236ea и HFC-236cb от смеси, содержащей HFC-1225ye, HF и по меньшей мере один из указанных HFC-236ea и HFC-236cb, посредством азеотропной дистилляции, где при дистилляции подается дополнительный азеотропообразователь.
Фиг.5 является иллюстрацией одного примера осуществления процесса отделения по меньшей мере одного из HFC-236ea и HFC-236cb от смеси, содержащей HFC-1225ye, HF и по меньшей мере один из указанных HFC-236ea и HFC-236cb, посредством азеотропной дистилляции, где HFC-1225ye действует в качестве азеотропообразователя, за которым следует процесс, в котором HFC-1225ye и HF отделяются от смеси, содержащей HFC-1225ye и HF, но по существу свободной от HFC-236ea и/или HFC-236cb, с помощью азеотропной дистилляции с добавлением азеотропообразователя.
Фиг.6 является иллюстрацией другого примера осуществления процесса, представленного на фиг.3, где двухфазная смесь, покидающая конденсатор первой колонки, подвергается декантации и разделению на HFC-1225ye-обогащенный и HF-обогащенный потоки, которые добавляются в колонки HFC-1225ye и HF, соответственно.
Фиг.7 является иллюстрацией другого примера осуществления процесса, представленного на фиг.5, где двухфазная смесь, покидающая конденсатор первой колонки, подвергается декантации и разделению на HFC-1225ye-обогащенный и HF-обогащенный потоки, которые добавляются в колонки HFC-1225ye и HF, соответственно.
Фиг.8 является иллюстрацией другого примера осуществления процесса, представленного на фиг.6, где три колонны 20, 110 и 220 имеют один общий декантатор.
Специалисты в данной области техники понимают, что объекты на фигурах представлены в качестве иллюстрации для простоты и ясности и не было необходимости изображать их в масштабе. Например, размеры некоторых объектов в фигурах могут быть преувеличены относительно других объектов, чтобы помочь лучше понять примеры осуществления изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Многие аспекты и примеры осуществления изобретения были описаны выше и являются только иллюстративными и не ограничивающими. После чтения данного описания специалистам в данной области техники станет понятно, что возможны другие аспекты и примеры осуществления изобретения без отступления за рамки изобретения.
Другие черты и преимущества любого одного или нескольких примеров осуществления изобретения будут очевидны из следующего детального описания и из формулы изобретения.
1. Определения и объяснение используемых терминов
Перед обращением к деталям примеров осуществления изобретения, описанных ниже, дано определение и объяснение.
Под азеотропной композицией, или композицией азеотропа, подразумевается смесь двух или более веществ с постоянной температурой кипения, которая испаряется с постоянным составом и, таким образом, ведет себя как одно вещество. Композиции с постоянной температурой кипения характеризуются как азеотропные, поскольку они демонстрируют либо максимум, либо минимум температуры кипения, по сравнению с температурами кипения индивидуальных компонентов. Азеотропные композиции также характеризуются минимумом или максимумом в значениях давления пара по сравнению с давлением пара чистых компонентов в PTx-диаграмме (PTx-cell) как функции состава при постоянной температуре. Для гомогенных азеотропов, где паровая фаза находится в равновесии с единой жидкой фазой, составы паровой и жидкой фаз являются одинаковыми. Однако в случае гетерогенных азеотропов, где паровая фаза находится в равновесии с двумя жидкими фазами, все три равновесные фазы могут иметь различный, но постоянный составы.
Используемый в настоящем описании термин «азеотропоподобная композиция» (также обычно называемая как «близкая к азеотропу композиция») означает кипящую при постоянной температуре или по существу постоянной температуре жидкую смесь двух или более веществ, которая ведет себя как одно вещество. Одним из способов отличить азеотропоподобную композицию является то, что состав пара, получаемого при частичном испарении или дистилляции жидкости, по существу не изменяется на всем протяжении частичного испарения или дистилляции. Аналогично, состав настоящей жидкой фазы или фаз по существу не изменяется в течение частичного испарения или дистилляции. То есть смесь испаряется/дистиллируется/кипит без существенного изменения состава. Это является отличием от не являющихся азеотропоподобными композиций, в которых состав жидкости изменяется в значительной степени в течение кипения или испарения. Другим способом отличить азеотропоподобную композицию является то, что давление пара в точке кипения композиции и давление пара в точке конденсации композиции при определенной температуре является по существу одинаковым. В настоящем описании композиция рассматривается как азеотропоподобная, если разница в давлении в точке конденсации и давлении в точке кипения составляет менее или равно 3% (исходя из давления в точке кипения).
Термин «азеотроп с высокой температурой кипения» означает, что азеотропная или азеотропоподобная композиция кипит при более высокой температуре при любом данном давлении, чем любое из составляющих ее соединений в отдельности кипело бы при данном давлении. С другой стороны, под азеотропом с высокой температурой кипения подразумевается любая азеотропная или азеотропоподобная композиция, которая имеет более низкое давление пара при любой данной температуре, чем любое из составляющих ее соединений в отдельности имело бы при данной температуре.
Термин «азеотроп с низкой температурой кипения» означает, что азеотропная или азеотропоподобная композиция кипит при более низкой температуре при любом данном давлении, чем любое из составляющих ее соединений в отдельности кипело бы при данном давлении. С другой стороны, под азеотропом с низкой температурой кипения подразумевается любая азеотропная или азеотропоподобная композиция, которая имеет более высокое давление пара при любой данной температуре, чем давление пара любого из составляющих азеотроп соединений в отдельности имело бы при данной температуре.
Можно охарактеризовать азеотропную или азеотропоподобную композицию как по существу кипящую при постоянной температуре смесь, которая имеет различный характер, в зависимости от выбранных условий, по нескольким критериям.
- Композиция может быть определена как азеотроп двух соединений, поскольку термин «азеотроп» является одновременно как определяющим, так и ограничивающим, и требуются эффективные количества тех двух или более соединений для данной уникальной смеси веществ, которая может быть кипящей при постоянной температуре композицией.
- Специалисту в данной области техники будет понятно, что при различных давлениях состав данной азеотропной или азеотропоподобной композиции будет варьироваться по меньшей мере до некоторой степени, как и температура кипения. Таким образом, азеотропная или азеотропоподобная композиция двух соединений представляет уникальный тип соотношений, но с различным составом, который зависит от температуры и/или давления. Поэтому изменение состава, а не постоянные составы часто используется для определения азеотропных или азеотропоподобных композиций.
- Азеотропная или азеотропоподобная композиция двух соединений может быть охарактеризована путем определения составов, свойственных точке кипения при данном давлении, с получением, таким образом, идентифицирующих характеристик без ограничения ненадлежащим образом объема изобретения посредством конкретного количественного состава, что ограничивается и является единственно точным как доступное аналитическое средство.
Известно из уровня техники, что как точка кипения, так и массовые (или мольные) проценты каждого компонента азеотропной композиции могут изменяться, когда азеотропной или азеотропоподобной композиции позволяют кипеть при различных значениях давления. Таким образом, азеотропная или азеотропоподобная композиция может быть определена по уникальному соотношению, которое существует между компонентами или по точным массовым (или мольным) процентам каждого компонента композиции, характеризующейся определенной точкой кипения при конкретном давлении.
Используемый в настоящем описании термин «азеотроп» относится к азеотропным композициям и/или азеотропоподобным композициям.
Под азеотропообразователем подразумевается любое соединение, которое, когда добавляется к первой смеси, образует один или более азеотропов с компонентами смеси для облегчения разделения компонентов смеси. Используемые в настоящем описании термины «азеотропообразователь» и «азеотропообразующий агент» используются взаимозаменяемо и должны пониматься как имеющие идентичное значение.
Технологическое оборудование для всех процессов, раскрытых в настоящем описании, и присоединенные трубопроводы, канализационные линии и вспомогательные устройства могут быть сконструированы из материалов, устойчивых к фтороводороду. Обычные строительные материалы, хорошо известные из уровня техники, включают нержавеющие стали, в частности, аустенитного типа, и хорошо известные сплавы с высоким содержанием никеля, такие как медно-никелевые сплавы Monel®, сплавы на основе никеля Hastelloy® и хромоникелевые сплавы Inconel®.
Под азеотропной дистилляцией подразумевается процесс, в котором дистилляционная колонна работает в условиях, которые обусловливают формирование одной или нескольких азеотропных или азеотропоподобных композиций и, таким образом, облегчают разделение компонентов смеси. Азеотропная дистилляция может протекать там, где дистиллируются только компоненты смеси, которые разделяются, или где добавляется азеотропообразователь, что приводит к образованию азеотропа с одним или несколькими компонентами первоначальной смеси. Азеотропообразователи, которые действуют таким образом, то есть которые образуют азеотроп с одним или несколькими компонентами смеси, которую разделяют, облегчая, таким образом, разделение этих компонентов путем дистилляции, обычно называют азеотропообразующие агенты или азеотропообразователи.
В обычной или азеотропной дистилляции верхний или дистиллятный поток, выходящий с колонны, может конденсироваться с применением традиционных обратных конденсаторов (дефлегматоров). По меньшей мере часть данного конденсированного потока может быть возвращена в верхнюю часть колонны в качестве флегмы, а оставшаяся часть выделена в качестве продукта или для необязательной обработки. Отношение конденсированного вещества, которое возвращается в верхнюю часть колонны в качестве флегмы, к продукту, который удаляется в качестве дистиллята, обычно называется флегмовым числом. Соединения и азеотропообразователь, покидающие колонну как дистиллят или поток кубового остатка дистилляции, могут затем быть пропущены через отпарную колонну или вторую дистилляционную колонну с применением обычной дистилляции или могут быть разделены другими методами, такими как декантация. Если необходимо, азеотропообразователь может быть возвращен обратно в первую дистилляционную колонну для повторного применения.
Конкретные условия, которые могут применяться для осуществления изобретения, зависят от ряда параметров, таких как диаметр дистилляционной колонны, точки подачи питания, число ступеней разделения (теоретических тарелок) в колонне, среди прочих. В одном примере осуществления изобретения рабочее давление дистилляционной системы может варьировать от приблизительно 5 до 500 фунт/кв.дюйм (34,47-3447,4 кПа), в другом примере осуществления изобретения приблизительно 20-400 фунт/кв.дюйм (137,9-2757,9 кПа). Обычно увеличение флегмового числа приводит в результате к увеличению чистоты потока дистиллята, но традиционно флегмовое число колеблется между 1/1 и 200/1. Температура конденсатора, который расположен по соседству с верхней частью колонны, обычно является достаточной для по существу полного конденсирования дистиллята, который выходит с верхней части колонны, или является температурой, требуемой для достижения желаемого флегмового числа при частичной конденсации.
Проблемы, связанные с обычной дистилляцией, могут быть решены путем процесса дистилляции с применением азеотропообразователей. Трудность применения данного способа состоит в том, что не существует известного пути, короткого эксперимента, предсказания, какое из того или иного соединения было бы эффективным азеотропообразователем.
Как используется в настоящем описании, «по существу свободный» означает, что композиция содержит менее приблизительно 100 млн.д. (исходя из молей), менее приблизительно 10 млн.д. или менее приблизительно 1 млн.д. указанного компонента. Если композиция является по существу свободной более чем от одного компонента, то общая концентрация этих компонентов составляет менее приблизительно 100 млн.д., менее приблизительно 10 млн.д. или менее приблизительно 1 млн.д.
Используемые в настоящем описании термины «содержит», «содержащий», «включает», «включающий», «имеет», «имеющий» или любые другие их вариации имеют целью охватывать неисключительное указание. Например, процесс, метод, изделие или оборудование, которые содержат ряд элементов, необязательно ограничиваются только этими элементами, но могут включать другие элементы, которые не являются специально перечисленными или присущими такому процессу, методу, изделию или оборудованию. Дополнительно, если специально не указано обратное, «или» относится к охватывающему или, а не к исключающему или. Например, условие A или B удовлетворяет любому одному из следующих: A является правильным (или действительным) и B является ложным (или недействительным), A является ложным (или недействительным) и B является правильным (или действительным), и оба A и B являются правильными (или действительными).
Также, применение "a" или "an" используется для описания элементов и компонентов, описанных в настоящем описании. Они предназначены только для удобства и дают общее ощущение объема изобретения. Данное описание следует понимать в том смысле, что включает один или по меньшей мере один, и единственное число также включает множественное число, если не очевидно, что подразумевается другое.
Номера групп, соответствующие колонкам в Периодической Таблице элементов, применяются в соответствии с конвенцией "New Notation", что представлено в CRC Handbook of Chemistry and Physics, 81st Edition (2000-2001).
Фтороводород (HF, безводный) является коммерчески доступным химическим соединением и может быть получен методами, известными из уровня техники.
Термин «фторолефин» имеет целью подразумевать соединение, содержащее углерод и фтор и необязательно водород, которое дополнительно содержит по меньшей мере одну двойную связь.
В одном примере осуществления изобретения фторолефины включают соединения с 2-12 атомами углерода, в другом примере осуществления изобретения фторолефины включают соединения с 3-10 атомами углерода и в еще одном примере осуществления изобретения фторолефины включают соединения с 3-7 атомами углерода. Иллюстративные фторолефины включают, но не ограничиваясь этим, все соединения, перечисленные в таблице 1, таблице 2 и таблице 3.
Настоящее изобретение обеспечивает фторолефины с формулой E- или Z-R1CH=CHR2 (формула I), где R1 и R2 независимо представляют собой C1-C6перфторалкильные группы. Примеры R1 и R2 групп включают, но не ограничиваясь этим, CF3, C2F5, CF2CF2CF3, CF(CF3)2, CF2CF2CF2CF3, CF(CF3)CF2CF3, CF2CF(CF3)2, C(CF3)3, CF2CF2CF2CF2CF3, CF2CF2CF(CF3)2, C(CF3)2C2F5, CF2CF2CF2CF2CF2CF3, CF(CF3) CF2CF2C2F5 и C(CF3)2CF2C2F5. В одном примере осуществления изобретения фторолефины формулы I имеют по меньшей мере 4 атома углерода в молекуле. В другом примере осуществления изобретения фторолефины формулы I имеют по меньшей мере 5 атомов углерода в молекуле. Иллюстративные неограничивающие соединения формулы I представлены в таблице 1.
| Таблица 1 | ||
| Код | Структура | Химическое название |
| F11E | CF3CH=CHCF3 | 1,1,1,4,4,4-гексафторбут-2-ен |
| F12E | CF3CH=CHC2F5 | 1.1,1,4,4,5,5,5-октафторпент-2-ен |
| F13E | CF3CH=CHCF2C2F5 | 1,1,1,4,4,5,5,6,6,6-декафторгекс-2-ен |
| F13iE | CF3CH=CHCF(CF3)2 | 1,1,1,4,5,5,5-гептафтор-4-(трифторметил)пент-2-ен |
| F22E | C2F5CH=CHC2F5 | 1,1,1,2,2,5,5,6,6,6-декафторгекс-3-ен |
| F14E | CF3CH=CH(CF2)3CF3 | 1,1,1,4,4,5,5,6,6,7,7,7-додекафторгепт-2-ен |
| F14iE | CF3CH=CHCF2CF-(CF3)2 | 1,1,1,4,4,5,6,6,6-нонафтор-5-(трифторметил)гекс-2-ен |
| F14sE | CF3CH=CHCF(CF3)-C2F5 | 1,1,1,4,5,5,6,6,6-нонфтор-4-(трифторметил)гекс-2-ен |
| F14tE | CF3CH=CHC(CF3)3 | 1,1,1,5,5,5-гексафтор-4,4-бис(трифторметил)пент-2-ен |
| F23E | C2F5CH=CHCF2C2F5 | 1,1,1,2,2,5,5,6,6,7,7,7-додекафторгепт-3-ен |
| F23iE | C2F5CH=CHCF(CF3)2 | 1,1,1,2,2,5,6,6,6-нонафтор-5-(трифторметил)гекс-3-ен |
| F15E | CF3CH=CH(CF2)4CF3 | 1,1,1,4,4,5,5,6,6,7,7,8,8,8-тетрадекафторокт-2-ен |
| F15iE | CF3CH=CH-CF2CF2CF(CF3)2 | 1,1,1,4,4,5,5,6,7,7,7-ундекафтор-6-(трифторметил)гепт-2-ен |
| F15tE | CF3CH=CH-C(CF3)2C2F5 | 1,1,1,5,5.6,6,6-октафтор-4,4-бис(трифторметил)гекс-2-ен |
| F24E | C2F5CH=CH(CF2)3CF3 | 1,1,1,2,2,5,5,6,6,7,7,8,8,8-тетрадекафторокт-3-ен |
| F24iE | C2F5CH=CHCF2CF-(CF3)2 | 1,1,1,2,2,5,5,6,7,7,7-ундекафтор-6-(трифторметил)гепт-3-ен |
| F24sE | C2F5CH=CHCF(CF3)-C2F5 | 1,1,1,2,2,5,6,6,7,7,7-ундекафтор-5-(трифторметил)гепт-3-ен |
| F24tE | C2F5CH=CHC(CF3)3 | 1,1,1,2,2,6,6,6-октафтор-5,5-бис(трифторметил)гекс-3-ен |
| F33E | C2F5CF2CH=CH-CF2C2F5 | 1,1,1,2,2,3,3,6,6,7,7,8,8,8-тетрадекафторокт-4-ен |
| F3i3iE | (CF3)2CFCH=CH-CF(CF3)2 | 1,1,1,2,5,6,6,6-октафтор-2,5-бис(трифторметил)гекс-3-ен |
| F33iE | C2F5CF2CH=CH-CF(CF3)2 | 1,1,1,2,5,5,6,6,7,7,7-ундекафтор-2-(трифторметил)гепт-3-ен |
| F16E | CF3CH=CH(CF2)5CF3 | 1,1,1,4,4,5,5,6,6,7,7,8,8,9,9,9-гексадекафторнон-2-ен |
| F16sE | CF3CH=CHCF(CF3)(CF2)2C2F5 | 1,1,1,4,5,5,6,6,7,7,8,8,8-тридекафтор-4-(трифторметил)гепт-2-ен |
| F16tE | CF3CH=CHC(CF3)2CF2C2F5 | 1,1,1,6,6,6-октафтор-4,4-бис(трифторметил)гепт-2-ен |
| F25E | C2F5CH=CH(CF2)4CF3 | 1,1,1,2,2,5,5,6,6,7,7,8,8,9,9,9-гексадекафторнон-3-ен |
| F25iE | C2F5CH=CH-CF2CF2CF(CF3)2 | 1,1,1,2,2,5,5,6,6,7,8,8,8-тридекафтор-7-(трифторметил)окт-3-ен |
| F25tE | C2F5CH=CH-C(CF3)2C2F5 | 1,1,1,2,2,6,6,7,7,7-декафтор-5,5-бис(трифторметил)гепт-3-ен |
| F34E | C2F5CF2CH=CH-(CF2)3CF3 | 1,1,1,2,2,3,3,6,6,7,7,8,8,9,9,9-гексадекафторнон-4-ен |
| F34iE | C2F5CF2CH=CH-CF2CF(CF3)2 | 1,1,1,2,2,3,3,6,6,7,8,8,8-тридекафтор-7-(трифторметил)окт-4-ен |
| F34sE | C2F5CF2CH=CH-CF(CF3)C2F5 | 1,1,1,2,2,3,3,6,7,7,8,8,8-тридекафтор-6-(трифторметил)окт-4-ен |
| F34tE | C2F5CF2CH=CH-C(CF3)3 | 1,1,1,5,5,6,6,7,7,7-декафтор-2,2-бис(трифторметил)гепт-3-ен |
| F3i4E | (CF3)2CFCH=CH-(CF2)3CF3 | 1,1,1,2,5,5,6,6,7,7,8,8,8-тридекафтор-2-(трифторметил)окт-3-ен |
| F3i4iE | (CF3)2CFCH=CH-CF2CF(CF3)2 | 1,1,1,2,5,5,6,7,7,7-декафтор-2,6-бис(трифторметил)гепт-3-ен |
| F3i4sE | (CF3)2CFCH=CH-CF(CF3)C2F5 | 1,1,1,2,5,6,6,7,7,7-декафтор-2,5-бис(трифторметил)гепт-3-ен |
| F3i4tE | (CF3)2CFCH=CH-C(CF3)3 | 1,1,1,2,6,6,6-гептафтор-2,5,5-трис(трифторметил)гекс-3-ен |
| F26E | C2F5CH=CH(CF2)5CF3 | 1,1,1,2,2,5,5,6,6,7,7,8,8,9,9,10,10,10-октадекафтордец-3-ен |
| F26sE | C2F5CH=CHCF(CF3)(CF2)2C2F5 | 1,1,1,2,2,5,6,6,7,7,8,8,9,9,9-пентадекафтор-5-(трифторметил)нон-3-ен |
| F26tE | C2F5CH=CHC(CF3)2CF2C2F5 | 1,1,1,2,2,6,6,7,7,8,8,8-додекафтор-5,5-бис(трифторметил)окт-3-ен |
| F35E | C2F5CF2CH=CH-(CF2)4CF3 | 1,1,1,2,2,3,3,6,6,7,7,8,8,9,9,10,10,10-октадекафтордец-4-ен |
| F35iE | C2F5CF2CH=CH-CF2CF2CF(CF3)2 | 1,1,1,2,2,3,3,6,6,7,7,8,9,9,9-пентадекафтор-8-(трифторметил)нон-4-ен |
| F35tE | C2F5CF2CH=CH-C(CF3)2C2F5 | 1,1,1,2,2,3,3,7,7,8,8,8-додекафтор-6,6-бис(трифторметил)окт-4-ен |
| F3i5E | (CF3)2CFCH=CH-(CF2)4CF3 | 1,1,1,2,5,5,6,6,7,7,8,8,9,9,9-пентадекафтор-2-(трифторметил)нон-3-ен |
| F3i5iE | (CF3)2CFCH=CH-CF2CF2CF(CF3)2 | 1,1,1,2,5,5,6,6,7,8,8,8-додекафтор-2,7-бис(трифторметил)окт-3-ен |
| F3i5tE | (CF3)2CFCH=CH-C(CF3)2C2F5 | 1,1,1,2,6,6,7,7,7-нонафтор-2,5,5-трис(трифторметил)гепт-3-ен |
| F44E | CF3(CF2)3CH=CH-(CF2)3CF3 | 1,1,1,2,2,3,3,4,4,7,7,8,8,9,9,10,10,10-октадекафтордец-5-ен |
| F44iE | CF3(CF2)3CH=CH-CF2CF(CF3)2 | 1,1,1,2,3,3,6,6,7,7,8,8,9,9,9-пентадекафтор-2-(трифторметил)нон-4-ен |
| F44sE | CF3(CF2)3CH=CH-CF(CF3)C2F5 | 1,1,1,2,2,3,6,6,7,7,8,8,9,9,9-пентадекафтор-3-(трифторметил)нон-4-ен |
| F44tE | CF3(CF2)3CH=CH-C(CF3)3 | 1,1,1,5,5,6,6,7,7,8,8,8-додекафтор-2,2-бис(трифторметил)окт-3-ен |
| F4i4iE | (CF3)2CFCF2CH=CH-CF2CF(CF3)2 | 1,1,1,2,3,3,6,6,7,8,8,8-додекафтор-2,7-бис(трифторметил)окт-4-ен |
| F4i4sE | (CF3)2CFCF2CH=CH-CF(CF3)C2F5 | 1,1,1,2,3,3,6,7,7,8,8,8-додекафтор-2,6-бис(трифторметил)окт-4-ен |
| F4i4tE | (CF3)2CFCF2CH=CH-C(CF3)3 | 1,1,1,5,5,6,7,7,7-нонафтор-2,2,6-трис(трифторметил)гепт-3-ен |
| F4s4sE | C2F5CF(CF3)CH=CH-CF(CF3)C2F5 | 1,1,1,2,2,3,6,7,7,8,8,8-додекафтор-3,6-бис(трифторметил)окт-4-ен |
| F4s4tE | C2F5CF(CF3)CH=CH-C(CF3)3 | 1,1,1,5,6,6,7,7,7-нонафтор-2,2,5-трис(трифторметил)гепт-3-ен |
| F4t4tE | (CF3)3CCH=CH-C(CF3)3 | 1,1,1,6,6,6-гексафтор-2,2,5,5-тетракис(трифторметил)гекс-3-ен |
Соединения формулы I могут быть получены путем контактирования перфторалкилйодида формулы R1I с перфторалкилтригидроолефином формулы R2CH=CH2 с образованием тригидройодперфторалкана формулы R1CH2CHIR2. Данный тригидройодперфторалкан может затем быть подвергнут дегидройодированию с образованием R1CH=CHR2. Альтернативно, олефин R1CH=CHR2 может быть получен дегидройодированием тригидройодперфторалкана формулы R1CHICH2R2, полученного, в свою очередь, путем взаимодействия перфторалкилйодида формулы R2I с перфторалкилтригидроолефином формулы R1CH=CH2.
Указанное контактирование перфторалкилйодида с перфторалкилтригидроолефином может быть произведено в периодическом режиме путем сочетания реагентов в подходящем реакционном сосуде, способном функционировать при возникающем давлении реагентов и продуктов при температуре реакции. Подходящие реакционные сосуды включают произведенные из нержавеющих сталей, в частности аустенитного типа, и хорошо известных сплавов с высоким содержанием никеля, таких как медно-никелевые сплавы Monel®, сплавы на основе никеля Hastelloy® и хромоникелевые сплавы Inconel®.
Альтернативно, реакция может быть произведена в полупериодическом режиме, в которой реагент перфторалкилтригидроолефин добавляют к реагенту перфторалкилйодиду посредством подходящего для добавления устройства, такого как насос, при температуре реакции.
Отношение перфторалкилйодида к перфторалкилтригидроолефину должно быть между приблизительно 1:1 и приблизительно 4:1, предпочтительно от приблизительно 1,5:1 до 2,5:1. Отношения менее 1,5:1 имеют тенденцию приводить в результате к большому количеству 2:1 аддукта, как сообщается Jeanneaux et al. в Journal of Fluorine Chemistry, Vol. 4, pages 261-270 (1974).
Предпочтительные температуры для контактирования указанного перфторалкилйодида с указанным перфторалкилтригидроолефином находятся предпочтительно в интервале приблизительно 150°C - 300°C, предпочтительно, от приблизительно 170°C до приблизительно 250°C и, наиболее предпочтительно, от приблизительно 180°C до приблизительно 230°C.
Приемлемое время контактирования при взаимодействии перфторалкилйодида с перфторалкилтригидроолефином составляет от приблизительно 0,5 часа до 18 часов, предпочтительно, от приблизительно 4 до приблизительно 12 часов.
Тригидройодперфторалкан, полученный взаимодействием перфторалкилйодида с перфторалкилтригидроолефином, может применяться непосредственно на стадии дегидройодирования или может предпочтительно быть выделен и очищен путем дистилляции перед стадией дегидройодирования. Стадия дегидройодирования протекает при контактировании тригидройодперфторалкана с основанием. Приемлемые основания включают гидроксиды щелочных металлов (например, гидроксид натрия или гидроксид калия), оксид щелочного металла (например оксид натрия), гидроксиды щелочноземельных металлов (например гидроксид кальция), оксиды щелочноземельных металлов (например оксид кальция), алкоголяты щелочных металлов (например метилат натрия или этилат натрия), водный раствор аммиака, амид натрия или смеси основных веществ, такие как натронная известь. Предпочтительными основаниями являются гидроксид натрия и гидроксид калия.
Указанное контактирование тригидройодперфторалкана с основанием может протекать в жидкой фазе предпочтительно в присутствии растворителя, способного к растворению по меньшей мере части обоих реагентов. Растворители, приемлемые для стадии дегидройодирования, включают один или несколько полярных органических растворителей, таких как спирты (например, метанол, этанол, н-пропанол, изопропанол, н-бутанол, изобутанол и третичный бутанол), нитрилы (например, ацетонитрил, пропионитрил, бутиронитрил, бензонитрил или адипонитрил), диметилсульфоксид, N,N-диметилформамид, N,N-диметилацетамид или сульфолан. Выбор растворителя может зависеть от точки кипения продукта и легкости отделения следов растворителя от продукта в течение очистки. Обычно хорошими растворителями для этой реакции являются этанол или изопропанол.
Обычно реакция дегидройодирования может протекать при добавлении одного из реагентов (либо основания, либо тригидройодперфторалкана) к другому реагенту в подходящем реакционном сосуде. Указанный реакционный сосуд может быть изготовлен из стекла, керамики или металла и реакция предпочтительно перемешивается с помощью мешалки или перемешивающего механизма.
Приемлемые для реакции дегидройодирования температуры составляют от приблизительно 10°C до приблизительно 100°C, предпочтительно, от приблизительно 20°C до приблизительно 70°C. Реакция дегидройодирования может протекать при атмосферном давлении или пониженном или повышенном давлении. Известны реакции дегидройодирования, в которых соединение формулы I отгоняется из реакционного сосуда по мере его образования.
Альтернативно, реакция дегидройодирования может быть проведена путем контактирования водного раствора указанного основания с раствором тригидройодперфторалкана в одном или нескольких органических растворителях с низкой полярностью, таких как алкан (например, гексан, гептан или октан), ароматический углеводород (например толуол), галогенированный углеводород (например, метиленхлорид, хлороформ, четыреххлористый углерод или перхлорэтилен) или простой эфир (например, диэтиловый эфир, метил-трет-бутиловый эфир, тетрагидрофуран, 2-метилтетрагидрофуран, диоксан, диметоксиэтан, диглим или тетраглим), в присутствии катализатора межфазного переноса. Приемлемые катализаторы межфазного переноса включают галоидные соли четвертичного аммония (например, бромид тетрабутиламмония, гидросульфат тетрабутиламмония, хлорид триэтилбензиламмония, хлорид додецилтриметиламмония и хлорид трикаприлилметиламмония), галоидные соли четвертичного фосфония (например, бромид трифенилметилфосфония и хлорид тетрафенилфосфония) или циклические полиэфирные соединения, известные из уровня техники как краун-эфиры (например, 18-краун-6 и 15-краун-5).
Альтернативно, реакция дегидройодирования может быть проведена в отсутствие растворителя при добавлении тригидройодперфторалкана к твердому или жидкому основанию.
Приемлемое время реакции дегидройодирования составляет от приблизительно 15 минут до приблизительно 6 часов или более, в зависимости от растворимости реагентов. Обычно реакция дегидройодирования протекает быстро и требует приблизительно 30 минут - приблизительно три часа для завершения.
Соединение формулы I может быть выделено из смеси реакции дегидройодирования путем разделения фаз после добавления воды, путем дистилляции или при их комбинации.
В другом примере осуществления настоящего изобретения фторолефины включают циклические ненасыщенные фторуглероды (цикло-[CX=CY(CZW)n-] (формула II), где X, Y, Z и W выбирают независимо из H и F и n является целым числом от 2 до 5). В одном примере осуществления фторолефины формулы II имеют по меньшей мере приблизительно 3 атома углерода в молекуле. В другом примере осуществления фторолефины формулы II имеют по меньшей мере приблизительно 4 атома углерода в молекуле. В еще другом примере осуществл