(3r,4r,5s)-5-амино-4-ациламино-3-(1-этил-пропокси)-циклогекс-1-ен-карбоновые кислоты, их эфиры и способ применения
Иллюстрации
Показать всеИзобретение относится к новым замещенным (3R,4R,5S)-5-амино-4-ациламино-3-(1-этил-пропокси)-циклогекс-1-ен-карбоновым кислотам общей формулы 1, их эфирам, фармацевтически приемлемым солям и/или гидратам, обладающим противовирусной активностью, связанной с ингибированием нейраминидазы, в частности нейраминидазы вируса гриппа. Соединения могут найти применение при лечении вируса гриппа и пневмонии, обусловленной вирусом гриппа. Изобретение также относится к фармацевтическим композициям и лекарственному средству на их основе, способу ингибирования нейраминидазы и способу лечения гриппа и пневмонии, обусловленной вирусом гриппа. В общей формуле 1
R1 представляет собой водород, С1-С7алкил, С1-С7алкенил или С2-С7алкинил, необязательно замещенные С3-С6циклоалкилом, фенилом, пиридилом, C1-С3алкокси; R2 представляет собой водород; -NH2; С2Н5О-, замещенный С1-С5алкил, выбранный из -СН2ОН, -CH2-NH2, -СН=СН2, -СН=СНСl, -С=СН, -CH2F, -CHF2, -CF3, -CH2CF3, цикло-C3H7, -CF2CF2CF2CF3, -CF2CF2CF2CHF2, -CH2CF2CF2CF2CF3. 6 н. и 4 з.п. ф-лы, 3 табл., 33 пр.
Реферат
Данное изобретение относится к новым соединениям - замещенным 4,5-диамино-3-алкилокси-циклогекс-1-ен-карбоновым кислотам и их эфирам - ингибиторам активности нейраминидазы.
Многие из микроорганизмов, содержащих нейраминидазу, патогенны по отношению к человеку и другим животным, включая птицу, лошадей, cвиней и тюленей. Такие патогенные организмы включают вирус гриппа. Нейраминидаза связана с патогенностью вируса гриппа.
В этой связи новые замещенные 4,5-диамино-3-алкилокси-циклогекс-1-ен-карбоновые кислоты и их эфиры представляют интерес в качестве лекарственных субстанций для препаратов, предназначенных для профилактики и лечения гриппа.
Наиболее известными ингибиторами нейраминидазы являются (3R,4R,5S)-5-амино-3-алкилокси-4-ацетиламино-циклогекс-1-ен-карбоновые кислоты общей формулы А1, причем наиболее активной из них является (3R,4R,5S)-5-амино-4-ацетиламино-3-(1-этил-пропокси)-циклогекс-1-ен-карбоновая кислота формулы А2, которая, на основании рентгеноструктурных данных ее комплекса с нейраминидазой вируса гриппа, эффективно связывается с активным центром фермента (Oseltamivir Carboxylate) [С.U.Kim, W.Lew, M.A.Williams, et al. J.Am.Chem. Soc. 1997, 119, 681-690.].
Этиловый эфир озельтамивир карбоксилата A3, известный как озельтамивир фосфат или Тамифлю (Oseltamivir Phosphate, Tamiflu) [J.С.Rohloff, К.M.Kent, М.J.Postich, et al. J. Org. Chem. 1998, 63, 4545.], является предшественником кислоты A2 и известным противогриппозным препаратом [https://integrity.thomson-pharma.com/].
R=H, C1-C7 алкил
В источнике RU 2181357 (публикация международной заявки WO 1996026933) используются соединения общей формулы А
где, среди прочего, (а) Е1 означает -СО2Н; G1 означает -N(H)(C(NH)(NH2)); Т1 означает -N(H)(Ac); U1 означает -CH2OH; (b) Е1 означает -СО2Н; G1 означает -NH2; Т1 означает -N(H)(Ac); U1 означает -CH2OH; (с) Е1 означает -СН2ОН, -CH2OTMS, -CO2H или -СНО; G1 означает -N3; Т1 означает -N(H)(Ac); и U1 означает -CH2OCH2Ph; (d) E1 означает -CO2H или -CO2CH3; G1 означает -NH3; Т1 означает -N(H)(Ac); и U1 означает -СН2ОН.
Получаемые соединения используются в качестве ингибиторов вирусных или бактериальных нейраминидаз, для лечения или профилактики инфекции вируса гриппа, Исследования in vitro проводились согласно описанным методикам тестов (например, Warner and O'Brien, Biochemistry, vol 18, No 13, pp.2783-2787, 1979). Авторы RU 2181357 проводили испытания на разбавленных растворах вирусов, а активность измеряли по флуоресценции раствора. Экспериментальные данные ингибирующей активности приведены в Таблице 1.
| Таблица 1. | |
| Определение ферментингибирующей активности согласно RU №2181357. | |
| Соединение | пк50 |
| А2 | +++ |
| А4/А5 (2:1) | ++ |
| А6 | ++ |
| А7 | ++ |
| А8 | ++ |
| А9 | ++ |
| А10 | + |
| А11/А12 (1.2:1) | + |
| А13 | +++ |
| А14 | +++ |
| А15 | +++ |
ПК50 - концентрация соединения, при которой наблюдается 50% ингибирование ферментативной активности (+соответствует ПК50=10-100 мкмоль, ++1-10 мкмоль, +++<1,0 мкмоль).
При осуществлении изобретения, описанного в RU №2181357, в примерах осуществления изобретения значение Т1 представляет собой преимущественно -NHC(O)CH3, и при этом не указывается на получение и свойства соединений со значением T1 -NHC(O)CH2F, -NHC(O)CHF2, -NHC(O)CF3.
Поиск высокоэффективных противогриппозных лекарственных препаратов, обладающих повышенной активностью и пониженной токсичностью, по-прежнему является одним из основных направлений создания новых фармакологических средств для лечения гриппа. В этой связи актуальным является разработка новых противогриппозных субстанций, фармацевтических композиций и лекарственных препаратов, а также способов их получения и применения.
Ниже приведены определения терминов, которые использованы в описании этого изобретения.
«Алкенил» означает алифатическую линейную или разветвленную углеводородную группу, содержащую от 2 до 7 атомов углерода и включающую по крайней мере одну углерод-углеродную двойную связь.
Разветвленная означает, что к линейной алкенильной цепи присоединены один или несколько низших алкильных групп, таких как метил, этил или пропил. Алкильная группа может иметь один или несколько заместителей, например, таких как галоген, алкенилокси, циклоалкил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероаралкилокси, гетероциклил, гетероциклилалкилокси, алкоксикарбонил, аралкоксикарбонил, гетроаралкилоксикарбонил или
где и независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или и вместе с атомом N, с которым они связаны, образуют через и 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбнилметил. Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил, и циклогексилбутенил.
«Алкенилокси» означает алкенил-О-группу, в которой алкенил определен в данном разделе. Предпочтительными алкенилоксигруппами являются аллилокси и 3-бутенилокси.
«Алкенилоксиалкил» означает алкенил-О-алкилгруппу, в которой алкил и алкенил определены в данном разделе.
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «низших алкильных» заместителей. Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей»), включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбнил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонилгетероаралкилокси, аннелированный гетероарил цикл оалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или
где и независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или и вместе с атомом N, с которым они связаны, образуют через и 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил метоксикарбонилметил и пиридилметилоксикарбнилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Алкинил» означает алифатическую линейную или разветвленную углеводородную группу, содержащую от 2 до 12 атомов углерода и включающую по крайней мере одну углерод-углеродную тройную связь.
Разветвленная означает, что к линейной алкинильной цепи присоединены один или несколько низших алкильных групп, таких как метил, этил или пропил. Алкильная группа может иметь один или несколько заместителей, например, таких как галоген, алкенилокси, циклоалкил, циано, гидрокси, алкокси, лкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероаралкилокси, гетероциклил, гетероциклилалкилокси, алкоксикарбонил, аралкоксикарбонил, гетроаралкилоксикарбонил или где и независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или и вместе с атомом N, с которым они связаны, образуют через и 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбнилметил, бензилоксикарбонилметил и пиридилметилоксикарбнилметил. Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил, бута-1,3-диин и гекса-1,3,5-триин.
«Алкокси» означает алкил-О-группу, в которой алкил определен в данном разделе. Предпочтительным алкилоксигруппами являются метокси, этокси, н-пропокси, изо-пропокси и н-бутокси.
«Арил» означает ароматическую моноциклическую или полициклическую систему, включающую от 6 до 14 атомов углерода, преимуществено от 6 до 10 атомов углерода. Арил может содержать один или более «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями арильных групп являются фенил или нафтил, замещенный фенил или замещенный нафтил. Арил может быть анелирован с неароматической циклической системой или гетероциклом.
«Гетероциклил» означает ароматическую или неароматическую насыщенную моноциклическую или полициклическую систему, включающую от 3 до 10 атомов углерода, преимущественно от 5 до 6 атомов углерода, в которой один или несколько атомов углерода заменены на гетероатом, такой как азот, кислород, сера. Приставка «аза», «окса» или «тиа» перед гетероциклилом означает наличие в циклической системе атома азота, атома кислорода или атома серы соответственно. Гетероциклил может иметь один или несколько «заместителей циклической системы», которые могут быть одинаковыми или разными. Атомы азота и серы, находящиеся в гетероциклиле, могут быть окислены до N-оксида, S-оксида или S-диоксида. Представителями гетероциклилов являются пиперидин, пирролидин, пиперазин, морфолин, тиоморфолин, тиазолидин, 1,4-диоксан, тетрагидрофуран, тетрагидротиофен и др.
«Гидрат» означает сольват, в котором вода является молекулой или молекулами растворителя.
«Заместитель» означает химический радикал, который присоединяется к скэффолду (фрагменту), например «заместитель алкильный», «заместитель аминогруппы», «заместитель карбамоильный», «заместитель циклической системы», значения которых определены в данном разделе.
«Лекарственное начало» (лекарственная субстанция) (лекарственное вещество), drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток капсул инъекций, мазей и др. готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
Нейраминидаза (сиалидаза, ацилнейраминил гидролаза и ЕС 3.2.1.18) является обычным для животных и ряда микроорганизмов ферментом. Она представляет собой гликогидролазу, которая отщепляет альфакетосидикально связанные сиаловые кислоты от гликопротеинов, гликолипидов и олигосахаридов. Многие из микроорганизмов, содержащих нейраминидазу, патогенны по отношению к человеку и другим животным, включая птицу, лошадей, свиней и тюленей. Такие патогенные организмы включают вирус гриппа. Нейраминидаза связана с патогенностью вируса гриппа. Предположительно она содействует элюированию вновь синтезированных вирионов из инфицированных клеток и движению вируса (благодаря ее гидролазной активности) через слизь респираторного тракта.
«Низший алкил» означает линейный или разветвленный алкил с 1-5 атомами углерода.
«Терапевтический коктейль» представляет одновременно администрируемую комбинацию двух и более лекарственных препаратов, обладающих различным механизмом фармакологического действия и направленных на различные биомишени, участвующие в патогенезе заболевания.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение формулы 1 и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлимых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как, парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как, холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
Авторы обнаружили новые ингибиторы нейраминидазы, представляющие собой неизвестные ранее (3R,4R,5S)-5-амино-4-ациламино-3-(1-этил-пропокси)-циклогекс-1-ен-карбоновые кислоты и их эфиры общей формулы 1 и их фармацевтически приемлемые соли или гидраты,
где R1 представляет собой водород, С1-С7алкил, С2-С7алкенил или С2-С7алкинил, необязательно замещенные С3-С6циклоалкилом, фенилом, пиридилом, C1-С3алкокси;
R2 представляет собой водород; -NH2; С2Н5О-; замещенный C1-С3алкил, выбранный из -СН2ОН, -CH2-NH2, -СН=СН2, -СН=CHCl, -С≡СН, -CH2F, -CHF2, -CF3, -CH2CF3, цикло-C3H7, -CF2CF2CF2CF3, -CF2CF2CF2CHF2, -CH2CF2CF2CF2CF3.
Согласно данному изобретению предпочтительными соединениями являются кислоты общей формулы 1.1 и их эфиры общей формулы 1.2,
в которых R1 представляет собой С1-С5алкил, С3-С5алкенил или С3-С5алкинил, а R2 имеет вышеуказанное значение.
Согласно данному изобретению более предпочтительными соединениями являются
(3R,4R,5S)-5-амино-4-формиламино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.1,
(3R,4R,5S)-5-амино-4-(2-гидрокси-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.2,
(3R,4R,5S)-5-амино-4-(2-амино-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.3,
(3R,4R,5S)-4-акрилоиламино-5-амино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.4,
(3R,4R,5S)-5-амино-4-пропиноиламино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.5,
(3R,4R,5S)-5-амино-4-(2-фтор-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.6,
(3R,4R,5S)-5-амино-4-(2,2-дифтор-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен карбоновая кислота 1.1.7,
(3R,4R,5S)-5-амино-4-(2,2,2-трифтор-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.8,
(3R,4E,5S)-5-амино-4-(3,3,3-трифтор-пропиониламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.9,
(3R,4R,5S)-5-амино-4-(2,2,3,3,4,4,5,5-октафтор-пентаноиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.10,
(3R,4R,5S)-5-амино-4-(2,2,3,3,4,4,5,5,5-нонафтор-пентаноиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.11,
(3R,4R,5S)-5-амино-4-(2,2,3,3,4,4,5,5,6,6,6-ундекафтор-гексаноиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.12,
(3R,4R,5S)-5-амино-4-(циклопропилкарбонил-амино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.14,
(3R,4R,5S)-5-амино-4-(этоксикарбонил-амино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.15,
(3R,4R,5S)-5-амино-4-уреидо-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.16,
(3R,4R,5S)-4-(3-хлорпроп-2-еноил-амино)-5-амино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновая кислота 1.1.17,
этиловый эфир (3R,4R,5S)-5-амино-4-формиламино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.1,
этиловый эфир (3R,4R,5S)-5-амино-4-(2-гидрокси-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.2,
этиловый эфир (3R,4R,5S)-5-амино-4-(2-амино-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.3,
этиловый эфир (3R,4R,5S)-4-акрилоиламино-5-амино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.4,
этиловый эфир (3R,4R,5S)-5-амино-4-пропиноиламино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.5,
этиловый эфир (3R,4R,5S)-5-амино-4-(2-фтор-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.6,
этиловый эфир (3R,4R,5S)-5-амино-4-(2,2-дифтор-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.7,
этиловый эфир (3R,4R,5S)-5-амино-4-(2,2,2-трифтор-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.8,
этиловый эфир (3R,4R,5S)-5-амино-4-(3,3,3-трифтор-пропиониламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.9,
этиловый эфир (3R,4R,5S)-5-амино-4-(2,2,3,3,4,4,5,5-октафтор-пентаноиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.10,
этиловый эфир (3R,4R,5S)-5-амино-4-(2,2,3,3,4,4,5,5,5-нонафтор-пентаноиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.11,
этиловый эфир (3R,4R,5S)-5-амино-4-(2,2,3,3,4,4,5,5,6,6,6-ундекафтор-гексаноиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.12,
этиловый эфир (3R,4R,5S)-5-амино-4-(циклопропилкарбониламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.14,
этиловый эфир (3R,4R,5S)-5-амино-4-уреидо-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.15,
этиловый эфир (3R,4R,5S)-5-амино-4-(этоксикарбониламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.16,
этиловый эфир (3R,4R,5S)-4-(3-хлорпроп-2-еноил-амино)-5-амино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.17,
аллиловый эфир (3R,4R,5S)-5-амино-4-(2,2,2-трифтор-ацетиламино)-3-(-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.18,
проп-2-иниловый эфир (3R,4R,5S)-5-амино-4-(2,2,2-трифтор-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.2.19.
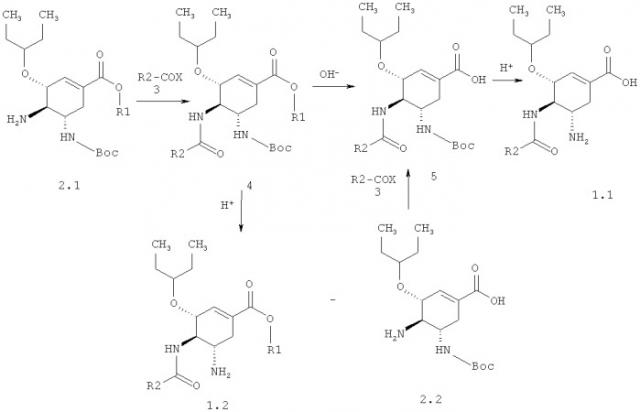
(3R,4R,5S)-5-амино-4-ациламино-3-(1-этил-пропокси)-циклогекс-1-ен-карбоновые кислоты и их эфиры общей формулы 1 получают по аналогии с синтезом известных соединений А2 и A3 [М.Morita et al. Bioorg. Med. Chem. Lett. 18, 600-602 (2008). F. Konno et al. Bioorg. Med. Chem. Lett. 18, 1260-1263 (2008)] по схеме, представленной ниже,
где R1 и R2 имеют вышеуказанное значение.
Новые замещенные 4,5-диамино-3-гидрокси-циклогекс-1-ен-карбоновые кислоты общей формулы 1 и их фармацевтически приемлемые соли и/или гидраты являются ингибиторами нейраминидазы и проявляют противогриппозную активность (Таблица 1).
Согласно данному изобретению новые соединения общей формулы 1 представляют собой лекарственное начало для приготовления фармацевтической композиции и готовых лекарственных форм для профилактики и лечения гриппа у теплокровных животных и людей.
Предметом данного изобретения является фармацевтическая композиция, включающая в качестве лекарственного начала соединения общей формулы 1 или их фармацевтически приемлемые соли и/или гидраты в терапевтически эффективном количестве.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемым эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция, наряду с соединением общей формулы 1 или их фармацевтически приемлемой солью и/или гидратом по настоящему изобретению, может включать и другие активные субстанции, в том числе обладающие противогриппозной активностью, при условии, что они не вызывают нежелательных эффектов.
При необходимости использования фармацевтической композиции по настоящему изобретению в клинической практике она может смешиваться с традиционными фармацевтическими носителями.
Носители, используемые в фармацевтических композиций по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в том числе в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, бесцветные агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Предметом данного изобретения является способ получения фармацевтической композиции смешением с инертным наполнителем и/или растворителем, по крайней мере, одного лекарственного начала общей формулы 1 или его фармацевтически приемлемой соли и/или гидрата в терапевтически эффективном количестве.
Предметом данного изобретения является также лекарственное средство для лечения гриппа в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, предназначенное для профилактики лечения гриппа у людей и теплокровных животных, включающее в свой состав противогриппозное лекарственное начало общей формулы 1 или новую фармацевтическую в терапевтически эффективном количестве.
Предметом данного изобретения являются также терапевтические коктейли для лечения гриппа, включающие в качестве одного из компонентов новое лекарственное средство или новую фармацевтическую композицию, содержащих в качестве активного компонента, по крайней мере, одно соединение общей формулы 1 или их фармацевтически приемлемую соль и/или гидрат.
Терапевтический коктейль для и лечения гриппа, наряду с лекарственным средством по данному изобретению, может включать другие известные препараты, предназначенные для лечения гриппа или препараты, усиливающие иммунную систему пациента.
В соответствии с данным изобретением способ профилактики и лечения гриппа у животных и людей заключается во введении пациенту нового лекарственного средства, новой фармацевтической композиции или нового терапевтического коктейля.
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно. Клиническая дозировка средства общей формулы 1 у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10~500 мг, предпочтительно 50~300 мг. Поэтому во время приготовления из фармацевтической композиции лекарственного средства по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10~500 мг средства общей формулы 1, предпочтительно 50~300 мг. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно от одного до шести раз).
Предметом данного изобретения является также способ ингибирования активности нейраминидазы в естественных условиях, в том числе нейраминидазы вируса гриппа, включающий стадию контактирования соединения общей формулы 1 и нейраминидазы.
Данное изобретение иллюстрируется, но не ограничивается следующими примерами.
Пример 1. Получение (3R,4R,5S)-5-амино-4-формиламино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.1. Растворили 250 мг (3R,4R,5S)-4-амино-5-(трет-бутоксикарбониламино)-3-(пентан-3-илокси)циклогекс-1-енкарбоновой кислоты 2.2 в 15 мл толуола, добавили 500 мг муравьиной кислоты и 1 г молекулярного сита 3А и кипятили реакционную массу с обратным холодильником в течение ночи. Затем реакционную массу отфильтровывали, осадок промывали этанолом, маточный раствор упаривали, сухой остаток растворяли в этилацетате, промывали 5% раствором соды, сушили над Mg2SO4 и затем упаривали. Очистку продукта реакции проводили методом HPLC. Получали (3R,4R,5S)-5-амино-4-формиламино-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.1: LSMS m/z 271 (М+1), C13H22N2O4.
Пример 2. Получение (3R,4R,5S)-5-амино-4-(2-гидрокси-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.2. К раствору 1000 мг (2.7 ммоль) исходного (3R,4R,5S)-этил-4-амино-5-(трет-бутоксикарбониламино)-3-(пентан-3-илокси)циклогекс-1-енкарбоксилата 2.1, 620 мг (3.24 ммоль) гидрохлорида N-[3-(диметиламино)пропил]-N'-этилкарбодиимида, 438 мг (3.24 ммоль) гидроксибензотриазола и 1150 мг (8.92 ммоль) N,N-диизопропилэтиламина в 10 мл сухого ТГФ прибавили 247 мг (3.24 ммоль) 2-гидрокиуксусной кислоты. Реакционную массу перемешивали при комнатной температуре в течение ночи. По окончании реакции растворитель отгоняли, сухой остаток растворяли в этилацетате, промывали 5% раствором соды, сушили над Mg2SO4 и затем упаривали. Получали этиловый эфир (3R,4R,5S)-4-(2-гидрокси-ацетиламино)-5-(трет-бутоксикарбониламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 4 (R1=Et, R2=СН2ОН) с выходом по данным LCMS 93%. Полученный продукт (100 мг) перемешивали в 1 мл 5% водного раствора гидроксида лития в течение 5-10 минут при комнатной температуре, затем растворитель отгоняли, остаток растворяли в диоксане, фильтровали, полученный раствор упаривали и сушили в вакууме. Получали кислоту 5 (R2=CH2OH), растворяли в 1 мл 3М раствора соляной кислоты в диоксане. Полученный раствор перемешивали при комнатной температуре до окончания реакции. Контроль за ходом реакции осуществляли методом HPLC. Продукт очищали методом HPLC. Получали (3R,4R,5S)-5-амино-4-(2-гидрокси-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновую кислоту 1.1.2: LSMS m/z 301 (М+1), C14H24N2O5.
Пример 3. Получение (3R,4R,5S)-5-амино-4-(2-амино-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновой кислоты 1.1.3. К раствору 500 мг (1.35 ммоль) исходного (3R,4R,5S)-этил-4-амино-5-(трет-бутоксикарбониламино)-3-(пентан-3-илокси)циклогекс-1-енкарбоксилата 2.1, 387 мг (2.027 ммоль) гидрохлорида N-[3-(диметиламино)пропил]-N'-этилкарбодиимида, 237 мг (1.76 ммоль) гидроксибензотриазола и 5 мл сухого ДМФА прибавляли 308 мг (1.76 ммоль) 2-(трет-бутоксикарбониламино)уксусной кислоты. Реакционную массу перемешивали при комнатной температуре в течение ночи. По окончании реакции растворитель отгоняли, сухой остаток растворяли в этилацетате, промыли 5% раствором соды, сушили над Mg2SO4 и затем упарили. Полученное соединение использовали в дальнейших реакциях без дополнительной очистки. Выход неочищенного продукта составил 604 мг. Щелочной гидролиз 4 (R1=Et, R2=CH2NH2) проводили, как описано в примере 2, а снятие Вос-защиты соединения 5 (R2=CH2NH2) проводили в трифторуксусной кислоте. Получали (3R,4R,5S)-5-амино-4-(2-амино-ацетиламино)-3-(1-этилпропокси)-циклогекс-1-ен-карбоновую кислоту в виде трифторацетата 1.1.3·CF3CO2H LSMS m/z 300 (М+1), C16H26F3N3O6.
Пример 4. Получение (3R,4R,5S)-4-акрилоиламино-5-амино-3-(1-этилпропокси)-циклогекс-1-ен-