Экспрессионная плазмидная днк pcid-proc, кодирующая протеин с человека, и клеточная линия dg-cid-proc-1, продуцирующая рекомбинантный протеин с человека
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, а именно к плазмидной ДНК pCID-PROC для экспрессии рекомбинантного протеина С человека, линии клеток яичника китайского хомячка DG-CID-PROC-1 и способу получения рекомбинантного протеина С человека. Предложенное изобретение может быть использовано для получения рекомбинантного протеина С человека. Плазмидная ДНК pCID-PROC для экспрессии рекомбинантного протеина С человека содержит последовательность полноразмерной кДНК гена протеина С человека, представленную в Перечне последовательностей как последовательность SEQ ID NO:1. Плазмидную ДНК pCID-PROC характеризуют физической картой, приведенной на Фиг.1. Линию клеток яичника китайского хомячка DG-CID-PROC-1 получают путем трансформации линии клеток яичника китайского хомячка DG-44 указанной экспрессионной плазмидной ДНК pCID-PROC. Способ получения рекомбинантного протеина С человека включает культивирование в питательной среде указанной линии клеток DG-CID-PROC-1 и выделение полученного целевого белка из культуральной жидкости. Предложенное изобретение позволяет увеличить продуктивность системы экспрессии протеина С и упростить выделение, активацию и очистку рекомбинантного активированного протеина С человека. 3 н.п. ф-лы, 3 ил., 2 пр.
Реферат
Изобретение относится к области биотехнологии, а именно к технологии получения биологически активных веществ (БАВ) методами генной инженерии, точнее к методам получения активированного и интактного (зимогенного) протеина С человека.
Протеин С является витамин К-зависимым белком плазмы крови. Он входит в систему гемостаза и играет исключительно важную роль при регулировании свертывания крови. Протеин С синтезируется в виде неактивной молекулы предшественника, проходит многостадийный посттрансляционный процессинг в клеточных компартментах и секретируется в виде интактной (зимогенной) формы. Активация белка С происходит в кровотоке при участии тромбомодулин-тромбинового комплекса. Активированный протеин С вместе с кофактором - протеином S выполняет антикоагулянтную функцию. Активированный белок С может предотвращать внутрисосудистый тромбоз и подавлять рост имеющихся тромбов. Механизм действия активированного протеина С и механизм активации зимогена в активную протеазу подробно изложен в работе (Gardiner I.E., Griffin I.H., Progress in Hematology, vol XIII. pp.265-278, ed Elmer B.Brown. Grime and Strattom Inc., 1983,).
Активация протеина С непосредственно осуществляется тромбином, последней сериновой протеиназой каскада свертывания крови, и опосредована связанным с мембраной эндотелиальных клеток гликопротеином тромбомодулин. Тромбомодулин образует прочный нековалентный комплекс состава 1:1 с тромбином и полностью меняет функциональные свойства тромбина. Свободный тромбин в нормальных условиях активирует тромбоциты, конвертирует фибриноген до фибрина и факторы свертывания крови V и VIII до активных формы Va и VIIIa. В то же время тромбин в комплексе с тромбомодулином теряет все вышеуказанные свойства, но эффективно активирует интактный протеин С при физиологических концентрациях ионов кальция.
Активированный протеин С, в свою очередь, избирательно инактивирует активированные формы факторов свертываемости крови V и VIII, но не их исходные формы. Следует отметить, что основные события при запуске каскада свертывания крови происходят на поверхности клеток и требуют участия мембранно-связанных белков и фосфолипидов, в то время как факторы V и VIII свободно циркулируют в кровотоке и участвуют в петле положительной обратной связи при работе системы свертывания. При их активации тромбином они ускоряют активацию фактора Х и протромбина на 5 порядков и резко ускоряют генерацию тромбина в месте запуска каскада свертывания.
Таким образом, физиологическая роль активированного протеина С может быть описана как ограничение области запуска системы свертывания крови.
Основным кофактором активированного протеина С является протеин S, другой витамин К-зависимый белок плазмы крови. Протеин S более чем в 10 раз усиливает вызываемую активированным протеином С деградацию факторов Va и VIIIa.
Протеин С является важным терапевтическим агентом (ЕР 215549, ЕР 0191606) в качестве специфического антикоагулянта, имеющего потенциально более широкую область применения, чем традиционные антикоагулянты гепарин, варфарин (оксикумарин) или производные последнего. В отличие от традиционных антикоагулянтов, активированный или интактный протеин С не воздействует на систему свертывания крови до момента появления тромбина и не вызывает падения концентрации зимогенных белков системы свертывания. Вследствие этого, антикоагулянтая терапия протеином С потенциально является более безопасной, поскольку не вызывает постоянного риска возникновения кровотечений. Экзогенный интактный протеин С также может использоваться для заместительной терапии при наследственном дефиците протеина С, вызывающего смерть в младенческом возрасте при гомозиготном дефиците и частые тромбоэмболические состояния при гетерозиготной форме дефицита.
Основной областью клинического применения активированного протеина С являются опасные для жизни тромботические состояния, в первую очередь синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром), возникающий, в том числе при развитии острого сепсиса.
Активированный протеин С является маркером сепсиса, а его уровень и дефицит коррелируют с тяжестью течения заболевания. Так, дефицит протеина С наблюдается более чем у 85% больных с тяжелым сепсисом; а также дефицит протеина С коррелирует с неблагоприятными клиническими исходами, такими как септический шок (тяжелый сепсис, сопровождающийся развитием артериальной гипотонии), ДВС-синдромом и полиорганной недостаточностью.
Поскольку концентрация протеина С в плазме крови очень мала и его отделение от других витамин К-зависимых белков системы гемостаза представляется весьма затруднительным, единственным способом получения активированного протеина С для медицинского применения является биосинтез, активация и очистка рекомбинатного белка. Наличие у протеина С так называемого Gla-домена, то есть кластера близкорасположенных остатков гамма-карбоксилированной глютаминовой кислоты, необходимо для нормального функционирования белка. Пост-трансляционное превращение остатков глютамина в остатки гамма-карбоксилированной глютаминовой кислоты возможно только в клетках млекопитающих и опосредовано сложной ферментной системой, использующей в качестве кофактора витамин К. Таким образом, единственным надежным источником рекомбинатного протеина С могут быть только культивируемые клетки млекопитающих.
Генетический вектор, содержащий полную кДНК протеина С человека, был получен путем скрининга фаговой библиотеки кДНК и описан в патентах США US4968626 и US 5302529.
Базовый способ экспрессии минигена протеина С в клетках млекопитающих описан в патенте США US 4959318. Он состоит в конструировании плазмиды, содержащей промотор вируса SV40, целевой ген и ген дигидрофолатредуктазы (DHFR), котрансфекции данной плазмиды и вспомогательной плазмиды, содержащей ген устойчивости к антибиотику неомицин, в клетки млекопитающих линий COS, BHK, A293, получению колоний стабильно трансфецированных клеток и их росту на селекционной среде, содержащей метотрексат. При использовании данного способа уровень секреции протеина С в культуральную среду оставался весьма низким и составлял около 0,05 мг/л. Кроме того, степень превращения интактного протеина С в нестабильную активированную форму была довольно значительной и при использовании линии клеток 293 достигала 90%.
Для увеличения уровня секреции протеина С были применены различные способы. В патенте США US 5618714 приведены данные об увеличении уровня секреции протеина С на 56-215% при увеличении температуры культивации клеток с 37°C до 39°C. Данный способ имеет ограниченную практическую пригодность, поскольку увеличение температуры культивации может приводить к падению жизнеспособности клеточной культуры и загрязнению секретированного протеина С продуктами распада клеток.
Другим способом увеличения продуктивности является использование систем экспрессии, основанных на введении в геном культивируемых клеток множественных копий гена протеина С. Такой подход был описан в патенте США US 5516650: при ко-трансфекции клеток линии BHK плазмидами pSV2-DHFR и pDX/PC962, содержащими ген DHFR и искусственный ген протеина С, соответственно, и последующем культивировании в присутствии метотрексата были получены клоны клеток-продуцентов, секретирующие протиеин С в культуральную среду с уровнем от 0,55 до 2,5 мг/л.
Наиболее близким по технической сущности аналогом настоящего изобретения является плазмида pL141, трансфецированная в клетки линии СНО-K1 (dhfr-), описанная в патенте США US 4775624. Использование данной системы позволяет достичь уровня секреции целевого белка в 1,8 мг/л культуры, но требует использования эмбриональной сыворотки в составе культуральной среды, что приводит к очень высокому загрязнению целевого белка посторонними полипептидами, в первую очередь бычьим сывороточным альбумином. Кроме того, уровень секреции протеина С оставался достаточно низким, что может быть связано с отсутствием полной сцепленности признаков устойчивости к метотрексату и секреции протеина С, вызванной использованием вектора с отдельными промоторами для целевого гена и гена DHFR.
Технической задачей, решаемой авторами, являлось создание технологии получения активированного и интактного протеина C с более высоким выходом.
Технический результат достигался путем создания новой экспрессионной плазмидной ДНК pCID-PROC, кодирующей интактный протеин С человека и создание на ее основе линии-продуцента.
В основе данной технологии лежит разработанная авторами плазмидная ДНК pCID-PROC длиной 6174 п.о., содержащая последовательность, кодирующую белок С человека. Она состоит из фрагмента ДНК длиной 1792 п.о., содержащего последовательность полноразмерной кДНК гена белка С человека, и фрагмента 4382 п.о. плазмиды pCID, содержащего
- регуляторные элементы, обеспечивающие экспрессию протеина C: конститутивный промотор вируса CMV, последовательность Козак (сайт связывания рибосом) и сигнал полиаденилирования вируса простого герпеса (HSV);
- последовательность фактора устойчивости трансфецированных клеток к воздействию метотрексата - дигидрофолатредуктазы (DHFR) и регуляторные элементы для экспрессии DHFR - последовательность IRES вируса энцефаломиокардита. (EMCV), обеспечивающая бицистронную экспрессию в животных клетках и сигнал полиаденилирования;
- ген устойчивости к антибиотику ампициллин и бактериальный промотор гена устойчивости к ампициллину, позволяющие проводить препаративную наработку плазмиды в E.coli.
Плазмида pCID-PROC содержит уникальные сайты узнавания эндонуклеазами рестрикции - PvuI (5640) SpeI (54) Hind III (2772).
Имеет молекулярную массу 3,82 мДа.
Плазмида была введена в клетки DG-44 методом липосомальной трансфекции (Straus S.E. et al. J Virol. 1981 Jul:390):290-4), был получен пул стабильно трансфицированных клеток при помощи культивирования в среде, не содержащей гипоксантина и тимидина. Амплификация кассеты в геноме клеток была проведена путем последовательных культивирований в присутствии возрастающих концентраций метотрексата. Был получен пул клеток, устойчивых к высокой концентрации метотрексата, и использован для клонирования методом предельного разведения. Полученные клоны клеток-продуцентов были проанализированы методом иммуноферментного анализа и были отобраны клоны, дающие максимальный уровень экспрессии протеина C. Среди них был выбран клон DG-CID-PROC-1, при культивировании которого в суспензионной форме в бессывороточной среде уровень секреции протеина С составлял не менее 4 мг/л.
Особенности созданной конструкции, линии клеток и результаты практического применения изобретения приведены на следующих фигурах.
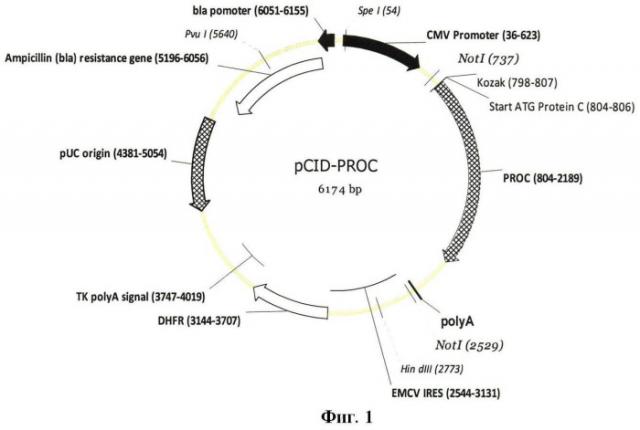
Фиг.1. Схематическая карта pCID-PROC, где используются следующие обозначения:
Pvul (5640) Spel (54) Hind 111 (2773) - уникальные сайты узнавания эндонуклеаз рестрикции;
Ampicillin (bla) resistance gene - ген устойчивости к ампициллину;
bla promoter - бактериальный промотор гена устойчивости к ампициллину;
CMYPromoter - эукариотический промотор цитомегаловируса;
Kozak - сайт связывания рибосом - последовательность Козак;
Start ATOprotein С - первый кодон рамки считывания белка С;
PROC - область, кодирующая открытую рамку считывания белка С;
polyA - область, соответствующая поли-А тракту кДНК PROC;
ЕСМУ IRES - сайт связывания рибосом - последовательность IRES энцефаломиокардита, обеспечивающая бицистронную экспрессию в животных клетках;
DHFR - последовательность фактора устойчивости трансфецированных клеток к воздействию метотрексата - дигидрофолатредуктазы (DHFR);
ТК polyA signal - сигнал полиаденилирования.
Фиг.2. Первичная нуклеотидная последовательность фрагмента NotI-NotI плазмиды pCID-PROC, содержащего кДНК человека (длина 1792 п.о.)
Фиг.3. Аминокислотная последовательность полипептида, транслирующегося с плазмиды pCID-PROC (длина 461 аминокислота; молекулярный вес 52078.06 Да).
Клеточная линия DG-CID-PROC-1 была депонирована в Специализированной коллекции культур клеток позвоночных Российской коллекции клеточных культур в Институте цитологии РАН 16.03.2010 г. под номером РККК (П) 732Д.
При этом зафиксированы следующие характеристики.
1. Наименование организации, где была получена линия культивируемых клеток животных: Общество с ограниченной ответственностью "Инновационный центр «Новые технологии и материалы»"
2. Автор или авторский коллектив, дата получения штамма: Ковнир СВ., Орлова Н.А., Воробьев И.И.; 25.06.2009
3. Адрес депозитора:
Юридический: 115093, г.Москва, ул. Большая Серпуховская 44, офис 33.
Почтовый: Гематологический Научный Центр РАМН, Москва, 125167, Новый Зыковский проезд, д.4а.
4. Регистрационный номер; авторское наименование штамма:
PKKK(H)732D; DG-CID-PROC-1.
5. Причины депонирования: продуцент рекомбинантного белка; штамм, перспективный для биотехнологии.
6. Происхождение штамма:
Родительские клетки: китайский хомячок, яичник, линия СНО DG44 (Invitrogen cGMP banked, США; Mol Cell Biol 5, 1750-1759 Kaufman RJ et al. 1985).
Трансфекция, клонирование: стабильная трансфекция выполнена в Лаборатории Медицинской Биотехнологии ГУ ГНЦ РАМН,
Трансфекционный агент: Unfectine-56sp.
Трансфецированная плазмида: pCID-PROC.
Система селекции: dhff knockout/метотрексат
Кратность клонирования: 2
7. Число пассажей к моменту паспортизации и депонирования:
36 пассажей от трансфекции родительской клеточной линии СНО DG44
8. Стандартные условия выращивания (состав питательной среды, температура и т.д.):
Среда: бессывороточная, определенного химического состава, CD Opti СНО (Invitrogen, США).
Температура: +37°С.
Концентрация СО2: 8%.
Скорость перемешивания: 120-130 об/мин.
9. Культуральные свойства (способ культивирования, посевная доза, кратность рассева, время субкультивирования и другие ростовые характеристики и особенности штамма):
Способ культивирования: суспензионный, в колбах Эрленмейра на орбитальной качалке 130-135 об/мин.
Посевная доза: 300000 на 1 мл.
Кратность рассева: 1:2-1:6
Другие ростовые характеристики и особенности штамма:
Селективная среда - бессывороточная, определенного химического состава, CD Opti CHO (Invitrogen, США) с добавлением L-глутамина 8 мМ + метотрексат натрия 500 нМ.
Процедура пересева: - центрифугирование суспензии на скорости 1200 об/мин, 5 мин, ресуспендирование в новой ростовой среде.
Оптимальная плотность: 1,0-1,2×106 клеток/мл.
10. Характеристика культивирования в организме животного:
не предусмотрена при использовании клеточной линии в качестве продуцента.
11. Данные по видовой принадлежности:
китайский хомячок Cricetulus griseus, яичник.
Контроль видовой идентичности: кариологический, изоферментный (ЛДГ и Г6ФДГ).
12. Маркерные признаки и методы их оценки: иммунологические, цитогенетические, биохимические, физиологические:
Морфология: эпителиоподобная.
Кариология: 2п=22, пределы изменчивости по числу хромосом 10-28, модальное число хромосом 22, псевдодиплоид, имеются микрохромосомы, количество полиплоидов 9,0%.
Биохимия: Дигидрофолатредуктазная активность по резистентности к метотрексату.
13. Контроль контаминации бактериями, микоплазмами, грибами и вирусами: бактерии, грибы методом прямого посева на питательные среды LB и Сабуро-Эммонса не обнаружены; микоплазма по ПЦР и флуоресцентному анализу не обнаружена; вирусы - нет данных.
14. Характеристика полезного вещества, продуцируемого штаммом (для иммуноглобулинов указание класса, специфичности и методов ее оценки):
рекомбинантный белок - активированный протеин С человека,
определение методами ИФА, вестерн-блоттинг с хемилюминесцентной детекцией.
15. Характеристика биосинтеза полезных продуктов, выход продукта в среду, уровень активности и метод определения с указанием сохранения полезного свойства при длительном культивировании:
Содержание активированного протеина С в культуральной среде (при суточном культивировании клеточной суспензии плотностью 1 млн кл./мл) не менее 4 мг/л, уровень постоянен в течение 12 последовательных пассажей.
16. Способ криоконсервирования (среда, криопротектор, режим замораживания и отгрева, условия длительного хранения, жизнеспособность после криоконсервирования с указанием методов ее оценки)
Среда: бессывороточная, определенного химического состава, CD
Opti CHO (Invitrogen, США).
Криопротектор: 10% ДМСО.
Режим замораживания и отгрева: замораживание клеточной суспензии в среде с добавлением криоконсерванта, скорость падения температуры не более 1°С/мин (теплоноситель - изопентанол); разморозка быстрая, на водяной бане при 37°С.
Условия длительного хранения: 10 клеток/мл в ампуле в жидком азоте. Жизнеспособность после криоконсервирования: 81% (окраска трепановым синим).
17. Другие особенности штамма (онкогенность, присутствие вирусов и т.д.)
Онкогенность: -
Чувствительность: везикулярный стоматит (Индиана), арбовирус Гета.
Устойчивость: полиовирус 2 типа, флавивирус Модок MODV, арбовирус Батон Виллоу.
Амплифицирванный ген: dhfr.
Копия справки о депонировании прилагается.
Практическая применимость заявляемого изобретения иллюстрируется следующими примерами.
Пример 1. Получение генетической конструкции pCID-PROC, кодирующей протеин С человека, для трансфекции линии клеток DG-44
В качестве источника кДНК для клонирования минигена протеина С использовали клон pCMY6-XL41NM_000312 (проприетарная коллекция компании Origene), содержащий полностью секвенированную последовательность полноразмерной кДНК гена PROC, совпадающую с теоретически определенной кДНК гена PROC человека по данным HUGO (депонирована в публичной базе данных GeneBank (http://www.ncbl.nlin.nih.gov/sites/entrez NM_000312).
Фрагмент ДНК длиной 1792 п.о., содержащий ген протеина С, получали из очищенной плазмиды pCMY6-XL41NM_000312, рестриктированной препаративно эндонуклеазой рестрикции NotI. Продукты рестрикции смешивали с 1 мкл буферного раствора для нанесения и проводили разделение в 1% агарозном геле с добавлением бромистого этидия (0,4 мкг/мл). Для выделения ДНК полосу, соответствующую продукту амплификации, визуализированную при помощи ультрафиолета (УФ), вырезали из агарозного геля, помещали в пробирку объемом 1,5 мл и проводили выделение ДНК, используя набор реактивов "Wizard SV Gel and PCR Clean-Up System" («Promega», США) согласно протоколу фирмы-производителя.
Реципиентную плазмиду pCID получили на основе коммерчески доступной линеаризованной плазмидной ДНК pOptivec-TOPO при инкубации в деионизованной воде 30 минут с последующим лигированием ДНК-лигазой фага Т4 (Fermentas, Литва), проводившимся в стандартном буферном растворе по методике производителя фермента. Полученной лигазной смесью трансформировали клетки Е.coli штамма DH5ά, с генотипом F-φ80lacZΔM15 Δ(lacZYA-argF) U169 recA1 endA1 hsdR17 (rk-, mk+) phoA supE44 λ-thi-1 gyrA96 relA1. Для этого к 200 мкл замороженной клеток Е.coli добавляли 5 мкл лигазной смеси, инкубировали на льду 30 минут для сорбции плазмидной ДНК, нагревали до 42°С на 60 секунд и инкубировали на льду 5 минут. После чего добавляли 800 мкл питательного бульона SOC (20 г/л триптона, 5 г/л дрожжевого экстракта, 0,5 г/л NaCl, 250 мМ КСl, 10 мМ MgCl2) и инкубировали при 37°С 60 мин. После инкубации переносили суспензию на чашку Петри с твердой агаризованной средой 2xYT-агар (16 г/л триптона, 10 г/л дрожжевого экстракта, 10 г/л NaCl, 18 г/л агара), содержащей ампициллин в концентрации 100 мкг/мл, и помещали в термостат на 18 часов при 37°С. Отдельные клоны трансформантов инокулировали в 5 мл питательного бульона LB с добавлением ампициллина в концентрации 50 мкг/мл, наращивали 18 часов при 37°С и проводили выделение плазмидной ДНК с использованием набора реактивов "Wizard Plus SV Minipreps" («Promega», США) по стандартному протоколу фирмы-производителя..
Очищенную плазмиду pCID рестрицировали эндонуклеазой NotI, после чего проводили дефосфорилирование вектора щелочной фосфатазой (Fermentas, Литва) согласно рекомендациям производителя. Шелочную фосфатазу инактивировали прогреванием до 85°С в течение 20 минут. Рестрицированную и дефосфорилированную плазмиду обрабатывали равным объемом смеси фенол-хлороформ 1:1 и переосаждали водную фазу 3 объемами этанола. Центрифугировали 10 минут на скорости 13200 об/мин при комнатной температуре, промывали осадок 70% спиртом, растворяли в воде и использовали для постановки реакции лигирования в рабочей концентрации 10-2 мкг/мкл.
Реакцию лигирования очищенного фрагмента, соответствующего кДНК гена PROC человека, и реципиентной плазмиды проводили с использованием ДНК-лигазы фага Т4 и стандартного буферного раствора (Fermentas, Литва). Лигирование вели в объеме 10 или 20 мкл, при молярном соотношении вектора и вставки 1:10, в течение 2-20 часов при комнатной температуре. Полученной лигазной смесью трансформировали клетки Е.coli штамма DH5ά, как описано выше, переносили суспензию трансформированных клеток на чашку Петри с твердой агаризованной средой 2xYT-агар, содержащей ампициллин в концентрации 100 мкг/мл, и помещали в термостат на 18 часов при 37°С.
Колонии Е.coli анализировали на наличие вставки в правильной ориентации методом полимеразной цепной реакции (ПНР) клонов с использованием праймерных олигонуклеотидов CMVfor и PROC-AS к последовательности вектора (прямой) и вставки (обратный), поскольку сайт узнавания эндонуклеазы NotI является палиндромным. Первичные нуклеотидные последовательности праймеров CMVfor - 5'CGCAAATGGGCGGTAGGCGTG3'; PROC-AS - 5'CCGTCGACGTGCTTGGACCA3'.
Полимеразную цепную реакцию (ПЦР) проводили на приборе Терцик МС2 («ДИК-технология», Россия) в объеме 12,5 мкл. Готовили инкубационную ПЦР-смесь следующего состава: 1х буфер для термостабильной ДНК-полимеразы; 10 пМ каждого праймерного олигонуклеотида; 2 мМ каждого дезоксирибонуклеотидтрифосфата; 1-2 ед. термостабильной ДНК-полимеразы с 0.1-0.2 мкг ДНК.
Бактериальные колонии переносили петлей в пробирки и одновременно делали штрихи на свежей, размеченной чашке Петри с твердой питательной средой 2xYT-агар с добавлением селективного антибиотика, которую затем помещали в воздушный термостат на 5-7 часов при 37°С.
Поверх ПЦР-смеси наслаивали 50 мкл легкого минерального масла и вели амплификацию по схеме: 1 цикл - денатурация - 94°С, 3 мин; 25 циклов - денатурация 94°С, 30 сек, отжиг Х°С 30 сек, достройка 72°С, 45-60 сек; 1 цикл - достройка 72°С, 7 мин, где расчет температуры отжига (X) производили по формуле: Х=2°С×n (А/Т)+4°С×n (Г/Ц) - 5°С, где n - число соответствующих нуклеотидов. Продукты ПЦР смешивали с 1 мкл буфера для нанесения и проводили разделение в 1% агарозном геле с добавлением бромистого этидия (0,4 мкг/мл).
Отобранные клоны, содержащие вставку в корректной ориентации наращивали 18 часов в 5 мл питательного бульона LB с добавлением ампициллина в концентрации 50 мкг/мл и проводили выделение плазмидной ДНК с использованием набора реактивов "Wizard Plus SV Minipreps" («Promega», США) по стандартному протоколу фирмы-производителя. Полученные плазмиды анализировали методом рестрикции эндонуклеазой NotI и отбирали клоны, несущие 1 копию вставки.
3 отобранных таким образом плазмидных клона дополнительно исследовали методом ПЦР-секвенирования ДНК в области вставки с использованием стандартных и специфических праймеров CMVfor, PROC-AS, 1RESrev; PROC_DS1; PROC_DS2; PROC_DS3; PROC_DS4; PROC_C01; PROC_C02; PROC_C03; PROC_C04; первичные нуклеотидные последовательности праймеров:
CMVfor - 5'СОСАААТОООСООТАООСОТО3';
PROC-AS - 5'ССОТСОАСОТОСТТООАССА3';
1RESrev - 5'CGAAGCCGCTTGGAATAAGG3'
PROC_DS1 - 5'CCCTACAGGTGCCAGTGCC3';
PROC_DS2 - 5'TGGGAGGGCCGCTTCTG3';
PROC_DS3 - 5'TGCATGGATGAGTCCAAGAAGC3';
PROC_DS4 - 5'ATCCTCGGGGACCGGC3';
PROC_C01 - 5'GGCCTCCTCGAAGTCACAGATC3';
PROC_C02 - 5'CCGCGGATCTACTTGGTCTTC3';
PROC_C03 - 5'CACGAGGGTCTCCTGGCC3';
PROC_C04 - 5'AAGCCCAGCCCTGCAGG3').
Для дальнейшей работы использовалась плазмида pCID-PROC, длиной 6174 п.о., не содержавшая мутаций, для которой были полные данные секвенирования. Методом ПЦР-секвенирования с использованием указанных выше праймерных олигонуклеотидов, для конструкции pCID-PROC определяли нуклеотидную последовательность обоих комплементарных цепей ДНК для области вставки кДНК гена PROC. Данные определения первичной нуклеотидной последовательности по двум цепям, полученные с прибора для автоматического капиллярного электрофореза, экспортировались в приложение ContigExpress программного пакета VectorNTI Suite (Invitrogen, США). С использованием стандартного алгоритма производился тримминг 5'-концевых и/или 3'-концевых областей фрагментов, после чего проводили сборку контига с использованием стандартных настроек. Проводили понуклеотидное сравнение полученной консенсусной последовательности с теоретически предсказанной. Помимо кодирующей области (ОРС) кДНК гена PROC, проводилось также секвенирование областей рестриктных сайтов NotI, по которым производилось клонирование фрагмента кДНК, а также наиболее значимых регуляторных элементов экспрессионного вектора (промотор, 1RES), анализ полученных данных проводился по аналогичному алгоритму. В результате секвенирования установили, что полученный препарат плазмиды не содержат мутаций в области вставки и кодирует кДНК гена PROC. Созданную генетическую конструкцию использовали для получения линии-продуцента.
Плазмидную ДНК pCID-PROC амплифицировали в клетках бактерий в препаративных количествах, выделили при помощи щелочного лизиса бактерий и трехстадийной хроматографической очистки (сорбенты Sepharose 4B Fast Flow, PlasmidSelect Xtra, Source 15 Q, Amersham) по методике производителя сорбентов, часть полученной высокоочищенной плазмидной ДНК, не содержащей пирогенов, дополнительно перевели в линейную форму рестрикцией PvuI и очистили от рестриктазы экстракцией фенолом-хлороформом и преципитацией этанолом. Полученные формы плазмиды для трансфекции клеток перевели в фосфатно-солевой раствор при помощи диализа и стерилизовали при помощи фильтра 0,22 мкм.
Пример 2. Конструирование эукариотических продуцентов протеина С DG-CID-PROC-1 трансфицированием клеток яичника хомячка линии DG-44 цитомегаловирусным вектором с использованием плазмиды pCID-PROC
Клетки яичника китайского хомячка линии DG-44, нокаутные по гену dhfr и адаптированные к культивированию в бессывороточной среде, были получены в компании Invitrogen, Ltd. (США). Описанная ниже методика трансформирования относится к клеткам DG-44, как линии клеток-хозяев, однако методика в целом применима и к большинству клеточных линий, включая другие линии клеток яичника китайского хомячка (СНО), человеческие эмбриональные почечные клетки линии 293, фибробласты почек сирийского хомячка ВНК, также пригодные для экспрессии конструкции pCID-PROC.
Клетки DG-44 полученные в криопробирках по 1 мл, содержащих замороженную суспензию клеток приблизительно 107 клеток в среде CD DG-44 (Gibco) с 10% диметилсульфоксида (DMSO). Содержимое сосуда размораживают при 37°С и добавляют к 30 мл полной среды DG-44. Полная среда состоит из ВП-44 (Cibco) с 8 mM L-глутамина и 1,8 мл/л сурфактанта Pluronic F-68 (BASF Inc.) и содержит достаточные для роста DHFR отрицательных клеток количества гипоксантина и тимидина. Клетки культивируют в колбах Эрленмеера на орбитальной качалке при 130 об/мин в атмосфере, содержащей 8% углекислого газа, при температуре 37°С. Подсчет плотности клеточной суспензии и доли живых клеток проводится в камере Горяева, при окрашивании трепановым синим. Субкультивируют с частотой 1 раз в 24-48 часов по достижении концентрации 1.2×106. Для этого удаляют старую среду центрифугированием в течение 5 минут на скорости 1200 об/мин, ресуспендируют клеточный осадок свежей средой и распределяют в новые колбы Эрленмеера с отношением субкультивирования 1:6.
За 48 часов до трансфекции клетки высевают по описанной методике в количестве 9×106 клеток на 1 колбу. В день трансфекции доля живых клеток должна составлять не менее 95%. Клетки в день трансфекции не центрифугируя разводят до конечной концентрации 1,5×107 клеток на 30 мл среды DG-44 в колбах Эрленмеера. Стерильную, осажденную этанолом плазмидную ДНК растворяют в PBS-буфере и используют для получения трансфекционной смеси, содержащей 18 мкг плазмидной ДНК, 15 мкл трансфекционного агента FreeStyle MAX (Invitrogen) в 1,2 мл вспомогательной среды Opti-Pro SFM MAX (Invitrogen). Плазмидная ДНК, используемая для трансфекции, представляет собой смешанные в соотношении 20:1 плазмиды pCID-PROC, линеаризованной эндонуклеазой рестирикции PvuI, и сверхспирализованной pEGFP. Трансфекционную смесь осторожно перемешивают и инкубируют 10-20 минут, а затем осторожно добавляют во вращающуюся колбу, содержащую клетки DG-44, в указанной выше концентрации. Экспрессируемый в трансфецированных клетках флуоресцентный белок используется для оценки эффективности трансфекции. Для этого через 12 часов после трансфекции в пробе клеток определяют долю флуоресцирующих при анализе с помощью пары оптических фильтров EGFP. Полученное соотношение характеризует интенсивность транзиентной экспрессии в трансфецированных клетках.
Данное изобретение включает вектор экспрессии, содержащий селективный маркер для эукариотических клеток, нокаутных по гену dhfr. Известно использование дигидрофолатредуктазного (dhfr) гена или производного dhfr-гена (dhfr-mix), придающего устойчивость к метотрексату (МТХ), в качестве селективного маркера для введения гена или плазмиды в клеточные линии, лишенные dhfr, и последующее применение метотрексата для размножения копий плазмид. Клетки DG-44 являются dhfr нокаутными (негативными), поэтому трансфектанты, содержащие плазмиду pCID-PROC с последовательностью гена dhfr, селектируются на основе dhfr-позитивного фенотипа, так как способны расти в среде, лишенной гипоксантина и тимидина. Клеточные линии, нокаутные по dhfr-гену и трансформированные dhfr-содержащими плазмидами, могут быть отобраны на основе dhfr-позитивного фенотипа.
Для отбора стабильных трансформантов с включением в хромосомную последовательность генетической конструкции pCID-PROC трансфецированные клетки DG-44 пересаживают в среду OptiCHO (Invitogen), не содержащую гипоксантин и тимидин, и культивируют по следующей методике. Проводят подсчет плотности клеточной суспензии и доли живых клеток в счетной камере Горяева при окрашивании трепановым синим. Затем удаляют старую среду центрифугированием в течение 5 мин на скорости 1200 об/мин, ресуспендируют клеточный осадок свежей средой CD OptiCHO (Invitogen), с добавлением L-глутамина в конечной концентрации 8 mM, и распределяют в новые колбы Эрленмеера по 9×106 клеток на колбу. Клетки культивируют в колбах Эрленмеера на орбитальной качалке при 130 об/мин в атмосфере, содержащей 8% углекислого газа при температуре 37°С. Субкультивируют с частотой 1 раз, в 3 дня в течение 10-14 дней до достижения доли живых клеток более 90%. В качестве контроля при отборе трансфектантов, положительных по dhfr, используют клетки, трансфецированные плазмидным вектором pOptiVec, экспрессирующие дигидрофолатредуктазу без сцепленности этого признака с другими. По достижении доли живых клеток 90% и более замораживается промежуточный клеточный банк с образцами, содержащими по 107 клеток в 1 мл среды CD OptiCHO с добавлением 10% DMSO.
Для амплификации целевого признака экспрессии активированного белка С проводится селекционное культивирование в присутствии нарастающих доз метотрексата. Для этого образцы из промежуточного банка размораживаются по описанному выше протоколу с теми изменениями, что в качестве культивационной среды используется CD OptiCHO (Invitrogen), с добавлением L-глутамина в конечной концентрации 8 mM. Затем в культивационную среду добавляется метотрексат в диапазоне концентраций от 250 нМ до 4 мкМс удвоением рабочей концентрации МТХ на каждом шаге амплификации. Переход к следующему шагу амплификации осуществляют каждые 14-21 день по достижении доли живых клеток более 90%. На каждом шаге амплификации уровень экспрессии протеина С в культуре клеток определяется иммуноферментным анализом. Клетки-продуценты последнего шага амплификации клонируются методом предельных разведений и адаптируются к культивированию на твердой подложке.
Описанные в данном примере методики применимы для создания линий клеток-продуцентов активированного белка С на основе любых эукариотических клеточных линий, имеющих генетический нокаут гена dhfr-, как прикрепленных, так и суспензионных, а также трансформированных как описанным методом, так и с использованием других липосомальных агентов, а также методами кальций-фосфатной трансфекции, нуклеофекции или микроинъекции.
1. Плазмидная ДНК pCID-PROC для экспрессии рекомбинантного протеина С человека, содержащая последовательность полноразмерной кДНК гена протеина С человека, представленную в Перечне последовательностей как последовательность SEQ ID NO:1, при этом указанная плазмида характеризуется физической картой, приведенной на фиг.1.
2. Линия клеток яичника китайского хомячка DG-CID-PROC-1 - продуцент рекомбинантного протеина С человека, полученная путем трансформации линии клеток яичника китайского хомячка DG-44 экспрессионной плазмидной ДНК pCID-PROC по п.1.
3. Способ получения рекомбинантного протеина С человека, включающий следующие стадии:- культивирование в питательной среде линии клеток по п.2 - продуцента рекомбинантного протеина С человека; и- выделение полученного целевого белка из культуральной жидкости.