Способ сочетанной стимуляции репаративного остеогенеза у животных
Иллюстрации
Показать всеИзобретение относится к области ветеринарии, а именно к ортопедии и травматологии, и может быть использовано для хирургического лечения переломов костей у животных. Способ сочетанной стимуляции репаративного остеогенеза у животных включает сочетание метода чрескостного остеосинтеза и нанесение остеоперфораций в зоне перелома, с использованием инфракрасного оптоволоконного лазера в импульсно-периодическом режиме 100×50, с длиной волны 1560 нм, мощностью 25-40 Вт. Лазерную остеоперфорацию в очаге перелома осуществляют однократно в пяти точках в течение 3-10 секунд. Первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома. Доставка энергии осуществлялась чрескожно, контактным путем, через кварцевый световод диаметром 0,4 мм. При этом формируются сквозные перфорационные отверстия в зоне перелома кости в перпендикулярных к кости плоскостях. Способ позволяет обеспечить полное анатомо-функциональное восстановление поврежденной кости, сократить сроки репаративного остеогенеза и предупредить развитие осложнений. 2 табл., 10 ил., 1 пр.
Реферат
Изобретение относится к области ветеринарии, ортопедии и травматологии и может быть использовано для хирургического лечения переломов костей у животных.
Для активизации репаративных процессов в настоящее время используются различные методы: медикаментозное воздействие [1, 3, 4, 10], использование стимулирующих свойств регенерации биологических субстратов (8), физические методы стимуляции [5, 9, 13, 15], однако разработка вопросов оптимизирующего и стимулирующего воздействий на процесс регенерации костной ткани до настоящего времени остается актуальным.
Для ускорения заживления переломов рекомендуют применять различные препараты.
Так, непосредственно в зону перелома рекомендуют вводить препарат коллапан в виде гранул, пластин и геля после репозиции отломков. Препарат представляет собой биокомпозиционный материал на основе особо чистого гидроксиапатита и коллагена, в его состав входят антибиотики - гентамицин и линкомицин.
Использование препарата коллапан ускоряет минерализацию костной мозоли травмированных животных после операции на 15% по сравнению с контролем (без коллапана), при этом реабилитация перелома трубчатых костей при интрамедуллярном остеосинтезе наступала на 13 дней раньше, чем без применения коллапана [1].
Кроме коллапана рекомендуют для стимуляции заживления переломов костей препараты, содержащие жизненно важные макро- и микроэлементы в сбалансированных физиологически допустимых для организма животных формах [4].
К данному ряду относится налоксона гидрохлорид, стимулятор нормального и репаративного остеогенеза. При использовании данного препарата была установлена тенденция к повышению прочности костной мозоли и ранняя консолидация переломов [10].
Известен способ стимуляции остеогенеза, основанный на введении в организм кальцийсодержащих препаратов, отличающийся тем, что однократно глубоко внутримышечно вводят в организм взвесь аллогенного гидроксилапатита в изотоническом растворе хлорида натрия, что ускоряет созревание костной ткани в регенерате [3].
Имеет место также способ стимуляции репаративного остеогенеза с использованием подкожного введения цитотоксической остеогенной сыворотки на фоне применения интрамедуллярного и чрескостного остеосинтеза [8].
Однако известные вышеперечисленные способы не всегда эффективны, предусматривают обязательную дополнительную стабильную фиксацию костных отломков, трудоемки, нередко возникают осложнения в виде остеомиелитов, формирования ложного сустава и другие осложнения, в результате чего животные, как правило, выбраковываются.
В комплексном лечении переломов у животных и человека, их последствий и различных заболеваний опорно-двигательной системы широко используются и различные физические факторы: УФО, УВЧ, Са- и Р-электрофорез, индуктотермия, ультразвук, оксибаротерапия, оптические квантовые генераторы, а также постоянное магнитное поле [5, 9, 13, 15].
Разработан способ стимуляции репаративного остеогенеза методом лазерной остеоперфорации при переломах трубчатых костей у собак. Автором отмечено, что лазерная остеоперфорация обеспечивает оптимальные условия для репаративной регенерации и сокращает сроки лечения переломов трубчатых костей до 26,6±1,6 дней [15]. При данном способе также необходима дополнительная иммобилизация.
Известен способ воздействия электрического тока на биологически активные точки (БАТ). Воздействуют электрическим током силой 15-30 мКА, частотой 8 Гц. Соотношение длительности импульсов положительной и отрицательной полярностей электрического тока 1:1. Воздействие осуществляют в течение 2 минут 1 раз в сутки. При переломе бедренной кости воздействуют на БАТ 108 и 109, а при переломе костей голени - на БАТ 115 и 116. Курс лечения 7 дней. Способ сокращает сроки лечения за счет использования электрического тока указанных параметров [14]. Выполнение данного способа требует точного определения БАТ, длительного контакта с пациентом.
В результате экспериментальных исследований в сравнительном аспекте отмечена эффективность физических методов стимуляции - транскраниальной электростимуляции (ТКЭС), бесконтактного электромагнитно-резонансного метода стимуляции (БЭРМС), а также их сочетанного применения при чрескостном остеосинтезе длинных трубчатых костей у собак. Определены оптимальные параметры тока для активизации остеогенеза: частота тока 300 Гц, продолжительность импульса 1 мс, сила тока 25-50 мА с биаурикулярным («ухо-ухо») наложением электродов.
Использование ТКЭС либо ее сочетание с БЭРМС-5 создает оптимальные условия для остеорепарации и восстановления функции конечности при переломах костей голени, позволяет сократить сроки реабилитации животных на 8-16 суток в сравнении с контролем.
Автором отмечено, что оптимальным методом стимуляции остеорепарации является ТКЭС, так как применяется однократно в отличие от сочетанного применения (ТКЭС-БЭРМС), а результат лечения существенных отличий не имеет. Курс лечения 7 дней. Способ сокращает сроки лечения за счет использования электрического тока указанных параметров [13]. Данный способ не всегда возможен из-за противопоказаний электростимуляций (повышенная температура тела, острые воспалительные процессы, наклонность к кровотечениям, новообразования).
В условиях замедленного репаративного остеогенеза рекомендуют проводить фиксацию отломков кости аппаратом для чрескостного остеосинтеза. Через 3-5 дней после операции к отломкам кости прикладывают дозированные дистракционные усилия с темпом 0,5 мм в сутки, на протяжении 4-х суток. Затем фиксируют отломки в достигнутом положении в течение 3 суток, после чего осуществляют компрессию, точно сопоставляя отломки, ориентируя их относительно продольной оси, и фиксируют до сращения. Способ обеспечивает стимуляцию остеогенеза, усиление микроциркуляции в области излома, сокращение сроков лечения. Способ является трудоемким, требует регулярной коррекции [7].
Известен способ стимуляции репаративного остеогенеза с применением низкоинтенсивного лазерного излучения. При этом после проведения интрамедуллярного остеосинтеза, наряду с общепринятыми в хирургии методами лечения, в послеоперационный период проводится курс лазеротерапии с применением гелий-неонового лазерного излучения лазерным аппаратом ЛНГ - 111, длина волны - 632,8 нм, мощность излучения - 12 мВт, экспозиция - 5 минут.
Автор рекомендует следующую схему лазеротерапии: облучение отломков непосредственно после восстановления целостности кости; облучение мягких тканей после проведенной операции и наложения швов; облучение мягких тканей в области перелома в радиусе 4-8 см на второй день после операции; облучение места перелома с третьего по десятый день после операции. При применении данного метода стимуляции репаративного остеогенеза к 25-26 дню после операции появлялась костная мозоль, формирование костной мозоли без стимуляции гелий-неоновым лазером заканчивалось к 35-40 дню.
Однако данный способ применим при свежих переломах, когда возможно проведение репозиции костных отломков с помощью интрамедуллярного остеосинтеза, требует довольно сложной и очень травматичной операции и длительного послеоперационного лечения с использованием гелий-неонового лазера [5].
Наиболее близок к заявляемому способ сочетания чрескостного остеосинтеза с интрамедуллярным армированием поврежденной кости и последующим вибрационным воздействием на введенную в костномозговой канал спицу.
Автор рекомендует проводить наружный чрескостный остеосинтез в сочетании с интрамедуллярным армированием поврежденной кости и последующим вибрационным воздействием на введенную в костномозговой канал спицу, которую необходимо вводить в костномозговой канал из проксимального или дистального метафиза (в зависимости от уровня перелома) до противоположного метафиза, закрепляя ее на ближайшей внешней опоре аппарата с помощью спицедержателя.
При этом ежедневно выполняется вибрационное воздействие на введенную в костномозговой канал спицу, предварительно освобождая ее из спицедержателя на время воздействия, с частотой 50 Гц и амплитудой 2 мм 3 раза в день по 30 минут с помощью вибромассажного прибора.
Сеансы вибрации на интрамедуллярно введенную спицу начинают на 3-5-е сутки с момента оперативного лечения и продолжают в течение всего срока фиксации в аппарате.
Для профилактики возникновения инфекционных осложнений ежедневно до начала каждого вибрационного воздействия и после него проводят обработку спицы, введенной в костномозговой канал, растворами антисептиков. Сравнительный анализ результатов лечения больных с диафизарными переломами длинных костей традиционным способом и с применением интрамедуллярного вибрационного воздействия на эндост выявил ускорение консолидации переломов диафизов длинных костей в среднем на 10-12% [12].
Однако данный способ очень трудоемкий, травматичный, требует длительного многократного послеоперационного лечения с помощью вибромассажного прибора, строгого соблюдения правил асептики и антисептики при работе со спицей в целях профилактики остеомиелита.
Целью изобретения является разработка способа сочетанной стимуляции репаративного остеогенеза у животных, обеспечивающего полное и быстрое анатомо-функциональное восстановление поврежденной кости, предупреждение развития осложнений в виде остеомиелитов, формирования ложных суставов.
Указанная цель достигается тем, что в заявляемом способе используют сочетание чрескостного остеосинтеза и лазерной остеоперфорации.
Чрескостный остеосинтез проводят по общепринятой методике.
Однократную остеоперфорацию выполняют в течение 3-10 сек в очаге перелома в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома. Используют инфракрасный оптоволоконный лазер в импульсно-периодическом режиме 100×50, с длиной волны 1560 нм, развивающий мощность 25-40 Вт (рис.1).
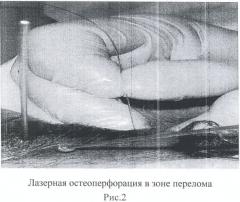
Доставку энергии осуществляют чрескожно, контактным путем, через кварцевый световод диаметром 0,4 мм. При этом формируют сквозные перфорационные отверстия в зоне перелома кости в перпендикулярных к кости плоскостях (рис.2).
Осуществляют остеоперфорацию следующим образом. Производят пункцию мягких тканей до кости иглой диаметром 1,5 мм. Вводят в полость иглы лазерный световод, осуществляют лазерную остеоперфорацию в проекции очага перелома. Время остеоперфорации (3-10 сек) зависит главным образом от породы, возраста и толщины кости у животных.
Способ позволяет обеспечить стабильную иммобилизацию, микроциркуляцию в зоне перелома за счет чрескостного остеосинтеза (механической остеоперфорации), бактерицидное действие, нормализацию внутрикостного давления с помощью лазерной остеоперфорации. Способствует восстановлению костной структуры и ускоряет заживление переломов костей.
Таким образом, в сравнении с прототипом выявлены следующие отличительные признаки:
1. Используется инфракрасный оптоволоконный лазер в импульсно-периодическом режиме 100×50, с длиной волны 1560 нм, развивающий мощность 25-40 Вт в условиях чрескостного остеосинтеза.
2. Используют однократную остеоперфорацию в течение 3-10 сек, в очаге перелома в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома.
3. Доставка энергии осуществляется чрескожно, контактным путем, через кварцевый световод диаметром 0,4 мм. При этом формируются сквозные перфорационные отверстия в зоне перелома кости в перпендикулярных к кости плоскостях.
Патентный поиск не выявил способов хирургического лечения переломов костей сочетанного использования чрескостного остеосинтеза с использованием лазеров высокоинтенсивного излучения, характеризующихся заявляемой совокупностью признаков, следовательно, можно предположить, что указанный способ соответствует критерию «новизна».
Использование совокупности существенных признаков также неизвестно, что говорит о соответствии критерию «изобретательский уровень».
Заявляемый способ может быть осуществлен в любом специализированном ветеринарном учреждении, следовательно, он соответствует критерию «промышленная применимость».
Пример выполнения
Заявленный способ иллюстрируется описанием его использования и клиническими примерами.
Экспериментальные исследования проводили на 18 беспородных животных, подобранных по принципу аналогов (возраст, вес, упитанность).
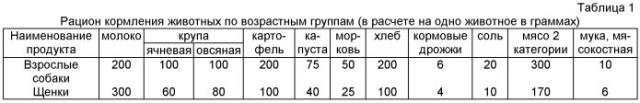
Животные содержались в индивидуальных клетках в условиях вивария УГАВМ. Кормили собак 3 раза в день по нормам, установленным приказом МЗ СССР №1179 от 10 октября 1983 г. Вода в поилках - постоянно. Собаки для поддержания физиологических функций получают полноценное, сбалансированное по основным элементам кормление. Основу их рациона составляют корма растительного и животного происхождения. Типичный рацион кормления собак приведен в таблице 1 (гр/сутки на 1 животное).
В условиях клиники хирургии под действием миорелаксантов, с соблюдением правил асептики и антисептики, у всех животных выполнялась чрездиафизарная остеотомия лучевой кости.
Сразу после перелома животных разделили на 2 группы, по 9 голов в каждой. Чрескостный остеосинтез проводился по общепринятой методике.
Первая группа - контрольная, для фиксации фрагментов кости использовался только метод чрескостного остеосинтеза,
Вторая группа - экспериментальная, для фиксации фрагментов кости использовался метод чрескостного остеосинтеза, для дополнительной стимуляции репаративных процессов в костной ткани использовали инфракрасный оптоволоконный лазер в импульсно-периодическом режиме, с длиной волны 1560 нм, развивающий мощность 25-40 Вт. Доставка энергии осуществлялась чрескожно, контактным путем, через кварцевый световод диаметром 0,4 мм. При этом формировались сквозные перфорационные отверстия в диафизе кости в зоне перелома в перпендикулярных к кости плоскостях.
Высокоинтенсивный оптоволоконный лазер обладает глубиной проникновения в биологические ткани до 10-15 мм. Условно была определена зона перелома около 6 см, для облучения которой было достаточно пяти точек с расстоянием друг от друга 15 мм. Расположение точек остеоперфорации в зависимости от размеров кости в нашем опыте не менялось, т.к. размеры костей предплечья (в частности, лучевой) были почти одинаковы.
В послеоперационный период у животных обеих групп проводили рентгенографию с интервалом 7 дней.
Через 14 дней после операции у собак контрольной группы отмечался отек тканей в зоне перелома, что хорошо видно на рис.3, выраженное пролиферативное воспаление и начиналось формирование костной мозоли. Смещения костных отломков не наблюдалось. При движении животные осторожно пытались опираться на поврежденную конечность.
В опытной группе (рис.4) через 14 дней после операции и лазерной остеоперфорации отека мягких тканей не наблюдалось, отмечено также формирование костной мозоли. Диастаз заполнен плотными тенями. Собаки опытной группы к 14-му дню наблюдений опирались на поврежденную конечность.
В дальнейшем при анализе рентгенограмм можно отметить, что консолидация и репаративная регенерация костных фрагментов наступила значительно быстрее в экспериментальной группе и завершилась в среднем на 21-й день (рис.6). При этом следует отметить, что на фоне сочетанного использования и лазерной остеоперфорации к 21-му дню сформировался кортикальный слой кости и животные при движении полностью опирались на поврежденную конечность. Клинически отмечалось полное выздоровление.
Снятие аппарата проводили на основании клинико-рентгенологических признаков полной консолидации перелома на 21-день.
В контрольной группе на 21-й день наблюдений формирование костной мозоли еще не завершилось (рис.5), и при движении животные этой группы частично опирались на поврежденную конечность, наблюдалась хромота опирающейся конечности. У 3-х собак из 9 в зоне перелома развивалась более обширная костная мозоль. Завершение формирования костной мозоли произошло только к 28-30 дню.
Отдаленные наблюдения показали, что на 60-й день после перелома в опытной группе у собак происходило полное анатомическое восстановление поврежденного участка лучевой кости (рис.8).
В контрольной группе, несмотря на видимое клиническое выздоровление, к 60-му дню у 3-х собак при рентгенографии в зоне перелома наблюдалась эндостальная реакция в стадии затухания, периостальная - в стадии компактизации (рис.7), что говорит о том, что восстановительные процессы еще не полностью завершились.
Динамика репаративных процессов по дням наблюдений приведена в таблице 2.
Таким образом, полученные результаты убедительно доказывают, что качество и сроки сращения при закрытых диафизарных переломах трубчатых костей зависят не только от точности репозиции костных фрагментов, но и от способа стимуляции репаративного остеогенеза. Анализ нашего клинического материала показал высокую эффективность применения высокоинтенсивного инфракрасного оптоволоконного лазера в условиях чрескостного остеосинтеза для стимуляции репаративных процессов в костной ткани при переломах костей.
Литература
1. Башкатова Н.А. Рациональные способы лечения и стимуляции остеосинтеза у собак при переломах трубчатых костей: автореф. дисс. на соиск. уч. степ. канд. вет. наук / Н.А.Башкатова. - Воронеж, 2000, 21 с.
2. Бетинарь, Н.Р. Стимуляция остеогенеза при переломах костей у собак при использовании цитоксической остеогенной сыворотки / Н.Р.Бетинарь, С.Ю.Концевая // Материалы XII Международного ветеринарного конгресса - М., ООО Испо-Сервис, 2004, с.106-108.
3. Волова Л.Т. Влияние аллогенеза гидрооксипатита на метобализм костной ткани / Л.Т.Волова // Вестник СамГу. - Естественно-научная серия. 2007, №8, с. 191-196.
4. Грищенко Н.В. Комбидаф - I - средство, ускоряющее регенерацию костей при переломах / Н.В.Грищенко // Материалы международной научной конференции, посвященной 125-летию Казанской госакадемии ветеринарной медицины им. Н.Э.Баумана. - Казань, 1998. - 4.2. - 20-21 (в соавт).
5. Грищенко Н.В. Влияние лазерного излучения и препарата комбидаф на регенерацию костной ткани при переломах трубчатых костей у собак. Автореф. дисс. на соиск. уч. степ. канд. вет. наук / Н.В.Грищенко. - Воронеж, 2000, 22 с.
6. Ерофеев С.А., Петровская Н.В., Кононович Н.А. Технология лечения переломов костей голени у мелких домашних животных методом чрескостного остеосинтеза / С.А.Ерофеев, Н.В.Петровская, Н.А.Кононович // Материалы 11 Московского международного конгресса. 17-19 апреля 2003 г. - Москва, 2003, с.153.
7. Кононович Н. А. Способ механической стимуляции замедленного остеогенеза при переломах костей / Н.А.Кононович, Е.В.Дюрягин, А.Н. Дьячков А.Н. // Патент на изобретение РФ №2007136426. Зарегистрирован в Гос. реестре 01.10.2007.
8. Концевая С.Ю. Стимуляция остеогенеза при переломах костей у собак. Автореф. дисс. на соиск. уч. стен. канд. вет. наук / С.Ю.Концевая. - Троицк, 1999, 21 с.
9. Кочетков Ю.С. Влияние экзогенного эритропоэтина на репаративный остегенез (экспериментальное исследование) / Ю.С.Кочетков, А.А.Ларионов, А.М.Чиркова, Л.С.Кузнецова, С.П.Изотова // Актуальные вопросы импланталогии и остеосинтеза: Сборник науч. трудов. 4.4. - Новокузнецк - СПб., 2002, с.56-58.
10. Лисков А.В. Средство для стимуляции нормального и репаративного остеогенеза / А.В.Лисков, С.А.Павловичев, Б.А.Фролов, В.А.Лисков. Патент на изобретение РФ №2240122. Зарегистрирован в Гос. реестре 20.11.2004.
11. Лукъяновский В.А. Болезни костной системы животных / В.А.Лукъяновский, А.Д.Белов, И.М.Беляков. - М., Колос, 1984, 254 с.
12. Марков Д.А. Стимуляция репаративного остеогенеза при лечении диафизарных переломов длинных костей: дис. канд. мед. наук / Д.А.Марков. - Саратов, 2008, 102 с.
13. Певень Т.В. Влияние физических методов стимуляции на остеорепарацию при чрескостном остеосинтезе костей голени у собак: дис. канд. вет. наук / Т.В.Певень. - Омск, 2005, 175 с.
14. Сахно Н.В. Лечение переломов трубчатых костей у животных / Н.В.Сахно, С.В.Тимофеев, В.А.Черванёв и др. // Учебное пособие. - СПб.: "Лань", 2007, 192 с.
15. Циулина Е.П. Стимуляция репаративного остеогенеза методом лазерной остеоперфорации при переломах трубчатых костей у собак: дис. канд. вет. наук / Е.П.Циулина. - Троицк, 2004, 129 с.
16. Чапкевич О.Б. Металлостеосинтез с применением накостных пластин / О.Б.Чапкевич // Актуальные проблемы ветеринарной хирургии: материалы международной научно-практической конференции, посвященной 70-летию кафедры хирургии. - Воронеж, 1999, с.107-109.
Способ сочетанной стимуляции репаративного остеогенеза у животных, включающий фиксацию костных фрагментов методом чрескостного остеосинтеза, отличающийся тем, что на фоне стабильной иммобилизации костных фрагментов в условиях чрескостного остеосинтеза используется инфракрасный оптоволоконный лазер в импульсно-периодическом режиме 100×50 с длиной волны 1560 нм мощностью 25-40 Вт, осуществляют однократную остеоперфорацию в течение 3-10 с, в области перелома в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома, доставку энергии осуществляют чрескожно контактным путем через кварцевый световод диаметром 0,4 мм, при этом формируют сквозные перфорационные отверстия в области перелома в перпендикулярных к кости плоскостях.