Способ химической модификации графита
Иллюстрации
Показать всеИзобретение относится к способу химической модификации природного графита, для использования в качестве смазочного материала. Способ химической модификации графита включает взаимодействие природного графита с калийными солями перфтор(ω-хлорперфтор)карбоновых кислот в присутствии персульфата калия при температуре 90-95°С в водной среде. Выделение целевого продукта осуществляют фильтрацией и промывкой горячей водой, с последующей сушкой на воздухе при температуре 120-130°С. Технический результат - создание более технологичного процесса получения фторграфита и улучшение его антифрикционных свойств. 5 ил., 2 табл., 13 пр.
Реферат
Графит как материал имеет огромное значение для многих областей современного производства и применяется для изготовления огнеупоров, тормозных накладок, химических источников тока, щелочных аккумуляторов, гальванических батарей, резинонаполненных смесей и др., а также является незаменимым в литейном производстве и в производстве сталей [Фиалков А.С. Углерод. Межслоевые соединения и композиты на его основе. М.: Аспект Пресс, 1997. 717 с.].
Более ста лет графит является наиболее распространенным твердым смазочным материалом [Кламанн Д. Смазки и родственные продукты. М.: Химия, 1988. С.167-169]. Он имеет высокие смазочные свойства и химическую стабильность. Однако применение графита в качестве смазочного материала в чистом виде нецелесообразно, поскольку графит не соответствует многим требованиям, предъявляемым к смазочным средствам. Обычно графит используют в качестве одного из ингредиентов в составе многокомпонентных смазок [Патент №2028374 РФ, МПК6 C10M 173/02 // (C10M 173/02, 125:18, 129:16, 129:40, 125:02, 133:08, 133:16) C10N 30:06, 40:20. Смазка для холодной обработки металлов давлением / Барыкин Н.П., Сергеева З.В., Абрамов А.Н., Рябинин С.Ю. - заявл. 15.05.1992; Опубл. 09.02.1995; Патент №2170756 РФ, МПК7 C10M 169/04 // (C10M 169/04, 125:02, 125:26, 125:28, 155:02, 159:04, 101:02) C10N 50:02. Рельсовый модификатор трения / Шаповалов В.В., Щербак П.Н., Черный B.C., Майба И.А., Ильин В.И., Колесников В.И., Могилевский В.А., Лубягов A.M., Червенко А.Н., Андриевский А.П., Розман О.А. - заявл. 01.02.2000; Опубл. 20.07.2001; Патент №2214449 РФ, МПК7 C10M 161/00 // (C10M 161/00, 125:02, 145:40, 143:00, 137:10, 101:02) C10N 40:34. Пластичная смазка / Муталлим-Заде Н.Ф., Волков П.В., Егоров И.Ф., Петров Н.Г., Саркисянц Н.Р., Тиньков А.А., Тимохин И.А. - заявл. 17.08.2001; Опубл. 20.10.2003; Патент №2321619 РФ, МПК7 C10M 103/02, 103/06, 177:00. Смазочное покрытие и способ его получения / Гайдар С.М. - заявл. 06.02.2007; Опубл. 10.04.2008 и др.].
Для успешного применения графита в качестве самостоятельного смазочного средства необходимо его модифицировать, например, химическим способом. Учитывая, что предпочтительными среди органических смазочных материалов, обладающих высокой гидрофобностью и превосходными антифрикционными свойствами, являются фторсодержащие соединения, то наиболее разумным способом химической модификации графита может стать введение в структуру графита атомов фтора или различных фторсодержащих групп.
Известен способ получения фторированного графита, заключающийся в обработке графита элементным фтором, в результате которого образуются новые связи C-F (схема 1).
СХЕМА 1.
Такой способ химической модификации графита всегда сопряжен с рядом возможных опасных инцидентов (например, взрывов), а реализовать его в лабораторных условиях практически невозможно, так как нужна сложная лабораторная техника. Результатом введения атомов фтора в структуру графита является материал фторграфит с превосходными антифрикционными свойствами как при использовании в составе смазочных композиций, так и в случае его применения в качестве самостоятельного смазочного материала [Фиалков А.С. Углерод. Межслоевые соединения и композиты на его основе. М.: Аспект Пресс, 1997. С.377-419]. Наилучшие антифрикционные показатели фторграфит проявляет при атмосферных условиях эксплуатации. При использовании его в вакууме коэффициент трения значительно возрастает. Фторграфит формулы (CFx)n или (C2Fx)n обладает высокой гидрофобностью, но низкой адгезией к различным поверхностям, в том числе к металлическим. В отличие от традиционных эффективных смазочных материалов, обладающих высокой адгезией к металлам, фторграфит обеспечивает трение по когезионному механизму [Фиалков А.С. Углерод. Межслоевые соединения и композиты на его основе. М.: Аспект Пресс, 1997. С.417].
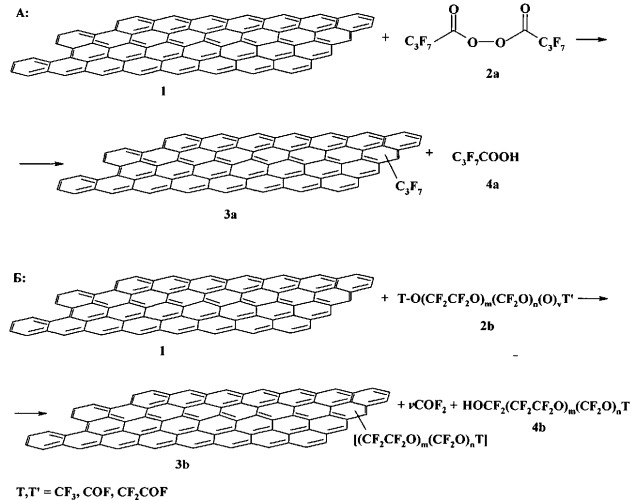
Известен способ введения перфторалкильных или перфтороксаалкильных групп в структуру графита путем его взаимодействия с фторорганическими пероксидами [Sansotera М., Navarrini W., Resnati G., Metrangolo P., Famulari A., Bianchi C.L., Guarda P.A. Preparation and characterization of superhydrophobic conductive fluorinated carbon blacks // Carbon. - 2010. - Vol.48. - P.4382-4390] - прототип. Химическая суть данного способа представлена на схеме 2.
СХЕМА 2.
При взаимодействии графита 1 с пероксидом перфтор-н-бутирила 2a или с пероксидом на основе перфторполиэфира 2b образуется соответственно перфторалкилсодержащий графит 3а или перфтороксаалкилсодержащий графит 3b.
В случае пероксида 2a (схема 2, A) процесс проводят с использованием порционной загрузки пероксида (период полураспада соединения 2a при 25°C составляет 4 ч). После каждой внесенной порции стеклянный реактор охлаждают до 0°C, продувают его в течение 5 мин азотом, затем ведут перемешивание в течение 4 ч, а затем снова вносят порцию пероксида 2a и повторяют те же операции. Время реакции составляет 12 ч. По окончании процесса доводят температуру реакционной массы до 25°C, оставляют ее еще на 12 ч, затем растворители выпаривают, а твердый остаток, представляющий собой соединение 3a, промывают фторсодержащим растворителем (CF3OCFClCF2Cl), затем 2%-ным раствором гидрокарбоната натрия (NaHCO3) и деионизированной водой. Далее целевой продукт 3a сушат при 180°C в течение 24 ч при давлении 10-3 мм рт. ст.
В случае пероксида 2b (схема 2, Б) процесс проводят с использованием разовой загрузки пероксида (период полураспада соединения 2b при 140-250°C составляет 30 мин). Затем нагревают реактор до 40°C до полного испарения растворителя, а далее в течение 3 ч доводят температуру до 150-195°C (скорость нагрева - 15°C/ч), разлагая пероксид 2b. По окончании нагревают реактор до 200°C и продолжают процесс еще 4 ч. Полученный твердый продукт 3b промывают 3 раза растворителем формулы CF3OCFClCF2Cl, затем 3 раза деионизированной водой и сушат 6 ч при температуре 200°C и давлении 10-2 мм рт. ст.
Необходимо отметить, что схема 2 является условной, поскольку невозможно точно указать, какое количество перфторалкильных или перфтороксаалкильных групп, ковалентно соединенных со структурой графита 1, находится в соединениях 3a, 3b соответственно. В прототипе приведены данные о том, что расход пероксида 2a составляет 6.6 мл (8.4 мас.%) на 250 мг графита 1, расход пероксида 2b - 10 мл его 2.3%-ного раствора на 500 мг графита 1.
Подтверждением того, что авторы способа-прототипа осуществили химическую модификацию графита 1, являются данные термогравиметрического и рентгено-структурного анализов и измерение контактного угла смачивания поверхности таблеток, спрессованных из соединений 3a, b.
Так, например, профили дериватограмм графита 1 и соединений 3a, b не совпадают: при температуре 800°C потеря массы образца 3a составляет около 7%, образца 3b - около 15%. При той же температуре аналогичный параметр исходного графита 1 составляет не более 2%.
Профили дифрактограмм порошка графита 1 и продуктов 3a, b также существенно отличаются, резко возрастает интенсивность пика при 2θ=25° в отличие от исходного графита 1.
Контактный угол смачивания таблетки, приготовленной из образца 3a, составляет более 150°, а для образца, приготовленного из соединения 3b, аналогичный параметр составляет примерно 170°. Данные по углу смачивания для графита 1 в статье отсутствуют из-за нестабильных свойств таблетированной формы образца.
Несмотря на достоинства способа получения перфторалкилсодержащих или перфтороксаалкилсодержащих производных графита, описанного в прототипе, он имеет ряд существенных недостатков:
- для химической модификации применяется не обычный природный графит, а графит специальной марки Cabot Vulcan XC72R. Графит марки Cabot Vulcan XC72R является искусственно получаемым материалом (производитель - Cabot Corporation) и характеризуется высокой физической и химической чистотой, пониженным содержанием серы и ионных загрязнений, высокой дисперсностью. Для его получения требуется высокотехнологичная термическая обработка обычного, в том числе природного, графита;
- используемые соединения перекисного типа являются опасными взрывчатыми продуктами и требуют при работе с ними специальных мер безопасности;
- для осуществления взаимодействия графита с фторорганическими пероксидами необходима инертная атмосфера, в частности азот;
- при малых загрузках реагентов процесс является сравнительно длительным: суммарное время реакции составляет 24 ч для пероксида 2a и 7 ч для пероксида 2b;
- сушку целевых продуктов осуществляют при пониженном давлении (10-3-10-2 мм рт. ст.) и высокой температуре (180-200°C).
Задачей настоящего изобретения является упрощение способа получения перфторалкилсодержащих производных графита.
Поставленная задача решается путем взаимодействия графита с фторсодержащими реагентами с последующим выделением и сушкой целевого продукта. При этом в качестве исходного графита используют природный графит, в качестве фторсодержащего реагента - калийные соли перфтор(ω-хлорперфтор)карбоновых кислот. Процесс ведут в присутствии персульфата калия при температуре 90-95°C в водной среде. Выделение целевого продукта осуществляют фильтрацией и промывкой горячей водой, а сушку - на воздухе при температуре 120-130°C.
Химическую модификацию природного графита, согласно предлагаемому способу, осуществляют в присутствии неперекисного инициатора радикального процесса - персульфата калия. Причем, как указывается в патенте [USP 6019548, Int. Cl.7 B09B 1/00; B01D 17/06. Chemical oxidation of volatile organic compounds / G.E.Hoag, P.V.Chheda, B.A.Woody, G.M.Dobbs. - №09/073049; заявл. 05.05.98; Опубл. 01.02.2000], при нагревании персульфата калия (K2S2O8) происходит распад персульфат-иона на два ион-радикала: S2O8 2-→2SO4 -•, что является выгодным с точки зрения расхода инициатора. Используемый персульфат калия «работает» в водной среде без применения инертной атмосферы (период полураспада K2S2O8 при 90-95°C составляет 40 мин), он взрывобезопасен, и его применение не требует специального оборудования.
Выделение модифицированного графита состоит в обычной фильтрации целевых продуктов через фильтр Шотта или воронку Бюхнера, отмывке отфильтрованного продукта от образовавшихся по реакции неорганических солей (K2SO4) и сушке на воздухе при температуре 120-130°C до постоянного веса (до полного выпаривания воды).
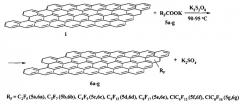
Химическая суть предлагаемого способа химической модификации природного графита калийными солями перфтор(ω-хлорперфтор)карбоновых кислот в присутствии персульфата калия при температуре 90-95°C представлена на схеме 3.
СХЕМА 3.
Полученные продукты 6 анализируют физико-химическими методами. Элементный анализ выполнен с помощью автоматического анализатора Perkin-Elmer «CHN РЕ 2400». ИК-спектры зарегистрированы на спектрофотометре Perkin-Elmer «Spectrum One». Термогравиметрический анализ выполнен на дериватографе Mettler Toledo TGA/DSC 1. Рентгенографические исследования проведены на автоматическом дифрактометре ДРОН-6 в монохроматизированном излучении KαCr.
Согласно данным элементного анализа все синтезированные соединения 6a-g содержат фтор, а продукты 6f, g - фтор и хлор (табл.1). Кроме того, содержание галогенов в соединениях 6a-g прямо пропорционально зависит от количества введенных в реакцию солей 5a-g: чем больше солей 5 вводится, тем больше содержание фтора (или хлора) в конечном продукте 6 и тем больше его масса.
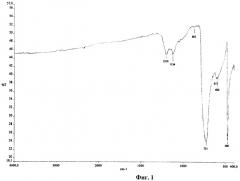
Зарегистрированные для продуктов 6 инфракрасные (ИК) спектры существенно отличаются от спектра исходного графита 1: ИК-спектр графита 1 не имеет никаких характеристических полос поглощения, а ИК-спектры соединений 6a-g, напротив, содержат по две полосы поглощения C-F - групп в области 1134-1221 см-1. Их интенсивность тем больше, чем больше количество солей 5a-g, введенных в реакцию с графитом 1. На фиг.1 представлен ИК спектр продукта 6c (пример №5, таблица 1).
Термогравиметрический анализ продуктов 6a-g и графита 1 также не совпадает: массовые потери для графита 1 при температуре 700°C составляют не более 2%, в случае соединения 6c (пример №3, табл.1) аналогичный показатель составляет более 4.5%, а для 6c (пример №5, табл.1) - более 10%. На фиг.2 представлены данные термогравиметрического анализа соединения 6c (пример №3, табл.1), на фиг.3 - соединения 6c (пример №5, табл.1). Данные рентгеноструктурного анализа свидетельствуют о присутствии в образцах продукта 6c фазы, структура которой отличается от структуры фазы классического графита 1. На это указывает присутствие дифракционных линий, наиболее сильные из которых находятся при 2θ=28.23, 46.95, 58.37, 105.57, что не свойственно дифрактограммам классического графита. На фиг.4 представлен участок дифрактограммы порошка исходного графита 1, на фиг.5 - продукта 6c (пример №5, табл.1). На фиг.5 стрелками обозначены отражения, не характерные для графита, цифрами над стрелками - межплоскостные расстояния в ангстремах.
Ниже приведены примеры получения фторсодержащих производных природного графита 6. Данные о загрузках реагентов и характеристика продуктов 6a-g приведены в таблице 1.
Пример 1. В трехгорлую круглодонную колбу, снабженную механической мешалкой, обратным водным холодильником с отводом на ловушку, захоложенную в сосуде Дьюара, термометром и помещенную на нагревающее устройство, вносят 0.3 л воды, 16.8 г (0.3 моль) калийной щелочи (КОН) и перемешивают. Затем добавляют 49.2 г (0.3 моль) перфторпропионовой кислоты (C2F5COOH), включают нагрев и перемешивают до образования однородной прозрачной массы, поддерживая температуру реакционной массы не более 50°C. Затем охлаждают, измеряют pH среды, добавляют необходимое количество КОН до рН=7, вносят 5.0 г природного графита 1, интенсивно перемешивают и снова нагревают до 50°C. При интенсивном перемешивании засыпают в реактор 13.0 г (0.048 моль) персульфата калия (K2S2O8), доводят температуру реакционной смеси до 90°C, нагрев отключают, доводят температуру до 50°C и снова засыпают 13.0 г (0.048 моль) персульфата калия (K2S2O8). Операцию повторяют 5 раз, пока в реактор не будет внесено 62.0 г (0.23 моль) персульфата калия (K2S2O8). По окончании реакционную массу охлаждают до комнатной температуры, содержимое реактора фильтруют через воронку Бюхнера или фильтр Шотта №1 и несколько раз промывают твердый остаток на фильтре горячей водой. Далее твердый темно-серый продукт 6a перекладывают в фарфоровую чашку, помещают в сушильный шкаф и высушивают до постоянной массы при температуре 120°C. Получают 9.1 г продукта 6a (пример №1 из табл.1).
Пример 2. В трехгорлую круглодонную колбу, снабженную механической мешалкой, обратным водным холодильником с отводом на ловушку, захоложенную в сосуде Дьюара, термометром и помещенную на нагревающее устройство, вносят 0.3 л воды, 16.8 г (0.3 моль) калийной щелочи (КОН) и перемешивают. Затем добавляют 64.1 г (0.3 моль) перфтормасляной кислоты (C3F7COOH), включают нагрев и перемешивают до образования однородной прозрачной массы, поддерживая температуру реакционной массы не более 50°C. Затем охлаждают, измеряют pH среды, добавляют необходимое количество КОН до рН=7, вносят 5.0 г природного графита 1, интенсивно перемешивают и снова нагревают до 50°C. При интенсивном перемешивании засыпают в реактор 13.0 г (0.048 моль) персульфата калия (K2S2O8), доводят температуру реакционной смеси до 90°C, нагрев отключают, доводят температуру до 50°C и снова засыпают 13.0 г (0.048 моль) персульфата калия (K2S2O8). Операцию повторяют 5 раз, пока в реактор не будет внесено 62.0 г (0.23 моль) персульфата калия (K2S2O8). По окончании реакционную массу охлаждают до комнатной температуры, содержимое реактора фильтруют через воронку Бюхнера или фильтр Шотта №1 и несколько раз промывают твердый остаток на фильтре горячей водой. Далее твердый темно-серый продукт 6b перекладывают в фарфоровую чашку, помещают в сушильный шкаф и высушивают до постоянной массы при температуре 130°C. Получают 11.2 г продукта 6b (пример №2 из табл.1).
Пример 3. Аналогично примеру 1 из 5 г природного графита, 4.5 г (0.08 моль) калийной щелочи (КОН), 21.1 г (0.08 моль) перфторвалериановой кислоты (C4F9COOH) и 16.0 г (0.06 моль) персульфата калия (K2S2O8) получают 7.0 г продукта 6с (пример №3 из табл.1).
Пример 4. Аналогично примеру 2 из 5 г природного графита, 8.4 г (0.15 моль) калийной щелочи (КОН), 39.6 г (0.15 моль) перфторвалериановой кислоты (C4F9COOH) и 31.0 г (0.1 моль) персульфата калия (K2S2O8) получают 10.0 г продукта 6с (пример №4 из табл.1).
Пример 5. Аналогично примеру 1 из 5 г природного графита, 16.8 г (0.30 моль) калийной щелочи (КОН), 79.2 г (0.30 моль) перфторвалериановой кислоты (C4F9COOH) и 65.0 г (0.24 моль) персульфата калия (K2S2O8) получают 13.3 г продукта 6с (пример №5 из табл.1).
Пример 6. Аналогично примеру 2 из 5 г природного графита, 8.4 г (0.15 моль) калийной щелочи (КОН), 54.6 г (0.15 моль) перфторэнантовой кислоты (C6F13COOH) и 30.0 г (0.11 моль) персульфата калия (K2S2O8) получают 12.0 г продукта 6d (пример №6 из табл.1).
Пример 7. Аналогично примеру 1 из 5 г природного графита, 16.8 г (0.30 моль) калийной щелочи (КОН), 109.2 г (0.30 моль) перфторэнантовой кислоты (C6F13COOH) и 60.0 г (0.22 моль) персульфата калия (K2S2O8) получают 17.5 г продукта 6d (пример №7 из табл.1).
Пример 8. Аналогично примеру 2 из 5 г природного графита, 16.8 г (0.30 моль) калийной щелочи (КОН), 139.2 г (0.30 моль) перфторпеларгоновой кислоты (C8F17COOH) и 65.0 г (0.24 моль) персульфата калия (K2S2O8) получают 13.5 г продукта 6e (пример №8 из табл.1).
Пример 9. Аналогично примеру 1 из 5 г природного графита, 5.6 г (0.10 моль) калийной щелочи (КОН), 38.0 г (0.10 моль) ω-хлорперфторэнантовой кислоты (ClC6F12COOH) и 13.5 г (0.05 моль) персульфата калия (K2S2O8) получают 7.5 г продукта 6f (пример №9 из табл.1).
Пример 10. Аналогично примеру 2 из 5 г природного графита, 8.4 г (0.15 моль) калийной щелочи (КОН), 57.0 г (0.15 моль) ω-хлорперфторэнантовой кислоты (ClC6F12COOH) и 21.6 г (0.08 моль) персульфата калия (K2S2O8) получают 8.8 г продукта 6f (пример №10 из табл.1).
Пример 11. Аналогично примеру 1 из 5 г природного графита, 16.8 г (0.30 моль) калийной щелочи (КОН), 114.0 г (0.30 моль) ω-хлорперфторэнантовой кислоты (ClC6F12COOH) и 54.0 г (0.20 моль) персульфата калия (K2S2O8) получают 11.4 г продукта 6f (пример №11 из табл.1).
Пример 12. Аналогично примеру 2 из 5 г природного графита, 16.8 г (0.30 моль) калийной щелочи (КОН), 144.0 г (0.30 моль) ω-хлорперфторпеларгоновой кислоты (ClC8F16COOH) и 54.0 г (0.20 моль) персульфата калия (K2S2O8) получают 12.7 г продукта 6g (пример №12 из табл.1).
Пример 13. Аналогично примеру 1 из 5 г природного графита, 5.6 г (0.10 моль) калийной щелочи (КОН), 48.0 г (0.10 моль) ω-хлорперфторпеларгоновой кислоты (ClC8F16COOH) и 13.5 г (0.05 моль) персульфата калия (K2S2O8) получают 11.0 г продукта 6g (пример №13 из табл.1).
| ТАБЛИЦА 1 | |||||||
| Данные о загрузке реагентов для синтеза фторсодержащих производных графита 6a-g и элементного анализа на галогены | |||||||
| № п./п. | № соед. | Загрузка реагентов, г (моль) | Данные элементного анализа, % | Масса выделенного продукта (6a-g), г | |||
| графит | соль (5a-g) | персульфат калия (K2S2O8) | F | Cl | |||
| 1. | 6a | 5 | 60.6 (0.30) | 62.0 (0.23) | 22.78 | - | 9.1 |
| 2. | 6b | 5 | 75.6 (0.30) | 62.0 (0.23) | 28.37 | - | 11.2 |
| 3. | 6c | 5 | 25.0 (0.08) | 16.0 (0.06) | 14.27 | - | 7.0 |
| 4. | 6c | 5 | 46.5 (0.15) | 31.0 (0.11) | 23.85 | - | 10.0 |
| 5. | 6c | 5 | 92.0 (0.30) | 65.0 (0.24) | 33.21 | - | 13.3 |
| 6. | 6d | 5 | 60.3 (0.15) | 30.0 (0.11) | 30.68 | - | 12.0 |
| 7. | 6d | 5 | 120.6 (0.30) | 60.0 (0.22) | 45.52 | - | 17.5 |
| 8. | 6e | 5 | 150.6 (0.30) | 65.0 (0.24) | 54.78 | - | 13.5 |
| 9. | 6f | 5 | 41.8 (0.10) | 13.5 (0.05) | 19.69 | 5.51 | 7.5 |
| 10. | 6f | 5 | 62.7 (0.15) | 21.6 (0.08) | 27.57 | 6.53 | 8.8 |
| 11. | 6f | 5 | 83.6 (0.30) | 54.0 (0.20) | 55.88 | 6.87 | 11.4 |
| 12. | 6g | 5 | 103.6 (0.30) | 54.0 (0.20) | 62.77 | 7.04 | 12.7 |
| 13. | 6g | 5 | 51.8 (0.10) | 13.5 (0.05) | 31.35 | 3.56 | 11.0 |
Таким образом, химическое взаимодействие природного графита с калийными солями перфтор(ω-хлорперфтор)карбоновых кислот в присутствии персульфата калия приводит к модификации графита с образованием новых C-C-связей за счет ароматического углерода графитовой структуры и углерода перфтор(ω-хлорперфтор)алкильного фрагмента RF.
Полученные фторсодержащие производные графита 6 подвергают испытаниям в качестве твердых смазочных материалов.
Исследование величины коэффициента трения (f) и интенсивности изнашивания (Ih) проведено при комнатной температуре по схеме «палец-пластина» в условиях трения скольжения при возвратно-поступательном движении пальца по пластине.
Палец и пластина представляют собой параллелепипеды, изготовленные из одноименной аустенитной стали 12Х18Н9. Размеры пальца - 7×7×20 мм, пластины - 60×40×10 мм. Скорость скольжения пальца по пластине - 0.07 м/с, длина пути трения пальца - 80 м (~1000 двойных ходов пальца).
Рабочие поверхности пальцев и пластин прошлифованы механически, класс шероховатости - 8. Перед испытанием пальцы и пластины тщательно обезжирены. Навеску соединений 6 (50 мг) втирали в рабочую поверхность образцов с помощью ткани. Коэффициент трения (f) определен как отношение силы трения (F) к нормальной нагрузке (N) по формуле:
f=F/N
Сила трения (F) измерена с помощью упругого элемента (стального кольца) с закрепленными на нем тензометрическими датчиками. Показания записаны на ленте электронного потенциометра КСП-4. Нормальная нагрузка (N) - 294 Н. Интенсивность изнашивания (Ih) пальцев рассчитана по формуле:
Ih=ΔQ/ρ·L·S,
где ΔQ - потеря массы образца-пальца, г; ρ - плотность материала образца, г/см3; L - путь трения, см, S - геометрическая площадь контакта, см2.
Потери массы (ΔQ) определены взвешиванием обезжиренных после испытаний образцов-пальцев на аналитических весах с точностью до 0.0001 г.
По результатам испытаний установлено, что по своим антифрикционным характеристикам производные графита 6 выгодно отличаются от исходного природного графита 1 и от коммерческого фторграфита (табл.2): установившийся коэффициент трения (f) для всех приведенных соединений серии 6 ниже, чем f графита и фторграфита, а в случае нехлорсодержащих соединений 6с интенсивность изнашивания (Ih) снижена на порядок.
| ТАБЛИЦА 2 | ||||
| Антифрикционные параметры фторсодержащих производных графита | ||||
| № п./п. | № соед. | Коэффициент трения | Интенсивность изнашивания образца-пальца, Ih | |
| пусковой (f0) | установивший-ся (f) | |||
| 1. | Природный графит | 0.62 | 0.57 | 1.9·10-6 |
| 2. | Фторграфит | 0.28 | 0.42 | 1.3·10-6 |
| 3. | 6c (пример №3 из табл.1) | 0.15 | 0.28 | 2.2·10-7 |
| 4. | 6c (пример №4 из табл.1) | 0.13 | 0.28 | 1.9·10-7 |
| 5. | 6c (пример №5 из табл.1) | 0.10 | 0.28 | 1.6·10-7 |
| 6. | 6g (пример №12 из табл.1) | 0.12 | 0.35 | 1.2·10-6 |
Суммируя имеющиеся сведения, можно отметить следующие преимущества предлагаемого способа химической модификации графита:
- для химической модификации используют обычный природный графит, который не требует дополнительной подготовки;
- процесс протекает в водной среде;
- модификация проводится при атмосферном давлении, без применения инертной атмосферы и опасных соединений;
- загрузки реагентов для осуществления предлагаемого способа модификации природного графита в несколько раз превышают загрузки в способе-прототипе;
- выделение модифицированного графита не требует специальных процедур и долгой сушки при пониженном давлении и состоит в многократной промывке горячей водой и сушке при температуре 120-130°C до постоянной массы.
Способ химической модификации графита, включающий взаимодействие графита с фторсодержащим реагентом, выделение и сушку целевого продукта, отличающийся тем, что в качестве исходного графита используют природный графит, в качестве фторсодержащего реагента - калийные соли перфтор(ω-хлорперфтор)карбоновых кислот, процесс ведут в присутствии персульфата калия при температуре 90-95°С в водной среде, выделение целевого продукта осуществляют фильтрацией и промывкой горячей водой, а сушку ведут на воздухе при температуре 120-130°С.