Окклюдер для чрезкожной транслюминальной процедуры (варианты), способ чрезкожного транслюминального закрытия отверстия в сердце, способ активизации васкуляризации ткани млекопитающего in vivo и способ активизации заживления места анастомоза
Иллюстрации
Показать всеЗаявленная группа изобретений относится к медицине, в частности к трансплантологии. Окклюдер состоит из поддерживающей структуры, соединенный с закупоривающей оболочкой, которая содержит конструкт клеточного матрикса, включающий клетки фибробластов и в норме выделяемые клетками фибробластов компоненты эндогенно-продуцированного внеклеточного матрикса. Посредством окклюдера осуществляют способ чрезкожного транслюминального закрытия отверстия в сердце путем установки в зоне дефекта. Кроме того, посредством окклюдера выполняется способ активации васкуляризации ткани млекопитающего. Заявленная группа изобретений позволяет закрыть дефекты органов, восстановить поврежденные ткани, активизировать васкуляризацию в месте дефекта. 5 н. и 16 з.п.ф-лы, 21 пр., 19 ил.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к тканевой инженерии, в частности к имплантации или прикреплению биоинженерных тканевых конструктов для активизации эндотелиализации и васкуляризации в сердце и в соответствующих тканях.
Уровень техники
Коронарная болезнь сердца является сегодня единственной главной причиной смерти в Америке (American Heart Association's "1999 Heart and Stroke Statistical Update"). Эта болезнь, как и другие различные сердечнососудистые заболевания, характеризуется сужением артерий и недостаточным кровотоком к критическим тканям.
Используемые в настоящее время клинические способы улучшения кровотока в больном или иным образом поврежденном сердце включают инвазивные хирургические технические приемы, такие как операция шунтирования на коронарных артериях, пластическая операция на сосудах и эндартерэктомия. Такие процедуры, конечно, включают высокие степени неотъемлемого риска во время и после проведения операции и часто обеспечивают только временным средством при сердечной ишемии. При попытке улучшить прогноз хирургических операций на сердце врачи и исследователи предпринимали попытки использования насосов для содействия кровотоку во время проведения операции. Однако такие насосы только выполняют роль временных содействующих приспособлений во время операции, их нельзя использовать в качестве разновидности лечения сердечного заболевания. Альтернативой коронарному шунтированию и другим хирургическим процедурам для улучшения кровотока в сердце является стимулирование тканей в сердце к образованию новых кровеносных сосудов.
Внутри сердца могут возникать, либо врожденно или быть приобретенными, аномальные отверстия, дыры или шунты между камерами сердца или между большими сосудами, которые могут являться причиной нецелесообразного протекания через них крови. Такие деформации обычно являются врожденными и происходят во время эмбрионального периода, когда сердце формируется из складчатой трубки в четырехкамерную, двухсекционную систему. Деформации перегородки возникают в результате неполного образования перегородки или мышечной стенки между камерами сердца и могут вызывать существенные проблемы.
Одна такая деформация или дефект, открытое овальное окно, является постоянным односторонним отверстием, как правило, подобным клапану, между правым предсердием и левым предсердием сердца. Поскольку давление левого предсердия обычно выше давления правого предсердия, клапан, как правило, остается закрытым. Однако при определенных условиях давление правого предсердия превышает давление левого предсердия, создавая возможность для сброса крови "справа-налево", которое позволяет сгусткам крови входить в большой круг кровообращения. Это является, в частности, проблематикой для больных, которые предрасположены к образованию венозных тромбов, например, для больных с глубоким венозным тромбозом или с нарушениями свертывания крови. Также предполагают, что сброс крови между камерами можно вовлечь в мигрени.
Более того, определенные пациенты предрасположены к предсердным аритмиям (т.е. ненормальным ритмам сердца, которые могут являться причиной того, что сердце качает менее эффективно). При такой общей аномалии, фибрилляции предсердий, две верхние камеры сердца (т.е. левое предсердие и правое предсердие) фибриллируют вместо эффективных сокращений. Поскольку предсердие не сокращается и почти незаполнено во время фибрилляции предсердий, то кровь может застаиваться в стенках и образовывать сгустки, которые затем проходят в сердце и в мозг, вызывая внезапный приступ или преходящее ишемическое нарушение мозгового кровообращения. Эти сгустки обычно образуются в слепом мешке в сердце, называемом левым ушком предсердия, из-за проявляющейся в нем тенденции к низкому или застойному току.
Чрезкожное закрытие открытого овального окна, а также похожие сердечные отверстия, такие как дефект межпредсердной перегородки или дефект межжелудочковой перегородки, и облитерацию левого ушка предсердия можно провести с использованием различных механических приспособлений. Эти приспособления обычно состоят из металлического структурного каркаса с подпирающим материалом, прикрепленным к нему. Однако доступные в настоящее время запирающие устройства часто сложны в изготовлении, нестабильны при работе, требуют проведения технически сложной процедуры имплантации, имеют недостаток анатомической совместимости и приводят к осложнениям (например, образованию тромбов, хроническому воспалению, остаточным протеканиям, перфорациям, переломам и повреждениям проводящей системы сердца).
Поэтому имеется необходимость в усовершенствованных приспособлениях и соответствующих способах закрытия сердечных отверстий, например, таких как открытое овальное окно, и облитерации сердечных слепых мешков, например, таких как левое ушко предсердия.
Область тканевой инженерии объединяет методы биоинженерии с принципами наук о жизни для понимания структурных и функциональных взаимосвязей в обычных и патологических тканях млекопитающих. Целью тканевой инженерии является разработка и конечное применение биологических заменителей для восстановления, поддержания или улучшения функций ткани. Таким образом, посредством тканевой инженерии можно сконструировать и изготовить биоинженерную ткань в лаборатории. Биоинженерные ткани могут включать в себя клетки, которые обычно связаны с нативными тканями млекопитающего или человека и с синтетическими или экзогенными матриксными каркасами. Новая биоинженерная ткань должна быть функциональной при пересаживании на организм-хозяин и быть постоянно включенной в организм хозяина или прогрессивно биореконструируемой клетками из организма реципиента. Изготовление эквивалента ткани без поддерживающего члена или без каркаса представляет собой научный вызов при создании новой биоинженерной ткани.
Раскрытие изобретения
Настоящее изобретение относится к способу активизации образования кровеносных сосудов в тканях и органах. В частности, способ относится к имплантации или прикреплению конструктов клеточного матрикса для активизации эндотелиализации и развития кровеносных сосудов в сердце и соответствующих тканях.
Изобретение имеет различные приложения, включая, без ограничений, активизацию восстановления и регенерации поврежденной сердечной мышцы, активизацию васкуляризации и заживления во время проведения операции на сердце (например, хирургии методом обходного шунтирования или замены сердечного клапана), активизацию образования кровеносных сосудов в местах анастомоза и активизацию васкуляризации и заживления ишемических или иным образом поврежденных тканей, таких как скелетная мышца, гладкая мышца, мозговая ткань или соединительная ткань.
Изобретение основано отчасти на открытии того, что конструкты клеточного матрикса при имплантации в раненном слое пациентов с диабетическими язвами стопы способны индуцировать быструю эндотелиализацию и васкуляризацию, приводя в результате к образованию новых капилляров и к уменьшению воспаления в области раненной ткани.
Конструкты клеточного матрикса выделяют различные факторы роста, критичные для регенерации ткани и развития кровеносных сосудов, наиболее заметно фактор роста васкулярного эндотелия, или VEGF. Изобретение охватывает нанесение конструкта клеточного матрикса на поврежденные ткани, например, поврежденную сердечную мышцу, для индуцирования нового местного кровоснабжения к области и поддержания быстрого реконструирования ткани.
Имплантат конструкта клеточного матрикса можно также использовать для активизации образования "природного" каротидного шунта для содействия или устранения необходимости в операции методом каротидной эндартерэктомии (которая часто может приводить к внезапному приступу из-за нисходящего тока частиц, перемещающихся во время операции).
Настоящее изобретение также включает как отличительный элемент приспособление и соответствующие способы для чрезкожного закрытия сердечного отверстия, например, такого как открытое овальное окно, дефект межпредсердной перегородки или дефект межжелудочковой перегородки, и для чрезкожной облитерации сердечного слепого мешка, например, такого как левой ушко предсердия. Подпирающий материал изобретенного приспособления включает, по меньшей мере отчасти, внеклеточный матрикс, сформированный из культивируемых клеток, например, конструкт клеточного матрикса. В предпочтительном варианте осуществления, конструкт клеточного матрикса содержит фибропласты, например, полученные из дермы, для образования культивируемого дермального конструкта со слоем кератиноцитов, культивированных на нем для образования эпидермального слоя, давая в результате культивированный двухслойный конструкт кожи. Культивируемые конструкты кожи изобретения выражают многие физические, морфологические и биохимические характеристики естественной кожи. В еще более предпочтительном варианте осуществления, конструктом клеточного матрикса является тканевый конструкт, который схож с дермальным слоем кожи, человеческий дермальный конструкт, который формируется в определенной системе, содержащие клетки человеческого происхождения без использования химически неопределенных компонентов во время его культивирования. В наиболее предпочтительных вариантах осуществления, конструкты клеточного матрикса изобретения изготавливают в системе определенного химического состава, содержащей клетки человеческого происхождения, но без химически неопределенных или нечеловеческих биологических компонентов или клеток. В результате такой структуры вышеупомянутые недостатки, связанные с приспособлениями, известными в данной области техники, минимизируются или устраняются.
В общем, в одном аспекте, изобретение содержит в себе как отличительный элемент окклюдер для чрезкожной транслюминальной процедуры. Окклюдер включает всеобъемлющую поддерживающую структуру и множество окклюзионных оболочек, соединенных с общей поддерживающей структурой. По меньшей мере одна из окклюзионных оболочек включает конструкт клеточного матрикса.
Полная поддерживающая структура включает металл или, в качестве альтернативы, саморассасывающийся полимер, например, такой как полимолочная кислота.
В еще одном варианте осуществления общая поддерживающая структура включает как проксимальную поддерживающую структуру, так и дистальную поддерживающую структуру. В одном варианте осуществления проксимальная поддерживающая структура и дистальная поддерживающая структура образуют вместе зажим. В другом варианте осуществления проксимальная поддерживающая структура включает множество вытягивающихся наружу проксимальных ветвей, а дистальная поддерживающая структура включает множество вытягивающихся наружу дистальных ветвей. Проксимальная поддерживающая структура может присоединяться к проксимальной закупоривающей оболочке, а дистальная поддерживающая структура может присоединяться к дистальной закупоривающей оболочке.
В другом аспекте изобретение содержит в себе как отличительный элемент - окклюдер для чрезкожной транслюминальной процедуры. Окклюдер включает общую поддерживающую структуру и, по меньшей мере, одну закупоривающую оболочку, присоединенную к общей поддерживающей структуре. По меньшей мере, одна закупоривающая оболочка включает конструкт клеточного матрикса. В особом варианте осуществления, по меньшей мере, одна закупоривающая оболочка включает антитромбообразующее вещество.
В еще одном аспекте изобретение содержит в себе как отличительный элемент - способ чрезкожного транслюминального закрытия сердечного отверстия в организме больного. Способ включает введение окклюдера в сердце больного и установку окклюдера в определенное положение, по меньшей мере, отчасти в пределах сердечного отверстия до существенного закупоривания сердечного отверстия. Окклюдер включает общую поддерживающую структуру и, по меньшей мере, одну закупоривающую оболочку, присоединенную к общей поддерживающей структуре. По меньшей мере, одна закупоривающая оболочка включает конструкт клеточного матрикса.
В некоторых вариантах осуществления данного изобретения сердечным отверстием является, например, открытое овальное окно, дефект межпредсердной перегородки или дефект межжелудочковой перегородки. В другом варианте осуществления общая поддерживающая структура окклюдера включает проксимальную поддерживающую структуру и дистальную поддерживающую структуру. Проксимальная поддерживающая структура присоединяется к проксимальной закупоривающей оболочке, а дистальная поддерживающая структура присоединяется к дистальной закупоривающей оболочке. Часть общей поддерживающей структуры располагается в пределах сердечного отверстия, в то время как проксимальная закупоривающая оболочка и дистальная закупоривающая оболочка располагаются на различных сторонах сердечного отверстия. В еще одном аспекте изобретение содержит в себе как отличительный элемент - способ чрезкожной транслюминальной облитерации слепого мешка в сердце пациента. Способ включает введение окклюдера в сердце пациента и размещение окклюдера, по меньшей мере, частично в пределах слепого мешка сердца и до значительной облитерации слепого мешка сердца. Окклюдер включает общую поддерживающую структуру и, по меньшей мере, одну закупоривающую оболочку, присоединенную к общей поддерживающей структуре. По меньшей мере, одна закупоривающая оболочка включает конструкт клеточного матрикса. В одном варианте осуществления данного аспекта изобретения слепым мешком сердца является левое ушко предсердия.
В дополнительном аспекте изобретение содержит в себе как отличительный элемент - способ изготовления окклюдера для чрезкожной транслюминальной процедуры. Способ включает приготовление общей поддерживающей структуры и присоединение множества закупоривающих оболочек к общей поддерживающей структуре. По меньшей мере, одна из множества закупоривающих оболочек включает конструкт клеточного матрикса.
В различных вариантах осуществления данного аспекта изобретения, по меньшей мере, одну закупоривающую оболочку, которая включает конструкт клеточного матрикса, например, пришивают, ламинируют или приклеивают к общей поддерживающей структуре и покрывают тромбонеобразующим веществом в виде слоя.
Изобретение, кроме того, относится к биоинженерным тканевым конструктам культивируемых клетокиэндогенно-продуцируемых компонентов внеклеточного матрикса, для которых не требуются компоненты эндогенного матрикса или сетевые поддерживающие или подпирающие элементы. Таким образом, изобретение можно преимущественно изготовить полностью из человеческих клеток и компонентов человеческого матрикса, продуцируемого теми клетками, например, при конструировании биоинженерного тканевого конструкта для использования в организме человека. Изобретение также относится к способам получения тканевых конструктов путем стимуляции клеток в культуре, таких как фибропласты, для получения компонентов внеклеточного матрикса либо без добавления компонентов экзогенного матрикса, сетевой поддержки, либо без добавления подпирающих элементов.
Изобретение также относится к способам получения тканевых конструктов путем стимуляции клеток в культуре, таких как фибропласты, к получению компонентов внеклеточного матрикса в системе с определенной средой и/или без использования неопределенных биологических компонентов или биологических компонентов нечеловеческого происхождения, таких как бычья сыворотка или экстракты органов.
Кроме того, этот тканевый конструкт можно изготовить посредством последовательных засевов различных типов клеток для получения культивируемого тканевого конструкта, который имитирует клеточный состав и тканевые структуры нативных тканей.
Более того, тканевый конструкт продуцируется и самособирается культивируемыми клетками без необходимости в подпирающей опоре или в добавлении компонентов экзогенного внеклеточного матрикса. Прочностные характеристики тканевых конструктов делают их управляемыми для их легкого отслаивания из аппарата по культивированию, в котором они образуются и непосредственно трансплантируются, не требуя какой-либо опоры или носителя в клинических и испытательных приложениях.
Тканевые конструкты изобретения пригодны в клинических целях, например, для пересаживания больному с дефектом ткани или органа, таким как кожная язва или рана, или для in vitro испытания ткани или для ксенотрансплантации, например для безопасности испытания или для оценки достоверности фармацевтических, косметических или химических продуктов.
Краткое описание чертежей
На чертежах похожие условные обозначения, как правило, относятся к одинаковым частям на всех различных проекциях. Также чертежы не нуждаются в обязательном масштабировании, выделении вместо принципов изобретения, обычно размещаемых при иллюстрации.
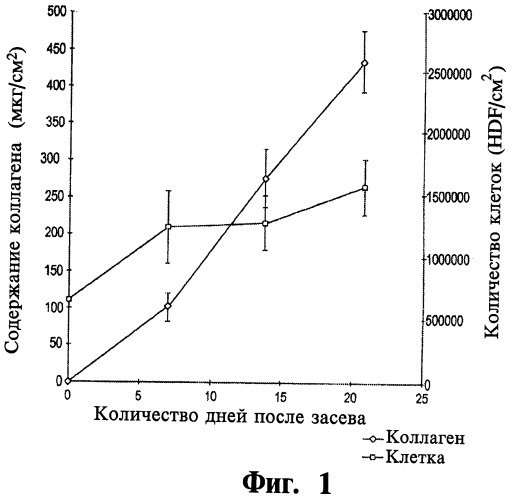
Фигура 1 - это графическое отображение увеличения концентрации коллагена, определяемой по анализу гидроксипролину, по сравнению с количеством клеток в дермальном конструкте, полученным из клеток крайней плоти новорожденного человека и описываемым в Примере 1.
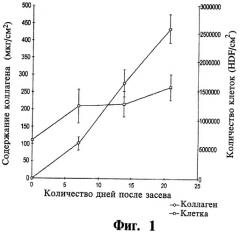
Фигура 2 - это микрофотография (объектив 20Х) зафиксированной, заделанной парафином, окрашенной гематоксилином и эозином секции конструкта клеточного матрикса, образованного из культивированных дермальных фибропластов человека в среде определенного химического состава на 21 день. Пористая мембрана имеет вид тонкой полупрозрачной полосы снизу от конструкта.
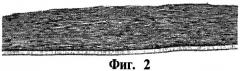
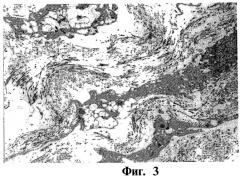
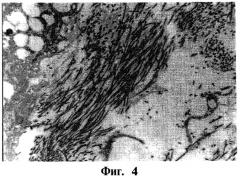
На фигуре 3 и 4 показаны изображения, полученные методом просвечивающей электронной микроскопии (ПЭМ), двух увеличений конструкта клеточного матрикса, образованного из культивированных дермальных фибропластов человека в среде неопределенного химического состава на 21 день, где
фигура 3 - это 7600-кратное увеличение, показывающее эндогенную матрицу, включая ряд коллагеновых волокон между фибропластами; фигура 4 - 19000-кратное увеличение полностью сформированных эндогенных коллагеновых волокон, показывающее расположение и упаковку фибрилл.
Фигура 5 - это микрофотография (объектив 20Х) зафиксированной, заделанной парафином, окрашенной гематоксилином и эозином секции конструкта кожи, образованного в среде определенного химического состава в отсутствии компонентов экзогенного матрикса, который содержит конструкт клеточного матрикса, образованный из культивированных дермальных фибропластов человека в среде определенного химического состава с многослойным, дифференцированным эпидермисом, сформированным из культивированных человеческих кератиноцитов в среде определенного химического состава.
Фигура 6 - это вид сердца в разрезе, иллюстрирующий открытое овальное окно.
Фигура 7 - это частный вид другого сердца в поперечном разрезе, иллюстрирующий левое ушко предсердия.
Фигура 8 - это схематический вид сверху окклюдера согласно иллюстративному варианту осуществления изобретения.
Фигура 9 - это схематический вид в поперечном разрезе иллюстративного окклюдера, показанного на Фигуре 7.
Фигура 10 - это схематический вид сверху окклюдера согласно другому иллюстративному варианту осуществления изобретения.
Фигура 11 - это схематический вид сбоку иллюстративного окклюдера, показанного на Фигуре 9.
Фигура 12 - это схематический перспективный вид окклюдера согласно другому иллюстративному варианту осуществления изобретения.
Фигура 13 - это схематический перспективный вид окклюдера для облитерации слепого мешка сердца согласно иллюстративному варианту осуществления изобретения.
Фигура 14 - это схематический перспективный вид окклюдера для облитерации слепого мешка сердца согласно другому иллюстративному варианту осуществления изобретения.
На фигурах 15-19 иллюстрируются этапы согласно иллюстративному варианту осуществления изобретения подачи окклюдера к анатомическому месту в теле больного.
Осуществление изобретения
Настоящее изобретение относится к способу активизации образования кровеносных сосудов в тканях и органах пациента, в частности человека. В частности, способ относится к имплантации или прикреплению конструкта клеточного матрикса для активизации эндотелиализации и развития кровеносных сосудов в сердце и в соответствующих тканях.
Изобретение имеет разнообразные приложения, включая, без ограничения, активизацию восстановления и регенерации поврежденной сердечной мышцы, активизацию васкуляризации и заживления во время проведения операции на сердце (например, операции обходного шунтирования или замены клапана сердца), активизацию образования кровеносных сосудов в местах анастомоза и активизацию васкуляризации и восстановления поврежденной скелетной мышцы, соединительной ткани и других тканей.
До сих пор, разрабатываемые в настоящее время живые тканевые конструкты собираются не полностью из клеток и должны полагаться либо на добавление или внедрение компонентов экзогенного матрикса, либо синтетических членов для структуры или опоры, либо на то и другое.
Биоинженерные тканевые конструкты, описываемые в этом документе, проявляются много нативных характеристик тканей, из которой происходят их клетки. Продуцируемые таким образом тканевые конструкты можно использовать для пересаживания пациенту или для in vitro тестирования.
Одним предпочтительным вариантом осуществления является конструкт клеточного матрикса, содержащий первый клеточный тип и эндогенно продуцируемый внеклеточный матрикс, в котором первый клеточный тип способен синтезировать и выделять внеклеточный матрикс для получения конструкта клеточного матрикса.
Другим предпочтительным вариантом осуществления является двухслойный конструкт, содержащий первый клеточный тип и эндогенно-продуцируемый внеклеточный матрикс и слой клеток второго типа, располагаемых на нем или в пределах конструкта клеточного матрикса, формируемого первым клеточным типом.
Более предпочтительным вариантом осуществления является конструкт клеточного матрикса, содержащий фибропласты, например фибропласты, полученные из дермы, для образования культивируемого дермального конструкта.
Другим более предпочтительным вариантом осуществления является конструкт клеточного матрикса, содержащий фибропласты, например фибропласты, полученные из дермы для образования культивируемого дермального конструкта со слоем кератиноцитов, культивируемых на нем для образования эпидермального слоя, что приводит в результате к культивируемому двухслойному кожному конструкту. Культивируемые кожные конструкты изобретения имеют многие физические, морфологические и биохимические характеристики естественной кожи.
В еще более предпочтительном варианте осуществления конструктом клеточного матрикса является тканевый конструкт, который похож на дермальный слой кожи, человеческий дермальный конструкт, который образуется в определенной системе, содержащей клетки человеческого происхождения без использования неопределенных химических компонентов во время его культивирования.
В наиболее предпочтительном варианте осуществления тканевые конструкты изобретения изготавливают в системе определенного химического состава, содержащей клетки человеческого происхождения, но не содержащей химически неопределенные и нечеловеческие биологические компоненты или клетки.
В альтернативном варианте осуществления изобретения конструкт клеточного матрикса, который обрабатывается методами генной инженерии, приобретая улучшенные свойства для индуцирования развития кровеносных сосудов, можно использовать для активизации образования новых кровеносных сосудов в сердце или в других тканях.
Надо понимать, что какой-либо специалист в данной области техники сможет регулировать ангиогенную активность конструкта клеточного матрикса путем включения клеток, которые выделяют различные количества ангиогенных факторов. Например, известно, что клетки васкулярной гладкой мышцы, предпочтительно клетки аортальной гладкой мышцы, выделяют существенно большее количество VEGF по сравнению с человеческими дермальными фибробластами. Поэтому можно культивировать конструкты клеточного матрикса с повышенной ангиогенной активностью путем использования клеток аортальной гладкой мышцы вместо фибробластов или в дополнение к ним.
В другом варианте осуществления изобретение включает способ лечения ишемического поражения сердца, мозга, внутренних органов или периферийных тканей. Например, не с целью ограничения, один вариант осуществления изобретения влечет за собой прикрепление конструкта клеточного матрикса к ишемической области сердца после инфаркта миокарда для активизации васкуляризации сердца и регенерации клеток поврежденной сердечной мышцы. В случае ишемии головного мозга (например, возникшей из-за внезапного приступа или и/или повышенного внутричерепного давления) конструкт клеточного матрикса может включать фибробласты, нервные глиальные клетки, нервные стволовые клетки, астроциты, фибробласты, трансфицированные фактором роста нервов, или их комбинацию. Такой конструкт клеточного матрикса, содержащий любые из этих клеток, помещают прямо на кору головного мозга или хирургически имплантируют в область ишемии.
В более предпочтительном варианте осуществления способ лечения обратимой ишемии миокарда и активизации развития кровеносных сосудов состоит в нанесении конструкта клеточного матрикса на область ишемического поражения, при этом конструкт клеточного матрикса содержит культивированные дермальные фибробласты новорожденного. Преимущества дермальных фибробластов новорожденного заключаются в том, что они, как предполагается, обладают пластическими качествами, т.е. они обладают способностью трансдифференциации; они являются идеальными для гипоксической среды; они, как предполагается, являются безопасными, биосовместимыми и иммунно-индиффирентными, поскольку не вызывают отторжение у пациента. Эти клетки также поставляют продукты, продуцируемые клетками, например, факторы роста и цитокины, и поэтому способствуют восстановлению ткани собственными клетками пациента. Это восстановление также приводит к образованию микрососудов, увеличивая локальное кровоснабжение в подвергаемом лечению миокарде. В наиболее предпочтительном варианте осуществления этот конструкт клеточного матрикса получают в отсутствии компонентов животного происхождения и в культуральной среде определенного химического состава, не содержащего какие-либо материалы экзогенного матрикса и синтетические полимеры, такие как сетчатая подложка. В разновидности данного варианта осуществления конструкт клеточного матрикса, кроме того, содержит клетки, выбираемые из группы, состоящей из: стволовых клеток костного мозга, эмбриональных стволовых клеток, клеток-предшественников (включая эндотелиальные клетки-предшественники, сердечные клетки-предшественники), скелетных миобластов, кардиомицитов; или эндотелиальных клеток, клеток гладкой мышцы, фибробластов и клеток-предшественников, полученных из жировой ткани.
В еще одном варианте осуществления изобретение включает нанесение конструкта клеточного матрикса на любую ткань или орган для активизации развития кровеносных сосудов. Пациенты с симптомами застойной сердечной недостаточности, включая истончение стенок, пониженную функциональность желудочковой стенки и фракции изгнания, могут получить пользу от приживления конструкта клеточного матрикса к нарушенной сердечной ткани для снижения этих симптомов.
Один предпочтительный вариант осуществления изобретения содержит структурный слой, состоящий, по меньшей мере, из одного типа клеток, образующих внеклеточный матрикс, и компоненты эндогенно-продуцируемого внеклеточного матрикса, более упрощенно обозначаемого термином "матрикс", при этом матрикс полностью синтезируется клетками и собирается посредством культивирования клеток. Такой слой в этом документе обозначается термином "конструкт клеточного матрикса" или "слой клеточного матрикса", потому что клетки секретируют и содержатся сами по себе в пределах и на всем протяжении их матрикса. Для культивируемых тканевых конструктов не требуются, тем самым они не включают, компоненты экзогенного матрикса, а именно компоненты матрикса не выделяются культивируемыми клетками, а вводятся другими способами. В более предпочтительном варианте осуществления показано, что конструкт клеточного матрикса, образованный человеческими дермальными фибробластами, имеет преобладающую концентрацию коллагена, сходную с таковой естественной кожи. Как доказано методом электронной микроскопии, матрикс по природе является волокнистым и содержит коллаген, который проявляет четырехступенчатый 67 нм характер исчерченности, а также организацию упаковки фибрилл и фибрилльных связок подобно природному коллагену. Методом электрофореза ПААГ-ДСН (полиакриламидный гель, додецилсульфат натрия) с задержанным снижением обнаружено наличие в этих конструктах коллагена как типа I, так и типа III, - преобладающие типы коллагена, найденные в естественной коже человека. Используя стандартные методики иммунногистохимиии (ИГХ), дермальный конструкт клеточного матрикса окрашивается положительно декорином - протеогликан дерматансульфат, который, как известно, ассоциирован с коллагеновыми фибриллами и, как предполагается, регулирует диаметр фибрилл in vivo. Декорин можно также визуализировать в конструкте посредством просвечивающей электронной микроскопии (ПЭМ). Продуцируемая ткань также окрашивается положительно тенасцином - гликопротеином внеклеточного матрикса, обнаруживаемым, например, в мезенхиме или в ткани при восстановлении. Подобно ткани при восстановлении in vivo, показано, что в ткани, полученной в культуре, увеличено содержание коллагена типа 1 по отношению к типу III при формировании матрикса. Не стремясь связать это с теорией, предполагают, что клетки быстро заполняют открытое пространство между ними рыхлым аналогом матрикса, состоящим главным образом из коллагена типа III и фибронектина, - для грануляции ткани, а затем реконструируют этот рыхлый матрикс плотным матриксом, состоящим главным образом из коллагена типа I. Показано, что продуцируемый клеточный матрикс содержит гликозаминогликаны (ГАГ), например, гиалуроновую кислоту (ГК); фибронектин; протеогликаны, кроме декорина, такие как бигликан и версикан; и профиль сульфированных гликозаминогликанов, например, дигиалуроновую кислоту; ди-хондроитин-O-сульфат; ди-хондроитин-4-сульфат; ди-хондроитин-6-сульфат; ди-хондроитин-4,6-сульфат; ди-хондроитин-4-сульфат-UA-2S; и ди-хондроитин-6-сульфат-UA-2S. Эти структурные и биохимические особенности проявляются сами по себе во время развития конструкта в культуре и становятся отчетливо различимыми, когда конструкт приближается к своей конечной форме. Присутствие этих компонентов в полностью сформированном культивированном дермальном конструкте клеточного матрикса указывает на то, что конструкт имеет структурные и биохимические характеристики, приближающиеся к обычной дерме.
Тогда как вышеупомянутый перечень является перечнем биохимических и структурных характерестик культивируемого конструкта клеточного матрикса, образованного из дермальных фибробластов, следует понимать, что культивируемые конструкты клеточного матрикса, образованные из других типов фибробластов будут обладать многими из этих и других характеристик, фенотипических для ткани, из которой они происходят. В некоторых случаях можно заставить фибробласты экспрессировать нефенотипические компоненты либо посредством физических нагрузок, химического воздействия или контакта, либо посредством трансгенных способов. Другим предпочтительным вариантом осуществления изобретения является слой клеточного матрикса, в котором есть второй слой клеток, располагаемых на нем. Второй слой клеток культивируется на слое клеточного матрикса для образования биоинженерного двухслойного тканевого конструкта. В более предпочтительном варианте осуществления клетки второго слоя по происхождению являются эпителиальными. В наиболее предпочтительном варианте осуществления второй слой содержит культивированные человеческие кератиноциты, которые вместе с первым слоем клеточного матрикса, конструктом клеточного матрикса, образованным из дермальных фибробластов и эндогенного матрикса для образования дермального слоя, составляют живой кожный конструкт. Полностью сформированный эпидермальный слой представляет собой многослойный, стратифицированный и хорошо дифференцированный слой кератиноцитов, который может проявлять себя в качестве базального слоя, надбазального слоя, зернистого слоя и рогового слоя. Кожный конструкт имеет хорошо развитую базальную мембрану, находящуюся при дермально-эпидермальном соединении, что показано методом просвечивающей электронной микроскопии (ПЭМ). Базальная мембрана выглядит самой толстой вокруг полудесмосом, маркированных фиксирующими фибриллами, которые состоят из коллагена типа VII, что визуализируется посредством ПЭМ. Фиксирующие фибриллы могут выглядеть выходящими из базальной мембраны, захватывая коллагеновые фибриллы в дермальном слое. Эти фиксирующие фибриллы, а также другие компоненты базальной мембраны, выделяются кератиноцитами. Также известно, что пока кератиноциты способны выделять компоненты базальной мембраны вокруг себя, то распознаваемая базальная мембрана не будет образовываться в отсутствии фибробластов. Иммунногистохимическое окрашивание кожного конструкта настоящего изобретения также показало присутствие ламинина - белка базальной мембраны.
В предпочтительном способе изобретения для образования конструкта клеточного матрикса первый клеточный тип, клеточный тип, образующий внеклеточный матрикс, засевают на субстрат, культивируют и индуцируют к синтезу и выделению упорядоченного внеклеточного матрикса вокруг них для образования конструкта клеточного матрикса. В другом предпочтительном способе изобретения поверхность конструкта клеточного матрикса засевают клетками второго клеточного типа, которые культивируют для образования двухслойного тканевого конструкта. В более предпочтительном способе полнослойный кожный конструкт, имеющий характеристики, схожие с естественной кожей человека, получают культивированием фибробластов, таких как человеческие дермальные фибробласты, в условиях, достаточных для индуцирования синтеза матрикса для образования клеточного матрикса дермальных клеток и матрикса дермального слоя, на который засевают человеческие эпителиальные клетки, такие как кератиноциты, и культивируют в условиях, достаточных для образования полностью дифференцированного, стратифицированного эпидермального слоя.
Таким образом, один способ получения тканевых конструктов настоящего изобретения включает в себя:
(а) культивирование, по меньшей мере, одного клеточного типа, образующего внеклеточный матрикс, в отсутствии компонентов экзогенного внеклеточного матрикса или структурного поддерживающего элемента; и,
(б) стимулирование клеток, полученных на стадии (а), к синтезу, выделению и упорядочиванию компонентов внеклеточного матрикса для образования тканевого конструкта, состоящего из клеток и матрикса, синтезируемого этими клетками; где стадии (а) и (б) могут проводить одновременно или последовательно.
Для образования двухслойного тканевого конструкта, содержащего конструкт клеточного матрикса и второй клеточный слой на нем, способ дополнительно включает стадию: (в) культивирования клеток второго типа на поверхности образованного тканевого конструкта для получения двухслойного тканевого конструкта.
В качестве клеточного типа, образующего внеклеточный матрикс, в изобретении можно исполь