Производные бензазепина, пригодные для использования в качестве антагонистов вазопрессина
Иллюстрации
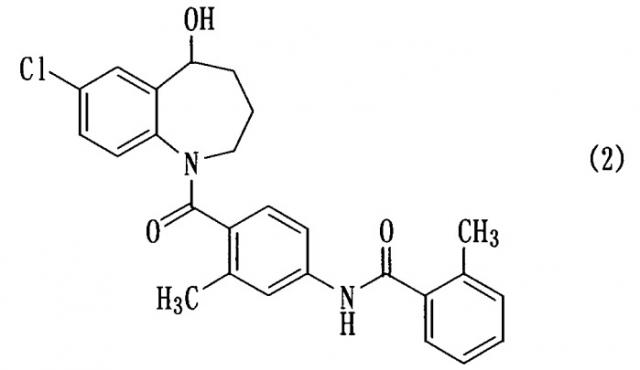
Показать всеИзобретение относится к соединению бензазепина общей формулы (1), обладающего свойством антагониста вазопрессина, и к фармацевтическому препарату на его основе. Соединение формулы (1) может поддерживать уровень толваптана в крови в течение длительного периода времени, что позволяет обеспечить желаемые фармацевтические эффекты. В общей формуле (1)
R1 обозначает группу (1-1) или с (1-3) по (1-7): (1-1) представляет собой группу -CO-(CH2)n-COR2, в которой п обозначает целое число от 1 до 4, R2 обозначает (2-1) гидроксильную группу; (2-2) низшую алкокси-группу, в случае необходимости замещенную гидроксильной группой, низшей алканоильной группой, низшей алканоилокси-группой, низшей алкоксикарбонилокси-группой, циклоалкилоксикарбонилокси-группой или 5-метил-2-оксо-1,3-диоксол-4-илом; или (2-3) аминогруппу, в случае необходимости замещенную гидрокси-низшим алкилом; (1-3) представляет собой группу -CO-(CH2)p-O-CO-NR5R6, в которой p обозначает целое число от 1 до 4, R5 обозначает низшую алкильную группу, и R6 обозначает группу низший алкоксикарбонил-низший алкил; (1-4) представляет собой группу -CO-(CH2)q-X-R7, в которой q обозначает целое число от 1 до 4, Х обозначает атом кислорода, атом серы или сульфонильную группу, и R7 обозначает группу карбокси-низший алкил или группу низший алкоксикарбонил-низший алкил; (1-5) представляет собой группу -CO-R8, (в которой R8 обозначает (8-1) алкильную группу, в случае необходимости замещенную атомом галогена, низшей алканоилокси-группой или фенильной группой (замещенной дигидроксифосфорилокси-группой, в которой гидроксильные группы могут быть замещены бензильными группами, и низшей алкильной группой), (8-2) низшую алкокси-группу, замещенную атомом галогена, низшей алканоилокси-группой или дигидроксифосфорилокси-группой, (8-3) пиридильную группу или (8-4) низшую алкоксифенильную группу; (1-6) представляет собой низшую алкильную группу, замещенную группой, выбранной из группы, состоящей из низшей алкилтио-группы, дигидроксифосфорилокси-группы и низшей алканоилокси-группы; и (1-7) представляет собой пептидный остаток, в случае необходимости защищенный одной или более защитными группами. 2 н. и 4 з.п.ф-лы, 4 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к новому соединению бензазепина и к фармацевтическому препарату.
УРОВЕНЬ ТЕХНИКИ
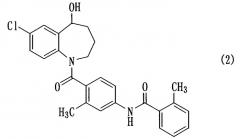
Толваптан, представленный следующей формулой (2), является известным соединением и раскрыт, например, в патенте США 5258510 (Пример 1199).
Известно, что толваптан может быть использован в качестве антагониста вазопрессина, имеющего акваретическую эффективность (Circulation, 107, pp. 2690-2696 (2003)). Однако из-за своей низкой водорастворимости толваптан имеет проблемы, связанные с его плохой абсорбцией из желудочно-кишечного тракта, и его лекарственная форма и путь введения ограничены. С точки зрения лечения было желательно разработать новое лекарственное средство, которое могло бы поддерживать в течение длительного периода времени уровень толваптана в крови, позволяющий обеспечить желаемые фармацевтические эффекты.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является получение нового соединения бензазепина, которое имело бы превосходные свойства, такие как поддержание уровня толваптана в крови в течение длительного периода времени, позволяющего обеспечить желаемые фармацевтические эффекты.
Авторы настоящего изобретения провели обширные исследования для решения указанной задачи и в результате обнаружили, что соединения бензазепина, представленные общей формулой (1), имеют превосходные свойства, такие как поддержание фармацевтических эффектов активного ингредиента толваптана в течение длительного периода времени в организме. Настоящее изобретение было осуществлено на основании указанных открытий.
Настоящее изобретение относится к следующим соединениям бензазепина и к фармацевтическим препаратам, содержащим соединения, показанные ниже в пунктах 1-3.
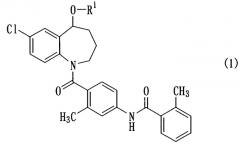
Пункт 1. Соединение бензазепина, представленное общей формулой (1)
в которой R1 обозначает группу с (1-1) по (1-7):
(1-1) представляет собой группу -CO-(CH2)n-COR2, в которой n обозначает целое число от 1 до 4, R2 обозначает (2-1) гидроксильную группу; (2-2) низшую алкокси-группу, в случае необходимости замещенную гидроксильной группой, низшей алканоильной группой, низшей алканоилокси-группой, низшей алкоксикарбонилокси-группой, циклоалкилоксикарбонилокси-группой или 5-метил-2-оксо-1,3-диоксол-4-илом; или (2-3) аминогруппу, в случае необходимости замещенную гидрокси-низшим алкилом;
(1-2) представляет собой группу -CO-(CH2)m-NR3R4, в которой m обозначает целое число от 0 до 4, R3 обозначает атом водорода или низшую алкил группу, R4 - (4-1) атом водорода; (4-2) низшую алкильную группу, в случае необходимости замещенную атомом галогена, низшей алкиламиногруппой, низшей алкоксикарбонильной группой или 5-метил-2-оксо-1,3-диоксол-4-илом; или (4-3) низшую алкоксикарбонильную группу, в случае необходимости замещенную атомом галогена, низшей алканоилокси-группой или 5-метил-2-оксо-1,3-диоксол-4-илом, R3 и R4 могут образовывать 5-6-членное насыщенное гетероциклическое кольцо путем связывания R3 и R4 друг с другом, вместе с атомом азота, с которым R3 и R4 связаны непосредственно или через атом азота или атом кислорода, причем гетероциклическое кольцо может быть замещено (4-4) низшей алкильной группой, в случае необходимости замещенной гидрокси-низшим алкокси; (4-5) низшую алкоксикарбонильную группу; (4-6) алкилкарбонильную группу (в случае необходимости замещенную по алкильной группе карбоксильной группой или низшей алкоксикарбонильной группой); (4-7) арилкарбонильную группу; или (4-8) фурилкарбонильную группу;
(1-3) представляет собой группу -CO-(CH2)p-O-CO-NR5R6, в которой p обозначает целое число от 1 до 4, R5 обозначает низшую алкильную группу, и R6 обозначает группу низший алкоксикарбонил-низший алкил;
(1-4) представляет собой группу -CO-(CH2)q-X-R7, в которой q обозначает целое число от 1 до 4, X обозначает атом кислорода, атом серы или сульфонильную группу, и R7 обозначает группу карбокси-низший алкил или группу низший алкоксикарбонил-низший алкил;
(1-5) представляет собой группу -CO-R8, в которой R8 обозначает (8-1) алкильную группу, в случае необходимости замещенную атомом галогена, низшей алканоилокси-группой или фенильной группой (замещенной дигидроксифосфорилокси-группой, в которой гидроксильные группы могут замещены бензильными группами, и низшей алкильной группой), (8-2) низшую алкокси-группу, замещенную атомом галогена, низшей алканоилокси-группой или дигидроксифосфорилокси-группой, (8-3) пиридильную группу или (8-4) низшую алкоксифенильную группу;
(1-6) представляет собой низшую алкильную группу, замещенную группой, выбранной из группы, состоящей из низшей алкилтио-группы, дигидроксифосфорилокси-группы и низшей алканоилокси-группы; и
(1-7) представляет собой аминокислотный или пептидный остаток, в случае необходимости защищенный одной или более защитными группами;
или его соль.
Пункт 2. Соединение согласно Пункту 1, в котором, в формуле (1), R1 обозначает группу, выбранную из группы, состоящей из: -CO-(CH2)n-COOH, в которой n обозначает целое число от 1 до 4; -CO-R8, в которой R8 обозначает алкильную группу; и аминокислотный или пептидный остаток, в случае необходимости защищенный одной или более защитными группами; или его соль.
Пункт 3. Соединение согласно Пункту 1, в котором, в формуле (1), R1 обозначает аланил, саркозил, N-этилглицил, N-пропилглицил, N-метил-N-этилглицил, N-метил-N-пропилглицил, N-метил-N-бутилглицил, N-метил-N-пентилглицил или N-метил-N-гексилглицил; или пептидный остаток, выбранный из группы, состоящей из следующих остатков: саркозил-глицил, глицил-глицил, глицил-саркозил, глицил-аланил, аланил-глицил, саркозил-саркоцил, фенилглицил-аланил, фенилаланил-глицил, фенилаланил-фенилаланил, глицил-глицил-глицил, N,N-диметилглицил-глицил, N-метил-N-этилглицил-глицил, саркозил-глицил-глицил и N,N-диметилглицил-глицил-глицил, каждый из которых может быть защищен одной или более защитными группами; или его соль.
Пункт 4. Соединение согласно Пункту 3, в котором, в формуле (1), R1 обозначает пептидные остатки, выбранные из группы, состоящей из следующих остатков: саркозил-глицил, глицил-глицил, глицил-саркозил, глицил-аланил, аланил-глицил, фенилглицил-аланил, фенилаланил-глицил, фенилаланил-фенилаланил, глицил-глицил-глицил, N,N-диметилглицил-глицил, N-метил-N-этилглицил-глицил и N,N-диметилглицил-глицил-глицил, каждый из которых может быть защищен одной или более защитными группами; или его соль.
Пункт 5. Фармацевтический препарат, содержащий соединение бензазепина по Пункту 1 или его фармакологически приемлемую соль и фармакологически приемлемый разбавитель и/или носитель.
Пункт 6. Фармацевтический препарат согласно Пункту 5, который используется в качестве сосудорасширяющего средства, гипотензивного лекарственного средства, акваретика или ингибитора агрегации тромбоцитов.
Частными примерами групп в общей формуле (1) являются следующие.
В этом описании термин "низший" относится к “C1-6”, если не указано иное.
Примеры низших алканоильных групп включают прямые или разветвленные C2-6 алканоильные группы, такие как ацетил, н-пропионил, н-бутирил, изобутирил, н-пентаноил, трет-бутилкарбонил и н-гексаноил.
Примеры низшей алканоилокси-группы включают прямые или разветвленные C2-6 алканоилокси-группы, такие как ацетилокси, н-пропионилокси, н-бутирилокси, изобутирилокси, н-пентаноилокси, трет-бутилкарбонилокси, и н-гексаноилокси группа.
Примеры низшей алкоксикарбонилокси-группы включают алкоксикарбонилокси-группы, в которых алкокси-группа является прямой или разветвленной C1-6 алкокси-группой, такие как метоксикарбонилокси, этоксикарбонилокси, н-пропоксикарбонилокси, изопропоксикарбонилокси, н-бутоксикарбонилокси, изобутоксикарбонилокси, трет-бутоксикарбонилокси, втор-бутоксикарбонилокси, н-пентилоксикарбонилокси, неопентилоксикарбонилокси, н-гексилоксикарбонилокси, изогексилоксикарбонилокси и 3-метилпентилоксикарбонилокси.
Примеры циклоалкилоксикарбонилокси-групп включают циклоалкилоксикарбонилокси-группы, в которых циклоалкильная группа является C3-8 циклоалкильной группой, такие как циклопропилоксикарбонилокси, циклобутилоксикарбонилокси, циклопентилоксикарбонилокси, циклогексилоксикарбонилокси, циклогептилоксикарбонилокси, и циклооктилоксикарбонилокси.
Примеры циклоалкилкарбонильных групп включают циклоалкилкарбонильные группы, в которых циклоалкильная группа является C3-8 циклоалкильной группой, такие как циклопропилкарбонил, циклобутилкарбонил, циклопентилкарбонил, циклогексилкарбонил, циклогептилкарбонил и циклооктилкарбонил.
Примеры низшей алкокси-группы включают прямые или разветвленные C1-6 алкокси-группы, такие как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси, втор-бутокси, н-пентилокси, изопентилокси, неопентилокси, н-гексилокси, изогексилокси и 3-метилпентилокси.
Примеры групп гидрокси-низший алкил включают прямые или разветвленные C1-6 алкильные группы, имеющие от одной до трех гидроксильных групп, такие как гидроксиметил, 2-гидроксиэтил, 1-гидроксиэтил, 3-гидроксипропил, 2,3-дигидроксипропил, 4-гидроксибутил, 3,4-дигидроксибутил, 1,1-диметил-2-гидроксиэтил, 5-гидроксипентил, 6-гидроксигексил, 3,3-диметил-3-гидроксипропил, 2-метил-3-гидроксипропил и 2,3,4-тригидроксибутил.
Примеры низшей алкильной группы включают прямые или разветвленные C1-6 алкильные группы, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втор-бутил, н-пентил, изопентил, неопентил, н-гексил, изогексил и 3-метилпентил.
Примеры атомов галогена включают фтор, хлор, бром и йод.
Примеры низшей алкиламиногруппы включают аминогруппы, замещенные одной-двумя прямыми или разветвленными C1-6 алкильными группами, такими как метиламино, этиламино, н-пропиламино, изопропиламино, н-бутиламино, трет-бутиламино, н-пентиламино, н-гексиламино, диметиламино, диэтиламино, ди-н-пропиламино, ди-н-бутиламино, ди-н-пентиламино, ди-н-гексиламино, N-метил-N-этиламино, N-этил-N-н-пропиламино, N-метил-N-н-бутиламино и N-метил-N-н-гексиламино.
Примеры низшей алкоксикарбонильной группы включают алкоксикарбонильные группы, в которых алкокси-группа является прямой или разветвленной C1-6 алкокси-группой, такой как метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, трет-бутоксикарбонил, втор-бутоксикарбонил, н-пентилоксикарбонил, неопентилоксикарбонил, н-гексилоксикарбонил, изогексилоксикарбонил и 3-метилпентилоксикарбонил.
Примеры 6-членных насыщенных гетероциклических колец, образованных соединением R3 и R4 друг с другом вместе с атомом азота, с которым R3 и R4 связаны непосредственно или через атом азота или атом кислорода, включают пиперазин, пиперидин, морфолин и т.п.
Примеры групп гидрокси-низший алкокси включают гидроксиалкокси-группы, которые имеют одну или две гидроксильных группы, причем алкокси-группа является прямой или разветвленной C1-6 алкокси-группой, такой как гидроксиметокси, 2-гидроксиэтокси, 1-гидроксиэтокси, 3-гидроксипропокси, 4-гидроксибутокси, 5-гидроксипентилокси, 6-гидроксигексилокси, 1,1-диметил-2-гидроксиэтокси и 2-метил-3-гидроксипропокси.
Примеры алкилкарбонильных групп включают алкилкарбонильные группы, в которых алкильная группа является прямой или разветвленной C1-20 алкильной группой, такой как метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, н-бутилкарбонил, изобутилкарбонил, трет-бутилкарбонил, втор-бутилкарбонил, н-пентилкарбонил, изопентилкарбонил, неопентилкарбонил, н-гексилкарбонил, изогексилкарбонил, 3-метилпентилкарбонил, н-гептилкарбонил, н-октилкарбонил, н-нонилкарбонил, н-децилкарбонил, н-ундецилкарбонил, н-додецилкарбонил, н-тридецилкарбонил, н-тетрадецилкарбонил, н-пентадецилкарбонил, н-гексадецилкарбонил, н-гептадецилкарбонил, н-октадецилкарбонил, н-нонадецилкарбонил и н-икозилкарбонил.
Примеры арилкарбонильных групп включают фенилкарбонил,
(1- или 2-)нафтилкарбонил и т.п.
Примеры фурилкарбонильных групп включают (2- или 3-)фурилкарбонил.
Примеры групп низший алкоксикарбонил-низший алкил включают алкоксикарбонилалкильные группы, в которых алкокси-группа является прямой или разветвленной C1-6 алкокси-группой, и алкильная группа является прямой или разветвленной C1-6 алкильной группой, такие как метоксикарбонилметил, этоксикарбонилметил, 2-метоксикарбонилэтил, 2-этоксикарбонилэтил, 1-этоксикарбонилэтил, 3-метоксикарбонилпропил, 3-этоксикарбонилпропил, 4-этоксикарбонилбутил, 5-изопропоксикарбонилпентил, 6-н-пропоксикарбонилгексил, 1,1-диметил-2-н-бутоксикарбонилэтил, 2-метил-3-трет-бутоксикарбонилпропил, 2-н-пентилоксикарбонилэтил и н-гексилоксикарбонилметил.
Примеры групп карбокси-низший алкил включают карбоксиалкильные группы, в которых алкильная группа является прямой или разветвленной C1-6 алкильной группой, такой как карбоксиметил, 2-карбоксиэтил, 1-карбоксиэтил, 3-карбоксипропил, 4-карбоксибутил, 5-карбоксипентил, 6-карбоксигексил, 1,1-диметил-2-карбоксиэтил и 2-метил-3-карбоксипропил.
Примеры низших алкокси-фенильных групп включают алкоксифенильные группы, в которых алкокси-группа является прямой или разветвленной C1-6 алкокси-группой, такие как метоксифенил, этоксифенил, н-пропоксифенил, изопропоксифенил, н-бутоксифенил, изобутоксифенил, трет-бутоксифенил, втор-бутоксифенил, н-пентилоксифенил, изопентилоксифенил, неопентилоксифенил, н-гексилоксифенил, изогексилоксифенил и 3-метилпентилоксифенил.
Примеры низшей алкилтио-группы включают прямые или разветвленные C1-6 алкилтио группы, такие как метилтио, этилтио, н-пропилтио, изопропилтио, н-бутилтио, трет-бутилтио, н-пентилтио и н-гексилтио.
Примеры аминокислотных или пептидных остатков включают аминокислотные остатки, такие как аланил, фенилаланил, саркозил, валил, лейцил, изолейцил, пролил, N-этилглицил, N-пропилглицил, N-изопропилглицил, N-бутилглицил, N-трет-бутилглицил, N-пентилглицил, N-гексилглицил, N,N-диэтилглицил, N,N-дипропилглицил, N,N-дибутилглицил, N,N-дипентилглицил, N,N-дигексилглицил, N-метил-N-этилглицил, N-метил-N-пропилглицил, N-метил-N-бутилглицил, N-метил-N-пентилглицил и N-метил-N-гексилглицил; и пептидные остатки, такие как саркозил-глицил, глицил-глицил, глицил-саркозил, саркозил-саркозил, аланил-глицил, фенилаланил-глицил, фенилаланил-фенилаланил, глицил-глицил-глицил, N-этилглицил-глицил, N-пропилглицил-глицил, N,N-диметилглицил-глицил, N,N-диэтилглицил-глицил, N-метил-N-этилглицил-глицил, саркозил-глицил-глицил, N-этилглицил-глицил-глицил и N,N-диметилглицил-глицил-глицил.
Примеры защитных групп для аминокислот и пептидов включают обычно используемые для защиты аминогрупп аминокислот или пептидов, такие как трет-бутоксикарбонил, бензилоксикарбонил, флуоренилметоксикарбонил и ацетил.
Соединения бензазепина, представленные общей формулой (1), могут быть получены различными способами; например, способами согласно следующим реакционным схемам.
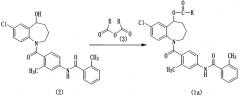
Среди соединений бензазепина, представленных общей формулой (1), или их солей, соединение (1a), в котором R1 обозначает группу с (1-1) по (1-5) или (1-7), как определено выше, может быть получено из толваптана формулы (2) согласно реакционной схеме 1, 2 или 3.
Реакционная схема 1
где R обозначает -(CH2)n-COR2 (в которой n и R2 имеют значения, определенные выше), -(CH2)m-NR3R4 (в которой m, R3 и R4 имеют значения, определенные выше), -(CH2)p-O-CO-NR5R6 (в которой p, R5 и R6 имеют значения, определенные выше), -(CH2)q-X-R7 (в которой q, X и R7 имеют значения, определенные выше), -R8 (в которой R8 имеет значения, определенные выше), или группу, образованную удалением карбонильной группы (группы СО) от аминокислотного или пептидного остатка, в случае необходимости защищенного одной или более защитными группами (например, аминометилом для глицила, (R)-1-аминоэтилом для аланила, (R)-1-амино-2-фенилпропилом для фенилаланила, (метиламино)метилом для саркозила, (R)-1-амино-3-метилбутилом для лейцила, трет-бутоксикарбонил(этил)аминометилом для N-трет-бутоксикарбонил-N-этилглицила, (S)-2-амино-пропанамидометилом для аланил-глицила, 2-(метиламино)ацетамидометилом для саркозил-глицила, (S)-2-амино-3-фенилпропанамидометилом для фенилаланил-глицила, (2-аминоацетамидо)ацетамидометилом для глицил-глицил-глицила, [2-(метиламино)ацетамидо]ацетамидометилом для саркозил-глицил-глицила и т.п.).
Согласно способу, показанному на реакционной схеме 1, соединение (1a) получают, вводя соединение (2) в реакцию с ангидридом кислоты (3) в присутствии или в отсутствие основного соединения в подходящем растворителе.
Количество ангидрида кислоты (3) обычно составляет от приблизительно 1 моль до большого избытка, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (2).
Растворитель может быть любым известным растворителем, который не воздействует неблагоприятным образом на реакцию. Примеры таких растворителей включают простые эфиры, такие как простой диэтиловый эфир, диоксан, тетрагидрофуран, моноглим и диглим; галогенированные углеводороды, такие как метиленхлорид, хлороформ, 1,2-дихлорэтан и тетрахлорметан; сложные эфиры, такие как этилацетат; ароматические углеводороды, такие как бензол, толуол и ксилол; апротонные полярные растворители, такие как ацетонитрил, диметилформамид (DMF),
диметилсульфоксид (ДМСО) и N-метилпирролидон (NMP); и смеси этих растворителей.
Примеры основных соединений включают триэтиламин, пиридин и т.п. Количество основного соединения обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (2). Такое основное соединение может также использоваться в качестве растворителя.
Когда катализатор, такой как 4-диметиламинопиридин, присутствует в реакционной системе в вышеуказанной реакции, реакция может быть промотирована.
Температура реакции вышеуказанной реакции обычно представляет собой температуру от температуры окружающей среды до 150°C, и предпочтительно от температуры окружающей среды до 100°C. Время реакции обычно составляет от 15 минут до 24 часов, предпочтительно от 30 минут до 6 часов, и более предпочтительно от 1 до 3 часов.
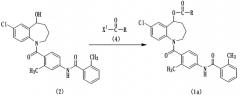
Реакционная схема 2
где R имеет значения, определенные выше, и X1 обозначает атом галогена.
Согласно способу, показанному на реакционной схеме 2, соединение (2) вводят в реакцию с галогенангидридом кислоты (4) в присутствии основного соединения в подходящем растворителе, получая соединение (1a).
Количество галогенангидрида кислоты (4) обычно составляет от приблизительно 1 моль до большого избытка, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (2).
Растворитель может быть любым известным растворителем, который не воздействует неблагоприятным образом на реакцию. Примеры таких растворителей включают простые эфиры, такие как простой диэтиловый эфир, диоксан, тетрагидрофуран, моноглим и диглим; галогенированные углеводороды, такие как метиленхлорид, хлороформ, 1,2-дихлорэтан и тетрахлорметан; сложные эфиры, такие как этилацетат; ароматические углеводороды, такие как бензол, толуол и ксилол; апротонные полярные растворители, такие как ацетонитрил, DMF, ДМСО и NMP; и смеси этих растворителей.
Примеры основных соединений включают карбонаты, такие как карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия и карбонат цезия; фосфаты, такие как фосфат калия и фосфат натрия; органические основания, такие как пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нонен-5 (DBN), 1,8-диазабицикло[5.4.0]ундецен-7 (DBU) и 1,4-диазабицикло[2.2.2]октан (DABCO); и их смеси.
Количество основного соединения обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (2). Такое органическое основание может также использоваться в качестве растворителя.
Когда катализатор, такой как 4-диметиламинопиридин, присутствует в реакционной системе в вышеуказанной реакции, реакция может быть промотирована.
Температура реакции вышеуказанной реакции обычно составляет от -10°C до 100°C, и предпочтительно от 0°C до 50°C, и более предпочтительно от 0°C до температуры окружающей среды. Время реакции обычно составляет от 15 минут до 24 часов, предпочтительно от 30 минут до 6 часов, и более предпочтительно от 1 до 3 часов.
Реакционная схема 3
где R имеет значения, определенные выше.
Согласно способу, показанному в реакционной схеме 3, соединение (2) конденсируют с карбоновой кислотой (5) в присутствии активатора, получая соединение (1a).
Количество карбоновой кислоты (5) обычно составляет от приблизительно 1 до приблизительно 10 моль, и предпочтительно от приблизительно 1 до приблизительно 5 моль на моль соединения (2).
Примеры активаторов включают дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид (WSC), карбонилдиимидазол и т.п. Такие активаторы могут использоваться отдельно или в комбинации двух или более.
Количество активатора обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 моль до приблизительно 5 моль на моль соединения (2).
Реакцию конденсации обычно осуществляют в подходящем растворителе в присутствии или в отсутствие основного соединения. Примеры растворителей, которые могут использоваться, включают простые эфиры, такие как простой диэтиловый эфир, диоксан, тетрагидрофуран, моноглим и диглим; галогенированные углеводороды, такие как метиленхлорид, хлороформ, 1,2-дихлорэтан и тетрахлорметан; сложные эфиры, такие как этилацетат; ароматические углеводороды, такие как бензол, толуол и ксилол; апротонные полярные растворители, такие как ацетонитрил, DMF, ДМСО и NMP; и смеси этих растворителей.
Примеры основных соединений включают триэтиламин, пиридин и т.п. Количество основного соединения обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (2). Такое основное соединение может также использоваться в качестве растворителя.
Когда катализатор, такой как 4-диметиламинопиридин, присутствует в реакционной системе, реакция может быть промотирована.
Реакцию обычно осуществляют при температуре от приблизительно -20°C до приблизительно 100°C, и предпочтительно от 0°C до температуры окружающей среды. Реакция обычно протекает от приблизительно 5 минут до приблизительно 90 часов.
Среди соединений бензазепина, представленных общей формулой (1), или их солей соединение (1b), в котором R1 обозначает группу (1-6), определенную выше (низшая алкильная группа, замещенная низшей алкилтио-группой), может быть получено из толваптана формулы (2) способом согласно следующей реакционной схеме 4:
Реакционная схема 4
где R1a обозначает низшую алкильную группу, замещенную низшей алкилтио-группой.
Способ, показанный на реакционной схеме 4, представляет собой реакцию превращения атома водорода гидроксильной группы соединения (2) в низшую алкильную группу, замещенную низшей алкилтио-группой. Например, для превращения атома водорода гидроксильной группы соединения (2) в метилтиометильную группу соединение (2) подвергают обычной реакции образования эфирной связи, так называемой реакции Pummerer, или подобной. Обычную реакцию образования эфирной связи обычно проводят в обычном растворителе, который не воздействует на реакцию, и температура реакции не является критической. Реакция Pummerer является такой, как показано ниже на реакционной схеме 4-1; соединение (2) вводят в реакцию с сульфоксидом (6), таким как диметилсульфоксид, в присутствии уксусного ангидрида и уксусной кислоты при температуре от температуры окружающей среды до приблизительно 70°C в течение времени от приблизительно 4 до приблизительно 72 часов.
Реакционная схема 4-1
где R1b и R1c независимо обозначают низшую алкильную группу.
Среди соединений бензазепина, представленных общей формулой (1), или их солей соединение (1c), в котором R1 обозначает группу (1-6), определенную выше (низшую алкильную группу, замещенную дигидроксифосфорилокси-группой), может быть получено, например, из соединения (1b) способом согласно следующей реакционной схеме 5:
Реакционная схема 5
где R1b обозначает низшую алкильную группу, замещенную дигидроксифосфорилокси-группой, и R1a имеет значения, определенные выше.
Способ, показанный на реакционной схеме 5, представляет собой реакцию превращения низшей алкильной группы, замещенной низшей алкилтио-группой R1, в низшую алкильную группу, замещенную дигидроксифосфорилокси-группой. Например, для превращения метилтиометильной группы R1 в дигидроксифосфорилоксиметильную группу, как показано ниже на реакционной схеме 5-1, соединение (1b") вводят в реакцию с галогенирующим реагентом (например, сульфурилхлоридом, N-йодсукцинимидом и т.д.), и полученное соединение затем вводят в реакцию с фосфорной кислотой в присутствии основного соединения.
Реакционная схема 5-1
где r обозначает целое число, которое может составлять от 1 до 4, и R1e обозначает низшую алкильную группу.
Реакцию соединения (1b") с галогенирующим реагентом предпочтительно осуществляют в галогенированном углеводороде (например, метиленхлориде, 1,2-дихлорэтане и т.д.) приблизительно при температуре окружающей среды. Количество галогенирующего реагента обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1b"). Эта реакция занимает от приблизительно 5 минут до приблизительно 1 часа.
Затем реакцию полученного соединения с фосфорной кислотой предпочтительно проводят в присутствии инертного органического растворителя (например, тетрагидрофурана, ацетонитрила и т.д.). Количество фосфорной кислоты обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1b"). Примеры основных соединений включают карбонаты, такие как карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия и карбонат цезия; фосфаты, такие как фосфат калия и фосфат натрия; органические основания, такие как пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, DBN, DBU и DABCO; и их смеси. Количество основного соединения обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1b"). Температура реакции вышеуказанной реакции обычно представляет собой температуру от температуры окружающей среды до приблизительно 200°C, и предпочтительно от 50°C до приблизительно 150°C. Реакция обычно занимает от приблизительно 10 минут до приблизительно 10 часов.
Среди соединений бензазепина, представленных общей формулой (1), или их солей соединение (1d), в котором R1 обозначает группу (1-6), определенную выше (низшую алкильную группу, замещенную низшей алканоилокси-группой), может быть получено, например, из соединения (1b) способом согласно следующей реакционной схеме 6:
Реакционная схема 6
где R1f обозначает низшую алкильную группу, замещенную низшей алканоилокси-группой, и R1a имеет значения, определенные выше.
Способ, показанный на реакционной схеме 6, представляет собой реакцию превращения низшей алкильной группы, замещенной низшей алкилтио-группой R1, в низшую алкильную группу, замещенную низшей алканоилокси-группой. Например, как показано ниже на реакционной схеме 6-1, соединение (1b") вводят в реакцию с галогенирующим реагентом (например, сульфурилхлоридом, N-йодсукцинимидом и т.д.), и полученное соединение затем вводят в реакцию с карбоновой кислотой или ее солью.
Реакционная схема 6-1
где R1g обозначает низшую алкильную группу и R1e имеет значения, определенные выше.
Реакцию соединения (1b") с галогенирующим реагентом предпочтительно проводят в галогенированном углеводороде (например, метиленхлориде, 1,2-дихлорэтане и т.д.) приблизительно при температуре окружающей среды. Количество галогенирующего реагента обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1b"). Эта реакция занимает от приблизительно 5 минут до приблизительно 1 часа.
Затем реакцию полученного соединения с карбоновой кислотой или ее солью предпочтительно проводят в присутствии инертного органического растворителя (например, тетрагидрофурана, ацетонитрила и т.д.). Количество карбоновой кислоты обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1b). Температура реакции обычно представляет собой температуру от температуры окружающей среды до приблизительно 200°C, и предпочтительно от 50°C до приблизительно 150°C. Время реакции обычно составляет от приблизительно 10 минут до приблизительно 10 часов.
Среди соединений бензазепина, представленных общей формулой (1), или их солей соединение (1f), в котором R1 обозначает группу (1-1), определенную выше, и R2 обозначает группу (2-2), определенную выше, может быть получено из соединения (1e), в котором R1 обозначает группу (1-1), определенную выше, и R2 обозначает группу (2-1), определенную выше, способом согласно следующей реакционной схеме 7:
Реакционная схема 7
где R2a обозначает низшую алкокси-группу, в случае необходимости замещенную гидрокси, низшим алканоилом, низшим алканоилокси, низшим алкоксикарбонилокси, циклоалкилоксикарбонилокси или 5-метил-2-оксо-1,3-диоксол-4-илом, R2a' обозначает низшую алкокси-группу, в случае необходимости замещенную гидрокси, низшим алканоилом, низшим алканоилокси, низшим алкоксикарбонилокси, циклоалкилоксикарбонилокси или 5-метил-2-оксо-1,3-диоксол-4-илом, и n и X1 имеют значения, определенные выше.
Реакцию соединения (1e) с соединением (8) проводят в присутствии основного соединения в подходящем растворителе.
Количество соединения (8) обычно составляет от приблизительно 1 моль до большого избытка, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1e).
Примеры растворителей реакции включают простые эфиры, такие как простой диэтиловый эфир, диоксан, тетрагидрофуран, моноглим и диглим; галогенированные углеводороды, такие как метиленхлорид, хлороформ, 1,2-дихлорэтан и тетрахлорметан; сложные эфиры, такие как этилацетат; ароматические углеводороды, такие как бензол, толуол и ксилол; апротонные полярные растворители, такие как ацетонитрил, DMF, ДМСО и NMP; и смеси этих растворителей.
Примеры основных соединений включают карбонаты, такие как карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия и карбонат цезия; фосфаты, такие как фосфат калия и фосфат натрия; органические основания, такие как пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, DBN, DBU и DABCO; и т.п. Такие соединения могут использоваться отдельно или в комбинации двух или более. Количество основного соединения обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1e). Такое основное соединение может также использоваться в качестве растворителя.
Температура реакции обычно представляет собой температуру от температуры окружающей среды до 150°C, и предпочтительно от температуры окружающей среды до 100°C. Время реакции обычно составляет от 15 минут до 24 часов, предпочтительно от 30 минут до 6 часов, и более предпочтительно от 1 до 3 часов.
Среди соединений бензазепина, представленных общей формулой (1), или их солей соединение (1g), в котором R1 обозначает группу (1-1), определенную выше, и R2 обозначает аминогруппу, замещенную одной или более группой гидрокси-низший алкил, может быть получено, например, из соединения (1e), в котором R1 обозначает группу (1-1), определенную выше, и R2 обозначает группу (2-1), определенную выше, способом согласно следующей реакционной схеме 8:
Реакционная схема 8
где R2b обозначает аминогруппу, замещенную одной или более группами гидрокси-низший алкил, и n имеет значения, определенные выше.
Реакцию соединения (1e) с соединением (9) проводят в условиях реакции, обычно используемых для карбодиимидного способа. Более конкретно, соединение (1e) конденсируют с соединением (9) в присутствии активатора, такого как дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид (WSC) или карбонилдиимидазол.
Количество активатора обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 5 моль на моль соединения (1e).
Реакцию конденсации проводят в подходящем растворителе в присутствии или в отсутствие основного соединения. Примеры растворителей, которые могут использоваться, включают простые эфиры, такие как простой диэтиловый эфир, диоксан, тетрагидрофуран, моноглим и диглим; галогенированные углеводороды, такие как метиленхлорид, хлороформ, 1,2-дихлорэтан и тетрахлорметан; сложные эфиры, такие как этилацетат; ароматические углеводороды, такие как бензол, толуол и ксилол; апротонные полярные растворители, такие как ацетонитрил, DMF, ДМСО и NMP; и смеси этих растворителей.
Примеры основных соединений включают триэтиламин, пиридин и т.п. Количество основного соединения обычно составляет по меньшей мере приблизительно 1 моль, и предпочтительно от приблизительно 1 до приблизительно 10 моль на моль соединения (1e). Такое основное соединение может также использоваться в качестве растворителя.
Когда WSC используется в качестве активатора в вышеуказанной реакции, присутствие катализатора, такого как 1-гидроксибензотриазол (HOBt), в реакционной системе может промотировать реакцию.
Реакцию обычно проводят при температуре от приблизительно -20°C до приблизительно 180°C, и предпочтительно от 0°C до приблизительно 150°C. Реакция обычно занимает от приблизительно 5 минут до приблизительно 90 часов.
Среди соединений бензазепина, представленных общей формулой (1), или их солей соединения, в которых аминогруппа защищена защитной группой, могут быть преобразованы путем удаления защитной группы в соответствующие соединения, в которых аминогруппа не защищена защитной группой, например, способом, показанным на следующей реакционной схеме 9:
Реакционная схема 9
где R1h является тем же самым, как R1, определенный выше, имеющий аминогруппу, из которой указанная аминогруппа защищена защитной группой для аминогруппы; R1i является тем же самым, как R1, определенный выше, имеющий аминогруппу, соответствующую R1h, у которой защитная группа для аминогруппы удалена.
Реакцию превращения соединения (1h) в соединение (1i) проводят в присутствии кислоты в подходящем растворителе или не используя никакого растворителя.
Примеры растворителей, которые могут использоват