1-(1-адамантил)-4-нитрозопиразолы
Иллюстрации
Показать всеИзобретение относится к области органической химии, в частности к 1-(1-адамантил)-4-нитрозопиразолам. Технический результат заключается в получении ранее не известных 1-(1-адамантил)-4-нитрозопиразолов. Описывается получение 1-(1-адамантил)-4-нитрозопиразолов общей формулы
где R=H, Me, которые могут найти применение как модификаторы резиновых смесей. 2 пр.
Реферат
Изобретение относится к области органической химии, в частности к 1-(1-адамантил)-4-нитрозопиразолам, которые могут найти применение как модификаторы резиновых смесей.
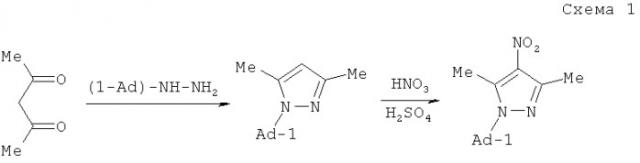
Аналогов веществ нет. До настоящего времени такие вещества не известны. Наиболее близким по строению к предлагаемым соединениям является 1-(1-адамантил)-3,5-диметил-4-нитро-1Н-пиразол [Cabildo P., Claramunt R.M. Synthesis and Reactivity of New 1-(1-Adamantyl)pyrazoles // Heterocyclic Chem. 1984. V.21. P.249-251] и 1-(1-адамантил)-3-метил-4-нитро-1Н-пиразол [Гаврилов А.С., Голод Е.Л., Качала В.В., Уграк Б.И. Адамантилазолы. VI. Кислотно-катализируемое адамантилирование пиразолов. // ЖОрХ. 2001. Т.37. Вып.12. С.1822-1827], полученные по схемам (1) и (2), соответственно:
Настоящее изобретение решает задачу синтеза новых адамантилированных пиразолов, в частности 1-(1-адамантил)-4-нитрозопиразолов.
Технический результат заключается в синтезе новых 1-(1-адамантил)-4-нитрозопиразолов.
Указанный технический результат достигается тем, что получены
1. 1-(1-Адамантил)-4-нитрозопиразолы общей формулы
где R=H, Me.
Неизвестные ранее 1-(1-адамантил)-4-нитрозопиразолы получают циклоконденсацией адамантилгидразина с 2-гидроксимино-1,3-дикарбонильными соединениями.
Этим способом впервые синтезированы следующие 1-(1-адамантил)-4-нитрозопиразолы.
1-(1-адамантил)-3,5-диметил-4-нитрозо-1Н-пиразол
Сине-зеленые кристаллы, растворимы в этаноле, хлороформе. Т.пл. 127°C. Электронный спектр, λмакс., нм (ε): 308 (16620), 661 (60). Спектр ЯМР 1H, δ, м.д.: 1.82-1.83 м (6Н, СН2), 2.22 м (3Н, СН), 2.30 уш. с (3Н, СН3), 2.40-2.41 д (6Н, СН2), 3.24 уш. с (3Н, СН3). Масс-спектр, m/z (1отн., %): 259 (68) [М]+, 135 (100), 125 (14), 107 (14), 93 (23), 79 (24), 67 (11), 55 (14).
1-(1-адамантил)-3-метил-4-нитрозо-1Н-пиразол
Сине-зеленые кристаллы, растворимы в этаноле, хлороформе. Т.пл. 142°C (этанол). Электронный спектр, εмакс., нм. (ε): 309 (16500), 680 (56) Спектр ЯМР 1Н, δ, м.д.: 1.82-1.83 м (6Н, СН2), 2.31 м (3Н, СН), 2.40-2.41 д (6Н, СН2), 3.35 уш. с (3Н, СН3), 7.16 уш.с. (1Н, Наром). Найдено, %: С 69.11, Н 8.01, N 17.83. C14H19N3O. Вычислено, %: С 68.54, Н 7.81, N 17.13. М 245.32.
1-(1-Адамантил)-4-нитрозопиразолы получены следующим способом.
Пример 1. 1-(1-Адамантил)-3,5-диметил-4-нитрозо-1Н-пиразол. К раствору 0.61 г (2.56 моль) дигидрохлорида адамантилгидразина в 14 мл спирта добавяют раствор 0.145 г (2.55 моль) едкого кали в 3 мл спирта, затем 0.34 г (2.6 моль) 3-гидроксиминопентан-2,4-диона и выдерживают 12 ч при 24°C. Отфильтровывают белый осадок хлористого калия, фильтрат упаривают до 5 мл объема, охлаждают до 0°C, выпавший осадок отфильтровывают, перекристаллизовывают из спирта. Выход 0.26 г (40%).
Пример 2. 1-(1-Адамантил)-3-метил-4-нитрозо-1Н-пиразол. Смесь 0.66 г 4,4-диметоксибутан-2-она (5 ммоль) в 5 мл 1 н. соляной кислоты (5 ммоль) перемешивают при 20°C 0.5 ч, охлаждают до 0°C и в течение 0.5 ч добавляют по каплям раствор 0.38 г (5.5 ммоль) нитрита натрия в 3 мл воды. Затем из реакционной смеси отдувают окислы азота в вакууме водоструйного насоса и добавляют раствор 0.89 г (3.75 ммоль) дигидрохлорида адамантилгидразина в 20 мл воды. Реакционную смесь перемешивают 10 мин при 20°C.
Выпавший осадок, светло-зеленого цвета, отфильтровывают, растворяют в 20 мл спирта и нагревают на водяной бане 3 ч. Спирт упаривают в вакууме до объема раствора 5 мл, выпавший осадок отфильтровывают, перекристаллизовывают из спирта. Выход 0.63 г (69%).
Авторами синтезированы не описанные ранее вещества, которые могут найти применение как модификаторы резиновых смесей.
1-(1-Адамантил)-4-нитрозопиразолы общей формулы: где R - H, Me.