Новая стандартизованная композиция, способ ее получения и применение в регрессии рнк-вирусной инфекции
Иллюстрации
Показать всеНастоящее изобретение относится к противовирусным препаратам, полученным из источников растительного происхождения, т.е. коричного дерева, литчи и арахиса. Согласно настоящему изобретению предложена композиция и способ получения указанной композиции, содержащей пентамерный, тримерный и тетрамерный флавоноид процианидин. Данная композиция улучшает иммунный ответ и, как обнаружено, подходит для лечения и контроля ВИЧ-инфекции и СПИДа, а также для предупреждения, лечения и контроля вируса и инфекции гриппа. 5 н. и 20 з.п. ф-лы, 5 табл., 14 пр., 5 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к противовирусным препаратам. Согласно настоящему изобретению предложены противовирусные препараты, полученные из растений и улучшающие иммунный ответ, а также эффективные в отношении ВИЧ-инфекции, СПИДа, вируса и инфекции гриппа.
УРОВЕНЬ ТЕХНИКИ
Катехины представляют собой полифенольные метаболиты растений, относящиеся к классу флавоноидов. Молекулярная формула и масса катехинов представляют собой C15H14O6 и 290 г/моль. Катехин и эпикатехин являются эпимерами, при этом (-)-эпикатехин и (+)-катехин представляют собой самые распространенные оптические изомеры, встречающиеся в природе.
Процианидины или конденсированные таннины представляют собой олигомеры флавоноидов, структурными элементами которых являются (+)-катехин и (-)-эпикатехин. Они являются олигомерными конечными продуктами биосинтетического пути метаболизма флавоноидов и в настоящее время идентифицированы и признаны оказывающими благоприятное воздействие на людей. Они в большом количестве присутствуют в царстве растений во фруктах, коре, листьях и семенах, где обеспечивают защиту от света, окисления и хищников. Процианидины встречаются во многих растениях, главным образом в яблоках, коре сосны, коре коричного дерева, перикарпии литчи, арахисе, виноградных косточках, какао, кожуре винограда, чернике, клюкве, черной смородине, зеленом чае и черном чае.
По типу связи между последовательными мономерными звеньями, процианидины относят к полифенолам типа А, В или С.
В целом, связь между последовательными мономерными звеньями процианидинов находится между четвертым положением «верхнего» звена и восьмым положением «нижнего» звена, что приводит к процианидину типа В. В качестве альтернативы указанная связь может находиться между C4 «верхнего» звена и С6 «нижнего» звена, что приводит к процианидину типа С. Полифенолы типов В и С в большом количестве встречаются во многих источниках растительного происхождения. В случае, когда последовательные мономерные звенья соединены простой эфирной связью между С2 и С4 «верхнего» звена и кислородом в положении С7 и положениях С6/С8 (соответственно) «нижнего» звена, образуется процианидин типа А. Процианидины типа А встречаются редко по сравнению с полифенолами типов В и С.
Иммунный ответ на антиген
Иммунная система представляет собой набор механизмов в организме хозяина, защищающий его от заболеваний путем идентификации и удаления патогена. Реакция системы на патоген начинается с идентификации чужеродного белка и заканчивается разрушением источника указанного белка, тем самым обеспечивая защиту хозяина. Даже распознавание простого белка одноклеточного организма включает ряд сложных этапов, которые приводят к конечному удалению указанного организма из хозяина. Весь процесс представляет собой иммунный ответ на присутствие чужеродного белка или антигена.
Разрешение инфекции иммунной системой представляет собой иммунный ответ на антиген и может быть разделено на 3 этапа:
Активация и мобилизация: Белые кровяные клетки (WBC) активируются, когда они идентифицируют чужеродную молекулу или антиген. Иммуноциты, такие как макрофаги и Т-лимфоциты, выделяют вещества, которые привлекают другие иммуноциты к месту идентифицированной чужеродной молекулы, и тем самым мобилизуют бесчисленное количество иммуноцитов на уничтожение патогена.
Регуляция: Вызываемый иммунный ответ должен быть под контролем для предупреждения чрезмерного повреждения хозяина. Регуляторные Т-лимфоциты облегчают контроль иммунных ответов путем выделения цитокинов, выполняющих функцию мессенджеров иммунной системы, и таким образом регулируют усиленный иммунный ответ.
Разрешение: Разрешение инфекции включает изоляцию патогена и его удаление из организма. После удаления патогена большинство белых кровяных клеток разрушается, а те, которые остаются, называются «клетками памяти» и защищают хозяина от будущего инфицирования тем же патогеном, вызывая своевременный иммунный ответ на указанный патоген.
Патогену удается вызвать инфекцию, когда хозяин неспособен усилить защиту, достаточную для удаления указанного патогена. В таких случаях количество антител, вырабатываемых хозяином, недостаточно для нейтрализации имеющегося количества антигена. Следовательно, свободным антигенам удается инфицировать хозяина. В таких случаях для снижения количества антигена используют внешние вспомогательные средства, такие как антибиотики и противовирусные средства. После уменьшения количества антигена иммунного ответа достаточно для удаления патогена.
ВИЧ-инфекция и СПИД:
Вирус иммунодефицита человека (ВИЧ) представляет собой ретровирус, разрушающий иммунную систему. Данная инфекция может в конечном счете приводить к синдрому приобретенного иммунодефицита (СПИД), серьезному и обладающему повышенным риском для жизни состоянию, при котором иммунная система не в состоянии правильно функционировать. ВИЧ в первую очередь инфицирует определенные клетки иммунной системы человека: «хелперные» Т-лимфоциты (в частности, CD4+ Т-клетки), макрофаги и дендритные клетки. Когда количество CD4+ Т-клеток снижается ниже критического уровня, утрачивается опосредуемый клетками иммунитет и организм становится все более восприимчивым к оппортунистическим инфекциям.
Цикл жизни ВИЧ: После проникновения ВИЧ в организм хозяина ВИЧ необходимы конкретные клетки-хозяева для облегчения репликации и распространения. В случае ВИЧ такая клетка-хозяин представляет собой Т-клетку или клетку CD4.
1. Распознавание хозяина и связывание: ВИЧ «ищет» клетки CD4 и присоединяется к ним посредством системы «замок-ключ» через корецепторы на поверхности клеток. Белки на поверхности ВИЧ присоединяются к комплементарным белкам клетки CD4.
2. Присоединение и проникновение в организм хозяина: После присоединения ВИЧ вводит вирусные белки в клеточные жидкости (цитоплазму) Т-клетки. Это вызывает слияние мембраны клетки с внешней оболочкой ВИЧ.
3. Разборка вирусных белков: Для использования генетического материала (РНК) для воспроизводства защитная оболочка вокруг РНК должна быть растворена. Без указанного этапа превращение РНК в ДНК (структурные элементы новых копий ВИЧ) не может происходить и репликация прекращается.
4. Обратная транскрипция: После проникновения в клетку, одноцепочечная РНК ВИЧ должна быть превращена в двухцепочечную ДНК. Данный этап осуществляется под действием фермента, обратной транскриптазы. Обратная транскриптаза использует структурные элементы Т-клетки, чтобы способствовать превращению вирусной РНК в ДНК. ДНК содержит генетическую информацию, необходимую для репликации ВИЧ.
5. Репликация и сборка с образованием нового вириона: Для репликации вновь образованная вирусная ДНК должна интегрироваться в ядро хозяина. Данный процесс еще не полностью изучен, но считают, что ему способствуют вирусные транспортные белки. После интеграции вирус вынашивается, в то время как клетка-хозяин «подготавливает» белки, которые ему необходимы для завершения репликации. Как только материалы становятся доступны, вирус их расщепляет исходя из необходимости и структуры, а затем они собираются в новый ВИЧ. Данному процессу способствует фермент протеаза.
6. Отпочковывание от клетки-хозяина: Заключительный этап цикла репликации вируса называется отпочковыванием. Со «спрятанным» генетическим материалом и новой внешней оболочкой, образованной из мембраны клетки-хозяина CD4, вновь образованный ВИЧ отсоединяется и поступает в кровоток, готовый начать весь процесс сначала.
Существующие на настоящий момент воздействия:
Существующие на настоящий момент способы прерывания репликации и распространения ВИЧ включают ингибиторы входа вируса; ингибиторы слияния мембран; ингибиторы обратной транскриптазы; ингибиторы интегразы; ингибиторы протеазы; ингибиторы созревания и т.д. FDA (Управление по контролю за качеством пищевых продуктов и лекарственных средств США) одобрило ряд лекарственных средств для лечения ВИЧ-инфекции. Большинство данных лекарственных средств работает за счет антиретровирусного (ARV) механизма действия.
Инфицирование вирусом иммунодефицита человека (ВИЧ) бросает вызов политике, экономике, здравоохранению, обществу и науке в странах всего мира. К концу 2007 г. насчитывалось приблизительно 33,2 миллиона человек с ВИЧ/СПИДом по всему миру. Соответственно, существует острая необходимость в контроле и/или лечении данного заболевания более безопасными и более эффективными лекарственными средствами. Дополнительная опасность, которую несет данный вирус, представляет собой его подверженность мутации. Вирусные белки ВИЧ склонны к мутации и, следовательно, резистентные к лекарственным средствам штаммы представляют собой дополнительную угрозу, которая создает необходимость в разработке более современных классов лекарственных средств.
Вирус гриппа:
Грипп представляет собой инфекционное заболевание, вызываемое РНК-вирусами семейства Orthomyxoviridae (вирусы гриппа), и поражает птиц и млекопитающих. Инфекция, вызванная данным вирусом, поражает главным образом нос, горло, бронхи и иногда легкие.
Структура Вируса Гриппа: Вирус гриппа делят на 3 категории: вирус Гриппа А, В и С. Указанные 3 подтипа вирусов гриппа обладают очень схожей общей структурой. Данные вирусы состоят из оболочки вируса, содержащей два основных типа гликопротеинов, которые обернуты вокруг центрального ядра. Центральное ядро содержит РНК-геном вируса и другие вирусные белки, которые «упаковывают» и защищают данную РНК. Гемагглютинин НА и нейраминидаза (NA) представляют собой два крупных гликопротеина на внешней поверхности вирусных частиц.
Вирус гриппа А: Вирусы типа А являются самыми вирулентными патогенами человека среди трех типов гриппа и вызывают наиболее тяжелое заболевание. Вирус гриппа А может быть подразделен на различные серотипы на основании антителогенеза к данным вирусам. Серотипы, подтвержденные у людей и расположенные по числу известных смертельных случаев у людей в результате пандемии, представляют собой: H1N1, H2N2, H3N2, H5N1, H7N7, H1N2, H9N2, H7N2, H7N3, H10N7. Вирусы гриппа А вызвали несколько пандемий в течение прошлого столетия и продолжают вызывать ежегодные эпидемии. Появление новых штаммов гриппа продолжает бросать вызов здравоохранению и научным сообществам. Вирус H1N1 представляет собой серотип вируса гриппа А и является одним из самых вирулентных штаммов, которые поражают людей. Серотип H1N1 ответственен за миллионы смертельных случаев в 1918 г. (испанка) и в последнее время вызывает глобальную пандемию свиного гриппа.
Цикл жизни вируса гриппа: Процесс репликации и распространения вируса гриппа приведен ниже:
1. Распознавание хозяина и связывание: Связывание вируса с клеткой-хозяином происходит в результате связывания белка НА с сиаловой кислотой, связанной с сахарами, на поверхностях клеток эпителия. Клетки эпителия, как правило, присутствуют в носу, горле и легких млекопитающих и в кишечнике птиц.
2. Присоединение и проникновение в организм хозяина: После связывания белок НА отщепляется и вирус проникает в клетку путем эндоцитоза.
3. Разборка вирусных белков: Как только вирус проникает в клетку, pH и внешние условия эндосомы приводят к следующему:
а. Часть НА осуществляет слияние оболочки вируса с мембраной вакуоли.
b. Ионный канал М2 позволяет проникать в ядро вируса протонам, которые подкисляют данное ядро вируса, что приводит к его разборке и последующему высвобождению вирусной РНК и капсидных белков в цитоплазму клетки-хозяина.
4. Обратная транскрипция: Далее вирусная РНК и капсидные белки транспортируются в ядро клетки, где РНК транскрибируется, а затем транслируется в вирусные белки.
5. Отпочковывание от клетки-хозяина: Белки НА и NA образуют кластеры рядом с мембраной клетки, которые в дальнейшем также заключают вирусную РНК и капсидные белки, которые затем приводят к «отпочковыванию» вируса и распространению для последующего инфицирования.
Как следует из описания этапов инфицирования и распространения, подробно описанных выше, НА и NA играют важную роль в инфицировании. Перед высвобождением вириона NA также расщепляет сиаловую кислоту для того, чтобы предотвратить связывание НА с сиаловой кислотой.
Существующие на настоящий момент воздействия на вирус гриппа А: Существует два класса лекарственных средств, одобренных FDA США, против вируса гриппа А: ингибиторы ионных каналов, такие как Адамантаны (амантадина гидрохлорид и римантадин); и ингибиторы нейраминидазы, такие как Оселтамивир (ТАМИФЛЮ) (Oseltamivir, TAMIFLU) и Занамивир (РЕЛЕНЦА) (Zanamivir, RELENZA).
Вирус гриппа А склонен к мутациям. Данные мутации прежде всего представляют собой мутации вирусных белков, таких как NA, НА и белки ионных каналов М2, и, следовательно, ингибиторы данных белков будут неэффективны в отношении мутантных штаммов. Способность к мутации и глобальная пандемия гриппа А 2009 г. создают острую необходимость в разработке видов терапии, предлагающих варианты лечения и предупреждения данного вируса.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Richard Anderson et al, "Isolation and characterization of polyphenols Type A polymers from cinnamon with insulin-like biological activity" в Journal of Agricultural and Food Chemistry, 2004, стр.52, 65-70.
В указанной публикации описан водный экстракт коммерческого коричного дерева и представлены идентифицированные полифенольные полимеры, повышающие метаболизм глюкозы примерно в 20 раз в линиях клеток in vitro. Авторы использовали Корицу Китайскую (Korintji cassia) для получения данного экстракта. Данный сорт обладает высоким содержанием кумарина и коричного альдегида.
В указанной публикации также описан метод препаративной ВЭЖХ для получения и определения характеристик данного водного экстракта.
В указанной публикации описан соединенный двойной связью процианидин А-типа из катехинов. В данной публикации также определен тример (молекулярная масса 864), тетрамер (молекулярная масса 1152) и олигомер катехинов, выделенных из коричного дерева.
Kilkuskie et al, "HIV and reverse transcriptase inhibition by tannins" в Bioorganic and Medicinal Chemistry Letters. 1992, Vol.2, стр.1529-1534.
В данной публикации оценивают таннины и конденсированные таннины на предмет их активности в отношении ВИЧ и их действия в отношении ингибирования фермента, обратной транскриптазы. Несмотря на то, что в результате данного исследования были обнаружены некоторые таннины, обладающее активностью в отношении ВИЧ, они были отягощены сопутствующей токсичностью. Данная публикация сообщает о 3 соединениях, представляющих собой конденсированные формы катехинов. Молекулы 40, 44 и 45 являются димерами, тримерами и тетрамерами катехинов. В указанной публикации был сделан вывод об отсутствии соответствия между ингибированием фермента RT и действием в отношении ВИЧ указанных таннинов. Кроме того, молекулы 44 и 45 демонстрировали активность в отношении ВИЧ, равную 90% и 73% соответственно, но не демонстрировали значительного ингибирования фермента RT.
Michael Ovadia et al. в заявке на патент США 2006275515 A1
В данной заявке на патент под названием «Противовирусные препараты, полученные из природного экстракта коричного дерева» ("Anti-viral preparations obtained from a natural cinnamon extract") описан природный водный экстракт, полученный из коричного дерева, который обладает противовирусными свойствами. Указанный документ описывает водный экстракт коричного дерева, который подвергают осаждению солью (высаливанию). Данный осадок повторно растворяют в воде или буфере и очищают путем хроматографии на сефарозе, а затем элюируют другим буфером и галактозой.
Широко используемый способ высаливания относится к отбору молекул с высокой молекулярной массой (как правило, пептидов). Соответственно, достаточно очевидно, что способ, описанный в указанном документе, направлен на извлечение молекул с высокой молекулярной массой (около 10 кДа).
Активный компонент композиции согласно формуле изобретения обладает молекулярной массой более 10 кДа и соответствует поглощению при 280 нм в диапазоне от приблизительно 15 до 20 ОП. В конечном итоге данное соединение элюируют с колонки Sepharon с использованием фосфатного буфера и галактозы. Соответственно, конечное соединение будет обладать высокими концентрациями фосфатов и галактозы.
Указанное высокомолекулярное соединение, описанное в данной заявке, было протестировано в исследовании вируса гриппа A PR 8, вируса парагриппа (Сендай), предварительного поглощения эритроцитами и увеличения массы у мышей, инфицированных гриппом или вирусом Сендай, и исследовании синцития ВИЧ.
Пример 13 в указанной заявке на патент описывает исследование, выполненное с использованием указанного экстракта в клетках МТ2, для проверки влияния на образование синцития. Согласно Фиг.15 в данной заявке, при концентрациях от 60 до 100 микрограммов он ингибирует образование синцития. Образование синцития не является подтверждающим тестом на предмет противовирусной активности. Это объяснено с доказательствами в следующей публикации [Gueseppe Pantaleo et al Eur J immunology 1991, 21, 1771:1774 'Dissociation between syncytia formation and HIV spreading. Suppressing Syncytia formation does not necessarily reflect inhibition of HIV infection].
Несмотря на то, что описанный экстракт демонстрировал эффективность в отношении ингибирования образования синцития, следует отметить, что только некоторые штаммы ВИЧ вызывают образование синцития. Кроме того, образование синцития не может быть связано с наличием или развитием ВИЧ-инфекции или СПИДа. Образование синцития является только фенотипом, который может быть экспрессирован некоторыми штаммами. Отсутствие образования синцития не может быть связано с отсутствием ВИЧ или контролем данной инфекции.
ЦЕЛИ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Первая цель настоящего изобретения заключается в обеспечении композиции, содержащей пентамерный флавоноид процианидин, тример и тетрамер из источника растительного происхождения.
Вторая цель настоящего изобретения заключается в предложении способа получения композиции, содержащей пентамерный флавоноид процианидин, тример и тетрамер из источников растительного происхождения, таких как коричное дерево (Cinnamomum), литчи (Litchi) и арахис (Arachis).
Третья цель настоящего изобретения заключается в обеспечении композиции, которая улучшает иммунный ответ у субъектов и которая также эффективна в отношении ВИЧ-инфекции, СПИДа и вируса и инфекции гриппа.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соответственно, настоящее изобретение относится к композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, возможно совместно с фармацевтически приемлемыми наполнителями; способу получения композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, при этом указанный способ включает этапы экстрагирования измельченной растительной массы с использованием органического растворителя с удалением токсических веществ; высушивания указанной массы с удалением органического растворителя; повторного экстрагирования сухой массы с использованием водного растворителя с получением экстракта и очистки указанного экстракта с помощью хроматографической колонки с последующим концентрированием, очисткой, стандартизированием и сушкой с получением композиции; способу улучшения иммунного ответа у нуждающегося в этом субъекта, включающему стадию введения указанному субъекту фармацевтически эффективного количества композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, возможно совместно с фармацевтически приемлемыми наполнителями; и способу лечения, предупреждения и контроля ретровирусных инфекций у нуждающегося в этом субъекта, включающему стадию введения указанному субъекту фармацевтически эффективного количества композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, возможно совместно с фармацевтически приемлемыми наполнителями.
КРАТКОЕ ОПИСАНИЕ ПРИЛАГАЕМЫХ ФИГУР
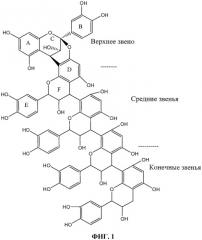
На Фиг.1 показана молекулярная структура пентамерного флавоноида.
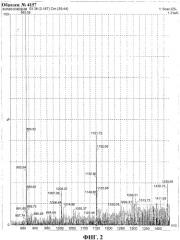
На Фиг.2 показана EI-MS (масс-спектрометрия с ионизацией электронным ударом) пентамерного флавоноида.
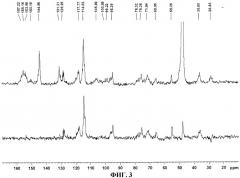
На Фиг.3 показан 13С ЯМР пентамерного флавоноида.
На Фиг.4 показана флэш-хроматограмма композиции с идентификацией пентамерного флавоноида.
На Фиг.5 показана хроматограмма ВЭЖХ пентамерного флавоноида.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, возможно совместно с фармацевтически приемлемыми наполнителями.
В одном из вариантов реализации настоящего изобретения композицию получают из источника растительного происхождения, выбранного из группы, включающей коричное дерево (Cinnamomum), литчи (Litchi) и арахис (Arachis).
В еще одном варианте реализации настоящего изобретения предпочтительная концентрация пентамерного флавоноида процианидина составляет примерно от 80 масс.% до примерно 99 масс.%, концентрация каждого из тримеров и тетрамеров находится в диапазоне от примерно 0,5 масс.% до примерно 20 масс.%.
В еще одном варианте реализации настоящего изобретения молекулярная масса указанного пентамерного флавоноида процианидина составляет около 1440.
В еще одном варианте реализации настоящего изобретения указанный пентамер представляет собой пентамерный процианидин типа А.
В еще одном варианте реализации настоящего изобретения указанные наполнители выбраны из группы, включающей камеди, гранулирующие агенты, связующие агенты, смазывающие вещества, дезинтегранты, подсластители, красители, ароматизаторы, глазировочные вещества, пластификаторы, консерванты, суспендирующие агенты, эмульгаторы, антистатические агенты и сферообразующие агенты.
В еще одном варианте реализации настоящего изобретения указанную композицию изготавливают в различных лекарственных формах, выбранных из группы, включающей таблетку, пастилки, леденцы, водные или масляные суспензии, диспергируемые порошки или гранулы, эмульсию в твердых или мягких гелевых капсулах, сиропы и эликсиры.
Настоящее изобретение относится к способу получения композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, включающему стадии экстрагирования измельченной растительной массы с использованием органического растворителя с удалением токсических веществ; высушивания указанной массы с удалением органического растворителя; повторного экстрагирования сухой массы с использованием водного растворителя с получением экстракта и очистки указанного экстракта с помощью хроматографической колонки с последующим концентрированием, очисткой, стандартизированием и сушкой с получением композиции.
В одном из вариантов реализации настоящего изобретения измельченная растительная масса выбрана из группы растений, включающей коричное дерево, литчи и арахис.
В еще одном варианте реализации настоящего изобретения органический растворитель выбран из группы, включающей этилацетат, бутилацетат, амилацетат, 2-этилгексилацетат и их любые комбинации.
В еще одном варианте реализации настоящего изобретения указанную экстракцию осуществляют в течение периода времени примерно от 8 часов до примерно 12 часов, предпочтительно в течение 10 часов.
В еще одном варианте реализации настоящего изобретения указанные токсические вещества включают кумарин и альдегиды.
В еще одном варианте реализации настоящего изобретения указанный экстракт фильтруют через колонку для двухступенчатой хроматографии.
В еще одном варианте реализации настоящего изобретения указанные хроматографические колонки выбраны из группы, включающей смолы XAD-1180, XAD-7НР и XAD-1140.
В еще одном варианте реализации настоящего изобретения указанное повторное экстрагирование водным растворителем осуществляют при значениях pH примерно от 3,8 до примерно 5,8, предпочтительно при значении pH около 4,0.
В еще одном варианте реализации настоящего изобретения указанное повторное экстрагирование осуществляют в течение периода времени примерно от 8 часов до примерно 12 часов, предпочтительно в течение 10 часов, при температуре в диапазоне от примерно 30°C до 90°C, предпочтительно в диапазоне от 31°C до 40°C.
В еще одном варианте реализации настоящего изобретения указанный водный растворитель представляет собой подкисленную деионизированную воду.
В еще одном варианте реализации настоящего изобретения указанная композиция дополнительно содержит наполнители, выбранные из группы, включающей камеди, гранулирующие агенты, связующие агенты, смазывающие агенты, разрыхлители, подсластители, красители, ароматизаторы, покрывающие агенты, пластификаторы, консерванты, суспендирующие агенты, эмульгаторы, антистатические агенты и сферообразующие агенты.
Настоящее изобретение относится к способу улучшения иммунного ответа у нуждающегося в этом субъекта, включающему стадию введения указанному субъекту фармацевтически эффективного количества композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, возможно совместно с фармацевтически приемлемыми наполнителями.
В еще одном варианте реализации настоящего изобретения иммунный ответ улучшают при заболеваниях, выбранных из группы, включающей, но не ограниченной перечисленными: грипп, ВИЧ-инфекцию и СПИД.
В еще одном варианте реализации настоящего изобретения иммунный ответ улучшают у субъекта, нуждающегося в таком лечении.
В еще одном варианте реализации настоящего изобретения фармацевтически эффективное количество композиции составляет примерно от 1 мг/кг до примерно 100 мг/кг массы тела субъекта.
В еще одном варианте реализации настоящего изобретения указанный способ используют в лечении, предупреждении и контроле инфекции у субъекта, вызванной патогеном.
В еще одном варианте реализации настоящего изобретения указанный патоген включает вирус гриппа А и вирусы ВИЧ.
В еще одном варианте реализации настоящего изобретения указанные типы вируса представляют собой H1N1, H3N2, Х4 и R5-тропный вирус.
В еще одном варианте реализации настоящего изобретения указанный субъект представляет собой животное или человека.
Настоящее изобретение относится к способу лечения, предупреждения и контроля вирусных инфекций у субъекта, нуждающегося в таком лечении, при этом указанный способ включает стадию введения указанному субъекту в качестве противовирусного препарата фармацевтически эффективного количества композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, возможно совместно с фармацевтически приемлемыми наполнителями,
В еще одном варианте реализации настоящего изобретения указанная композиция ингибирует вирус гриппа А, Х4-тропный и R5-тропный вирус ВИЧ.
В еще одном варианте реализации настоящего изобретения фармацевтически эффективное количество композиции составляет примерно от 1 мг/кг до примерно 100 мг/кг массы тела субъекта.
В еще одном варианте реализации настоящего изобретения указанный субъект представляет собой животное или человека.
Настоящее изобретение относится к способу лечения, предупреждения и контроля ретровирусных инфекций у субъекта, нуждающегося в таком лечении, при этом указанный способ включает этап введения указанному субъекту фармацевтически эффективного количества композиции, содержащей пентамерный флавоноид процианидин в концентрации примерно от 55 масс.% до примерно 99 масс.%, тримеры и тетрамеры, каждый в концентрации примерно от 0,5 масс.% до примерно 35 масс.%, возможно совместно с фармацевтически приемлемыми наполнителями.
В одном из вариантов реализации настоящего изобретения указанные ретровирусные инфекции включают инфекцию гриппа А, ВИЧ-инфекцию и СПИД.
В еще одном варианте реализации настоящего изобретения фармацевтически эффективное количество композиции составляет примерно от 1 мг/кг до примерно 100 мг/кг массы тела субъекта.
В еще одном варианте реализации настоящего изобретения указанный субъект представляет собой животное или человека.
Настоящее изобретение относится к новой стандартизированной композиции, полученной из источников растительного происхождения, стандартизированной до 50%-99% пентамера флавоноида процианидина типа А, показанного на Фиг.1. Настоящее изобретение также относится к способу получения новой стандартизированной композиции, получаемой из источников растительного происхождения, стандартизированной до 50%-99% пентамера флавоноида процианидина типа А. Настоящее изобретение также относится к применению новой стандартизированной композиции, полученной из источников растительного происхождения, стандартизированной до 50%-99% пентамера флавоноида процианидина типа А, для предупреждения, лечения и контроля ВИЧ-инфекции и инфекции гриппа.
Настоящее изобретение также относится к применению новой стандартизированной композиции, полученной из источников растительного происхождения, стандартизированной до 50%-99% пентамера флавоноида процианидина типа А, с достижением улучшенного иммунного ответа на антиген у субъекта, нуждающегося в таком лечении.
В другом варианте реализации настоящего изобретения указанный иммунный ответ по своей природе может представлять собой лечение, контроль или профилактику.
В одном из вариантов реализации настоящего изобретения источники растительного происхождения, используемые для получения композиции, представляют собой коричное дерево, литчи и арахис.
В одном из вариантов реализации настоящего изобретения новую стандартизированную композицию, полученную из источников растительного происхождения, стандартизируют до пентамера флавоноида процианидина типа А.
В другом варианте реализации настоящего изобретения молекулярная масса указанного пентамера составляет 1440, как показано на Фиг.1.
В другом варианте реализации настоящего изобретения указанная композиция содержит пентамер в диапазоне от 50% до 99%.
В другом варианте реализации настоящего изобретения указанная композиция содержит тример и тетрамер в диапазоне от 1% до 35%.
В другом варианте реализации настоящего изобретения композиция представляет собой композицию, как она охарактеризована с помощью хроматограммы на Фиг.5.
В другом варианте реализации настоящего изобретения мономерное звено новой композиции выбрано из группы катехинов, предпочтительно катехина или эпикатехина.
Настоящее изобретение также относится к способу получения новой композиции, проиллюстрированному в настоящем документе.
В одном из вариантов настоящего изобретения указанная стандартизированная композиция возможно содержит фармацевтически приемлемый носитель.
В другом варианте реализации настоящего изобретения указанные наполнители выбраны из группы, включающей добавки, камеди, подсластители, покрытия, связующие агенты, разрыхлители, смазывающие вещества, дезинтегранты, суспендирующие агенты, растворители, красители, вещества, способствующие скольжению, антиадгезивы, антистатические агенты, поверхностно-активные вещества, пластификаторы, эмульгаторы, ароматизаторы, усилители вязкости и антиоксиданты.
В еще одном варианте реализации настоящего изобретения указанную композицию изготавливают в лекарственных формах, таких как жидкость, порошок, капсула, таблетка, форма для инъекций, пластырь, мазь, гель, эмульсия, крем, лосьон, средство для чистки зубов, спрей и капли. В еще одном варианте реализации настоящего изобретения указанная композиция представляет собой либо порошок, либо жидкость.
Настоящее изобретение также относится к способу получения новой стандартизированной композиции, получаемой из источников растительного происхождения, стандартизированной до 50%-99% пентамера флавоноида процианидина типа А; при этом указанный способ включает следующие стадии:
1. Измельчение сырья растительного происхождения до заранее определенного размера.
2. Экстракцию органическим растворителем с удалением нежелательных токсических веществ.
3. Водную экстракцию порошка растительного происхождения деионизированной водой.
4. Очистку экстракта с использованием установки для очистки путем двухступенчатой хроматографии.
5. Сушка, смешивание и просеивание с получением композиции, содержащей пентамер флавоноида с чистотой 50%-99%, как показано на Фиг.1.
Настоящее изобретение также относится к применению новой композиции возможно совместно с наполнителями для изготовления лекарственного средства для лечения и контроля ВИЧ и для предупреждения, лечения и контроля вирусной инфекции гриппа.
Настоящее изобретение также относится к применению настоящей композиции возможно совместно с наполнителями для изготовления лекарственного средства для лечения и контроля ВИЧ-инфекции и для предупреждения, лечения и контроля инфекции гриппа у субъекта, нуждающегося в таком лечении.
Настоящее изобретение также относится к применению настоящей композиции возможно совместно с наполнителями для изготовления лекарственного средства для улучшения иммунного ответа у субъекта, нуждающегося в таком лечении. Настоящее изобретение также относится к применению настоящей композиции с обеспечением улучшенного иммунного ответа у субъекта, нуждающегося в таком лечении.
В еще одном варианте реализации настоящего изобретения указанные субъекты представляют собой животных и людей.
Настоящее изобретение также относится к способу получения новой стандартизированной композиции, получаемой из источников растительного происхождения, стандартизированной до 50%-99% пентамера флавоноида процианидина типа А, включающему следующие стадии:
1. Измельчение растительного перикарпия коричного дерева или литчи, или скорлупы земляного ореха с красной кожурой.
2. Экстракцию указанного материала с удалением жиров и токсинов, и других ароматических соединений с использованием органического (предпочтительно сложно эфирного) растворителя, главным образом включающего этилацетат, бутилацетат, амилацетат или 2-этилгексилацетат, в виде либо одного растворителя, либо смеси вышеуказанных растворителей. Данный этап необязателен для коричного дерева.
3. Сушку экстрагированного растительного материала с удалением растворителя.
4. Экстракцию деионизированной водой при значении рН, равном 4, или при значениях рН от 3,8 до 5,8, предпочтительно при рН, равном 4.0. Очистку экстракта с использованием разделения путем двухступенчатой хроматографии, причем на одной стадии проводят разделение полярных и на другой стадии неполярных молекул.
5. Адсорбированное вещество элюируют с использованием спиртового растворителя.
6. Элюированный растворитель концентрируют до мелкодисперсного порошка.
7. Концентрированную массу разбавляют водой и возможно сушат распылением с удалением остатков растворителей.
Новая композиция, полученная вышеуказанным способом, содержит 50%-99% пентамера, 1%-35% тримера и 1%-35% тетрамера и характеризуется как показано на Фиг.5.
Далее настоящее изобретение подробно описано с помощью следующих примеров. Однако данные примеры не ограничивают объем настоящего изобретения.
Пример 1
1000 г измельченного порошка коричн