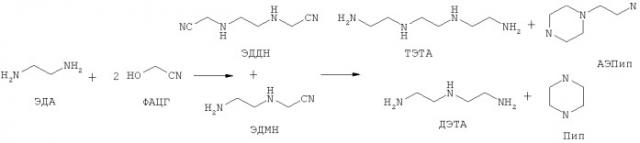
Способ получения триэтилентетрамина (тэта) через этилендиаминдиацетонитрил (эддн)
Иллюстрации
Показать всеИзобретение относится к способу получения триэтилентетрамина (ТЭТА). Способ включает этапы а) и b). На этапе а) формальдегид подвергают реакции с синильной кислотой (HCN) с получением формальдегидциангидрина (ФАЦГ), который затем взаимодействует с этилендиамином (ЭДА) с получением этилендиаминдиацетонитрила (ЭДДН), возможно, в смеси с другими аминонитрилами, содержащими этилендиаминмоноацетонитрил (ЭДМН). При этом мольное соотношение между ЭДА и ФАЦГ составляет от 1:1,5 до 1:2 [моль/моль] и мольное соотношение между ЭДА, формальдегидом и HCN составляет от 1:1,5:1,5 до 1:2:2 [моль/моль/моль]. На этапе b) ЭДДН, полученный на этапе а), гидрируют в присутствии катализатора Ренея и растворителя с получением ТЭТА, возможно, в смеси с другими этиленаминами. Способ является достаточно простым и позволяет получать ТЭТА с высокой селективностью и выходом. 10 з.п. ф-лы, 9 пр.
Реферат
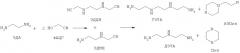
Изобретение касается способа синтеза триэтилентетрамина (ТЭТА) гидрированием этилендиаминдиацетонитрила (ЭДДН) на катализаторе, причем ЭДДН синтезируют посредством реакции этилендиамина (ЭДА) с формальдегидом и синильной кислотой (HCN). ЭДДН может при необходимости также представлять собой составную часть смеси аминонитрилов, содержащую помимо этого этилендиаминмоноацетонитрил (ЭДМН). Благодаря рециркуляции диэтилентриамина (ДЭТА), при необходимости полученного гидрированием, в смеси аминонитрилов может дополнительно содержаться диэтилентриаминмоноацетонитрил (ДЭТМН) или диэтилентриаминдиацетонитрил (ДЭТДН). Путем гидрирования этих дополнительных аминонитрилов получают также тетраэтиленпентаамин (ТЭПА).
Общеизвестно, что в присутствии катализаторов алифатические нитрилы, имеющие при необходимости еще и заместители в виде других функциональных групп, можно гидрировать с образованием соответствующих аминов. Как показано ниже, такие процессы гидрирования с образованием некоторых аминов известны также для различных аминонитрилов. До сих пор, однако, нигде не описывалось, что путем прямого гидрирования аминонитрила можно также синтезировать ТЭТА из аминонитрила ЭДДН или, при необходимости, из смеси аминонитрилов, содержащей ЭДДН и ЭДМН. Однако способы синтеза ТЭТА, известные до настоящего момента, отягощены недостатками, как это показано ниже.
На нынешнем техническом уровне описаны множество способов гидрирования α-аминонитрилов аминоацетонитрила (ААН) и иминодиацетонитрила (ИДАН) или β-аминонитрилов. Так, известно, что гидрирование β-аминонитрилов, как правило, проходит без каких-либо проблем, в то время как гидрирование α-аминонитрилов связано с проявлением различных сложностей, как то: гидрогенолизом связи C-CN или связи R2N-C. В издании „Handbook of Heterogeneous Catalytic Hydrogenation for Organic Synthesis" на стр.213-215 показаны проблемы гидрирования α-аминонитрилов на примере α-аминонитрилов или циклических α-аминонитрилов в сравнении с β-аминонитрилами. Известные проблемы стабильности α-аминонитрилов являются, вероятно, основной причиной того, почему более подробное описание дано только для гидрирования α-аминонитрилов ААН или ИДАН, при котором получают ЭДА (этилендиамин) или ДЭТА (диэтилентриамин). В промышленном масштабе, однако, ЭДА или ДЭТА синтезируют с помощью описанных ниже способов с ЭДХ или МЭА. Соответствующее гидрирование для высших α-аминонитрилов неизвестно.
В германской заявке DE-A 3003729 описан способ гидрирования алифатических нитрилов, алкиленоксинитрилов и алкиленаминонитрилов с получением первичных аминов в присутствии системы растворителей на кобальтовом или рутениевом катализаторе. Используемая система растворителей, кроме воды и аммиака, содержит простой эфир или простой полиэфир. Пригодные к использованию в качестве исходных компонентов алкиленаминонитрилы или алкиленоксинитрилы в каждом случае определены посредством сложных общих формул. В качестве соединений или примеров, для которых возможно гидрирование до соответствующего диамина, приведены в числе прочего этилендиаминпропионитрил (ЭДДПН; имеет также название N,N'-бис(цианоэтил)-этилендиамин) или 3,3'-(этилендиокси)-дипропионитрил. Напротив, в заявке DE-A 3003729 отсутствуют какие-либо указания на применение отдельных соединений из производных ЭДА с цианометиловыми заместителями, например ЭДДН или ЭДМН. Последний к тому же не подпадает, согласно этому документу, под общее определение алкиленаминонитрилов.
В европейской заявке ЕР-А 0382508 описан способ порционного синтеза нециклических алифатических полиаминов путем гидрирования нециклических алифатических полинитрилов в жидкой фазе на кобальтовых катализаторах Ренея, предпочтительно в присутствии безводного аммиака. При этом раствор полинитрила подают в зону реакции, включающую в себя кобальтовый катализатор Ренея, в атмосфере, в основном не содержащей кислорода. На протяжении всего времени реакции раствор полинитрила подают со скоростью, не превышающей максимальной скорости, с которой полинитрил реагирует с водородом в реакционной зоне. Этот способ позволяет синтезировать полиамины из полинитрилов, таких как иминодиацетонитрил (ИДАН), нитрилотриацетонитрил (НТАН), этилендиаминтетраацетонитрил (EDTN) или других, не описанных более подробно, соединений с 2 или более цианогруппами. Непосредственный продукт гидрирования ИДАН - это диэтилентриамин (ДЭТА).
Европейская заявка ЕР-А 212986 касается еще одного способа, позволяющего гидрировать такие же алифатические полинитрилы, как и в заявке ЕР-А 0382508, в присутствии содержащегося в системе жидкого первичного или вторичного амина на гранулярном кобальтовом катализаторе Ренея с образованием соответствующих полиаминов. В качестве аминного компонента, присутствие которого обязательно, в числе прочего, помимо множества других первичных или вторичных аминов, указан этилендиамин (ЭДА).
Европейская заявка ЕР-А 1209146 касается еще одного способа непрерывного гидрирования нитрилов с образованием первичных аминов, причем соответствующие нитрилы применяют в жидкой фазе на суспендированном и активированном катализаторе Ренея на основе алюминиевого сплава, а реакцию проводят в отсутствие аммиака и основных соединений щелочных или щелочноземельных металлов. В качестве нитрилов, помимо множества других, в соответствующие этиленамины можно преобразовывать также ИДАН, ЭТДН, ЭДДПН или этилендиаминмонопропионитрил (ЭДМПН).
Европейская заявка ЕР-В 0913388 касается способа каталитического гидрирования нитрилов, который включает в себя в качестве условий преобразования нитрильной группы в первичный амин контакт нитрила с водородом в присутствии кобальтового катализатора губчатой структуры. Кобальтовый катализатор губчатой структуры предварительно обрабатывали каталитическими количествами гидроксида лития и реализовывали способ в присутствии воды. В качестве нитрилов можно применять алифатические нитрилы с 1-30 атомами углерода, в числе прочего также и β-аминонитрилы, как то: диметиламинопропионитрил. Еще один способ синтеза полиаминов из соответствующих полинитрилов опубликован в германской заявке DE-A 2755687. В этом способе гидрирование проводят на катализаторе гидрирования, имеющем форму таблеток, в присутствии стабилизатора, ингибирующего распад катализатора. В качестве полинитрила можно, помимо прочего, применять этилендиаминдипропионитрил (ЭДДПН). В качестве же стабилизатора пригоден в том числе ЭДА.
Патент США US-A 2006/0041170 касается способа синтеза ТЭТА, в особенности солей ТЭТА, и их применения в качестве лекарственного средства. В этом многоступенчатом процессе сначала синтезируют ЭДДН. Затем проводят реакцию ЭДДН с бензальдегидом с образованием (циклического) производного имидазолидина. Это циклическое соединение, имеющее две цианогруппы, восстанавливают, например, проводя его реакцию с водородом, причем получают соответствующее циклическое диамино-соединение. Это диамино-соединение, в свою очередь, гидролизуют в присутствии кислоты, получая соответствующую соль ТЭТА. В альтернативном варианте исполнения также проводят реакцию диамино-соединения с бензальдегидом, причем получают соответствующее дииминовое соединение, которое затем в свою очередь гидролизуют в присутствии кислоты с получением соответствующей соли ТЭТА. В качестве еще одного варианта способа в этом документе описана реакция ЭДДН с защитными Вос-группами (трет-бутоксикарбонильными группами). Полученное при этом производное ЭДДН, защищенное двумя Вос-группами, затем гидрируют с получением соответствующего защищенного производного ТЭТА. Удаление защитных Вос-групп осуществляют кислотным гидролизом, получая соответствующую соль ТЭТА. Недостаток этого способа, описанного в заявке США US-A 2006/0041170, состоит, в частности, в том, что речь идет о многоступенчатом способе гидрирования, при котором, чтобы провести гидрирование, сначала необходимо получить химические производные применяемого исходного компонента ЭДДН. Еще один недостаток - это то, что ТЭТА получают сначала в виде соли, а не в форме свободного основания.
Таким образом, на нынешнем техническом уровне нигде нет указаний на то, что ЭДДН или смеси аминонитрилов, содержащие ЭДДН и ЭДМН, можно применять для прямого гидрирования аминонитрила в целях синтеза ТЭТА и, возможно, прочих этиленаминов. Известны, однако, другие (промышленные) способы синтеза ТЭТА.
Европейская заявка ЕР-А 222934 касается способа синтеза высших алкиленполиаминов путем реакции вицинального дигалоалкана с избытком аммиака в водной фазе с добавлением сильного основания, причем образуется промежуточный иминовый продукт, который затем подвергают реакции с алкиленполиамином с образованием высшего алкиленполиамина. В качестве вицинального дигалоалкана в особенности удобно применять этилендихлорид (ЭДХ или 1,2-дихлорэтан). В качестве алкиленполиаминов применяют, в частности, этилендиамин или высшие этиленамины, как то: ДЭТА, а также и ТЭТА, и тетраэтиленпентаамин (ТЭПА). При реализации этих способов (ЭДХ-способ) получают смесь различных этиленаминов (линейных этиленаминов, таких как ЭДА, ДЭТА, ТЭТА, ТЭПА, или высших этиленаминов, а также циклические производные, такие как пиперазин (Пип) или аминоэтил-пиперазин (АЭПип)). В зависимости от того, какой этиленамин добавляют к исходным компонентам ЭДХ и аммиаку (NH3), реакционная смесь содержит соответствующую долю высших этиленаминов. Если, например, стоит цель синтезировать ТЭПА, то к исходным компонентам ЭДХ и NH3 добавляют этилендиамин ТЭТА. Полученный таким способом продукт (смесь этиленаминов) содержит более высокую долю ТЭПА, но также, однако, и другие вышепоименованные линейные и циклические этиленамины. Недостаток этого способа работы состоит, в частности, в том, что реализация способа происходит с низкой селективностью (избирательностью относительно компонентов получаемой смеси этиленаминов) и что сначала необходимо синтезировать конкретный этиленамин (например, ДЭТА), который затем вводят в процесс, чтобы целенаправленно синтезировать следующий по гомологической линейке высший этиленамин (например, ТЭТА) или же повысить его выход. Кроме того, ввиду применяемых исходных компонентов (галогеналканов), а также получаемой соляной кислоты этот способ отягощен сложностями, связанными с коррозией, а получаемые соли вредны для окружающей среды.
Заявка США US-A 3,462,493 касается способа синтеза ТЭТА, в котором проводят реакцию ЭДА с этилендихлоридом или этилендибромидом при по меньшей мере пятикратном мольном избытке ЭДА. В качестве побочных продуктов получают, в частности, Пип или пиперазиноэтилэтилендиамин.
В германской публикации DE-T 68911508 описан альтернативный способ производства линейно-удлиненных полиалкиленполиаминов, как, например, ТЭТА. В этом процессе проводят реакцию бифункционального алифатического спирта с аминным реагентом в присутствии содержащего вольфрам катализатора. В качестве бифункционального алифатического спирта можно, в особенности, применять моноэтаноламин (МЭА), а в качестве аминных реагентов - например, ЭДА или ДЭТА. В принципе, с помощью этого способа получают смеси линейно-удлиненных полиалкиленполиаминов (то есть смеси этиленаминов). Из этиленаминов в этих смесях содержатся ДЭТА, ТЭТА, ТЭПА, Пип, АЭПип или пиперазиновые производные высших этиленаминов, причем доля конкретного компонента варьирует в зависимости от использованных аминных реагентов. Постольку, поскольку в качестве аминного реагента применяют ДЭТА, получают смесь этиленаминов с высоким содержанием ТЭТА и ТЭПА. Недостаток этого способа тот, что реализация его происходит с низкой селективностью (избирательностью относительно компонентов получаемой смеси этиленаминов) и что сначала необходимо синтезировать дополнительный этиленамин, который потом подвергают реакции с бифункциональным алифатическим спиртом (например, МЭА). При этом в больших количествах образуются побочные продукты, как то: аминоэтилэтаноламин (АЭЭА) или более тяжелые гидрокси-содержащие этиленамины, представляющие меньший экономический интерес. Причиной образования побочных продуктов в больших количествах является то, что МЭА или высшие этаноламины (например, АЭЭА) могут реагировать сами с собой вместо того, чтобы реагировать с используемым амином. Ввиду большого количества возможных реакций (статистически) избирательность формирования линейного ТЭТА очень низка из-за сопряженных продуктов, а также не поддается регулировке. Синтез возможен только с частичным оборотом.
Обзор синтеза этиленаминов представлен в отчете SRI "CEH Product Review Ethyleneamines"; SRI International, 2003; стр.53-54, в котором соответственно описанным выше способам (с применением исходных компонентов ЭДХ или МЭА) приведены, в частности, синтезы ЭДА или ДЭТА. При этом высшие этиленамины, такие как ТЭТА или ТЭПА образуются как побочные продукты либо же их получают повторной реакцией исходных компонентов с ЭДА или ДЭТА с более высоким выходом.
Кроме того, в литературе имеются отдельные описания способов синтеза ЭДДН или ЭДМН. Так, в K.Masuzawa et al., Bull. Chem. Soc. Japan, т.41 (1968), стр.702-706, описан способ синтеза и реакция азотных и серных аналогов производных 2-пиперазинона. Для синтеза этого класса веществ сначала используют исходные компоненты ЭДА и ФАЦГ (формальдегидциангидрин). Реакцию обоих исходных компонентов проводят в эквимолярном соотношении, используя в качестве растворителя метанол. После того как реакционный раствор оставили на два дня при комнатной температуре, и после удаления растворителя, а также не прошедших реакцию исходных компонентов при сниженном давлении получают маслянистый продукт. Помимо циклического соединения этот маслянистый продукт содержит в качестве побочного компонента ЭДМН. Реакцию проводили в безводной среде. Затем маслянистый продукт подвергают в многоэтапном процессе дальнейшему преобразованию с образованием желательных производных 2-пиперазинона. В этом документе в качестве нежелательного побочного процесса при реакции ЭДА с ФАЦГ описан также синтез ЭДДН. ЭДДН получают, когда идет реакция избытка ЭДА с ФАЦГ в метаноле при 55-60°С. После повышения концентрации при пониженном давлении осуществляют выделение продукта путем дистилляции в вакууме. При этом добиваются выхода около 27,3% относительно использованного ЭДА.
Н.Baganz et al., Chem. Ber, 90 (1957), стр.2944-2949, описывают способ получения производных N,N'-этилен-бис-аминокислот, при котором исходным компонентом для этого многоступенчатого синтеза служит дигидрохлорид ЭДДН. В этом документе имеется также пропись синтеза дигидрохлорида ЭДДН. При этом в реакционный сосуд помещают дигидрохлорид ЭДА и цианид калия (KCN), а затем по каплям добавляют в сосуд 30%-ный формальдегид, причем температура реакции не превышает 25°С. По прошествии 12 часов реакции и добавления едкого натра продукт встряхивают с простыми эфирами, сушат и добавлением хлороводорода переводят в осадок в виде соли аммония. Затем полученный продукт кристаллизуют. Особыми недостатками этого процесса являются применение хлороводорода, а также KCN, что ведет к очень высокому содержанию солей в водной фазе. Кроме того, проблемой является экстракция простыми эфирами, поскольку ввиду хорошей растворимости ЭДДН продукт реакции не полностью поступает в эфирную фазу.
Н.Brown et al., Helvetica Chimica Acta, т.43 (1960), стр.659-666, описывают способ синтеза комплексообразователей тиазолового ряда. В этом многоступенчатом процессе в качестве исходного материала применяют ЭДДН, а кроме того, этот документ содержит пропись синтеза ЭДДН. В соответствии с описанным там способом в реакционную аппаратуру помещают ЭДА в воде, после чего, перемешивая и охлаждая льдом, добавляют одновременно синильную кислоту (HCN), а также цианид кальция (Ca(CN)2) в воде. В этом процессе, однако, формальдегид не применяют. После трудоемкой дальнейшей обработки получают ЭДДН с относительно низким выходом.
Уже упомянутая выше патентная заявка США US-A 2006/0041170 также содержит прописи для синтеза описанного там исходного компонента ЭДДН. С одной стороны, возможен синтез ЭДДН путем прямого алкилирования ЭДА галоацетонитрилом, например хлорацетонитрилом или бромацетонитрилом. С другой стороны, ЭДДН синтезируют посредством уже описанного выше преобразования ЭДА, в особенности дигидрохлорида ЭДА, реакцией сначала с формальдегидом, а потом с солями цианида, как то: KCN. Полученный при этом продукт реакции дополнительно обрабатывают кислотой. Поскольку в качестве исходного компонента используют ЭДА, то перед дальнейшей реакцией с формальдегидом сначала дополнительно осуществляют перевод ЭДА в форму соли, особенно в дигидрохлорид. Недостаток этого способа состоит в выпадении соли ввиду применения солей цианида. Также недостатком является применение солей ЭДА в виде твердых веществ, поскольку ЭДА либо применяют непосредственно в виде соли, либо сначала переводят его в форму соли. Кроме того, описанный в заявке US-A 2006/0041170 способ непригоден для непрерывного применения.
Следовательно, задача настоящего изобретения состоит в том, чтобы представить простой и недорогой способ синтеза ТЭТА и, при необходимости, прочих этиленаминов в заранее заданных количествах.
Задачу решают посредством способа синтеза триэтилентетрамина (триэтилентетраамина, ТЭТА), включающего в себя следующие этапы:
a) этилендиамин (ЭДА) подвергают реакции с формальдегидом и синильной кислотой (HCN) с получением этилендиаминдиацетонитрила (ЭДДН), причем мольное соотношение между ЭДА, формальдегидом и HCN составляет от 1:1,5:1,5 до 1:2:2 [моль/моль/моль],
b) гидрирование ЭДДН, полученного на этапе а), в присутствии катализатора и растворителя.
Способ согласно изобретению обладает тем преимуществом, что ТЭТА и при необходимости еще один главный компонент ДЭТА можно синтезировать с высокой степенью превращения и/или высокой селективностью. Повышенная селективность проявляется, в частности, в том, что примененный ЭДДН гидрируется преимущественно с получением ТЭТА. Образующиеся при этом побочные продукты - это в основном другие линейные этиленамины. Доля циклических этиленаминов при реализации способа согласно изобретению сравнительно низка. Прочие этиленамины, однако, отчасти сами представляют интерес как продукты (в основном линейные этиленамины, например ДЭТА), выделение которых имеет смысл, например, в промышленном процессе. Напротив, циклические этиленамины, например АЭПип, представляют скорее незначительный интерес, однако возможно их дальнейшее преобразование при возвращении в процесс.
Избирательность способа согласно изобретению можно выгодным образом повысить, проведя перед гидрированием отделение легкокипящих компонентов, в особенности синильной кислоты (HCN). Формирование синильной кислоты при этом возможно как продукта разложения формальдегидциангидрина (ФАЦГ). В частности, синильная кислота может действовать при гидрировании как каталитический яд.
После отделения легкокипящих компонентов возможен более быстрый и обладающий более высокой избирательностью синтез ЭДДН, а также при необходимости прочих аминонитрилов, таких как ЭДМН или ДЭТДН. Это также благоприятно сказывается на селективности последующего гидрирования.
Целесообразно, чтобы реакция ЭДДН и при необходимости ЭДМН проходила полностью или почти полностью. Это имеет значение прежде всего в промышленном процессе, поскольку не прошедший преобразование исходный компонент, как правило, приходится возвращать в производственный контур циркуляции или утилизировать. Способы, в которых реакцию не проходят большие количества ЭДДН и/или ЭДМН, особо невыгодны ввиду высокой нестабильности ЭДДН и ЭДМН. С одной стороны, как ЭДДН, так и ЭДМН при высокой температуре склонны к разложению, так что отсутствует возможность вернуть продукты разложения в соответствующий контур циркуляции, а с другой стороны, это разложение может проходить взрывообразно. Поскольку при реализации способа согласно изобретению возможно полное преобразование аминонитрилов, необходимости в каких-либо мероприятиях по возвращению в цикл производства нет.
Еще одно преимущество способа согласно изобретению состоит в том, что в отличие от способа с ЭДХ можно обойтись без использования хлорированных углеводородов в качестве исходного компонента. Кроме того, в качестве дополнительного продукта реакции не получают соляной кислоты или ее солей. Утилизация вышеуказанных веществ представляет собой проблему (экологическую), в особенности в промышленном процессе. В сравнении со способом с МЭА преимущество состоит в том, что благодаря применению иных исходных компонентов формирование АЭЭА, а также других соединений с гидроксильными функциональными группами не играет никакой роли. Также преимуществом является то, что способ согласно изобретению можно реализовывать непрерывно.
Поскольку при реализации способа согласно изобретению гидрируют смесь аминонитрилов, можно рассматривать как преимущество тот факт, что в зависимости от потребностей рынка можно синтезировать большие или меньшие доли ТЭТА или ДЭТА. Причина этого лежит в том, что в принципе соотношение исходных компонентов ЭДМН и ЭДДН друг к другу отражается в продукте реакции в виде соотношения ДЭТА и ТЭТА. Так, при реализации способа согласно изобретению можно специально использовать конкретные составы смесей аминонитрилов, чтобы обеспечивать производство в желательных для рынка количественных соотношениях. При высокой избирательности способ согласно изобретению позволяет получать смесь этиленаминов, которая содержит в качестве обладающих ценностью продуктов по меньшей мере 30% ТЭТА, по меньшей мере 5% ДЭТА, а также при необходимости прочие этиленамины, как производные пиперазина.
Способ согласно изобретению обладает, благодаря наличию этапа а), еще и тем преимуществом, что ЭДДН, а также при необходимости обладающую заданным составом смесь, содержащую ЭДДН и прочие аминонитрилы, как то: ЭДМН, можно синтезировать просто, а также с высокой чистотой. Как ЭДДН, так и, при необходимости, ЭДМН поддаются изоляции простым способом в виде чистых кристаллов, в то время как при реализации способов, соответствующих нынешнему техническому уровню, напротив, продукт получают в виде вязкой жидкости, из которой желаемый продукт можно выделить только путем трудоемких этапов дополнительной обработки и с низкой степенью очистки.
Еще одно преимущество способа согласно изобретению состоит в том, что можно обойтись без солей цианида, например KCN и Са(CN)2. Кроме того, при реализации способа согласно изобретению, что целесообразно, ЭДА как исходный компонент применяют не в виде соли, а в форме свободного основания. Следовательно, при реализации способа согласно изобретению доля солей в реакционном растворе невысока, и, таким образом, получают меньше содержащих соли побочных продуктов или не прошедших преобразование исходных компонентов. Это выгодно, в частности, в промышленных процессах. Более высокое содержание солей в реакционном растворе невыгодно в особенности тогда, когда способ согласно изобретению реализуют в водной фазе. Следовательно, желаемый продукт можно синтезировать проще, с меньшим количеством этапов реакции. Кроме того, преимуществом является то, что способ согласно изобретению, особенно этап а), можно реализовывать непрерывно.
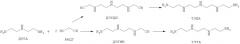
Еще одним существенным преимуществом способа согласно изобретению следует считать то, что из одного лишь исходного компонента (ЭДА) можно синтезировать смесь этиленаминов, содержащую два (главных) продукта (ТЭТА и ДЭТА), причем соотношение между ними можно целенаправленно регулировать. Еще в одной форме исполнения настоящего изобретения ДЭТА, содержащийся в смеси этиленов, можно после этапа а) полностью или частично возвращать, чтобы провести его реакцию, предпочтительно с ФАЦГ. Таким образом синтезируют ДЭТДН и/или ДЭТМН, которые затем подвергают дальнейшему гидрированию с образованием ТЭПА либо же ТЭТА, соответственно. Следовательно, посредством способа согласно изобретению можно, используя всего один исходный компонент (ЭДА), а также частичный возврат продукта гидрирования ДЭТА, синтезировать различные этиленамины ТЭПА, ТЭТА и ДЭТА. В зависимости от выбранных исходных условий можно синтезировать смеси этиленаминов, в которых вышеуказанные главные продукты присутствуют в различных соотношениях друг с другом, причем из смеси этиленаминов можно выделить отдельные этиленамины (ТЭТА, ТЭПА и/или ДЭТА, а также при необходимости прочие побочные продукты).
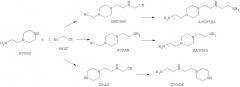
Еще в одной форме исполнения после этапа а) допустимо также возвращение АЭПип, образовавшегося при гидрировании в качестве циклического побочного продукта. Преобразование АЭПип в соответствующие аминонитрилы с последующим гидрированием позволяет получать диаминоэтилпиперазин (ДАЭПип), пиперазинэтилэтилендиамин (ПЭЭДА), а также аминоэтилпиперазинилэтилэтилендиамин (АЭПЭЭДА). Эти циклические этиленамины также представляют интерес как обладающие ценностью продукты.
Этап а)
На этапе а) этилендиамин (ЭДА) подвергают реакции с формальдегидом и синильной кислотой (HCN), причем мольное соотношение между ЭДА, формальдегидом и HCN составляет от 1:1,5:1,5 до 1:2:2 [моль/моль/моль], с получением этилендиаминдиацетонитрила (ЭДДН).
Если ниже не указано иное (опции а1)-а4)), то исходные компоненты для этапа а) можно вводить в соответствующий реакционный сосуд в произвольной последовательности. Например, можно полностью ввести один из исходных компонентов и добавить второй исходный компонент. Целесообразно синтезировать ЭДДН в соответствии с одной из приведенных ниже опций а1)-а4). Особо предпочтительно синтезировать ЭДДН в соответствии а1).
В соответствии с опцией а1) сначала проводят реакцию формальдегида и HCN с образованием формальдегидциангидрина (ФАЦГ), после чего в свою очередь проводят реакцию ЭДА с ФАЦГ, а мольное соотношение между ЭДА и ФАЦГ составляет от 1:1,5 до 1:2 [моль/моль]. ЭДА, формальдегид и HCN представляют собой коммерчески доступные продукты, либо же их можно синтезировать известными специалистам методами. Предпочтительно использовать ЭДА при реализации способа согласно изобретению в виде свободного основания, при необходимости, однако, можно также применять в качестве исходного компонента соли, как дигидрохлорид ЭДА.
Реакция формальдегида и HCN друг с другом известна специалистам. Синтез ФАЦГ можно проводить путем реакции водного формальдегида с синильной кислотой. Предпочтительно, чтобы формальдегид находился в форме водного раствора концентрацией от 30 до 50%, синильную кислоту применяют с чистотой от 90 до 100%. Эту реакцию предпочтительно проводить при значении pH, составляющем 5,5, доводить показатель предпочтительно едким натром или аммиаком. Реакцию можно проводить в реакторе в виде змеевика и/или в виде трубы при температуре от 20 до 70°С.
Вместо очищенной синильной кислоты (HCN) можно получить ФАЦГ, проводя при вышеуказанных условиях хемосорбцию неочищенного газа HCN в водном растворе формальдегида. Неочищенный газ HCN предпочтительно получить пиролизом формамида, помимо воды он содержит, в частности, небольшие количества аммиака.
При необходимости можно путем щадящего выпаривания в вакууме, например, с помощью испарителя с падающей пленкой или тонкослойного испарителя, повысить концентрацию полученного раствора ФАЦГ и освободить его от легкокипящих компонентов, в частности от синильной кислоты. Предпочтительно повышать концентрацию раствора ФАЦГ до от 50 до 80%. Перед повышением концентрации целесообразно стабилизировать раствор ФАЦГ путем снижения значения pH до величины, меньшей или равной 4, предпочтительно - меньшей или равной 3, например, путем добавления кислоты, например фосфорной или - предпочтительно - серной кислоты.
В соответствии с опцией а1) предпочтительно, чтобы мольное соотношение между ЭДА и ФАЦГ составляло около от 1:1,8 до 1:2 [моль/моль], особенно около 1:2 [моль/моль].
В соответствии с опцией а2) проводят преобразование ЭДДН путем реакции этилендиамин-формальдегид-аддукта (ЭДФА) с синильной кислотой (HCN), причем мольное соотношение ЭДФА и HCN составляет от 1:1,5 до 1:2 [моль/моль]. В соответствии с опцией а1) предпочтительно, чтобы мольное соотношение между ЭДА и ФАЦГ составляло около от 1:1,8 до 1:2 [моль/моль], особенно около 1:2 [моль/моль]. ЭДФА предпочтительно синтезировать путем смешения примерно эквимолярных количеств ЭДА и формальдегида.
В соответствии с опцией а3) проводят реакцию ЭДА со смесью формальдегида и синильной кислоты (СФС), причем мольное соотношение ЭДА и СФС составляет от 1:1,5 до 1:2 [моль/моль]. Предпочтительно, чтобы мольное соотношение между ЭДА и СФС составляло около от 1:1,8 до 1:2 [моль/моль], особенно около 1:2 [моль/моль]. СФС предпочтительно синтезировать путем смешения примерно эквимолярных количеств формальдегида и синильной кислоты.
В соответствии с опцией а4) ЭДА подвергают параллельной реакции с формальдегидом и синильной кислотой (HCN), причем мольное соотношение между ЭДА, формальдегидом и HCN составляет от 1:1,5:1,5 до 1:2:2 [моль/моль/моль]. Предпочтительно, чтобы мольное соотношение между ЭДА, формальдегидом и HCN составляло около от 1:1,8:1,8 до 1:2:2 [моль/моль/моль], особенно около 1:2:2 [моль/моль/моль]. В этой форме исполнения предпочтительно добавлять три исходных компонента в реакционный сосуд одновременно или поэтапно равными мольными порциями относительно общего количества соответствующего исходного компонента.
При определенных обстоятельствах конкретные исходные компоненты либо же промежуточные продукты можно применять в реализации способа согласно изобретению сразу же после их синтеза. Например, ФАЦГ в опции а1) можно применять в качестве исходного компонента для способа согласно изобретению без его предварительного отделения. При необходимости, однако, после синтеза ФАЦГ можно сначала изолировать его, чтобы впоследствии использовать при реализации способа согласно изобретению.
В одной из форм исполнения настоящего изобретения этап а) осуществляют без применения цианистых солей, таких как KCN, или в основном без их применения.
Обычно этап а) способа согласно изобретению реализуют в присутствии растворителя. При реализации способа согласно изобретению предпочтительно осуществлять реакцию исходных компонентов для синтеза ЭДДН в водной фазе. Кроме воды можно при необходимости использовать другие известные специалисту растворители, способные смешиваться с водой. Менее предпочтительны в качестве растворителей, однако, спирты, в особенности метанол.
Этап а) предпочтительно реализовывать при температуре от 10 до 90°С, в особенности при температуре от 30 до 70°С. Реакцию можно проводить при нормальном или же - при необходимости - при повышенном давлении. Предпочтительно осуществлять этап а) в трубчатом реакторе или в каскаде котлов с мешалками. Также целесообразно реализовывать этап а) в виде непрерывного процесса, в особенности как технический процесс.
Кроме основного продукта ЭДДН на этапе а) способа согласно изобретению в качестве важного побочного продукта получают этилендиаминмоноацетонитрил (ЭДМН). В зависимости от выбранных параметров способа (например, исходных компонентов, температуры, растворителя или давления) можно регулировать способ согласно изобретению так, что доля ЭДМН в продукте реакции варьирует и ЭДМН получают не как побочный продукт, а как второй главный продукт реакции. В этом варианте исполнения настоящего изобретения, следовательно, синтезируют смесь аминонитрилов, которая кроме ЭДДН содержит также (как главный продукт) ЭДМН. При этом предпочтительно синтезировать смеси аминонитрилов, содержащие по меньшей мере 30% мас. ЭДДН и по меньшей мере 5% мас. ЭДМН. ЭДДН обычно содержится в смеси аминонитрилов в количестве от 30 до 95% мас., предпочтительно от 50 до 95% мас., особо предпочтительно в количестве от 75 до 90% мас. Смесь аминонитрилов обычно содержит ЭДМН в количестве от 5 до 70% мас., предпочтительно от 5 до 50% мас., особо предпочтительно в количестве от 10 до 25% мас. Приведенные выше значения относятся только к соотношению ЭДДН к ЭДМН без учета прочих аминонитрилов, которые образованы благодаря возврату продуктов гидрирования с этапа b).
Данные по массовой процентной доле ЭДДН либо же ЭДМН относятся к общему количеству аминонитрилов, содержащихся в смеси. Эти количественные данные не учитывают дополнительно присутствующую воду или прочие растворители.
Повышения доли ЭДМН в смеси аминонитрилов предпочтительно достигать, применяя в опциях а1)-а4) в каждом случае меньшую (в указанных пределах параметров) мольную долю ФАЦГ (опция а1)), HCN (опция а2)), СФС (опция а3)) или формальдегида и HCN (опция а4)). Так, например, в соответствии с опцией а) для повышения доли ЭДМН применяют мольное соотношение ЭДА к ФАЦГ, равное от 1:1,5 до 1:1,8 [моль/моль].
Кроме того, для синтеза смеси аминонитрилов, которая содержит меньшую долю ЭДМН, например 10% мас., особенно от 5 до 10% мас., в одной из форм исполнения настоящего изобретения можно проводить реакцию ЭДА с по возможности наиболее высокой мольной долей ФАЦГ. При этом целесообразно применять водный раствор, содержащий не менее 40% мас. ФАЦГ или чистый ФАЦГ. В этом случае предпочтительно, чтобы мольное соотношение ЭДА и ФАЦГ составляло 1:2 [моль/моль].
При необходимости в соответствии с настоящим изобретением можно синтезировать также очень чистый ЭДДН с низкой долей ЭДМН. Предпочтительно, чтобы доля ЭДМН, а также, возможно, присутствующих других побочных продуктов, например прочих аминонитрилов, составляла не более 10% мас., особенно не более 5% мас., относительно ЭДДН.
Этап b)
Этап b) включает в себя гидрирование ЭДДН, полученного на этапе а), в присутствии катализатора и растворителя. В рамках настоящего изобретения гидрирование означает реакцию ЭДДН и при необходимости ЭДМН, а также присутствующих, возможно, других аминонитрилов с водородом.
Этап b) можно реализовывать непосредственно после этапа а), при необходимости между этапами а) и b) можно осуществить один или несколько шагов очистки (приведенных ниже).
i) Отделение легкокипящих компонентов
В одной из форм исполнения настоящего изобретения перед гидрированием от продуктов реакции этапа а) отделяют легкокипящие компоненты. Поскольку для синтеза ЭДДН и при необходимости ЭДМН используют ФАЦГ, отделение легкокипящих компонентов можно проводить еще до реакции ФАЦГ с ЭДА.
Синильную кислоту (HCN) предпочтительно отделять как легкокипящий компонент. При этом HCN может представлять собой продукт разложения ФАЦГ. Кроме того, в это время можно отделить, возможно, имеющийся аммиак. Предпочтительно проводить отделение путем дистилляции, например, в форме испарения в тонком слое, например, в испарителе Sambay (Chemie Ingenieur Technik, Vol.27, S.257-261). При необходимости можно также провести отгонку легких фракций из реакционной смеси с использованием азота.
ii) Снижение содержания воды
Снижение содержания воды, полное или частичное, можно проводить либо (предпочтительно) одновременно с таковым легкокипящих компонентов, либо после них. Предпочтительно проводить снижение содержания воды дистилляцией. Это можно осуществлять в испарителе или в каскаде испарителей в один или несколько этапов, причем на различных этапах можно задавать различные значения давления или температуры. Отделение воды можно также проводить в дистилляционной колонне. Предпочтительно проводить отделение воды в вакууме. Аминонитрил или смесь аминонитрилов могут после этого содержать еще остаточные количества воды или легкокипящих компонентов. Предпочтительно остаточное количество воды по меньшей мере 10% мас. Легкокипящие компоненты присутствуют лишь в небольших следовых количествах. Также допустимо отделение легкокипящих компонентов и воды после синтеза ФАЦГ.
iii) Адсорбция примесей
Аминонитрил или смесь аминонитрилов, полученные на этапе а), можно очищать от примесей путем адсорбции их на адсорбенте, например активированном угле или ионообменнике, либо непосредственно после отделения легкокипящих компонентов, либо после отделения легкокипящих компонентов и воды. Это можно осуществлять, например, в адсорбционной кол