Производные пиридинона и пиридазинона в качестве ингибиторов поли(adp-рибоза) полимеразы (parp)
Иллюстрации
Показать всеНастоящее изобретение относится к соединениям формулы (IX), в которой радикалы и символы имеют значения, определенные в формуле изобретения, и их фармацевтически приемлемым солям или таутомерам. Данные соединения являются ингибиторами поли(АDР-рибоза)полимеразы (PARP) и могут быть применены для лечения рака, воспалительных заболеваний, реперфузионных повреждений, ишемических состояний, удара, почечной недостаточности, кардиососудистых заболеваний, сосудистых заболеваний, отличных от кардиососудистых заболеваний, сахарного диабета, нейродегенеративных заболеваний, ретровирусных инфекций, повреждения сетчатки, старения кожи и индуцированного УФ-светом повреждения кожи и в качестве химио- или радиосенсибилизаторов при лечении рака. Изобретение также относится к фармацевтической композиции, их содержащей, применению этих соединений и способу лечения указанных выше заболеваний. 7 н. и 3 з.п. ф-лы, 18 пр., 1 табл.
Реферат
Настоящее изобретение относится к производным пиридинона и пиридазинона, которые являются ингибиторами фермента поли(ADP-рибоза)полимеразы (PARP), ранее известной как поли(ADP-рибоза)синтаза и поли(ADP-рибозил)трансфераза. Соединения по настоящему изобретению могут быть применены для монотерапии опухолей со специфическими нарушениями в путях восстановления ДНК и как усиливающие агенты для определенных повреждающих ДНК агентов, таких как противораковые средства и радиотерапия. Далее соединения по настоящему изобретению могут быть применены для лечения клеточного некроза (при ударе и инфаркте миокарда), уменьшения воспаления и тканевого повреждения, лечения ретровирусных инфекций и защиты от токсичности химиотерапии.
Поли(ADP-рибоза)полимераза (PARP) образована надсемейством восемнадцати белков, содержащих каталитические домены PARP (Bioassays (2004) 26:1148). Эти белки включают PARP-1, PARP-2, PARP-3, танкиразу-1, танкиразу-2, vaultPARP и TiPARP. PARP-1, основной представитель надсемейства, состоит из трех доменов: амино (N)-концевого ДНК-связывающего домена (DBD), содержащего два цинк-содержащих фрагмента, автомодифицирующего домена и карбокси-(C)-концевого каталитического домена.
PARP представляют собой ядерные и цитоплазматические ферменты, которые расщепляют NAD+ до никотинамида и ADP-рибозы для получения длинных и разветвленных полимеров ADP-рибозы на целевых белках, включая топоизомеразы, гистоны и конкретно PARP (Biochem. Biophys. Res. Commun. (1998) 245:1-10).
Поли-ADP-рибозилирование участвует в нескольких биологических процессах, включая восстановление ДНК, генной транскрипции, прохождении клеточного цикла, гибели клеток, хроматиновых функциях и стабильности генома.
Каталитическая активность PARP-1 и PARP-2, как было показано, прямо активируется разрывами нити ДНК (см. Pharmacological Research (2005) 52:25-33). В ответ на повреждение ДНК PARP-1 связывается с однонитевым и двунитевым разрывами ДНК. В нормальных физиологических условиях активность PARP минимальна, однако при повреждении ДНК имеет место немедленная активация активности PARP, возрастающей до 500 раз. Как PARP-1, так и PARP-2 обнаруживают обрывы нити ДНК, действуя в качестве определителей разрыва ДНК, обеспечивая быстрые сигналы остановки транскрипции и притока ферментов, требующихся для восстановления ДНК в точке повреждения. Поскольку радиотерапии и многие химиотерапевтические способы терапии рака действуют под влиянием индуцирующего повреждения ДНК, ингибиторы PARP могут быть применены как химио- и радиосенсибилизаторы при лечении рака. Ингибиторы PARP, как сообщалось, являются эффективными в радиосенсибилизации гипоксических опухолевых клеток (патенты US 5032617, 5215738 и 5041653).
Большинство биологических эффектов PARP относятся к этому процессу поли-ADP-рибозилирования, который влияет на свойства и функции целевых белков; к PAR-олигомерам, которые, когда отщепляются от поли-ADP-рибозилированных белков, создают различные клеточные эффекты; физической ассоциации PARP с ядерными белками с образованием функциональных комплексов и снижению клеточного уровня их субстрата, NAD+ (Nature Review (2005) 4:421-440).
Кроме участия в восстановлении ДНК, PARP также может действовать как медиатор гибели клеток. Его избыточная активация при патологических состояниях, таких как ишемия и реперфузионное повреждение, может приводить к значительному уменьшению уровня межклеточного NAD+, что может вести к ослаблению нескольких NAD+ зависимых метаболических путей и приводить к гибели клеток (см. Pharmacological Research (2005) 52:44-59). В результате активации PARP уровни NAD+ значительно падают. Экстенсивная активация PARP ведет к значительному уменьшению уровней NAD+ в клетках, страдающих от крупного повреждения ДНК. Короткий период полураспада поли(ADP-рибозы) приводит к большой скорости круговорота, если один раз поли(ADP-рибоза) образуется, она быстро разлагается всегда активной поли(ADP-рибоза) гликогидролазой (PARG). PARP и PARG образуют цикл, который конвертирует большое количество NAD+ в ADP-рибозу, вызывая падение NAD+ и ATP до уровня менее чем 20% от нормального уровня. Такой сценарий является особенно пагубным при ишемии, когда потеря кислорода уже значительно подрывает выход клеточной энергии. Последующее продуцирование свободных радикалов в течение реперфузии, как предполагается, является основной причиной повреждения ткани. Часть падения уровня ATP, которое является типичным для многих органов при ишемии и реперфузии, может быть связана со снижением уровня NAD+ благодаря кругообороту поли(ADP-рибозы). Таким образом, ингибирование PARP, как ожидается, сберегает уровень клеточной энергии, таким образом потенцируя выживание ишемических тканей после удара. Соединения, которые являются ингибиторами PARP, следовательно, могут быть применены для лечения состояний, которые возникают из опосредованной PARP гибели клеток, включая неврологические состояния, такие как удар, травма и болезнь Паркинсона.
Ингибиторы PARP, как было показано, могут быть применены для специфического уничтожения BRCA-1 и BRCA-2 дефицитных опухолей (Nature (2005) 434:913-916 и 917-921; и Cancer Biology & Therapy (2005) 4:934-936).
Ингибиторы PARP, как было показано, являются селективными для уничтожения клеток с дефектами в ATM, ДНК_PK или KU80 (Nucleic Acid Research (2006) 34: 1685-1691).
Ингибиторы PARP, как было показано, усиливают эффективность противораковых лекарственных средств (Pharmacological Research (2005) 52:25-33), включая соединения платины, такие как цисплатин и карбоплатин (Cancer Chemother. Pharmacol. (1993) 33:157-162 и Mol. Cancer Ther. (2003) 2:371-382). Ингибиторы PARP, как было показано, увеличивают антиопухолевую активность ингибиторов топоизомеразы I, таких как иринотекан и топотекан (Mol. Cancer Ther. (2003) 2:371-382; и Clin. Cancer Res. (2000) 6:2860-2867), и это было продемонстрировано на моделях in vivo (J. Natl. Cancer Inst. (2004) 96:56-67).
Ингибиторы PARP, как было показано, возвращают чувствительность к цитотоксическим и антипролиферативным эффектам темозоломида (TMZ) (см. Curr. Med. Chem. (2002) 9:1285-1301 и Med. Chem. Rev. Online (2004) 1: 144-150). Это было продемонстрировано на ряде моделей in vitro (Br. J. Cancer (1995) 72:849-856; Br J. Cancer (1996) 74:1030-1036; Mol Pharmacol (1997) 52:249-258; Leukemia (1999) 13:901-909; Glia (2002) 40:44-54; и Clin. Cancer Res. (2000) 6:2860-2867 и (2004) 10:881-889) и моделях in vivo (Blood (2002) 99:2241-2244; Clin. Cancer Res. (2003) 9:5370-5379 и J. Natl. Cancer Inst. (2004) 96:56-67). Как было показано, ингибиторы PARP также предотвращают появление некроза, индуцируемого селективными N3-аденинметилирующими агентами, такими как MeOSO2(CH2)-лекситропсин (Me-Lex) (Pharmacological Research (2005) 52:25-33).
Ингибиторы PARP, как было показано, действуют как радиационные сенсибилизаторы. Ингибиторы PARP, как сообщалось, являются эффективными в отношении радиосенсибилизированных (гипоксических) опухолевых клеток и эффективны при предотвращении восстановления опухолевых клеток после потенциально летального (Br. J. Cancer (1984) 49 (Suppl. VI):34-42; и Int. J. Radiat Bioi. (1999) 75:91-100) и близкого к летальному (Clin. Oncol. (2004) 16(l):29-39) повреждения ДНК после радиационной терапии, предположительно посредством их способности предотвращать соединения разрывов нити ДНК и путем сильного влияния на несколько сигнальных путей при повреждении ДНК.
Ингибиторы PARP, как было показано, могут быть применены для лечения острых и хронических миокардиальных заболеваний (см. Pharmacological Research (2005) 52:34-43). Например, было продемонстрировано, что одиночные инъекции ингибиторов PARP уменьшают размер инфаркта, вызываемого ишемией и реперфузией сердца или скелетной мышцы на кроликах. В этих исследованиях одиночная инъекция 3-аминобензамида (10 мг/кг), за одну минуту до окклюзии или за одну минуту до реперфузии, вызывает аналогичные уменьшения размера инфаркта в сердце (32-42%), в то время как 1,5-дигидроксиизохинолин (1 мг/кг), другой ингибитор PARP, уменьшает размер инфаркта в сопоставимой степени (38-48%). Эти результаты делают корректным предположение, что ингибиторы PARP могут восстанавливать поврежденное ранее ишемией сердце или реперфузионное повреждение скелетной мышечной ткани (PNAS (1997) 94:679-683). Подобные результаты также были установлены на свиньях (Eur. J. Pharmacol. (1998) 359:143-150 и Ann. Thorac. Surg. (2002) 73:575-581) и на собаках (Shock. (2004) 21:426-32).
Ингибиторы PARP, как было показано, могут быть применены для лечения определенных сосудистых заболеваний, септического шока, ишемического повреждения и нейротоксичности (Biochim. Biophys. Acta (1989) 1014:1-7; J. Clin. Invest. (1997) 100: 723-735). Повреждение ДНК радикалами кислорода, которое ведет к разрывам нити в ДНК, которое затем идентифицируется PARP, является основным фактором, вносящим вклад в такие болезненные состояния, как показано исследованиями ингибитора PARP (J. Neurosci. Res. (1994) 39:38-46 и PNAS (1996) 93:4688-4692). Также, как было продемонстрировано, PARP играет роль в патогенезе геморрагического шока (PNAS (2000) 97:10203-10208).
Ингибиторы PARP, как было показано, могут быть применены для лечения воспалительных заболеваний (см. Pharmacological Research (2005) 52:72-82 и 83-92).
Также было продемонстрировано, что эффективная ретровирусная инфекция клеток млекопитающих блокируется ингибированием активности PARP. Такое ингибирование рекомбинантных ретровирусных векторных инфекций, как было показано, имеет место в различных типах клеток (J. Virology, (1996) 70(6):3992-4000). Таким образом, ингибиторы PARP исследуются для применения в качестве антивирусных терапий и для лечения рака (WO 91/18591).
Эксперименты in vitro и in vivo продемонстрировали, что ингибиторы PARP могут быть применены для лечения или предупреждения аутоиммунных заболеваний, таких как диабет I типа и осложнения при диабете (Pharmacological Research (2005) 52:60-71).
Ингибирование PARP было предположено в качестве причины отсрочки характеристик старения в человеческих фибробластах (Biochem. Biophys. Res. Comm. (1994) 201(2):665-672 и Pharmacological Research (2005) 52:93-99). Это может быть связано с ролью, которую PARP играет в контролировании теломерной функции (Nature Gen., (1999) 23(l):76-80).
Огромное большинство ингибиторов PARP, опубликованных к настоящему времени, взаимодействует с никотинамид-связывающим доменом фермента и ведет себя как конкурентные ингибиторы в отношении NAD+ (Expert Opin. Ther. Patents (2004) 14:1531-1551). Структурные аналоги никотинамида, такие как бензамид и производные, были среди первых соединений, исследованных в качестве ингибиторов PARP. Однако эти молекулы имеют слабую подавляющую активность и обладают другими эффектами, не связанными с ингибированием PARP. Таким образом, существует необходимость в нахождении мощных ингибиторов фермента PARP.
US 2005/0234236 описывает способ для синтеза пиридазинонов, WO 2004/085406 описывает бензилпиридазиноны в качестве ингибиторов обратной транскриптазы и EP 0810218 описывает бензилпиридазиноны в качестве ингибиторов COX I и COX II.
Теперь неожиданно впервые найдено, что производные пиридинона и пиридазинона по настоящему изобретению проявляют высокую степень ингибирования активности PARP.
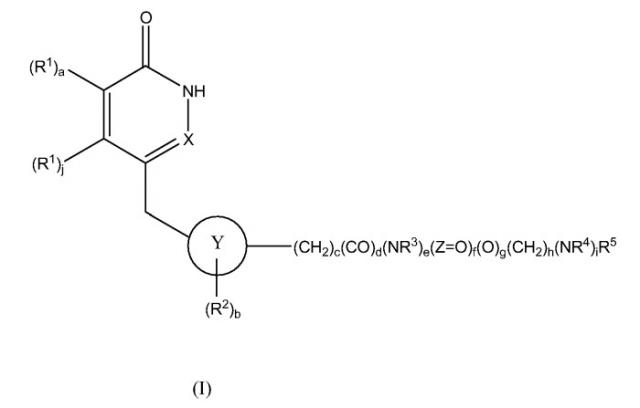
Соединения по настоящему изобретению могут быть применены для ингибирования поли(ADP-рибоза)полимеразы (PARP). В частности, они могут быть применены в качестве ингибиторов PARP-1 и/или PARP-2. Настоящее изобретение предоставляет применение соединения формулы I:
,
где
a равно 0 или 1;
b равно 0, 1, 2 или 3;
c равно 0, 1, 2, 3, 4, 5 или 6;
d равно 0 или 1;
e равно 0 или 1;
f равно 0 или 1;
g равно 0 или 1;
h равно 0, 1, 2, 3, 4, 5 или 6;
i равно 0 или 1;
j равно 0 или 1;
X представляет собой N или CH;
Y представляет собой C6-10-арил, 5-членный ненасыщенный гетероцикл, содержащий 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N и S, но не более чем один из которых представляет собой O или S, или 6-членный ненасыщенный гетероцикл, содержащий 1, 2, 3 или 4 атома азота;
Z представляет собой C или SO;
R1, каждый независимо, представляет собой C1-6-алкил, галоген-C1-6-алкил, галоген или циано;
R2, каждый независимо, представляет собой гидрокси, галоген, циано, нитро, C1-6-алкил, галоген-C1-6-алкил, C1-6-алкокси, галоген-C1-6-алкокси или NRaRb;
R3 представляет собой водород или C1-6-алкил;
R4 представляет собой водород или C1-6-алкил;
R5 представляет собой водород, гидрокси, циано, оксо, галоген, C1-6-алкил, C2-10-алкенил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкилкарбонил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкоксикарбонил, карбокси, нитро или цикл, который представляет собой C6-10-арил; C6-10-арилкарбонил; C3-10-циклоалкил; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-15-членное ненасыщенное, частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6;
A, каждый независимо, представляет собой простую связь, O, C=O, (C=O)NR7, NR7(C=O), (C=O)O, O(C=O), (C=S)NR7, NR7 или S(O)r;
q, каждый независимо, равен 0, 1, 2, 3 или 4;
r равно 0, 1 или 2;
R6, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6-алкил, C2-10-алкенил, галоген-C1-6-алкил, NRaRb или цикл, который представляет собой: C3-10-циклоалкил; C6-10-арил; C6-10-арилокси; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома, независимо выбранных из N, О и S; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из R8;
R7 представляет собой водород или R6;
R8, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6-алкил, C1-6-алкокси, C2-10-алкенил, галоген-C1-6-алкил, галоген-C1-6-алкокси, -O(C=O)C1-6-алкил, -(C=O)OC1-6-алкил, NRaRb или цикл, который представляет собой C3-10-циклоалкил, C6-10-арил, C6-10-арил-C1-6-алкил, C6-10-арилкарбонил, C6-10-арилоксикарбонил, C6-10-арил-C1-6-алкоксикарбонил, 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; или 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из галогена, C1-6-алкила или галоген-C1-6-алкила;
каждый из R9 и R10 независимо представляет собой водород, галоген, С1-6-алкил или галоген-C1-6-алкил;
каждый из Ra и Rb независимо представляет собой водород, C1-6-алкил, C3-10-циклоалкил, C3-10-циклоалкил-C1-6-алкил, C6-10-арил или C6-10-арил-C1-6-алкил;
или его фармацевтически приемлемой соли или таутомера для приготовления лекарственного средства для лечения или предупреждения состояний, при которых может быть достигнуто улучшение путем ингибирования поли(ADP-рибоза)полимеразы (PARP).
Настоящее изобретение также предоставляет способ лечения или предупреждения состояний, при которых может быть достигнуто улучшение путем ингибирования поли(ADP-рибоза)полимеразы (PARP), где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
В варианте осуществления состояния, которые могут быть излечены путем ингибирования поли(ADP-рибоза)полимеразы (PARP), включают воспалительные заболевания; реперфузионные травмы; ишемические состояния; удар; хроническую и острую почечную недостаточность; сосудистые заболевания, отличные от кардиососудистых заболеваний; кардиососудистые заболевания; сахарный диабет; рак, особенно рак, который является дефицитным в отношении зависимой от гомологичной рекомбинации (HR) репаразной активности в отношении двухнитевого разрыва ДНК, например BRCA-1 или BRCA-2 дефицитных опухолях; нейродегенеративные заболевания; ретровирусные инфекции; повреждение сетчатки; старение кожи; индуцированное УФ-светом повреждение кожи и преждевременное старение.
В варианте осуществления состояния, при которых могут быть достигнуты улучшения путем ингибирования поли(ADP-рибоза)полимеразы (PARP), являются выбранными из реперфузионных травм; ишемических состояний; удара; хронической и острой почечной недостаточности; сосудистых заболеваний, отличных от кардиососудистых заболеваний; кардиососудистых заболеваний; сахарного диабета; рака, особенно рака, который является дефицитным в отношении зависимой от гомологичной рекомбинации (HR) репаразной активности в отношении двухнитевого разрыва ДНК, например BRCA-1 или BRCA-2 дефицитных опухолях; нейродегенеративных заболеваний; ретровирусных инфекций; повреждения сетчатки; старения кожи; индуцированного УФ-светом повреждения кожи и преждевременного старения.
В варианте осуществления для каждого из указанных выше вариантов осуществления
R2, каждый независимо, представляет собой гидрокси, галоген, циано, нитро, C1-6-алкил, галоген-C1-6-алкил, C1-6-алкокси или галоген-C1-6-алкокси;
R5 представляет собой водород, гидрокси, циано, оксо, галоген, C1-6-алкил, C2-10-алкенил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкилкарбонил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкоксикарбонил, карбокси, нитро или цикл, который представляет собой C6-10-арил; C6-10-арилкарбонил; C3-10-циклоалкил; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CH2)qR6;
R6, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6алкил, C2-10-алкенил, галоген-С1-6-алкил или цикл, который представляет собой C6-10-арил; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из R8;
R8, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6-алкил, C1-6-алкокси, C2-10-алкенил, галоген-C1-6-алкил, галоген-C1-6-алкокси, -O(C=O)C1-6-алкил, -(C=O)OC1-6-алкил, амино, C1-6-алкиламино, ди(C1-6-алкил)амино, C6-10-арил, 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; или 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота.
Настоящее изобретение также предоставляет новые соединения формулы I:
,
в которой
a, b, c, d, e, f, g, h, i, j, X, Y, Z, R1, R2, R3, R4 и R5 определены выше; при условии что:
(a) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой O-мостик, R2 представляет собой фтор, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным циклом, выбранным из C6-10-арила, 5-членного гетероароматического кольца, 6-членного гетероароматического кольца или 7-15-членного ненасыщенного или частично насыщенного гетероциклического кольца;
(b) если X представляет собой N и Y представляет собой фенил, нафтил или 9- или 10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1 или 2 гетероатома, выбранных из N, O и S, то R5 не представляет собой C1-6-алкил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкилкарбонил или необязательно замещенный C3-10-циклоалкил, фенил, нафтил, пиридинил, пиридин-N-оксид, индол, индол-N-оксид, хинолин, хинолин-N-оксид, пиримидинил, пиразинил или пирролил; и
(c) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой CO-мостик, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным фенилом, пиридинилом, тиенилом или фурилом;
или их фармацевтически приемлемые соли или таутомеры.
В варианте осуществления:
(a) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой O-мостик, R2 представляет собой фтор, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным циклом, выбранным из C6-10-арила, 5-членного гетероароматического кольца, 6-членного гетероароматического кольца или 7-10-членного ненасыщенного или частично насыщенного гетероциклического кольца;
(b) если X представляет собой N и Y представляет собой фенил, нафтил или 9- или 10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1 или 2 гетероатома, выбранные из N, O и S, то R5 не представляет собой C1-6-алкил, галоген-C1-6-алкил, гидрокси-C1-6-алкил или необязательно замещенный C3-10-циклоалкил, фенил, нафтил, пиридинил, пиридин-N-оксид, индол, индол-N-оксид, хинолин, хинолин-N-оксид, пиримидинил, пиразинил или пирролил; и
(c) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой CO-мостик, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным фенилом, пиридинилом, тиенилом или фурилом.
В варианте осуществления сумма a и j равна 1 или 2.
В варианте осуществления b равно 0 или 1. В другом варианте осуществления b равно 1.
В варианте осуществления c равно 0.
В варианте осуществления d равно 1.
В варианте осуществления e равно 0.
В варианте осуществления f равно 0.
В варианте осуществления g равно 0.
В варианте осуществления h равно 0.
В варианте осуществления i равно 0.
В варианте осуществления j равно 0. В другом варианте осуществления j равно 1.
В варианте осуществления X представляет собой N. В другом варианте осуществления X представляет собой CH.
В варианте осуществления Y представляет собой фенил, пиридинил, пиримидинил, фурил или тиенил.
В другом варианте осуществления Y представляет собой C6-10-арил.
В частности, группа Y представляет собой фенил.
В варианте осуществления R1 представляет собой фтор-C1-3-алкил, галоген или C1-6-алкил. В другом варианте осуществления R1 представляет собой C1-6-алкил.
Предпочтительная R1 группа представляет собой этил. Более предпочтительные R1 группы представляют собой метил и изопропил.
В варианте осуществления R2 представляет собой галоген, C1-6-алкокси, амино, C1-6-алкиламино или ди(C1-6-алкил)амино.
В другом варианте осуществления R2 представляет собой фтор-C1-3-алкил или галоген.
В другом варианте осуществления R2 представляет собой галоген, например фтор или хлор.
Предпочтительно, R2 группа представляет собой фтор. Более предпочтительные R2 группы представляют собой диметиламино, изопропокси и метокси.
В варианте осуществления R5 представляет собой водород, гидрокси, циано, галоген, C2-10-алкенил, С1-6-алкилкарбонил, C1-6-алкокси, C1-6-алкоксикарбонил, карбокси, нитро или цикл, который представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; или 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CH2)qR6.
В другом варианте осуществления R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное ненасыщенное, частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6.
В другом варианте осуществления R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6.
В другом варианте осуществления R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N или 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CH2)qR6.
В варианте осуществления R5 представляет собой диазепанил, пиперидинил, пиперазинил, пирролидинил, спиробензофуранпиперидинил, тетрагидроимидазопиразинил, тетрагидротриазолопиразинил, диазаспиродеканил, тетрагидропиразолопиридинил, диазаспирононанил, имидазолидинил, азетидинил или тетрагидротриазолопиридинил; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6.
В варианте осуществления, когда R5 представляет собой цикл, цикл является необязательно замещенным одной, двумя или тремя независимо выбранными A-(CR9R10)qR6 группами. В варианте осуществления, когда R5 представляет собой цикл, цикл является незамещенным или монозамещенным.
В варианте осуществления, когда R6 представляет собой цикл, он является необязательно замещенным одной, двумя или тремя группами, независимо выбранными из R8. В другом варианте осуществления, когда R6 представляет собой цикл, он является незамещенным, монозамещенным или дизамещенным.
В варианте осуществления, когда R8 представляет собой цикл, он является необязательно замещенным одной, двумя или тремя группами из независимо выбранных групп. В другом варианте осуществления, когда R8 представляет собой цикл, он является незамещенным, монозамещенным или дизамещенным.
В варианте осуществления R7 представляет собой водород.
В варианте осуществления A представляет собой прямую связь, O, CO или NH.
В другом варианте осуществления A представляет собой прямую связь, CO или NH. В другом варианте осуществления A представляет собой прямую связь или карбонил. Предпочтительная A группа представляет собой CO.
В варианте осуществления q равно 0, 1 или 2. В другом варианте осуществления q равно 0.
В варианте осуществления R6 представляет собой оксо, C1-6-алкил, галоген-C1-6-алкил, амино, C1-6-алкиламино, (диC1-6-алкил)амино или цикл, который представляет собой пиримидинил, пиридинил, пиразолил, фенил, пиразинил, тетрагидроизохинолинил, циклопентил, тетрагидрофуранил, пирролидинил, пиперидинил, хиназолинил, фенокси, фурил, бензодиоксолил, тиенил, циклопропил или азетидинил; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из R8.
В другом варианте осуществления R6 представляет собой C1-6-алкил.
В варианте осуществления R8 представляет собой циано, галоген, C1-6-алкил, галоген-C1-6-алкил, C1-6-алкокси, амино, C1-6-алкиламино, ди(C1-6-алкил)амино, (C3-10-циклоалкил-C1-6-алкил)амино, C6-10-ариламино, (C6-10-арил-C1-6-алкил)амино или цикл, который представляет собой C6-10-арил, C6-10-арил-C1-6-алкил, C6-10-арилкарбонил, C6-10-арилоксикарбонил или C6-10-арил-C1-6-алкоксикарбонил; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из галогена и C1-6-алкила.
Предпочтительные R8 группы включают метокси, хлор, метил, трифторметил, фтор, циано, метиламино, пропил, диметиламино, бензил, бензоксикарбонил, фениламино, амино, бензиламино, (циклопропилметил)амино, изобутиламино, фторбензил, метилбензил, нафтилметил и этил.
В варианте осуществления каждый из R9 и R10 независимо представляет собой водород, метил, фтор или трифторметил.
В другом варианте осуществления каждый из R9 и R10 представляет собой атом водорода.
Предпочтительная R6 группа представляет собой метил. Более предпочтительные R6 группы включают пиримидинил, пиридинил, метоксипиридинил, диметиламино, пиразолил, хлорпиридинил, фенил, диметилпиразинил, метоксифенил, тетрагидроизохинолинил, циклопентил, трифторметил, метиламино, дифторметил, изопропил, тетрагидрофуранил, пирролидинил, пиперидинил, хиназолинил, метилфенил, (трифторметил)фенил, фторфенокси, цианопиридинил, дифторфенил, фурил, метилпирролидинил, бензодиоксолил, тиенил, циклопропил, оксо, дифторазетидинил, (метиламино)циклопентил, пропилпирролидинил, метилпиперидинил, (диметиламино)циклопропил, бензилпирролидинил, (метиламино)циклопропил, метилазетидинил, (бензоксикарбонил)метилпиперидинил, (фениламино)циклопентил, аминоциклопентил, (бензиламино)циклопентил, [(циклопропилметил)амино]циклопентил, (изобутиламино)циклопентил, (фторбензил)пирролидинил, (метилбензил)пирролидинил, (нафтилметил)пирролидинил и этилпирролидинил.
Таким образом, предпочтительные R5 группы представляют собой диазепанил и ацетилдиазепанил. Более предпочтительные R5 группы представляют собой пиримидинилдиазепанил, пиридинилпиперидинил, [(пиридинилметил)окси]пиперидинил, (метоксипиридинил)пиперазинил, пиридинилпирролидинил, [(диметиламино)метил]пиперидинил, спиробензофуранпиперидинил, (пиразолилэтил)пиперидинил, (хлорпиридинил)пиперазинил, бензилтетрагидроимидазопиразинил, (диметилпиразинил)пиперазинил, фенилтетрагидроимидазопиразинил, (метоксибензил)пиперазинил, тетрагидроизохинолинилпиперидинил, пиперазинил, фенилпиперазинил, бензилпиперазинил, (пиридинилметил)пиперазинил, (циклопентилкарбонил)диазепанил, (трифторметил)тетрагидротриазолопиразинил, пропионилпиперазинил, [(метил)(метиламино)пропаноил]пиперазинил, (дифторацетил)пиперазинил, (трифторпропаноил)пиперазинил, изобутирилпиперазинил, (пиридинилкарбонил)пиперазинил, (тетрагидрофурилкарбонил)пиперазинил, [(метил)(диметиламино)пропаноил]пиперазинил, (пентафторпропаноил)пиперазинил, (пирролидинилкарбонил)пиперазинил, (трифторацетил)пиперазинил, пиперидинилпиперидинил, пирролидинилпиперидинил, хиназолинилпиперазинил, пиримидинилпиперазинил, диазаспиродеканил, (метилфенил)тетрагидротриазолопиразинил, [(трифторметил)фенил]тетрагидротриазолопиразинил, [(фторфенокси)метил]тетрагидротриазолопиразинил, (цианопиридинил)пиперазинил, (метил)диазаспиродеканил, (дифторфенил)тетрагидротриазолопиразинил, [(диметиламино)метил]тетрагидротриазолопиразинил, фурилтетрагидротриазолопиразинил, (пентафторэтил)тетрагидротриазолопиразинил, {[(трифторметил)фенил]амино}тетрагидротриазолопиразинил, (метилпролил)пиперазинил, фенилтетрагидротриазолопиразинил, бензодиоксолилтетрагидротриазолопиразинил, тиенилтетрагидротриазолопиразинил, циклопропилтетрагидропиразолопиридинил, (трифторметил)тетрагидропиразолопиридинил, пиридинилтетрагидротриазолопиразинил, диазаспирононанил, метилдиоксиимидазолидинил, (пирролидинилметил)азетидинил, (дифторазетидинил)пиперидинил, (трифторэтил)тетрагидротриазолопиридинил, {[(метиламино)циклопентил]карбонил}пиперазинил, метилдиазаспирононанил, [(пропилпирролидинил)карбонил]пиперазинил, (пиперидинилкарбонил)пиперазинил, [(метилпиперидинил)карбонил]пиперазинил, {[(диметиламино)циклопропил]карбонил}пиперидинил, [(диметиламино)пропаноил]пиперидинил, [(бензилпирролидинил)карбонил]пиперазинил, (пирролидинилкарбонил)пиперазинил, {[(метиламино)циклопропил]карбонил}пиперазинил, [(метилазетидинил)карбонил]пиперазинил, [(метилпирролидинил)карбонил]пиперидинил, [(диметиламино)трифторпропанонил]пиперазинил, [(метилпиперидинил)карбонил]пиперидинил, {[(бензоксикарбонил)метилпиперидинил]карбонил}пиперидинил, [(диметиламино)метилэтил]тетрагидротриазолопиразинил, (трифторэтил)тетрагидротриазолопиридинил, [(пирролидинил)ацетил]пиперидинил, этилдиазаспиродеканил, (циклопропилметил)диазаспиродеканил, [(анилиноциклопентил)карбонил]пиперазинил, [(аминоциклопентил)карбонил]пиперазинил, {[(бензиламино)циклопентил]карбонил}пиперазинил, ({[(циклопропилметил)амино]циклопентил}карбонил)пиперазинил, {[(изобутиламино)циклопентил]карбонил}пиперазинил, [(фторбензил)пролил]пиперазинил, [(метилбензил)пролил]пиперазинил, [(нафтилметил)пролил]пиперазинил и (этилпролил)пиперазинил.
Предпочтительные R5 группы представляют собой 1,4-диазепан-1-ил и 4-ацетил-1,4-диазепан-1-ил. Более предпочтительные R5 группы представляют собой 4-(пиримидин-2-ил)-1,4-диазепан-1-ил, 4-(пиридин-4-ил)пиперидин-1-ил, 4-[(пиридин-2-илметил)окси]пиперидин-1-ил, 3-[(пиридин-2-илметил)окси]пиперидин-1-ил, 4-(5-метоксипиридин-2-ил)пиперазин-1-ил, 4-(4-метоксипиридин-2-ил)пиперазин-1-ил, 3-пиридин-4-илпирролидин-1-ил, 3-[(диметиламино)метил]пиперидин-1-ил, 1'H-спиро[1-бензофуран-3,4'-пиперидин]-1'-ил, 4-(1H-пиразол-1-илэтил)пиперидин-1-ил, 4-(5-хлорпиридин-2-ил)пиперазин-1-ил, 4-(6-метоксипиридин-2-ил)пиперазин-1-ил, 3-бензил-5,6,7,8-тетрагидроимидазо[1,2-a]пиразин-7-ил, 4-(3,6-диметилпиразин-2-ил)пиперазин-1-ил, 3-фенил-5,6,7,8-тетрагидроимидазо[1,2-a]пиразин-7-ил, 4-(3-метоксибензил)пиперазин-1-ил, 4-(1,2,3,4-тетрагидроизохинолин-2-ил)пиперидин-1-ил, пиперазин-1-ил, 2-фенилпиперазин-1-ил, 2-бензилпиперазин-1-ил, 3-(пиридин-3-илметил)пиперазин-1-ил, 4-(циклопентилкарбонил)-1,4-диазепан-1-ил, 3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил, 4-пропионилпиперазин-1-ил, 4-[2-метил-2-(метиламино)пропаноил]пиперазин-1-ил, 4-(дифторацетил)пиперазин-1-ил, 4-(3,3,3-трифторпропаноил)пиперазин-1-ил, 4-изобутирилпиперазин-1-ил, 4-(пиридин-2-илкарбонил)пиперазин-1-ил, 4-(тетрагидрофуран-2-илкарбонил)пиперазин-1-ил, 4-[2-метил-2-(диметиламино)пропаноил]пиперазин-1-ил, 4-(2,2,3,3,3-пентафторпропаноил)пиперазин-1-ил, 4-(пирролидин-1-илкарбонил)пип