Новое соединение хризена и органическое светоизлучающее устройство, в котором применяют это соединение
Иллюстрации
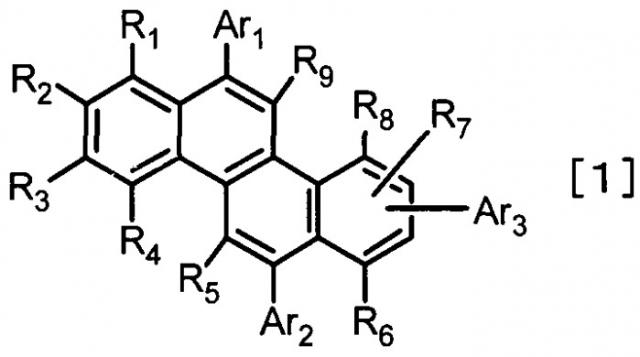
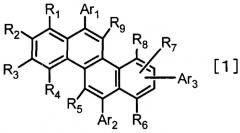
Показать всеИзобретение относится к соединению хризена, представленному общей формулой [1]:
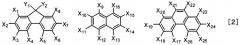
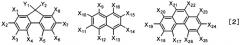
где каждый из R1-R9 представляет собой атом водорода, и Ar1, Ar2 и Ar3 каждый независимо выбирают из группы, представленной общими формулами [2]:
где Х1-Х26 каждый независимо выбирают из группы, состоящей из атома водорода, алкильной группы, состоящей только из углерода и водорода, содержащей 1-4 атома углерода, фенильной группы, которая может быть замещена алкильной группой, состоящей только из углерода и водорода, содержащей 1-4 атома углерода, нафтильной группы, которая может быть замещена алкильной группой, состоящей только из углерода и водорода, содержащей 1-4 атома углерода, фенантрильной группы, которая может быть замещена алкильной группой, состоящей только из углерода и водорода, содержащей 1-4 атома углерода, и флуоренильной группы, которая может быть замещена алкильной группой, состоящей только из углерода и водорода, содержащей 1-4 атома углерода, при условии, что один из X1-X8, один из X9-X16 и один из Х17-Х26 каждый представляет хризеновое кольцо, представленное общей формулой [1]; и Y1 и Y2 каждый независимо выбирают из алкильной группы, состоящей только из углерода и водорода, содержащей 1-4 атома углерода. Также изобретение относится с органическому светоизлучающему устройству, а также дисплею, использующим указанное соединение. Использование заявляемого соединения позволяет в достаточной степени увеличивать эффективность эмиссии и соответствующий срок службы. 3 н. и 5 з.п. ф-лы, 50 пр., 9 табл., 1 ил.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новому соединению хризена и органическому светоизлучающему устройству, в котором применяют это соединение.
Уровень техники
Органическое светоизлучающее устройство является таким устройством, в котором между анодом и катодом, служащими в качестве пары электродов, установлена тонкая пленка, содержащая флуоресцирующее органическое соединение или фосфоресцирующее органическое соединение.
При этом эффективность эмиссии и срок службы органического светоизлучающего устройства поддаются совершенствованию.
Производное хризена известно в качестве одного из видов конденсированного полициклического ароматического соединения. В патентном документе Japanese Patent Application Laid-Open No. 2004-75567 раскрывается производное 6,12-диарилзамещенного хризена. В патентном документе Japanese Patent Application Laid-Open No. 2007-273055 раскрывается производное 3,6,9,12-тетраарилзамещенного хризена и в публикации Chem. Commun. 2008, 2319 описано производное 2,6,8,12-тетраарилзамещенного хризена. Кроме того, в WO 2009/008311 раскрывается производное 2,6,12-трифенилзамещенного хризена.
Описание изобретения
Задачей настоящего изобретения является создание нового соединения, способного в достаточной степени обеспечивать эффективность эмиссии и соответствующий срок службы. Более конкретно, задачей изобретения является создание нового соединения хризена и органического светоизлучающего устройства, в котором применяют это соединение.
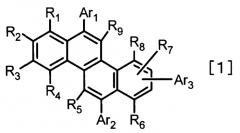
Согласно настоящему изобретению предлагается соединение хризена, представленное следующей общей формулой [1].
(В общей формуле [1] R1-R9 каждый независимо выбирают из группы, состоящей из атома водорода, замещенной или незамещенной алкильной группы и замещенной или незамещенной алкоксигруппы, и Ar1, Ar2 и Ar3 каждый независимо выбирают из группы, представленной следующими формулами [2]).
(В формуле [2] X1-X26 каждый независимо выбирают из группы, состоящей из атома водорода, замещенной или незамещенной алкильной группы, замещенной или незамещенной алкоксигруппы, замещенной или незамещенной фенильной группы, замещенной или незамещенной нафтильной группы, замещенной или незамещенной фенантрильной группы и замещенной или незамещенной флуоренильной группы, при условии, что один из X1-X8, один из X9-X16 и один из X17-X26 каждый представляет хризеновое кольцо, представленное общей формулой [1], и Y1 и Y2 каждый независимо выбирают из атома водорода и замещенной или незамещенной алкильной группы).
Согласно настоящему изобретению может быть предложено новое соединение хризена, обладающее высокой химической стабильностью, глубоким энергетическим уровнем высшей заполненной молекулярной орбитали (HOMO), широкой запрещенной энергетической зоной, малым двухгранным углом и высокой способностью переноса носителей заряда. Кроме того, может быть предложено органическое светоизлучающее устройство, в котором применяют это соединение, при этом устройство характеризуется высокой эффективностью эмиссии и высоким сроком службы.
Краткое описание чертежей
На фиг.1 схематически показан вид в поперечном разрезе органического светоизлучающего устройства и переключающего устройства, подсоединенного к органическому светоизлучающему устройству.
Предпочтительный вариант осуществления изобретения
Соединение хризена согласно настоящему изобретению представлено следующей общей формулой [1].
В формуле [1] R1-R9 каждый независимо выбирают из группы, состоящей из атома водорода, замещенной или незамещенной алкильной группы и замещенной или незамещенной алкоксигруппы.
Конкретные примеры алкильной группы включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, втор-бутильную группу, трет-бутильную группу, н-пентильную группу, неопентильную группу, н-гексильную группу, н-октильную группу, н-децильную группу, н-додецильную группу, циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, норборнильную группу и адамантильную группу.
Конкретные примеры алкоксигруппы включают метоксигруппу, этоксигруппу, изопропоксигруппу, трет-бутоксигруппу, арилоксигруппу и бензилоксигруппу.
Упомянутые выше алкильная группа и алкоксигруппа могут иметь заместитель. Примеры заместителя включают алкильные группы, такие как метильная группа, этильная группа и пропильная группа; углеводородные ароматические кольцевые группы, такие как фенильная группа, нафтильная группа, фенантрильная группа и флуоренильная группа; гетероароматические кольцевые группы, такие как тиенильная группа, пирролильная группа и пиридильная группа; замещенные аминогруппы, такие как диметиламиногруппа, диэтиламиногруппа, дибензиламиногруппа, дифениламиногруппа, дитолиламиногруппа и дианизолиламиногруппа; алкоксигруппы, такие как метоксигруппа и этоксигруппа; арилоксигруппы, такие как феноксигруппа и нафтоксигруппа; атомы галогена, такие как фтор, хлор, бром и йод; гидроксильную группу; цианогруппу; и нитрогруппу.
Заместители Ar1, Ar2 и Ar3 в формуле [1] каждый независимо выбирают из группы заместителей, представленных следующими формулами [2].
В формуле [2] X1-X26 каждый независимо представляет заместители, выбранные из группы, состоящей из атома водорода, замещенной или незамещенной алкильной группы, замещенной или незамещенной алкоксигруппы, замещенной или незамещенной фенильной группы, замещенной или незамещенной нафтильной группы, замещенной или незамещенной фенантрильной группы и замещенной или незамещенной флуоренильной группы, при условии, что один из X1-X8, один из X9-X16 и один из X17-X26 каждый представляет хризеновое кольцо, представленное общей формулой [1].
Конкретные примеры алкильной группы, представленной любым одним из X1-X26, являются такими же, как упомянутые выше конкретные примеры алкильной группы, представленной любым одним из R1-R9 в формуле [1]. Конкретные примеры заместителя, который может дополнительно иметь алкильная группа, являются такими же, как упомянутые выше конкретные примеры заместителя, который может дополнительно иметь алкильная группа, когда любой один из R1-R9 в формуле [1] представляет алкильную группу.
Конкретные примеры алкоксигруппы, представленной любым одним из X1-X26, являются такими же, как упомянутые выше конкретные примеры алкоксигруппы, представленной любым одним из R1-R9 в формуле [1]. Конкретные примеры заместителя, который может дополнительно иметь алкоксигруппа, являются такими же, как упомянутые выше конкретные примеры заместителя, который может дополнительно иметь алкоксигруппа, когда любой один из R1-R9 в формуле [1] представляет алкоксигруппу.
Конкретные примеры заместителя, который могут дополнительно иметь фенильная группа, нафтильная группа, фенантрильная группа и флуоренильная группа, представленные любым одним из X1-X26, включают алкильную группу, такую как метильная группа, этильная группа, изопропильная группа, трет-бутильная группа, н-гексильная группа и циклогексильная группа; ароматическую углеводородную кольцевую группу, такую как фенильная группа, толильная группа, трет-бутилфенильная группа, ксилильная группа, мезитильная группа, нафтильная группа, фенантрильная группа, флуоренильная группа, 9,9-диметилфлуоренильная группа, 9,9-диэтилфлуоренильная группа и 9,9-ди-(н-гексил)флуоренильная группа; ароматическую гетероциклическую группу, такую как тиенильная группа, пирролильная группа, пиридильная группа и фенантролинильная группа; замещенную аминогруппу, такую как диметиламиногруппа, диэтиламиногруппа, дибензиламиногруппа, дифениламиногруппа, дитолиламиногруппа и дианизолиламиногруппа; алкоксигруппу, такую как метоксигруппа и этоксигруппа; арилоксигруппу, такую как феноксигруппа и нафтоксигруппа; атом галогена, такой как фтор, хлор, бром и йод; гидроксильную группу; цианогруппу; и нитрогруппу.
Y1 и Y2 в формуле [2] каждый независимо выбирают из атома водорода и замещенной или незамещенной алкильной группы.
Конкретные примеры алкильной группы, представленной любым одним из Y1 и Y2, являются такими же, как упомянутые выше конкретные примеры алкильной группы, представленной любым одним из R1-R9 в формуле [1]. Конкретные примеры заместителя, который может дополнительно иметь алкильная группа, являются такими же, как упомянутые выше конкретные примеры заместителя, который может дополнительно иметь алкильная группа, когда любой один из R1-R9 в формуле [1] представляет алкильную группу.
Кроме того, все или часть атомов водорода, присутствующих в главной структуре (это относится к структуре хризена, представленной в общей формуле [1]), или в заместителях в главной структуре соединения хризена, представленного формулой [1], могут быть заменены на дейтерий.
Соединение хризена, представленное формулой [1], предпочтительно является соединением, представленным любой одной из формул [3] и [4].
Необходимо отметить, что заместители Ar1-Ar3 в каждой из формул [3] и [4] являются такими же, как заместители Ar1-Ar3 в формуле [1].
Далее описываются способы синтеза 2,6,12-триарилзамещенного соединения хризена, представленного формулой [3], и 3,6,12-триарилзамещенного соединения хризена, представленного формулой [4], в соответствии с этим вариантом осуществления.
2,6,12-Триарилзамещенное соединение хризена может быть синтезировано при помощи реакции сочетания Сузуки-Мияуры, представленной следующей схемой реакций [5].
А именно синтезируют 2-Cl промежуточное соединение из 6,12-дибром-2-хлорхризена и затем вводят арильную группу с получением 2,6,12-триарилзамещенного соединения хризена.
(На схеме реакций Ar и Ar' представляют заместители, каждый из которых независимо выбран из группы, состоящей из замещенной или незамещенной нафтильной группы, замещенной или незамещенной фенантрильной группы и замещенной или незамещенной флуоренильной группы).
Аналогичным образом может быть синтезировано 3,6,12-триарилзамещенное соединение хризена из 6,12-дибром-3-хлорхризена через 3-Cl промежуточное соединение, как показано на схеме реакций [6].
(На схеме реакций Ar и Ar' представляют заместители, каждый из которых независимо выбран из группы, состоящей из замещенной или незамещенной нафтильной группы, замещенной или незамещенной фенантрильной группы и замещенной или незамещенной флуоренильной группы).
Когда, в каждой из схем реакций [5] и [6], синтезируют Cl промежуточное соединение, в которое вводят требуемую арильную группу в виде Ar, и при последующий реакции сочетания вводят соответствующий заместитель Ar', может быть синтезировано соединение хризена, замещенное с помощью требуемых заместителей Ar и Ar'. В этом случае, в каждой из схем реакций в качестве соединения бороновой кислоты используют соединение бороновой кислоты, соответствующее каждому из требуемых заместителей Ar и Ar'.
Необходимо отметить, что, когда в соединение хризена как окончательно синтезированное вещество вводят алкильную группу или алкоксигруппу, дибромхлорхризен в каждой схеме реакций должен быть только алкилированным или алкоксилированным.
Далее приводятся примеры конкретных структурных формул соединения хризена согласно настоящему изобретению.
Приведенные выше соединения C101-C112 (в дальнейшем в данном описании именуемые как "группа C100"), C501-C520 (в дальнейшем в данном описании именуемые как "группа C500") и C701-C722 (в дальнейшем в данном описании именуемые как "группа C700") являются конкретными примерами 2,6,12-триарильного соединения хризена, представленного общей формулой [3].
Приведенные выше соединения C201-C215 (в дальнейшем в данном описании именуемые как "группа C200"), C601-C615 (в дальнейшем в данном описании именуемые как "группа C600") и C801-C821 (в дальнейшем в данном описании именуемые как "группа C800") являются конкретными примерами 3,6,12-триарильного соединения хризена, представленного общей формулой [4].
Приведенные выше соединения C301-C303 (в дальнейшем в данном описании именуемые как "группа C300") и C401-C403 (в дальнейшем в данном описании именуемые как "группа C400") являются конкретными примерами соединения, в котором по меньшей мере один из R1-R9 в общей формуле [1] представляет заместитель, не являющийся атомом водорода.
В группе C100 соединения C102, C107, C109 и C112 каждое обладает такими же свойствами, как и соединение C101, с точки зрения относительно глубокого энергетического уровня высшей заполненной молекулярной орбитали (HOMO) и высокой способности блокирования дырок при использовании в слое транспорта электронов. Каждое из этих соединений может быть в целом представлено следующей общей формулой [7].
В группе C100 соединения C104, C105, C110 и C111 каждое обладает такими же свойствами, как и соединение C103, с точки зрения относительно неглубокого энергетического уровня высшей заполненной молекулярной орбитали (HOMO) и высокой способности инжекции дырок при использовании в качестве основного материала для эмиссионного слоя. Каждое из этих соединений может быть в целом представлено следующей общей формулой [8].
В группе C200 соединения C205, C208, C209 и C215 каждое обладает такими же свойствами, как и соединение C201, с точки зрения относительно глубокого энергетического уровня высшей заполненной молекулярной орбитали (HOMO) и высокой способности блокирования дырок при использовании в слое транспорта электронов. Каждое из этих соединений может быть в целом представлено следующей общей формулой [9].
В группе C200 соединения C203, C210, C211, C212 и C213 каждое обладает такими же свойствами, как и соединение C202, с точки зрения относительно неглубокого энергетического уровня высшей заполненной молекулярной орбитали (HOMO) и высокой способности инжекции дырок при использовании в качестве основного материала для эмиссионного транспортного слоя. Каждое из этих соединений может быть в целом представлено следующей общей формулой [10]
В группе C500 соединения C506, C507, C510, C511 и C517 каждое обладает такими же свойствами, как и соединение C501. Каждое из этих соединений может быть в целом представлено следующей общей формулой [11]. Эти соединения являются подобными друг другу с точки зрения высокой способности блокирования дырок и высокой способности блокирования экситонов при использовании в слое транспорта электронов ввиду глубокого энергетического уровня высшей заполненной молекулярной орбитали (HOMO) и относительно широкой запрещенной энергетической зоны.
(В формуле [11] Z1-Z7 каждый независимо представляет атом водорода или алкильную группу).
В группе C500 соединение C509 обладает такими же свойствами, как и соединение C505, с точки зрения относительно широкой запрещенной энергетической зоны и высокой способности блокирования экситонов при использовании в слое транспорта электронов. Соединение может быть в целом представлено следующей общей формулой [12].
(В формуле [12] Z8-Z14 каждый независимо представляет атом водорода или алкильную группу).
В группе C700 соединения C702, C704, C705, C708, C709, C710, C711, C712, C713, C720, C721 и C722 каждое обладает такими же свойствами, как и соединение C703. Каждое из этих соединений может быть в целом представлено следующей общей формулой [13].
Эти соединения являются подобными друг другу с точки зрения глубокого энергетического уровня высшей заполненной молекулярной орбитали (HOMO) и широкой запрещенной энергетической зоны, и высокой способности блокирования дырок и высокой способности блокирования экситонов при использовании в слое транспорта электронов.
(В формуле [13] Z1-Z7 каждый независимо представляет атом водорода или алкильную группу).
Необходимо отметить, что заместители Ar1-Ar3 в каждой из формул [8]-[13] являются такими же, как заместители Ar1-Ar3 в формуле [1].
Далее подробно описывается органическое светоизлучающее устройство согласно настоящему изобретению.
Органическое светоизлучающее устройство согласно настоящему изобретению является органическим светоизлучающим устройством, состоящим из пары электродов, образованных анодом и катодом, и слоем органического соединения, установленным между парой электродов, где слой органического соединения содержит органическое соединение, представленное общей формулой [1].
Устройство может иметь между парой электродов слой соединения помимо упомянутого выше слоя органического соединения. Альтернативно, между парой электродов могут быть размещены два или более слоев соединений, включая слой органического соединения, и устройство в этом случае называют многослойным органическим светоизлучающим устройством.
Далее описываются предпочтительные примеры многослойного органического светоизлучающего устройства, а именно примеры от первого до шестого.
Органическое светоизлучающее устройство такой конструкции, в которой на подложку последовательно наносят анод, эмиссионный слой и катод, может быть приведено в качестве первого примера многослойного органического светоизлучающего устройства. Органическое светоизлучающее устройство такой конструкции, в которой на подложку последовательно наносят анод, слой транспорта дырок, слой транспорта электронов и катод, может быть приведено в качестве второго примера многослойного органического светоизлучающего устройства. В этом случае, эмиссионный слой является любым одним из слоя транспорта дырок и слоя транспорта электронов.
Органическое светоизлучающее устройство такой конструкции, в которой на подложку последовательно наносят анод, слой транспорта дырок, эмиссионный слой, слой транспорта электронов и катод, может быть приведено в качестве третьего примера многослойного органического светоизлучающего устройства. Органическое светоизлучающее устройство такой конструкции, в которой на подложку последовательно наносят анод, слой инжекции дырок, слой транспорта дырок, эмиссионный слой, слой транспорта электронов и катод, может быть приведено в качестве четвертого примера многослойного органического светоизлучающего устройства.
Органическое светоизлучающее устройство такой конструкции, в которой на подложку последовательно наносят анод, слой инжекции дырок, слой транспорта дырок, эмиссионный слой, слой транспорта электронов слой инжекции электронов и катод, может быть приведено в качестве пятого примера многослойного органического светоизлучающего устройства. Органическое светоизлучающее устройство такой конструкции, в которой на подложку последовательно наносят анод, слой транспорта дырок, эмиссионный слой, слой блокирования дырок или слой блокирования экситонов, слой транспорта электронов и катод, может быть приведено в качестве шестого примера многослойного органического светоизлучающего устройства.
Однако примеры, от первого до шестого, многослойного органического светоизлучающего устройства иллюстрируют только конструкцию базового устройства, и конструкция органического светоизлучающего устройства согласно настоящему изобретению не ограничивается этими примерами. Могут быть предложены различные конструкции слоев, например конструкция, при которой на контактную поверхность электрода наносят изолирующий слой и наносят органический слой, клеевой слой или интерференционный слой, образуют слой транспорта электронов или слой транспорта дырок из двух слоев с различными потенциалами ионизации, или эмиссионный слой имеет многослойную структуру, образованную из двух или более слоев.
Слой органического соединения в органическом светоизлучающем устройстве согласно настоящему изобретению может содержать один вид соединения хризена согласно настоящему изобретению, или может содержать много видов соединений хризена согласно настоящему изобретению.
В органическом светоизлучающем устройстве согласно настоящему изобретению соединение хризена по настоящему изобретению предпочтительно используют в качестве основного материала для эмиссионного слоя.
В качестве варианта, соединение хризена согласно настоящему изобретению может быть использовано в качестве легирующего материала для эмиссионного слоя.
Более того, соединение хризена согласно настоящему изобретению может быть использовано, помимо эмиссионного слоя, в любом одном из соответствующих слоев, т.е. слое инжекции дырок, слое транспорта дырок, слое блокирования дырок, слое блокирования экситонов, слое транспорта электронов и слое инжекции электронов. Кроме того, соединение хризена согласно настоящему изобретению предпочтительно наносят на слой транспорта электронов.
Органическое светоизлучающее устройство является таким устройством, в котором размещенный между парой электродов эмиссионный материал в виде органического соединения излучает свет. Слой, содержащий эмиссионный материал, является эмиссионным слоем.
Эмиссионный слой может быть образован только из соединения хризена согласно настоящему изобретению, или может частично содержать соединение хризена согласно настоящему изобретению. Если эмиссионный слой частично содержит соединение хризена согласно настоящему изобретению, то соединение хризена может быть эмиссионным материалом в эмиссионном слое, или может быть неэмиссионным материалом в слое.
Если эмиссионный слой образуют из многих типов компонентов, то компоненты могут быть подразделены на основной компонент и субкомпоненты. Термин "основной компонент" относится к соединению, присутствующему в большом количестве, например, по массе или числу молей, в сравнении со всеми соединениями, из которых образован эмиссионный слой, и термин "субкомпонент" относится к соединению, присутствующему в небольшом количестве, выраженном любым таким количественным показателем. Материал, используемый в качестве основного компонента, может быть назван основным материалом. Материалы, используемые в качестве субкомпонентов, могут быть названы легирующим (допирующим) материалом, способствующим эмиссии материалом и инжектирующим заряд материалом. В данном описании легирующим материалом является соединение, которое играет роль главного источника светового излучения внутри эмиссионного слоя. С другой стороны, основной материал является соединением, которое представляет собой матрицу для легирующего материала внутри эмиссионного слоя, и он главным образом выполняет функцию транспортирования носителей заряда и донора энергии возбуждения для легирующего материала.
Концентрация легирующего материала относительно основного материала составляет от 0,01 масс.% до 50 масс.% и предпочтительно от 0,1 масс.% до 20 масс.% в расчете на общее количество составляющих эмиссионный слой материалов. Более предпочтительно, для предотвращения концентрационного гашения, чтобы концентрация легирующего материала составляла, если это требуется, 10 масс.% или менее. Кроме того, легирующий материал может быть введен и равномерно распределен по всему слою, образованному из основного материала, может быть введен в слой с концентрационным градиентом или может быть частично включен в конкретную область с формированием области, образованной слоем основного материала, в которую легирующий материал не вводится.
Далее приводится доказательство того, что соединение хризена согласно настоящему изобретению может использоваться для увеличения срока службы органического светоизлучающего устройства.
Существуют несколько возможных причин ухудшения эмиссионных характеристик органического светоизлучающего устройства, обусловленного электризацией.
Возможные причины включают эмиссию самого по себе материала и причину, относящуюся к изменению внешних условий вокруг эмиссионного материала, обусловленному окружающими материал молекулами. Кроме того, возможные причины включают ухудшение качества аморфной пленки слоя вследствие, например, кристаллизации, так же как и разрушение с течением времени органического слоя вследствие самопроизвольной электризации. Одним из видов разрушения эмиссионного материала является разрушение материала вследствие окисления, и известно, что присутствие оксида в органическом светоизлучающем устройстве укорачивает срок службы устройства.
Соединение антрацена, имеющее антраценовое кольцо в качестве ядра его молекулы, было широко известно в качестве эмиссионного материала для органического светоизлучающего устройства. Углеродные атомы в 9- и 10-положениях антраценового кольца чрезвычайно легко окисляются. В связи с этим, использование соединения антрацена в качестве основного материала для эмиссионного слоя органического светоизлучающего устройства часто сокращает срок службы органического светоизлучающего устройства в результате упомянутого выше разрушения материала вследствие окисления.
Между тем, хризен можно представить как углеводородное ароматическое кольцо с числом углеродных атомов, сопоставимым с числом углеродных атомов в антрацене. В отличие от антраценового кольца, хризеновое кольцо обладает высокой устойчивостью к окислению, и соединение хризена, имеющее хризеновое кольцо в качестве ядра его молекулы, обладает чрезвычайно высокой химической стабильностью. На основании вышеизложенного, авторы настоящего изобретения пришли к выводу, что использование соединения хризена в органическом светоизлучающем устройстве эффективно увеличивает срок службы устройства. Кроме того, авторы настоящего изобретения пришли к выводу, что, в этом случае, для того чтобы соединение хризена обладало химической стабильностью, важно, чтобы на хризеновом кольце присутствовал центр распределения заряда каждой из высшей заполненной молекулярной орбитали (HOMO) и низшей незаполненной молекулярной орбитали (LUMO), тесно связанных с процессом эмиссии. Авторы изобретения обратили внимание на тот факт, что, в отношении ароматического кольцевого заместителя на хризеновом кольце такого соединения хризена, синглетная энергия ароматического кольца должна быть больше, чем синглетная энергия хризена. Причина состоит в том, что, подразделяя молекулы на молекулу в ядре (в основной структуре) и молекулу заместителя, авторы изобретения предполагают, что основную функцию выполняет хризен в качестве ядра, а заместитель только корректирует эту функцию. Если синглетная энергия ароматического кольцевого заместителя хризенового кольца больше, чем синглетная энергия хризена, то поле для рекомбинации носителей заряда или транспортировки носителей заряда, служащее в качестве энергически высокой загрузки в единицах энергии, может сходиться на хризеновом кольце, обладающем высокой химической стабильностью в одной молекуле.
На основании такого подхода сравниваются синглетные энергии хризена и различных ароматических колец.
В таблице 1 ниже приведены типичные ароматические кольца и их синглетные энергии, выраженные через длину волны. Кроме того, в этой таблице также приведена синглетная энергия хризена, выраженная через длину волны. Среди этих ароматических колец, фенильная группа, флуоренильная группа, нафтильная группа и фенантрильная группа каждая имеет более высокую синглетную энергию, чем синглетная энергия хризена. Если соединение хризена имеет любое такое ароматическое кольцо в качестве заместителя, то высшая заполненная молекулярная орбиталь (HOMO) и низшая незаполненная молекулярная орбиталь (LUMO) соединения, имеющего заместитель, локализуются на хризеновом кольце как ядре.
| Таблица 1 | |
| Ароматическое кольцо | Синглетная энергия (выраженная через длину волны) |
| Бензол | 261 нм |
| Флуорен | 301 нм |
| Нафталин | 310 нм |
| Фенантрен | 345 нм |
| Хризен | 361 нм |
| Пирен | 371 нм |
| Антрацен | 376 нм |
| Перилен | 435 нм |
С другой стороны, например, когда ароматической кольцевой группой, являющейся заместителем в хризеновом кольце, является ароматическое кольцо с меньшей синглетной энергией, чем синглетная энергия хризена, такое как пиренильная группа, существует вероятность того, что получаемый хризен не будет обладать химической стабильностью.
Кстати, из фенильной группы, флуоренильной группы, нафтильной группы и фенантрильной группы, предпочтительными заместителями могут быть указанные группы, за исключением фенильной группы, т.е. флуоренильная группа, нафтильная группа и фенантрильная группа.
Даже когда ароматической кольцевой группой, являющейся заместителем в хризеновом кольце, является фенильная группа, центр распределения заряда каждой из высшей заполненной молекулярной орбитали (HOMO) и низшей незаполненной молекулярной орбитали (LUMO) молекулы хризена присутствует на хризеновом кольце, как и в случае каждой из флуоренильной группы, нафтильной группы и фенантрильной группы. Кроме того, в этом случае, запрещенная энергетическая зона молекулы хризена становится очень широкой. Термин "запрещенная энергетическая зона" означает разницу между уровнем заполненной молекулярной орбитали (HOMO) и уровнем низшей незаполненной молекулярной орбитали (LUMO) соединения. Это связано со следующей причиной. Поскольку синглетная энергия фенильной группы является чрезвычайно высокой и фенильная группа имеет меньшую величину π-сопряжения, чем величина π-сопряжения каждой из трех других ароматических кольцевых групп, расширение π-сопряжения соединения хризена в целом является небольшим. Как описано ниже, нежелательно использовать в качестве основного материала для эмиссионного слоя такое соединение хризена, которое имеет чрезвычайно широкую запрещенную энергетическую зону.
Как следует из вышеизложенного, соединение хризена согласно настоящему изобретению имеет заместитель, представленный формулой [2], в хризеновом ядре, представленном общей формулой [1]. В результате достигается химическая стабильность.
Когда в органическом светоизлучающем устройстве, излучающем голубой свет, используют соединение хризена согласно настоящему изобретению в качестве основного материала для его эмиссионного слоя, предпочтительно, чтобы запрещенная энергетическая зона соединения хризена составляла примерно 3,0 эВ или, в частности, 3,0±0,2 эВ, или более предпочтительно от 3,0 эВ до 3,1 эВ.
Это объясняется тем, что различие потенциального барьера для инжекции носителей заряда между HOMO и LUMO эмиссионного слоя и HOMO или LUMO органического слоя, расположенного рядом с эмиссионным слоем, такого как слой транспорта дырок или слой транспорта электронов, должно быть небольшим. Это также связано с тем, что, для того чтобы энергия могла беспрепятственно подводиться к легирующему материалу, необходимо, чтобы основной материал имел более широкую запрещенную энергетическую зону, чем запрещенная энергетическая зона эмиссионного материала, который излучает голубой свет, т.е. легирующего материала.
Соединение хризена согласно настоящему изобретению может быть предпочтительно использовано в качестве основного материала для эмиссионного слоя органического светоизлучающего устройства, излучающего голубой свет, поскольку соединение отвечает требованиям к величине запрещенной энергетической зоны внутри любой такой области числовых значений.
Далее приводится доказательство того, что заместитель, представленный формулой [2], должен быть связан с хризеновым ядром в конкретном положении хризенового ядра. Как описано выше, соединением хризена согласно настоящему изобретению является соединение хризена, имеющее величину запрещенной энергетической зоны, предпочтительной для использования в качестве основного материала для эмиссионного слоя, излучающего голубой свет.
Число положений для замещения в хризеновом кольце показано ниже.
Прежде всего, диарилзамещенное соединение хризена, в котором две ароматические кольцевые группы являются заместителями для хризенового кольца, или конкретно, 6,12-диарильное соединение хризена, имеет широкую запрещенную энергетическую зону. Соответственно, для того чтобы соединение можно было использовать в качестве основного материала для эмиссионного слоя, излучающего голубой свет, соединение необходимо усовершенствовать.
Это связано с тем, что, даже когда каждый из двух ароматических кольцевых заместителей заменяют вместо фенильной группы на флуоренильную группу, нафтильную группу или фенантрильную группу, при которых дополнительно расширяется π-сопряженная поверхность, расширение π-сопряжения соединения хризена в целом является все еще небольшим в случае только этих заместителей. Использование соединения в качестве основного материала для эмиссионного слоя, изучающего голубой свет, увеличивает напряжение, при котором начинает функционировать светоизлучающее устройство, и снижает эффективность эмиссии устройства.
Кроме того, запрещенная энергетическая зона тетраарилзамещенного соединения хризена, в котором четыре ароматические кольцевые группы являются заместителями для хризенового кольца, является небольшой. Это связано со следующей причиной. Так как число ароматических кольцевых заместителей достигает четырех, то расширение π-сопряжения соединения хризена в целом становится чрезмерно большим. Соединение не подходит для использования в качестве основного материала для органического светоизлучающего устройства, излучающего голубой свет. Производное 3,6,9,12-тетраарилзамещенного хризена в патентном документе Japanese Patent Application Laid-Open No. 2007-273055 и производное 2,6,8,12-тетраарилзамещенного хризена в публикации Chem. Commun. 2008, 2319, каждое, в основном используют в качестве легирующего материала для эмиссионного слоя, излучающего голубой свет.
В публикации Chem. Commun. 2008, 2319 сообщается, что органическое светоизлучающее устройство, в эмиссионном слое которого используют только 3,6,9,12-тетракис(4-трет-бутилфенил)хризен, имеет максимум эмиссии при длине волны 450 нм. Исходя из сдвига Стокса для углеводородного ароматического полициклического соединения, которое характеризуется обычной эмиссией света π-π* типа, ожидается, что запрещенная энергетическая зона соединения хризена в виде пленки будет составлять не более чем около 2,95 эВ (420 нм, выраженная через длину волны). Следовательно, можно легко предположить, что, когда любое такое тетраарилзамещенное соединение хризена используют в качестве основного материала для эмиссионного слоя, излучающего голубой свет, передачи энергии возбуждения к легирующему материалу не происходит и в результате снижается эффективность эмиссии. То есть тетраарилзамещенное соединение хризена имеет слишком малое значение запрещенной энергетической зоны для того, что