Инданильные соединения
Иллюстрации
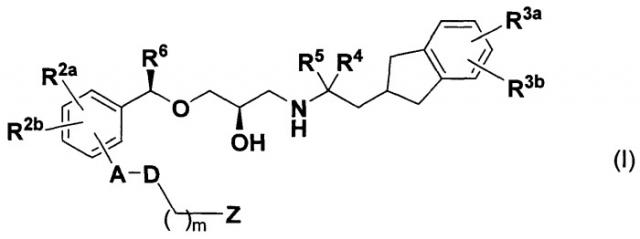
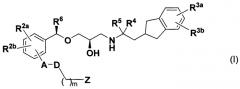
Показать всеИзобретение относится к новым инданильным производным и их фармацевтически приемлемым солям, обладающим активностью антагониста кальциевого рецептора. В формуле (I):
А - одинарная связь или фениленовая группа, которая замещена R1; R1 - метальная группа; D - одинарная связь; R2a и R2b - одинаковые или отличные друг от друга, означают атом водорода, атом фтора, атом хлора, метальную группа, метоксигруппу, этоксигруппу или трифторметильную группу; R3a и R3b - атом водорода; R4 и R5 - метальные группы, или R4 и R5 связаны друг с другом с образованием этиленовой группы; R6 - метильная группа или этильная группа; m - целое число от 0 до 4; Z - карбоксигруппа. Изобретение также относится к фармацевтической композиции, содержащей указанные соединения, к применению указанных соединений для производства лекарственного средства для лечения или предупреждения расстройства, связанного с аномальным костным или минеральным гомеостазом, такого как гипопаратиреоз, остеопороз, и к способу улучшения костного метаболизма. 5 н. и 10 з.п. ф-лы, 78 табл., 85 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к соединению, обладающему антагонистической активностью относительно кальцийчувствительных рецепторов (CaSR, здесь далее обозначены просто как кальциевые рецепторы).
УРОВЕНЬ ТЕХНИКИ
Известно, что кость является динамическим органом, в котором осуществляется восстановление кости посредством непрерывно повторяющегося образования и резорбции ради морфологического изменения самой кости или поддержания концентрации кальция в крови. В нормальной кости существует равновесное соотношение между остеогенезом, осуществляемом остеобластами, и резорбцией кости, осуществляемой остеокластами, что поддерживает массу кости в постоянном состоянии. Однако нарушение равновесного соотношения между остеогенезом и резорбцией костей вызывает метаболические болезни костей, такие как остеопороз (непатентные документы 1 и 2).
Сообщается о многих типах системных гормонов или локальных цитокинов как факторов, регулирующих метаболизм костной ткани, и остеогенез и сохранность костей управляются взаимодействием этих факторов (непатентные документы 1 и 3). Наличие остеопороза широко известно как возрастное изменение костной ткани. Однако так как механизм появления остеопороза включает много аспектов, в том числе пониженную секрецию половых гормонов или вызванную этим патологию рецепторов, изменения экспрессии цитокинов в отдельной кости, экспрессию и дифференциацию генов старения или ослабленную функцию остеокластов или остеобластов и т.д., трудно понять его как простое физиологическое явление, которое происходит при старении. Во-первых, остеопороз подразделяется, главным образом, на постклимактерический остеопороз, результат пониженной секреции эстрогена, и старческий остеопороз, результат старения. Для объяснения механизма появления остеопороза и разработки терапевтического агента для его лечения существенным является прогресс в фундаментальных исследованиях регуляторных механизмов при резорбции и остеогенезе костей.
Остеокласты представляют собой многоядерные клетки, возникающие из гематопоэтических стволовых клеток, и посредством высвобождения хлорид-ионов и ионов водорода на их стороне, прилепленной к кости, они подкисляют щель между клеткой и липкой стороной кости и одновременно секретируют катепсин K, который является кислотной протеазой (непатентный документ 4). В результате происходит разрушение матричного белка кости и фосфата кальция, что дает пополнение кальция в крови.
Концентрация кальция в сыворотке здоровых млекопитающих строго поддерживается около 9-10 мг/дл (примерно 2,5 мМ) (т.е., кальциевый гомеостаз). Паратиреоидный гормон (PTH) представляет собой гормон, который играет ключевую роль в поддержании гомеостаза кальция, и если концентрация Ca2+ в крови снижается, то немедленно активизируется секреция PTH паращитовидными железами. В кости секретированный таким образом PTH пополняет Ca2+ в крови, промотируя резорбцию костей, и в почках он промотирует повторное поглощение Ca2+ в дистальных канальцах, таким образом, функционирование повышенной концентрации Ca2+ в крови.
Так как известно, что PTH может повышать костную массу, когда его вводят периодически человеку или животному, его уже применяют клинически в качестве терапевтического агента для лечения остеопороза. Также согласно тестам на животных сообщается, что и остеогенез, и резорбция бедренной губчатой кости промотируются при непрерывном введении бычьего PTH (1-84) крысе, у которой удалены щитовидная/паращитовидные железы, что впоследствии приводит к фактическому снижению костной массы. Однако в результате периодического подкожного его введения не происходит промотирования резорбции костей, а только промотирование остеогенеза, что приводит к увеличению костной массы (непатентный документ 5). Дополнительно, если периодически вводить крысе человеческий PTH (1-34) в течение 15 недель через 4 недели после овариэктомии, то наблюдают промотирование остеогенеза и ингибирование резорбции костей в течение периода с 5-10 неделю после начала введения, демонстрирующие примерно двукратное увеличение костной массы по сравнению с имитационной рабочей группой (непатентный документ 6). В этом отчете предполагается, что PTH не только предупреждает снижение костной массы на модели остеопороза, но также имеет эффект восстановления костной массы даже у животных, уже страдающих от заметного уменьшения костной массы.
Хотя PTH-препараты являются терапевтическими агентами для лечения остеопороза, которые демонстрируют подтверждаемый существенный эффект уменьшения степеней переломов костей согласно клиническим тестам у пациентов, страдающих от постклимактерического остеопороза, будучи биологическими препаратами, они также имеют недостатки. Конкретно, в качестве способа введения следует применять инъекцию, и поэтому существует проблема, что пациент может испытывать связанную с этим боль. Таким образом, ожидается разработка фармацевтического препарата, который периодически повышает концентрацию PTH в крови и может вводиться перорально.
Кальциевый рецептор представляет собой G-белок, связанный с рецептором, который экспрессируется, главным образом, в клетках паращитовидных желез, и он регулирует секрецию PTH, чувствуя концентрацию Ca2+ в крови (непатентный документ 7). Человеческий кальциевый рецептор состоит из 1078 аминокислот, и сообщается, что человеческий кальциевый рецептор экспрессируется в почках, С-клетках щитовидной железы, головном мозге, клетках костного мозга и др., а также в паращитовидной железе. Кальциевый рецептор, как лиганд, связывая Ca2+, активирует фосфолипазу С посредством связывания с G-белком, вызывает производство инозиттрифосфата и повышение концентрации внутриклеточного Ca2+ и, как результат, подавляет секрецию PTH (непатентный документ 8). Таким образом, ожидается, что фармацевтический агент, который ингибирует активацию кальциевого рецептора, т.е. фармацевтический агент, который является антагонистом кальциевого рецептора, будет промотировать секрецию PTH из клеток паращитовидных желез и повышать концентрацию PTH в крови живого организма. В этом отношении, если повышение концентрации PTH в крови является скорее кратковременным, чем постоянным, ожидается получение такого же эффекта повышения костной массы, как эффект, обеспечиваемый при периодическом введении PTH.
Между тем, соединения, раскрытые в патентном документе 1, известны как соединения, содержащие инданильную группу. Однако хотя они аналогичны соединениям по изобретению, так как они включают инданильную группу, структура другого конца и др. отличается.
СПИСОК ЛИТЕРАТУРЫ
НЕПАТЕНТНЫЕ ДОКУМЕНТЫ
Непатентный документ 1: Endocrinological Review, (1992) 13, p 66-80.
Непатентный документ 2: Principles of Bone Biology, Academic Press, New York, (1996) p 87-102.
Непатентный документ 3: Endocrinological Review, (1996) 17, р 308-332
Непатентный документ 4: American Journal of Physiology, (1991) 260, C1315-C1324.
Непатентный документ 5: Endocrinology, 1982, 110, 506-512.
Непатентный документ 6: Endocrinology, 1993, 132, 823-831.
Непатентный документ 7: Brown, E. M., «Homeostatic mechanisms regulating extracellular and intracellular calcium metabolism in the parathyroids», (US), Raven press, 1994, 19.
Непатентный документ 8: Nature, 1993, 366, 575-580.
ПАТЕНТНЫЕ ДОКУМЕНТЫ
Патентный документ 1: WO2004/047751 (US 2006058391)
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
ЗАДАЧИ, РЕШАЕМЫЕ ИЗОБРЕТЕНИЕМ
Задачей изобретения является обеспечение новых низкомолекулярных соединений, которые демонстрируют антагонистическую активность относительно кальциевого рецептора, являются высокобезопасными и которые можно вводить перорально.
СРЕДСТВА РЕШЕНИЯ ЗАДАЧ
Фармацевтический препарат, который ингибирует активацию кальциевого рецептора, т.е. фармацевтический препарат, который является антагонистом кальциевого рецептора, промотирует секрецию PTH клетками паращитовидных желез, вызывая, таким образом, повышение концентрации PTH в крови живых организмов. В этом отношении, если повышение концентрации PTH в крови является скорее кратковременным, чем постоянным, то ожидается получение такого же эффекта увеличения костной массы, как эффект, обеспечиваемый периодическим введением PTH.
Инданильные соединения по изобретению представляют собой соединения, обладающие антагонистической активностью относительно кальциевых рецепторов. Выражение «обладающие антагонистической активностью относительно кальциевых рецепторов» означает, что происходит ингибирование одной или более активностей кальциевых рецепторов, которые индуцируются внеклеточным Ca2+.
Конкретно, изобретение относится к следующему.
(1) Соединение, представленное следующей далее формулой (I) или его фармацевтически приемлемая соль.
[в формуле каждая замещающая группа определена следующим образом:
А: одинарная связь, С1-С6 алкиленовая группа или фениленовая группа, которая может быть замещена R1;
R1: атом галогена, цианогруппа, С1-С6 алкильная группа, С1-С6 алкоксигруппа, галогенированная С1-С6 алкильная группа, или галогенированная С1-С6 алкоксигруппа;
D: одинарная связь, атом кислорода или атом серы;
R2a и R2b: одинаковые или отличные друг от друга, атом водорода, атом галогена, цианогруппа, С1-С6 алкильная группа, С1-С6 алкоксигруппа, галогенированная С1-С6 алкильная группа, или галогенированная С1-С6 алкоксигруппа;
R3a и R3b: одинаковые или отличные друг от друга, атом водорода, атом галогена, цианогруппа, С1-С6 алкильная группа, С1-С6 алкоксигруппа, галогенированная С1-С6 алкильная группа или галогенированная С1-С6 алкоксигруппа;
R4 и R5: одинаковые или отличные друг от друга, атом водорода, атом галогена или С1-С6 алкильная группа, или R4 и R5 связаны друг с другом с образованием С2-С6 алкиленовой группы;
R6: атом галогена, цианогруппа, С1-С6 алкильная группа, С1-C6 алкоксигруппа, галогенированная С1-С6 алкильная группа или галогенированная C1-С6 алкоксигруппа;
m: целое число от 0 до 6;
Z: карбоксигруппа или группа, эквивалентная карбоксигруппе (-SO 2NHRz, тетразолильная группа или подобные);
Rz: атом водорода или С1-С6 алкильная группа].
Предпочтительные варианты изобретения включают следующие.
(2) Соединение, описанное в (1), или его фармацевтически приемлемая соль, где R1 представляет собой атом водорода или метильную группу.
(3) Соединение, описанное в (1) или (2), или его фармацевтически приемлемая соль, где R2a и R2b, которые являются одинаковыми или отличаются друг от друга и представляют собой атом водорода, атом фтора, атом хлора, цианогруппу, метильную группу, метоксигруппу, этоксигруппу, трифторметильную группу или трифторметоксигруппу.
(4) Соединение, описанное выше в любом из пунктов (1)-(3), или его фармацевтически приемлемая соль, где R3a и R3b, одинаковые или отличные друг от друга, представляют собой атом водорода, атом фтора, атом хлора, цианогруппу, метильную группу, метоксигруппу, этоксигруппу, трифторметильную группу или трифторметоксигруппу.
(5) Соединение, описанное в любом из пунктов (1)-(4), или его фармацевтически приемлемая соль, где R4 и R5 представляют собой метильные группы.
(6) Соединение, описанное в любом из пунктов (1)-(4), или его фармацевтически приемлемая соль, где R4 и R5 представляют собой этиленовую группу.
(7) Соединение, описанное в любом из пунктов (1)-(6), или его фармацевтически приемлемая соль, где m равно 0 или 1.
(8) Соединение, описанное в любом из пунктов (1)-(6), или его фармацевтически приемлемая соль, где m равно от 2 до 4.
(9) Соединение, описанное в любом из пунктов (1)-(8), или его фармацевтически приемлемая соль, где A обозначает одинарную связь.
(10) Соединение, описанное в любом из пунктов (1)-(9), или его фармацевтически приемлемая соль, где D обозначает одинарную связь.
(11) Соединение, описанное в любом из пунктов (1)-(10), или его фармацевтически приемлемая соль, где Z обозначает карбоксигруппу.
(12) Соединение, описанное в любом из пунктов (1)-(11), или его фармацевтически приемлемая соль, где R6 представляет собой метильную группу или этильную группу.
(13) Соединение, выбранное из следующей группы соединений или их фармацевтически приемлемых солей:
{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]фенил}пропановая кислота,
{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]фенил}бутановая кислота,
2'-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-3-метилбифенил-4-карбоновая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-6-метилфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-5-метилфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-4-метилфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-6-фторфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-5-фторфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-4-фторфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-6-(трифторметил)фенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-5-(трифторметил)фенил}пропановая кислота,
2'-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-илметил)циклопропил]амино}-2-гидроксипропил]окси}этил]-3-метилбифенил-4-карбоновая кислота,
5-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]фенил}пентановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-илметил)циклопропил]амино}-2-
гидроксипропил]окси}этил]фенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-6-метилфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-5-фторфенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]-6-фторфенил}пропановая кислота,
3-{2-хлор-6-[(1R)-1-{[(2R)-3-{[1-(2,3-дигидро-1H-инден-2-ил)-2-метилпропан-2-ил]амино}-2-гидроксипропил]окси}этил]фенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[2-(2,3-дигидро-1H-инден-2-ил)-1,1-диметилэтил]амино}-2-гидроксипропил]оксилпропил]-6-метоксифенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[2-(2,3-дигидро-1H-инден-2-ил)-1,1-диметилэтил]амино}-2-гидроксипропил]оксилэтил]-6-этоксифенил}пропановая кислота,
3-{2-[(1R)-1-{[(2R)-3-{[2-(2,3-дигидро-1H-инден-2-ил)-1,1-диметилэтил]амино}-2-гидроксипропил]окси}этил]-4-фтор-6-метоксифенил}пропановая кислота.
(14) Соединение, описанное в любом из пунктов (1)-(13), или его фармацевтически приемлемая соль для применения в качестве антагониста кальциевого рецептора.
(15) Фармацевтическая композиция, которая содержит соединение, описанное в любом из пунктов (1)-(13), или его фармацевтически приемлемую соль в качестве эффективного компонента.
(16) Фармацевтическая композиция, описанная выше в (15), для применения в качестве антагониста кальциевого рецептора.
(17) Фармацевтическая композиция, описанная выше в (15), для применения для лечения или предупреждения расстройства, связанного с аномальным костным или минеральным гомеостазом.
(18) Фармацевтическая композиция, описанная выше в (17), где расстройство, связанное с аномальным костным или минеральным гомеостазом, является гипопаратиреозом; остеосаркомой; периодонтитом; срастанием переломов костей; деформационным артритом; ревматоидным артритом; болезнью Педжета; синдромом гуморальной гиперкальциемии, связанным со злокачественной опухолью и срастанием переломов костей; или остеопорозом.
(19) Фармацевтическая композиция, описанная выше в (17), где расстройство, связанное с аномальным костным или минеральным гомеостазом, является остеопорозом.
(20) Способ улучшения костного метаболизма, который характеризуется тем, что эффективное количество фармацевтической композиции, описанной выше в (15), вводят млекопитающему.
(21) Способ предупреждения или лечения остеопороза, который характеризуется тем, что эффективное количество фармацевтической композиции, описанной выше в (15), вводят млекопитающему.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
Соединения по изобретению или их фармацевтически приемлемые соли пригодны для лечения или профилактики расстройства, связанного с аномальным костным или минеральным гомеостазом, например, гипопаратиреоза, остеосаркомы, периодонтита, срастания переломов костей, деформационного артрита, ревматоидного артрита, болезни Педжета, синдрома гуморальной гиперкальциемии, связанного со злокачественной опухолью и срастанием переломов костей, и остеопороза.
НАИЛУЧШИЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Изобретение будет объяснено далее ниже.
Предпочтительные примеры соединений, имеющих формулу (I), включают соединения, имеющие следующую комбинацию замещающих групп:
A и D обозначают одинарную связь,
R2a и R2b одинаковые или отличные друг от друга, представляют собой атом водорода, атом фтора, атом хлора, цианогруппу, метильную группу, метоксигруппу, трифторметильную группу или трифторметоксигруппу,
R3a и R3b, одинаковые или отличные друг от друга, представляют собой атом водорода, атом фтора, атом хлора, цианогруппу, метильную группу, метоксигруппу, этоксигруппу, трифторметильную группу или трифторметоксигруппу,
R4 и R5 обозначают метильную группу или этиленовую группу,
R6 обозначает метильную группу или этильную группу,
Z обозначает карбоксигруппу, и
m равно от 2 до 4.
Более предпочтительные примеры соединений, имеющих формулу (I), включают соединения, описанные в примерах.
«Атом галогена» относится, например, к атому фтора, атому хлора, атому брома или атому йода и предпочтительно к атому фтора или атому хлора.
«C1-C6 алкильная группа» относится к линейной или разветвленной алкильной группе, имеющей от 1 до 6 атомов углерода, и предпочтительно обозначает метильную группу, этильную группу, пропильную группу, изопропильную группу или трет-бутильную группу, более предпочтительно метильную группу.
«C1-C6 алкоксигруппа» относится к группе, в которой атом кислорода связан с указанной выше «C1-C6 алкильной группой», и предпочтительно обозначает метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу или трет-бутоксигруппу, более предпочтительно метоксигруппу.
«C1-C6 галогенированная алкильная группа» относится к группе, в которой атом галогена является заместителем на указанной выше «C1-C6 алкильной группе». Их примеры включают фторметильную группу, дифторметильную группу, трифторметильную группу, фторэтильную группу, дифторэтильную группу и трифторэтильную группу и предпочтительно трифторметильную группу.
«C1-C6 галогенированная алкоксигруппа» относится к группе, в которой атом галогена является заместителем на указанной выше «C1-C6 алкоксигруппе». Их примеры включают фторметоксигруппу, дифторметоксигруппу, трифторметоксигруппу, фторэтоксигруппу, дифторэтоксигруппу и трифторэтоксигруппу и предпочтительно трифторметоксигруппу.
«С2-С6 алкиленовая группа» относится к линейной или разветвленной алкиленовой группе, имеющей от 2 до 6 атомов углерода, и предпочтительно обозначает этиленовую группу или пропиленовую группу и более предпочтительно этиленовую группу.
«Лечение» обозначает лечение или улучшение при расстройстве, или улучшение симптома, или ингибирование симптома.
«Его фармацевтически приемлемая соль» относится к соли, которую можно применять в качестве фармацевтического агента. Соединение по изобретению можно преобразовать в соль основания или соль кислоты посредством его взаимодействия с основанием или кислотой, если соединение имеет кислотную группу или основную группу, и эти соли обозначаются соответственно.
Примеры фармацевтически приемлемой «соли основания» и соединения по изобретению предпочтительно включают соли щелочных металлов, такие как соль натрия, соль калия и соль лития; соли щелочноземельных металлов, такие как соль магния и соль кальция; соли органических оснований, такие как соль N-метилморфолина, соль триэтиламина, соль трибутиламина, соль диизопропилэтиламина, соль дициклогексиламина, соль N-метилпиперидина, соль пиридина, соль 4-пирролидинопиридина и соль пиколина, или соли аминокислот, такие как соль глицина, соль лизина, соль аргинина, соль орнитина, соль глутаминовой кислоты и соль аспарагиновой кислоты. Предпочтительной является соль щелочного металла.
Предпочтительные примеры фармацевтически приемлемой «соли кислоты» и соединения по изобретению включают соли галогенводородной кислоты, такие как соль фтористого водорода, соль хлористого водорода, соль бромистого водорода и соль йодистого водорода, соли неорганических кислот, такие как нитрат, перхлорат, сульфат или фосфат; соли низших алкансульфонатов, такие как метансульфонат, трифторметансульфонат или этансульфонат, соли арилсульфонатов, такие как бензолсульфонат или пара-толуолсульфонат; соли органических кислот, такие как ацетат, малат, фумарат, сукцинат, цитрат, аскорбат, тартрат, оксалат или малеат; и соли аминокислот, такие как соль глицина, соль лизина, соль аргинина, соль орнитина, соль глутаминовой кислоты и соль аспарагиновой кислоты. Наиболее предпочтительна соль хлористо-водородной кислоты.
Соединение или его фармацевтически приемлемая соль по изобретению может дополнительно содержать абсорбционную воду или образовать гидрат, образующийся посредством включения молекул воды при стоянии в атмосфере или при перекристаллизации, и такие гидраты, а также сольваты и кристаллические полиморфы также включены в изобретение. Соединение, его соль или сольват соединения или соли по изобретению могут иметь различные изомеры, такие как геометрический изомер, например, цис-форму и транс-форму, или оптический изомер, например, таутомер, или d-форму и l-форму, и др. в зависимости от типа и комбинации замещающих групп. Пока нет конкретного ограничения, соединения по изобретению включают все изомеры, стереоизомеры и смеси изомеров и стереоизомеров в любом соотношении. Смеси изомеров можно разделить способами разделения, которые хорошо известны в данной области.
Соединение по изобретению включает меченые соединения, т.е. соединения, в которых один или более атомов соединения по изобретению замещены изотопом (например, 2H, 3H, 13C, 14C и 35S и т.д.).
Изобретение включает фармацевтически приемлемые пролекарственные соединения по изобретению. Под фармацевтически приемлемым пролекарством понимают соединение, имеющее группу, которую можно преобразовать в аминогруппу, гидроксигруппу или карбоксигруппу и другие группы соединения по изобретению посредством гидролиза или в физиологических условиях. Примеры групп, которые образуют такие пролекарства, включают группы, описанные в работе Prog. Med., Vol. 5, pages 2157-2161, 1985 или «Development of Drugs», Molecular Design (Hirokawa Shoten, 1990), Vol. 7, pages 163-198. Если в соединении по изобретению присутствует аминогруппа, конкретные примеры пролекарств включают соединение, в котором аминогруппа ацилирована, алкилирована или фосфорилирована (например, соединение, в котором аминогруппа эйкозаноилирована, аланилирована или пентиламинокарбонилирована, (5-метил-2-оксо-1,3-диоксолен-4-ил)метоксикарбонилирована, тетрагидрофуранилирована, пирролидилметилирована, пивалоилоксиметилирована или трет-бутилирована и др.) и др. Если в соединении по изобретению присутствует гидроксигруппа, примеры включают соединение, в котором гидроксигруппа ацилирована, алкилирована, фосфорилирована или борирована (например, соединение, в котором гидроксигруппа ацетилирована, пальмитоилирована, пропаноилирована, пивалоилирована, сукцинилирована, фумарилирована, аланилирована или диметиламинометилкарбонилирована и т.д.) и др. Кроме того, если в соединении по изобретению присутствует карбоксигруппа, примеры включают соединение, в котором карбоксигруппа этерифицирована или амидирована (например, соединение, в котором карбоксигруппа этилэтерифицирована, фенилэтерифицирована, карбоксиметилэтерифицирована, диметиламинометилэтерифицирована, пивалоилоксиметилэтерифицирована, этоксикарбонилоксиэтилэтерифицирована, амидирована или метиламидирована и т.д.) и др.
Дополниетльно, изобретение включает соединения, в которых функциональная группа соединения по изобретению замещена так называемой эквивалентной группой. Примеры так называемых эквивалентных групп включают группы, описанные, например, в работе The Practice of Medicinal Chemistry (Camille Georges Wermuth, Academic Press, 1996). В частности, группы, эквивалентные карбоксигруппе, описаны на страницах 215-217 работы The Practice of Medicinal Chemistry.
(Способ получения)
Соединение по изобретению можно получить, используя различные хорошо известные способы синтеза согласно характеристикам, которые базируются на основном каркасе или типе замещающих групп соединения. Примеры хорошо известных способов включают способы, описанные в работе «ORGANIC FUNCTIONAL GROUP PREPARATIONS», 2nd edition, ACADEMIC PRESS, INC., 1989 или «Comprehensive Organic Transformations», VCH Publishers Inc., 1989.
В таком случае в зависимости от типа функциональной группы может быть эффективно с точки зрения технологии производства защитить функциональную группу подходящей защитной группой на стадии перехода от исходного вещества к промежуточному продукту или заместить функциональную группу группой, которая легко преобразуется.
Примеры функциональных групп включают аминогруппу, гидроксигруппу, карбоксигруппу и др., и защитные группы для них включают группы, описанные в «Protective groups in Organic Synthesis», авторы T. W. Greene и P.G. Wuts, 3rd edition, (1999). В зависимости от реакционных условий их можно выбрать и применять подходящим образом. Согласно этим способам вводят защитную группу, проводят взаимодействие и, если необходимо, защитную группу удаляют или преобразуют в требуемую группу, получая требуемое соединение.
Кроме того, пролекарство из соединения по изобретению можно получить, вводя определенную группу на стадии преобразования исходного вещества в промежуточный продукт аналогично введению описанной выше защитной группы или проводя взаимодействие с использованием полученного соединения по изобретению. Можно проводить взаимодействие, используя способы, хорошо известные специалистам в данной области, основанные на обычной этерификации, амидировании, дегидратации, гидрировании и др.
Здесь далее будут объяснены способы получения соединений по изобретению. Однако способ получения не ограничен следующими способами.
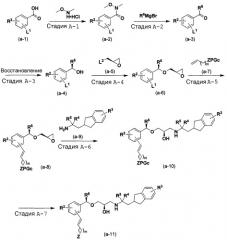
Способ А
[в формуле R2 и R3 каждый имеет такие же значения, как R2a или R2b и R3a или R3b,
R4, R5, Z и m имеют такие же значения, как указанные выше, R6 представляет собой C1-C6 алкильную группу,
L1 и L2 представляют собой уходящую группу для реакции замещения, и
PGc представляет собой защитную группу для карбоксигруппы или группы, эквивалентной карбоксигруппе].
Стадия A-1:
Эта стадия представляет способ получения соединения (a-2) с использованием соединения (a-1), т.е. замещенной бензойной кислоты, и соли N,O-диметилгидроксиламин гидрохлорида, и его можно получить согласно способу, описанному в Tetrahedron 1999, 55, 13159-13170, Kunishima и др.
Стадия A-2:
Эта стадия является стадией получения соединения (a-3), т.е. кетона, с использованием соединения (a-2) и реагента Гриньяра.
Стадия A-3:
Эта стадия является стадией преобразования соединения (a-3) в соединение (a-4) посредством восстановления кетона.
Стадия A-4:
Эта стадия является стадией получения соединения (a-6) при связывании соединения (a-4) с соединением (a-5).
Стадии A-2-A-4 можно осуществить согласно способу, описанному на странице 40, International Publication Pamphlet No. WO 02/14259. Более конкретно, стадию A-2 можно осуществить согласно стадии 2 примера 23, которая описана на странице 49 WO 02/14259. Стадию A-3 можно осуществить согласно стадии 1 примера 21, которая описана на странице 66 WO 02/14259. Стадию A-4 можно осуществить согласно стадии 2 примера 1, которая описана на странице 50, WO 02/14259.
Стадия A-5:
Эта стадия является стадией получения соединения (a-8) по реакции сочетания между соединением (a-6) и соединением (a-7).
Стадия A-6:
Эта стадия является стадией получения соединения (a-10) по реакции сочетания между соединением (a-8) и соединением (a-9).
Стадия A-7:
Эта стадия является стадией получения соединения (a-11) посредством удаления защитной группы соединения (a-10).
Стадии A-5-A-7 можно осуществить согласно примеру взаимодействия, который описан в WO 04/106280 на странице 61. Более конкретно, стадию A-5 можно осуществить на основании стадии 2 примера 1, который описан в WO 04/106280 на странице 67. Стадию A-6 можно осуществить согласно стадии 4 примера 1, который описан в WO 04/106280 на странице 68. Стадию A-7 можно осуществить согласно стадии 5 примера 1, который описан в WO 04/106280 на странице 68.
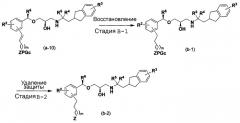
Способ B
[в формуле R2, R3, R4, R5, R6, Z, PGc и m имеют такие же значения, как указанные выше].
Стадия В-1:
Эта стадия является стадией получения соединения (В-1) восстановлением соединения (а-10).
Стадия В-2
Эта стадия является стадией получения соединения (b-2) посредством удаления защитной группы соединения (В-1).
Стадию В-1 можно осуществить согласно примеру 2, показанному в WO 2005/07788 6 на странице 16. Стадию В-2 можно осуществить аналогично стадии А-7, описанной выше.
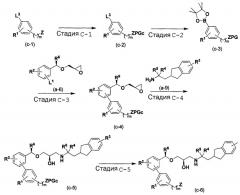
Способ С
[в формуле R1, R2, R3, R4, R5, R6, Z, L1, PGc и m имеют такие же значения, как указанные выше, и L3 представляет собой уходящую группу для реакции замещения].
Стадия C-1:
Эта стадия является стадией защиты карбокислотной группы соединения (c-1) или его эквивалентной группы при помощи защитной группы.
Стадия C-2:
Эта стадия является стадией получения соединения (c-3), то есть борного эфира, посредством реакции присоединения.
Стадия C-3:
Эта стадия является стадией получения соединения (c-4) по реакции сочетания между соединением (c-3) и соединением (a-6) с использованием катализатора.
Стадия C-4:
Эта стадия является стадией получения соединения (c-5) по реакции сочетания между соединением (c-4) и соединением (a-9) через реакцию замещения на эпоксиде.
Стадия C-5:
Эта стадия является стадией получения соединения (c-6) посредством удаления защитной группы соединения (c-5).
Стадии C-1-C-5 можно осуществить согласно примеру взаимодействия, показанному в WO 2004/094362 на странице 77. Более конкретно, стадию C-1 можно осуществить согласно стадии 2 примера 1-1, который описан в WO 2004/094362 на странице 99. Стадию C-2 и стадию C-3 можно осуществить согласно стадии 3 примера 1-1, который описан в WO 2004/094362 на странице 100. Стадию C-4 можно осуществить согласно стадии 8 примера 1-1, который описан в WO 2004/094362 на странице 103. Стадию C-5 можно осуществить согласно стадии 9 примера 1-1, который описан в WO 2004/094362 на странице 103.
Соединение (a-9) можно получить согласно примеру взаимодействия и примеру 1 из WO 01/53254, которые описаны на страницах 15 и 23, соответственно.
Соединение (d-2) можно получить согласно следующему способу D.
Способ D
[в формуле R3 имеет такое же значение, как указанное выше].
Стадия D-1:
Ее можно осуществить согласно способу, описанному в J. Org. Chem. 2002, 67, 3965-3968, используя соединение (d-1), раскрытое в WO 98/05651.
Способ E
[в формуле R2, R3, R4, R5, R6, Z, L1, PGc и m имеют такие же значения, как указанные выше].
Способ E является способом получения соединения (b-2) по изобретению, аналогичный способу B.
Стадия E-1:
Эта стадия является стадией получения соединения (e-1) из соединения (a-8) посредством проведения реакции восстановления аналогично стадии B-1.
Стадия E-2:
Эта стадия является стадией получения соединения (b-1) посредством проведения реакции сочетания аналогично стадии A-6.
Стадия E-3:
Эта стадия является стадией получения соединения (b-2) посредством проведения реакции по удалению защитной группы аналогично стадии B-2.
Способ F является способом получения соединения (a-3)', которое представляет собой промежуточный продукт для соединений по изобретению.
Способ F
[в формуле R6 и L1 имеют такие же значения, как указанные выше, R2' представляет собой C1-C6 алкильную группу или галогенированная C1-C6 алкильную группу, и PGh представляет собой защитную группу для гидроксигруппы].
Стадия F-1:
Эта стадия является стадией получения соединения (f-2) посредством удаления защитной группы для гидроксигруппы соединения (f-1).
Стадия F-2:
Эта стадия является стадией получения соединения (a-3)' при взаимодействии гидроксигруппы соединения (f-2) с алкилирующим реагентом.
Способ G является способом получения соединения (a-1), которое представляет собой промежуточный продукт при получении соединения по изобретению.
Способ G
[в формуле R2, L1 и PGc имеют такие же значения, как указанные выше, и X представляет собой галогеновую группу].
Стадия G-1:
Эта стадия является стадией получения соединения (g-2) посредством проведения реакции включения CO в соединение (g-1) в присутствии палладиевого катализатора.
Стадия G-2:
Эта стадия является стадией получения соединения (g-3) посредством преобразования аминогруппы соединения (g-2) в уходящую группу.
Стадия G-3:
Эта стадия является стадией получения соединения (a-1) посредством удаления защитной группы для карбоксигруппы соединения (g-3).
Способ H является способом получения соединения (a-3)'', которое представляет собой промежуточный продукт при получении соединения по изобретению.
Способ H
[в формуле R2 и L1 имеют такие же значения, как указанные выше].
Стадия H-1:
Эта стадия является стадией получения соединения (h-2) посредством взаимодействия соединения (h-1) с оловоорганическим соединением в присутствии палладиевого катализатора.
Стадия H-2:
Эта стадия является стадией получения соединения (c-3)'' посредством проведения взаимодействия, аналогичного взаимодействию на описанной выше стадии G-2.
Способ I является способом получения соединения (c-3), которое представляет собой промежуточный продукт при получении соединения по изобретению.
Способ I
[в формуле R2, R6 и L1 имеют такие же значения, как указанные выше].
Стадия I-1:
Эта стадия является стадией получения соединения (i-1) посредством восстановления карбоксигруппы соединения (a-1).
Стадия I-2:
Эта стадия является стадией получения соединения (i-2) посредством окисления гидроксигруппы соединения (i-1) до альдегида.
Стадия I-3:
Эта стадия является стадией получения соединения (i-3) посредством взаимодействия соединения (i-2) с реагентом Гриньяра.
Стадия I-4:
Эта стадия является стадией получения соединения (a-3) посредством окисления гидроксигруппы соединения (i-3) до кетона.
Способ J является способом получения соединения (a-4)', которое представляет собой промежуточный продукт при получении соединения по изобретению.
Способ J
[в формуле R2 и L1 имеют такие же значения, как указанные выше].
Стадия J-1:
Эта стадия является стадией получения соединения (a-4)' посредством взаимодействия альдегидной группы соединения (i-2) с цинкорганическим реагентом.
Способ К