Противовирусное средство на основе штамма нематофагового гриба duddingtonia flagrans f-882
Иллюстрации
Показать всеИзобретение относится к противовирусным средствам и может быть использовано в медицине, ветеринарии, вирусологии и фармакологии. Противовирусное средство представляет собой водный экстракт из штамма нематофагового гриба Duddingtonia flagrans F-882, полученный экстракцией биомассы гриба водой при соотношении биомасса:вода 1:5, с последующим удалением нерастворимого осадка. Средство обладает высокой активностью против вируса иммунодефицита человека первого типа, вирусов гриппа человека и птиц типа А и вируса осповакцины. Индекс нейтрализации вируса гриппа человека А в культуре клеток MDCK составляет 3,5 lg. A вируса гриппа птиц А - 2,5-3,0 lg. Вируснейтрализующее действие средства в отношении вируса осповакцины на клетках Vero составляет 25-50% клеток. При внесении средства в концентрации 25 мкг/мл в клетки МТ-4 одновременно с адсорбцией вируса подавление репродукции ВИЧ-1 либо в концентрации 12,5 мкг/мл после адсорбции в клетках составляет 100%. 1 з.п. ф-лы, 6 табл., 5 пр.
Реферат
Изобретение относится к противовирусным средствам, в частности к ингибиторам репродукции вирусов человека и животным, и может быть использовано в медицине, ветеринарии, вирусологии и фармакологии.
Вирусы, поражающие человека и животных, наносят серьезный урон здоровью населения, птице и другим животным. Вирусы иммунодефицита человека и гриппа являются социально значимыми и опасными для здоровья человека.
Известен штамм Duddingtonia flagrans T-89, зарегистрированный в Коллекции культур микроорганизмов ГНЦ ВБ "Вектор" под номером F-882 (патент РФ 2253671, МПК C12N 1/14, опубл. 10.06.2005 г.), проявляющий свойства против галловых нематод растений и паразитических нематод животных и стимулирующий рост и развитие растений, а также препаративные формы на основе его хламидоспор (патент РФ №2366178, МПК А01N 63/04, опубл. 10.09.2009 г.). Штамм обладает высокими показателями стимуляции роста, развития растений и проявлением нематофагового эффекта. Проведенные исследования со штаммом хищного гриба Duddingtonia flagrans F-882 показали, что он способен продуцировать нематициды, растворимые в метил-трет-бутиловом эфире, обездвиживающие нематод видов Steinernema carpocarsae и Panagrellus redivivus.
Однако из известных источников научно-технической и патентной информации не известна противовирусная активность хищного гриба Duddingtonia flagrans, в том числе и штамма F-882.
Anderson и др. (Anderson MG, Rickards RW, Lacey E. 1999. Structures of flagranones А, В and C, cyclohexenoxide antibiotics from the nematode-trapping fungus Duddingtonia flagrans. J Antibiot (Tokyo). 52(11):1023-1028) идентифицировали новые метаболиты в поверхностной культуре Duddingtonia flagrans - флагрононы А, В и С, структурно родственные фарнезилированным циклогексеноксидам группы олигоспорона (famesylated cyclohexenoxides of the oligosporon group). Флагрононы А и В имели антибактериальную и фунгицидную активность, подобную группе олигоспоронов, но не проявляли существенной нематицидной активности. Исследования антибактериальной активности глубинной культуры штамма D.flagrans F-882 выявили явно выраженную антибиотическую активность по отношению к Bacillus subtilis и менее выраженное ингибирование роста Pseudomonas putida, Staphylococcus aureus и Salmonella thyphimurium.
Как указывалось выше, данных по противовирусной активности нематофаговых грибов авторами не найдено. Однако есть данные по другим грибам, не относящимся к микромицетам, таким как нематофаговый гриб Duddingtonia flagrans.
При анализе антивирусной активности экстракта базидиального Ganoderma pfeifferi против вируса гриппа типа А и вируса простого герпеса 1 типа было установлено, что основным антивирусным компонентом экстракта были тритерпеноиды: ганодермадиол, луцидодиол, апланоксиновая кислота G (Mothana R.A.A., Awadh Ali N.A., Jansen R., Wegner U., Mentel R., Lindequist U. Antiviral lanostanoid triterpenes from the fungus Ganoderma preifferi // Fitoterapia. - 74 (2003). - P.177-180).
Вещества хиспидин и хисполон, имеющие изопреноидную природу и найденные в этанольном экстракте гриба Inonotus hispidus, проявляли антивирусную активность против вируса гриппа типа А и типа В. Антивирусную активность проявляли как экстракты плодовых тел, так и мицелиальные экстракты [Ali N.A.A., Jansen R., Pilgrim H., Liberra K., Lindequist U. Hispolon, a yellow pigment from Inonotus hispidus // Phytochemistry. 1996. - V.41, I.3, P.927-929; Awadh Аli N.A., Mothana R.A.A., Lesnau A., Pilgrim H., Lindequist. Antiviral activity of Inonotus hispidus // Fitoterapia. - 74 (2003). - P.483-485].
В американских заявках на изобретения (№20050238655, МПК А61K 35/84, опубл. 27.10.2005 г. и №20050276815 МПК А61K 35/84, опубл. 15.12.2005 г.) приводится описание активности композиции из трех видов грибов Fomitopsis officinalis, Piptoporus betulinus, Ganoderma resinaceum против вирусов оспы и иммунодефицита человека.
Известно применение экстракта черной наружной части гриба Fuscoporia oblique (Fr.) Aoshima в качестве активного ингредиента, ингибирующего вирус иммунодефицита человека (Заявка Японии №9191891, МПК А61К 35/84, С12Р 1/02, опубл. 29.07.1997 г.). Указанный гриб растет на древесине японской березы.
Наиболее близким аналогом (прототипом) является применение экстракта мицелиальной культуры клеток гриба Fuscoporia oblique (Fr.) Aoshima, выращенных на искусственной жидкой питательной среде, в качестве активного ингредиента, ингибирующего вирус иммунодефицита человека (Заявка США №20040105869, МПК А61 35/78, опубл. 03.06.2004 г.).
Однако данный экстракт обладает только профилактическим эффектом (экстракт добавляют к клеткам МТ-4 и инкубируют до адсорбции вируса на клетках) и имеет низкий терапевтический эффект (слабо действует на вирус при его проникновении в клетки МТ-4).
Техническим результатом предлагаемого изобретения является получение средства, обладающего ингибирующим действием в отношении вируса иммунодефицита человека первого типа, вирусов гриппа человека и птиц типа А и вируса осповакцины.
Указанный технический результат достигается получением противовирусного средства, обладающего активностью против вируса иммунодефицита человека первого типа, вирусов гриппа человека и птиц типа А и вируса осповакцины и представляющее собой водный экстракт из штамма нематофагового гриба Duddingtonia flagrans штамма F-882, полученный экстракцией биомассы гриба водой при соотношении биомасса:вода 1:5, с последующим удалением нерастворимого осадка. Биомасса нематофагового гриба Duddingtonia flagrans штамма F-882 получена путем ее культивирования на жидкой питательной среде на основе мелассы и кукурузного экстракта.
Ниже приведены примеры 1-2 получения противовирусного средства из биомассы нематофагового гриба Duddingtonia flagrans.
Пример 1. Получение образца 10-25 из нематофагового гриба Duddingtonia flagrans
Биомассу получали путем культивирования гриба на жидкой питательной среде, содержащей мелассу и кукурузный экстракт. Состав среды, %:
| Меласса | 3,0 |
| Кукурузный экстракт | 0,75 |
| KН2РО4 | 0,5 |
| NaNO3 | 0,5 |
| MgSO4×7H2O | 0,2 |
| Вода водопроводная | до 1 л |
Засев питательной среды производили водной суспензией гриба Duddingtonia flagrans, штамм F-882 с титром спор 3×104 в 1 мл, из расчета 1 мл суспензии на 75 мл жидкой питательной среды. Гриб культивировали в стационарных условиях в течение 20 суток. Биомасса имела желеобразную консистенцию, при микроскопии на мицелии выявлялись многочисленные хламидоспоры. Далее биомассу смешивали с дистиллированной водой в соотношении 1:5 по массе и измельчали в гомогенизаторе в течение 2 минут при 600 об/мин, затем биомассу подвергали обработке ультразвуком с помощью ультразвукового дезинтегратора (MSE, Англия) при амплитуде 24 мкм в течение 10 минут. Для осаждения разрушенных клеточных стенок гиф использовали центрифугирование (10000 об/мин, 20 мин). Концентрация полученных биологически активных веществ составляла 0,5 мг/мл.
Полученный продукт сушили до остаточной влажности не более 5 мас.% и измельчали до порошкообразного состояния.
Пример 2. Получение образца 10-25/1 из нематофагового гриба Duddingtonia flagrans Биомассу получали путем погруженного культивирования гриба на питательной среде, содержащей мелассу и кукурузный экстракт. Состав среды, %:
| Меласса | 3,0 |
| Кукурузный экстракт | 0,75 |
| KН2РО4 | 0,5 |
| NaNO3 | 0,5 |
| MgSO4×7H2O | 0,2 |
| Вода водопроводная | до 1 л |
Засев питательной среды производили водной суспензией гриба Duddingtonia flagrans, штамм F-882 с титром спор 3×104 в 1 мл, из расчета 1 мл суспензии на 75 мл жидкой питательной среды. Гриб культивировали в течение 6 суток при 27°С в термостатированной качалке при 180 об/мин. Биомасса имела густую консистенцию и содержала сухих веществ не менее 12-15 мг/мл. Хламидоспоры на мицелии отсутствовали. Далее биомассу смешивали с дистилированной водой в соотношении 1:5 по массе и обрабатывали в гомогенизаторе в течение 2 минут при 600 об/мин, затем биомассу подвергали обработке ультразвуком при амплитуде 24 мкм в течение 10 минут. Для осаждения разрушенных клеточных стенок гиф использовали центрифугирование (10000 об/мин, 20 мин). Концентрация полученных биологически активных веществ составляла 0,5 мг/мл.
Пример 3. Определение противовирусной активности в отношении вирусов гриппа
Культуры клеток. Для тестирования противовирусной активности препаратов использовали перевиваемую культуру клеток MDCK, полученных из коллекции культур клеток ФГУН ГНЦ ВБ «Вектор». В стерильном месте суспензию клеточной культуры MDCK разводили предварительно подогретой до температуры +37°С средой RPMI-1640, содержащей 5% сыворотки крови плодов коровы (Gibco, США), до концентрации 1,0-1,5×105 клеток/мл. По 100 мкл/лунку суспензии клеток MDCK вносили в 96-луночные планшеты 8-канальной автоматической пипеткой. Планшеты с клетками помещали в термостат при температуре +37°С, 5% CO2 и 100% влажности на 1-2 сут до образования сплошного клеточного монослоя.
Поддерживающая среда для клеток MDCK по составу была идентична ростовой среде за исключением того, что среда содержала 2 мкг/мл трипсина ТРСК (Sigma, США) и не содержала сыворотку.
Вирусы. В работе использовали штаммы вируса гриппа птиц (A/chicken/Kurgan/05/2005 (H5N1)) и человека (A/Aichi/2/68 (H3N2)), полученные из отдела «Коллекция микроорганизмов» ФГУН ГНЦ ВБ «Вектор». Наработку производили на 10-суточных развивающихся куриных эмбрионах (РКЭ). Концентрация вируса A/chicken/Kurgan/05/2005 (H5N1) в вирусаллантоисной жидкости (ВАЖ) при титровании на культуре клеток MDCK составляла 8,5 lg ТЦД50/мл (50% тканевых цитопатических доз в мл), вируса A/Aichi/2/68 (H3N2) - 7,5 lg ТЦД50/мл.
Определение цитотоксичности препаратов на культуре клеток MDCK. Исследовали препараты на основе нематофаговых грибов: 10-25, 10-25/1 на цитотоксичность на культуре клеток MDCK (таблица 1). Для определения токсических доз препараты разводили в несколько раз и оценивали наличие токсического действия в монослоях культуры клеток MDCK с помощью инвертированного микроскопа. Для этого делали разведения исходных препаратов в 2,5 раз и далее от 10-1 до 10-6 на среде RPMI-1640, затем вносили по 100 мкл/лунку разведений в лунки 96-луночного планшета и ставили в термостат при температуре +37°С, 5% CO2 и 100% влажности на 1-2 сут. Через 1-2 сут с помощью инвертированного микроскопа оценивали наличие токсического действия в монослоях клеток MDCK, инкубированных с разными концентрациями препаратов.
В качестве контроля использовали интактные клетки MDCK (без внесения препаратов).
| Таблица 1 | |||||||
| Результаты определения токсических концентраций препаратов в монослое клеток MDCK | |||||||
| № препарата и его исходная концентрация | Разведения препаратов, вызывающих (+) и не вызывающих (-) токсическое действие на клетки | ||||||
| 1:2 | 1:5 | 1:10-1 | 1:10-2 | 1:10-3 | 1:10-4 | 1:10-5 | |
| 10-250,5 мг/мл | + | - | - | - | - | - | - |
| 10-25/10,5 мг/мл | + | - | - | - | - | - | - |
Для определения противовирусной активности (таблица 1) использовали нетоксические концентрации препаратов (0,1 мг/мл и ниже).
Определение противовирусного действия препаратов в отношении вирусов гриппа A/chicken/Kurgan/05/2005 (H5N1) и A/Aichi/2/68 (H3N2) на клетках MDCK
Готовили разведения вируссодержащей жидкости (ВАЖ) от 1 до 8 с десятикратным шагом с использованием среды RPMI-1640 фирмы ООО «Биолот», С-Петербург, содержащей 2 мкг/мл трипсина ТРСК (Sigma, США).
Исследование противовирусной активности препаратов проводили по двум схемам: профилактической (сначала на культуру клеток вносится препарат и затем вирус) и лечебной (сначала на культуру клеток вносится вирус и затем препарат).
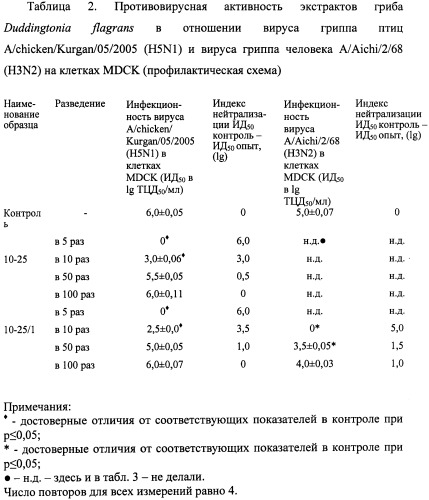
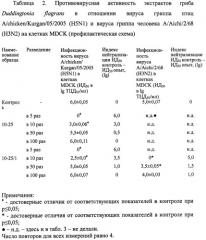
Схема 1 (профилактическая). Для определения противовирусной активности препаратов в монослой культуры клеток MDCK вносили по 100 мкл/лунку выбранного разведения препарата (таблица 2), через 1 ч инкубации при температуре +37°С, 5% CO2 и 100% влажности вносили по 100 мкл/лунку разведенного от 1 до 8 разведения ВАЖ. Клетки инкубировали 2-3 сут при температуре +37°С в атмосфере 5% СО2 в термостате ТС-1/80 СПУ (Россия). Через 2-3 сут в каждой лунке с помощью инвертированного микроскопа регистрировали ЦПД в монослое клеток и определяли наличие вируса в среде культивирования по реакции гемагглютинации (РГА) с 1% эритроцитами петуха. В качестве контроля использовали:
1. Контроль клеток MDCK, культивируемых в питательной среде RPMI-1640, фирмы ООО «Биолот», С-Петербург, содержащей 2 мкг/мл трипсина ТРСК (Sigma, США).
2. Контроль репродукции вирусов гриппа A/chicken/Kurgan/05/2005 (H5N1) и A/Aichi/2/68 (H3N2) в разведениях с 1 до 8 с десятикратным шагом без внесения препаратов, но с предварительным внесением питательной среды RPMI-1640, содержащей 2 мкг/мл трипсина ТРСК, в объеме 100 мкл/лунку.
3. Повторный контроль цитотоксичности препаратов в выбранных дозах.
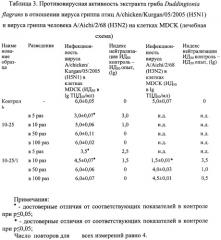
Схема 2 (лечебная). Для определения противовирусной активности препаратов (таблица 3) в монослой культуры клеток MDCK вносили по 100 мкл/лунку разведенного на среде RPMI-1640, содержащей 2 мкг/мл трипсина ТРСК, от 1 до 8 разведения ВАЖ. Через 1 ч инкубации при температуре +37°С, 5% СО2 и 100% влажности вносили по 100 мкл/лунку выбранного разведения препарата. Клетки инкубировали 2-3 сут при температуре +37°С в атмосфере 5% CO2 в термостате ТС-1/80 СПУ (Россия). Через 2-3 сут в каждой лунке с помощью инвертированного микроскопа регистрировали ЦПД в монослое клеток и определяли наличие вируса в среде культивирования по реакции гемагглютинации (РГА) с 1% эритроцитами петуха.
В качестве контроля использовали:
1. Контроль клеток MDCK, культивируемых в питательной среде RPMI-1640, фирмы ООО «Биолот», С-Петербург, содержащей 2 мкг/мл трипсина ТРСК (Sigma, США).
2. Контроль репродукции вирусов гриппа A/chicken/Kurgan/05/2005 (H5N1) и A/Aichi/2/68 (H3N2) в разведениях с 1 до 8 с десятикратным шагом без внесения препаратов, но с последующим внесением питательной среды RPMI-1640, содержащей 2 мкг/мл трипсина ТРСК, в объеме 100 мкл/лунку.
3. Повторный контроль цитотоксичности препаратов в выбранных дозах.
Определение противовирусной активности исследуемых препаратов показало, что образцы препаратов на основе нематофагового гриба 10-25, 10-25/1 в отношении вируса гриппа на клетках MDCK обладают противовирусной активностью. При этом препараты 10-25 и 10-25/1 обнаружили противовирусную активность как в отношении вируса гриппа птиц A/chicken/Kurgan/05/2005, так и вируса гриппа человека A/Aichi/2/68: при профилактической схеме при разведении препаратов в 10 раз индексы нейтрализации для вируса гриппа птиц составили 3,0 и 3,5 lg, соответственно, в то время, как более концентрированные препараты 10-25 и 10-25/1 нейтрализовали 6,0 lg этого вируса; препарат 10-25/1 при разведении в 10 раз нейтрализовал 5,0 lg вируса гриппа человека.
В лечебной схеме противовирусная активность всех изученных образцов препаратов при тех же разведениях была ниже по сравнению с профилактической схемой. Ингибирующую активность против вируса гриппа птиц проявили препараты 10-25 и 10-25/1 при разведении в 5 раз (индексы нейтрализации составили 3,0 и 2,5 lg, соответственно), а против гриппа человека - препарат 10-25/1 при разведении в 10 раз (индекс нейтрализации составил 3,5 lg).
Пример 4. Определение противовирусной активности в отношении вируса осповакцины
Культуры клеток. Для тестирования противовирусной активности препарата на основе гриба Duddingtonia flagrans использовали перевиваемую культуру клеток Vero, полученных из коллекции культур клеток ФГУН ГНЦ ВБ «Вектор». Для получения монослоя клетки Vero выращивали в 96-луночных пластиковых планшетах в течение 2,0-3,0 суток в ростовой среде RPMI-1640, содержащей 0,125 ед./мл канамицина, 150 мкг/мл L-глутамина и 5% эмбриональной сыворотки плодов коров (Fetal Bovine Serum, HyClone, США, Lot. No. CSC0518), инактивированной при 56°С в течение 30 мин).
Поддерживающая среда для клеток Vero по составу была идентична ростовой среде за исключением того, что концентрация эмбриональной сыворотки составляла 1%.
Вирусы. В работе использовали штамм Л-ИВП вируса осповакцины, полученный из отдела «Коллекция микроорганизмов» ФГУН ГНЦ ВБ «Вектор», с титром 4,6 lg ТЦД50/мл.
Определение цитотоксичности препарата на культуре клеток Vero.
Для изучения токсического действия препарата на монослой клеток Vero, выращенных в 96-луночных планшетах, препарат вносили в разведениях с двукратным шагом от 1:2 до 1:512 в поддерживающей среде в объеме 100 мкл/лунку. Планшеты с клетками инкубировали при температуре +37°С, 5% CO2 и 100% влажности. Токсическое действие препарата оценивали визуально ежедневно в течение 5 суток с помощью инвертированного микроскопа (Ломо Биолам П2-1) и выражали в % повреждение монослоя клеток. На 6 сутки после внесения препарата клетки окрашивали раствором генциан фиолетового (1 г генциан фиолетового, 50 мл 96% этилового спирта, 700 мл дистиллированной воды, 300 мл 40% раствора формалина), результаты учитывали визуально и выражали в % повреждение монослоя клеток.
В качестве контроля использовали интактные клетки Vero (без внесения препарата).
В опытах по определению противовирусной активности препарата в отношении вируса осповакцины использовали максимально переносимые концентрации препарата на клетках Vero (таблица 4).
| Таблица 4 | ||
| Токсичность препарата на основе гриба Duddingtonia flagrans на клетках Vero | ||
| Образец, концентрация | Разведение препарата | Поражение клеток (% ЦПД) через 6 сут |
| неразведенный | 100 | |
| 1:2 | 100 | |
| 1:4 | 100 | |
| 10-25/1 | 1:8 | 100 |
| 0,5 мг/мл | 1:10 | 50 |
| 1:16 | 0 | |
| 1:32 | 0 | |
| 1:64 | 0 | |
| 1:128 | 0 | |
| 1:512 | 0 |
Вируснейтрализующее действие препарата в отношении вируса осповакцины на клетках Vero
Для определения вируснейтрализующего действия к двукратным разведениям препарата в поддерживающей среде (объем 100 мкл/лунку) вносили вирус, разведенный в поддерживающей среде (объем 100 мкл/лунку), в дозе 100 ТЦД50/лунку. Планшеты с инфицированными культурами клеток и внесенным в них препаратом, а также планшеты с контрольными клетками инкубировали при температуре +37°С, 5% СО2 и 100% влажности в течение 5 сут, при этом ежедневно просматривали монослой клеток с помощью инвертированного микроскопа. На 6 сутки после заражения клетки окрашивали раствором генциан фиолетового (1 г генциан фиолетового, 50 мл 96% этилового спирта, 700 мл дистиллированной воды, 300 мл 40% раствора формалина) и результаты учитывали визуально, оценивая поражение клеточного монослоя в %.
За 50%-ную вирусингибирующую концентрацию препарата (IС50) принимали максимальное его разведение, при котором наблюдали защиту 50% клеток от действия вируса в дозе 100 ТЦД50/лунку.
В качестве отрицательного контроля (контроля сохранности жизнеспособности клеток) использовали интактные клетки в поддерживающей среде без добавления препарата не менее чем в 16 лунках каждого планшета, которые инкубировали в течение того же времени, что и в опыте.
В качестве положительного контроля использовали клетки, зараженные вирусом в дозе 100 ТЦД50/лунку без добавления препарата (таблица 5).
| Таблица 5 | |||
| Вируснейтрализующее действие препарата на основе гриба Duddingtonia flagrans в отношении вируса осповакцины на клетках Vero | |||
| Наименование образца | Концентрация исходного препарата | Разведение препарата | Поражение клеток (%) через 6 сут |
| 1:16 | 50 | ||
| 10-25/1 | 0,5 мг/мл | 1:32 | 75 |
| 1:64 | 75 | ||
| 1:128 | 100 | ||
| 1:512 | 100 | ||
| Контроль вируса (без препарата) | - | - | 100 |
| Примечание: | |||
| Число повторов для всех измерений равно 4. |
Определение токсичности препарата на основе гриба Duddingtonia flagrans на клетках Vero показало, что препарат на основе нематофагового гриба 10-25/1 на клетках Vero был токсичен при разведении 1:8 на 100%, при разведении 1:10 - на 50%. В связи с этим в опытах по определению противовирусной активности мы использовали препарат в максимально нетоксичных разведениях, а именно 10-25/1 - в разведениях от 1:16 до 1:512. Определение вируснейтрализующего действия показало, что препарат на основе нематофагового гриба 10-25/1 при разведении 1:16 защищал от этого вируса 50% клеток Vero и в разведении 1:32 - 25% этих клеток.
На основании полученных данных можно заключить, что образцы на основе гриба Duddingtonia flagrans перспективны для дальнейшего изучения в плане разработки препаратов против вирусов гриппа и осповакцины.
Пример 5. Определение противовирусной активности в отношении вируса иммунодефицита человека 1 типа
Исследование противовирусной активности соединений в отношении ВИЧ-1 проводили на перевиваемой линии лимфоцитов человека МТ-4. Клетки культивировали на среде RPMI-1640 с добавлением 10% фетальной сыворотки КРС, предварительно инактивированной прогреванием при 56°С в течение 30 минут, 300 мг/мл L-глютамина и 80 мкг/мл гентамицина. Использовали клетки после 3 пассажа, на 3 сутки культивирования, в логарифмической фазе роста. После микроскопирования и оценки морфологии подсчитывали концентрацию и жизнеспособность клеток методом исключения трипанового синего. Для эксперимента использовали клетки с концентрацией не менее 2,0×106 клеточных частиц в миллилитре и жизнеспособностью не менее 90%.
Для заражения использовали супернатант клеток МТ-4, инфицированных ВИЧ-1 штамм ГКВ 4046, хранившийся в жидком азоте. Множественность заражения 0,2-0,5 инфекционных единиц на клетку.
Исследовали токсичность соединений. Для этого суспензию клеток МТ-4, разведенную до посевной концентрации 0,5×106 клеток в миллилитре питательной средой RPMI-1640 с добавлением 10% фетальной сыворотки, предварительно инактивированной прогреванием при 56°С в течение 30 минут, 300 мг/мл L-глютамина, 80 мкг/мл гентамицина и 30 мг/мл линкомицина, помещали в лунки 96-луночных планшетов по 180 мкл в лунку. К клеткам добавляли растворы исследуемых соединений (по 20 мкл в лунку). Проводили оценку токсичности в два этапа: при конечных разведениях препарата 1:10, 1:50, 1:100, 1:1000. При выявлении низкой токсичности препарата применяли дополнительное разведение препарата до конечных разведений 1:2,5; 1:5; 1:10; 1:20. Использовали по 3 лунки на каждую дозу. Контролем служат клетки, в которые вместо исследуемого соединения добавляют то же количество растворителя (среда RPMI-1640 без сыворотки и антибиотиков). Планшеты инкубировали в термостате при 37°С. На 3-и сутки культивирования подсчитывают концентрацию и жизнеспособность клеток методом прижизненного окрашивания клеток МТТ (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide). Разведение, не оказывающее токсического действия на клетки МТ-4 (при котором клетки сохраняли 50% и 100% жизнеспособность), определяли по графику зависимости оптической плотности от концентрации и жизнеспособности клеток.
Профилактическое действие препаратов оценивали по подавлению вируспродукции в клетках МТ-4 при добавлении препарата при адсорбции вируса.
В суспензию клеток МТ-4 добавляли вируссодержащий материал и немедленно разносили ее по лункам 96-луночных планшетов. Сразу же добавляли препараты, разведенные в среде RPMI-1640, до конечных разведений 1:10, 1:20, 1:40, 1:80… (по три лунки на каждую дозу). Планшеты инкубировали в течение часа при 37°С для адсорбции вируса. Затем клетки разводили до посевной концентрации питательной средой RPMI-1640 с добавлением 10% фетальной сыворотки, предварительно инактивированной прогреванием при 56°С в течение 30 минут, 300 мг/мл L-глютамина, 80 мкг/мл гентамицина и 30 мг/мл линкомицина, содержащей соответствующие дозы препаратов.
Терапевтическое действие препаратов оценивали по подавлению продукции ВИЧ-1 в клетках МТ-4 при добавлении препарата гриба чаги после адсорбции вируса на поверхности клетки.
В суспензию чувствительных клеток вносили вируссодержащий материал и инкубировали в течение часа при 37°С в атмосфере 5% СО2 при постоянном перемешивании содержимого для адсорбции вируса.
После этого клетки разводили до посевной концентрации питательной средой RPMI-1640 с сывороткой и антибиотиками и разносили по лункам 96-луночных планшетов по 180 мкл в лунку. В каждую лунку добавляли аликвоты исследуемых соединений, разведенных в среде RPMI-1640 без добавок, до конечных разведений 1:10, 1:20, 1:40, … 1:64000.
Контролями служили инфицированные ВИЧ-1 клетки МТ-4 без добавления препаратов. Планшеты инкубировали при 37°С в атмосфере 5% СO2 в течение 3-х суток. Анти-ВИЧ активность препаратов оценивали по подавлению накопления вирусного белка р24 в инфицированных клетках с использованием количественного определения р24 методом прямого иммуноферментного анализа. Подавление прироста вирусспецифического белка р24 различными разведениями исследуемых препаратов при внесении вируса и препарата (50% и 100% инактивация вируса) определяли по графикам зависимости оптической плотности от концентрации р24, пересчитывали концентрацию р24 по графику для стандартного антигена.
Суммарные данные по оценке токсичности и эффективности в отношении ВИЧ-1 препарата гриба 10-25 представлены в таблице 6.
| Таблица 6 | ||||||
| Подавление репродукции ВИЧ-1 в клетках МТ-4 при внесении препарата на основе гриба Duddingtonia flagrans до и после адсорбции ВИЧ-1 на поверхности клеток и оценка токсичности препарата | ||||||
| Наименование образца | Концентрация препарата, ингибирующая репродукцию ВИЧ-1 при одновременном внесении с вирусом (мкг/мл) | Концентрация препарата, ингибирующая репродукцию ВИЧ-1 при внесении препарата после адсорбции вируса (мкг/мл) | Нетоксичная концентрация препарата (мкг/мл) | |||
| На 50% | На 100% | На 50% | На 100% | Для 50% клеток | Для 100% клеток | |
| 10-25/1 | 12,5 | 25 | 6,25 | 12,5 | более 500 | 200 |
При добавлении препарата гриба 10-25/1 одновременно с адсорбцией вируса показано полное подавление репродукции ВИЧ-1 в клетках МТ-4 при концентрации препарата 25 мкг/мл. При добавлении препарата гриба 10-25/1 после адсорбции ВИЧ показано полное подавление репродукции ВИЧ-1 в клетках МТ-4 при концентрации препарата 12,5 мкг/мл.
Необходимо отметить, что данный препарат при рабочей концентрации более 500 мкг/мл не проявляет токсичных свойств для 50% клеток.
При этом химиотерапевтический индекс (рассчитанный как отношение максимально переносимой дозы к минимальной эффективной дозе) при оценке терапевтического действия препарата гриба 10-25/1 превышает 80. Пример 5 показывает перспективность использования анти-ВИЧ препарата на основе экстракта гриба Duddingtonia flagrans (образец 10-25/1).
1. Противовирусное средство, обладающее активностью против вируса иммунодефицита человека первого типа, вирусов гриппа человека и птиц типа А и вируса осповакцины и представляющее собой водный экстракт из штамма нематофагового гриба Duddingtonia flagrans F-882, полученный экстракцией биомассы гриба водой при соотношении биомасса: вода 1:5, с последующим удалением нерастворимого осадка.
2. Средство по п.1, отличающееся тем, что биомасса нематофагового гриба Duddingtonia flagrans штамма F-882 получена путем ее культивирования на жидкой питательной среде на основе мелассы и кукурузного экстракта.