Способ определения хлорзамещенных фенолов в водных средах
Иллюстрации
Показать всеНастоящее изобретение относится к аналитической химии органических соединений и описывает способ определения хлорзамещенных фенолов в водных средах, включающий их химическую модификацию, экстракционное концентрирование и газохроматографическое детектирование, где на стадии химической модификации в качестве реагента-модификатора применяют йод в количестве 0.01-0.03% в присутствии бета-аланина и аммиака в количестве 0.5-2.0% и 0.005-0.02% от массы водной пробы соответственно. Изобретение обеспечивает более низкий предел обнаружения хлорзамещенных фенолов в воде. 2 табл., 2 ил., 7 пр.
Реферат
Изобретение относится к аналитической химии органических соединений (концентрирование и определение) и может быть использовано для санитарно-эпидемиологического контроля питьевых вод, воды объектов, имеющих рыбохозяйственное значение, а также степени очистки сточных вод различных химических производств.
Наиболее близким по технической сущности к заявляемому решению является газохроматографический способ определения монохлорфенолов в виде их бромпроизводных [Патент Россия №2142627, МПК 6 G01N 30/00, 31/00, 33/18. Способ определения монохлорфенолов в водных средах / Я.И.Коренман, И.В.Груздев, В.Н.Фокин, Б.М.Кондратенок (Россия). - 99101425/04; Заявлено 26.01.99; Опубл. 10.12.99, Бюл. №34 (ч. II) // Изобретения. - 1999. - №34(ч.II). - С.316.].
Недостатком прототипа является высокий предел обнаружения хлорзамещенных фенолов, связанный с малоэффективным экстракционным концентрированием и частичным окислением хлорфенолов при получении их бромпроизводных в водной среде.
Задачей изобретения является разработка способа, позволяющего снизить предел обнаружения хлорфенолов (2-хлорфенол, 4-хлорфенол, 2,4-дихлорфенол и 2,6-дихлорфенол) за счет применения более эффективного модифицирующего реагента и исключения окисления получаемых производных. В этом состоит технический результат.
Решение поставленной задачи достигается тем, что в способе определения хлорзамещенных фенолов в водных средах, включающем их химическую модификацию, экстракционное концентрирование и газохроматографическое детектирование, новым является то, что в качестве реагента-модификатора применяют йод в количестве 0.01-0.03% в присутствии бета-аланина в количестве 0.5-2.0% и аммиака в количестве 0.005-0.02% от массы водной пробы.
Положительный эффект по предлагаемому способу достигается за счет того, что применяемый реагент-модификатор (йод) при взаимодействии с хлорфенолами в водной среде образует соответствующие йодпроизводные хлорфенолов. Как известно, атомы йода имеют больший радиус, чем атомы брома, и, как следствие, большую площадь захвата электронов при детектировании электронозахватным детектором [Poole C.F., Zlatkis A. Electron capture. Journal of Chromatography library. New York: Elsevier, 1981. 322 p.]. Таким образом, пределы обнаружения хлорзамещенных фенолов при определении их в виде йодпроизводных будут ниже, чем при определении их в виде аналогичных бромпроизводных.
Кроме того, йодпроизводные хлорфенолов по сравнению с аналогичными бромпроизводными эффективней экстрагируются, так как атомы йода обладают большим гидрофобным действием [Коренман И.М. Экстракция органических веществ. Горький: Изд-во Горьков. гос. ун-та, 1973. 158 с]. Увеличение степени извлечения йодпроизводных при экстракционном концентрировании (до 80-92% при r=500), также снижает пределы обнаружения хлорфенолов в воде.
Применение молекулярного йода в качестве модифицирующего реагента повышает и устойчивость к окислению как исходных хлорфенолов, так и их йодпроизводных, поскольку водные растворы йода характеризуются в два раза меньшим окислительно-восстановительным потенциалом по сравнению с бромом [Ксензенко В.И., Стасиневич Д.С. Химия и технология брома, йода и их соединений. М.: Химия, 1995. 432 с].
Проведение йодирования хлорфенолов в присутствии бета-аланина связано с наличием сольватационного взаимодействия между йодом и NH2-группой аминокислоты, которое вызывает поляризацию молекул йода и ускорение реакции йодирования хлорфенолов. Следует отметить, что в присутствии других аминокислот (глицин, альфа-аланин) этот эффект выражен слабо, что связано, на наш взгляд, со стерическими препятствиями, возникающими при взаимодействии крупных молекул йода и аминогруппы в альфа-положении.
Наличие аммиака при йодировании хлорфенолов, который обратимо реагирует с йодом,
I2+NH3 → ←NH2I+H++I-
позволяет поддерживать постоянную концентрацию йода в системе и дополнительно снижать ее окислительно-восстановительный потенциал. Кроме того, введение аммиака вызывает смещение реакционной среды в слабощелочную область, что сопровождается переходом хлорфенолов в фенолят-анионы и повышением их активности в реакциях галогенирования [Агрономов А.Е. Избранные главы органической химии. М: Химия, 1990. 560 с.].
Йодирование в этих условиях завершается за 8-10 мин с количественным образованием йодпроизводных хлорфенолов, а получаемые йодпроизводные устойчивы в воде и органических растворителях, по крайней мере, в течение 24 часов.
Способ определения хлорзамещенных фенолов в водных средах включает три этапа:
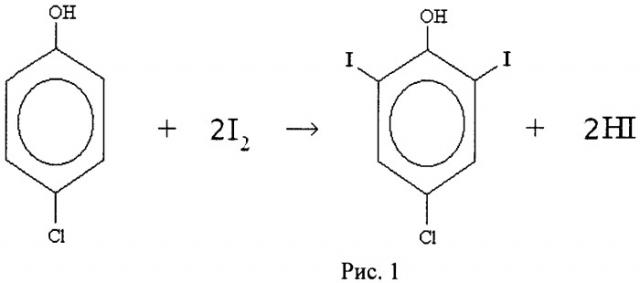
1. Получение йодпроизводных хлорфенолов (химическая модификация) - обработка водного образца молекулярным йодом в присутствии бета-аланина и аммиака. При йодировании атомы йода замещают атомы водорода в ароматическом ядре хлорфенолов в положениях 2, 4 и 6, если они не заняты атомами хлора. Таким образом, 2- и 4-хлорфенолы образуют дийодпроизводные, 2,4- и 2,6-дихлорфенолы - монойодпроизводные. На рис.1 приведена реакция образования йодпроизводного 4-хлорфенола.
2. Экстракционное концентрирование йодпроизводных хлорфенолов методом жидкостной экстракции. Эта стадия предназначена для перевода йодпроизводных из воды в более удобную для последующего газохроматографического анализа органическую фазу (толуол), повышения их концентрации в экстракте и отделения мешающих примесей.
3. Анализ йодпроизводных хлорзамещенных фенолов методом капиллярной газовой хроматографии с галогенселективным электронно-захватным детектором (ДЭЗ).
Для улучшения хроматографических свойств йодпроизводных хлорфенолов (форма пика) в экстракте может быть проведено получение их производных по гидроксильной группе (ацилирование, силирование и др.)
Определение хлорфенолов выполняют по следующей методике. В мерную колбу помещают 1000 см3 анализируемой пробы, добавляют бета-аланин в количестве 0.5-2.0% и аммиак в количестве 0.005-0.02% от массы образца. Исходную пробу делят на две равные части, в одну из которых вводят стандартные добавки хлорфенолов; расчетная концентрация индивидуальных хлорфенолов составляет 0.01 мкг/дм3. В обе части пробы добавляют йодную воду; расчетное содержание молекулярного йода в пробе 0.01-0.03%. Йодирование проводят в течение 10 минут при комнатной температуре. После завершения йодирования избыток йода удаляют раствором тиосульфата натрия; расчетная концентрация в пробе - 0.001 моль/дм3. Далее подкисляют водные растворы до значения рН 2-3 раствором серной кислоты, вводят внутренний стандарт (4,6-дибром-1,2-диметоксибензол); расчетная концентрация в пробе - 0.5 мкг/см3 и экстрагируют образовавшиеся йодпроизводные 1 см3 толуола в течение 12 минут на магнитной мешалке. После расслаивания фаз полученные экстракты анализируют на газовом хроматографе с ДЭЗ.
Условия газохроматографического определения: кварцевая капиллярная колонка 30 м × 0.25 мм × 0.25 мкм с неподвижной жидкой фазой SE-30, SE-52, SE-54 или их аналогами; газ-носитель - азот (ос.ч.), программирование давления газа-носителя: 100 кПа (5 мин) - 20 кПа/мин - 240 кПа, поддув детектора - 25 см3/мин, деление потока - 1:25. Температура детектора 300°С, испарителя 340°С, термостата колонок 190°С.
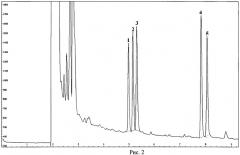
На рис.2 приведена хроматограмма стандартного раствора хлорфенолов с концентрацией 1 мкг/дм3: 1 - 6-йод-2,4-дихлорфенол, 2 - 4-йод-2,6-дихлорфенол, 3 - внутренний стандарт, 4 - 2,6-дийод-4-хлорфенол, 5 - 4,6-дийод-2-хлорфенол.
Идентификацию йодпроизводных хлорфенолов проводят по относительным временам удерживания (t*):
t*=t/tст,
где t и tст - исправленные времена удерживания компонентов анализируемой пробы и внутреннего стандарта (4,6-дибром-1,2-диметоксибензол), соответственно.
Относительные времена удерживания компонентов анализируемой пробы сравнивают с относительными временами удерживания йодпроизводных хлорфенолов, полученных для стандартной смеси (табл.1).
| Таблица 1 | |
| Относительные времена удерживания | |
| Вещество | t* |
| 6-йод-2,4-дихлорфенол | 0.904 |
| 4-йод-2,6-дихлорфенол | 0.956 |
| внутренний стандарт | 1.000 |
| 2,6-дийод-4-хлорфенол | 1.738 |
| 4,6-дийод-2-хлорфенол | 1.805 |
Концентрации хлорфенолов в пробе воды рассчитывают по уравнению [Новак Й. Количественный анализ методом газовой хроматографии. - М.: Мир, 1978. - 179 с.]:
где Cs - концентрация определяемого хлорфенола в растворе стандартной добавки, мкг/см3;
Vs - объем вводимого раствора стандартной добавки, см3;
Vi - объем анализируемой пробы, в который вводится добавка, см3;
, - площади пиков определяемого йодпроизводного хлорфенола и внутреннего стандарта соответственно на хроматограмме пробы с добавкой;
Si, Sv - площади пиков определяемого йодпроизводного хлорфенола и внутреннего стандарта соответственно на хроматограмме пробы без добавки.
Примеры осуществления способа
Пример 1
В мерную колбу помещают 1000 см3 анализируемой пробы, добавляют бета-аланин в количестве 0.2% и аммиак в количестве 0.0005% от массы образца. Исходную пробу делят на две равные части, в одну из которых вводят стандартные добавки хлорфенолов; расчетная концентрация индивидуальных хлорфенолов составляет 0.01 мкг/дм3. В обе части пробы добавляют йодную воду; расчетное содержание молекулярного йода в пробе 0.005%. Йодирование проводят в течение 10 минут при комнатной температуре. После завершения йодирования избыток йода удаляют раствором тиосульфата натрия; расчетная концентрация в пробе - 0.001 моль/дм3. Далее подкисляют водные растворы до значения рН 2-3 раствором серной кислоты, вводят внутренний стандарт (4,6-дибром-1,2-диметоксибензол); расчетная концентрация в пробе - 0.5 мкг/см3 и экстрагируют образовавшиеся йодпроизводные 1 см3 толуола в течение 12 минут на магнитной мешалке. После расслаивания фаз полученные экстракты анализируют на газовом хроматографе с ДЭЗ. На полученных хроматограммах проводят идентификацию и количественное определение хлорированных фенолов.
Способ неосуществим, поскольку предел обнаружения хлорфенолов выше, чем по прототипу.
Пример 2
Содержание бета-аланина в пробе - 0.4%, аммиака - 0.002% и йода - 0.01%. Анализируют, как указано в примере 1. Предел обнаружения - 0.2 мкг/дм3. Способ неосуществим, так как предел обнаружения хлорфенолов выше, чем по прототипу.
Пример 3
Содержание бета-аланина в пробе - 0.5%, аммиака - 0.005% и йода - 0.02%. Анализируют, как указано в примере 1. Предел обнаружения - 0.002 мкг/дм3. Способ осуществим.
Пример 4
Содержание бета-аланина в пробе - 1%, аммиака - 0.01% и йода - 0.02%. Анализируют, как указано в примере 1. Предел обнаружения - 0.002 мкг/дм3. Способ осуществим.
Пример 5
Содержание бета-аланина в пробе - 2%, аммиака - 0.02% и йода - 0.03%. Анализируют, как указано в примере 1. Предел обнаружения - 0.002 мкг/дм3. Способ осуществим.
Пример 6
Содержание бета-аланина в пробе - 3%, аммиака - 0.03% и йода - 0.03%. Анализируют, как указано в примере 1. Предел обнаружения - 0.002 мкг/дм3. Способ осуществим.
Пример 7
Содержание бета-аланина в пробе - 4%, аммиака - 0.04% и йода - 0.05%. Анализируют, как указано в примере 1. Предел обнаружения - 0.01 мкг/дм3. Способ осуществим.
Результаты определения хлорированных фенолов в воде предлагаемым способом приведены в табл.2.
| Таблица 2 | |||||
| Примеры осуществления способа | |||||
| № примера | Содержание NH3,% | Содержание бета-аланин, % | Содержание I2, % | Предел обнаружения, мкг/дм3 | Возможность осуществления заявляемого способа |
| По прототипу | - | - | - | 0.1 | - |
| 1 | 0.0005 | 0.2 | 0.005 | 1 | неосуществим |
| 2 | 0.002 | 0.4 | 0.01 | 0.2 | неосуществим |
| 3 | 0.005 | 0.5 | 0.02 | 0.01 | осуществим |
| 4 | 0.01 | 1.0 | 0.02 | 0.01 | осуществим |
| 5 | 0.02 | 2.0 | 0.03 | 0.01 | осуществим |
| 6 | 0.03 | 3.0 | 0.03 | 0.01 | осуществим |
| 7 | 0.04 | 4.0 | 0.05 | 0.01 | осуществим |
Из примеров 1-7 и табл.2 следует, что предлагаемый способ определения хлорфенолов осуществим при содержании бета-аланина 0.5-2.0%, аммиака 0.005-0.02% и йода 0.01-0.03% по отношению к массе пробы. Дальнейшее увеличение концентрации компонентов нецелесообразно, поскольку не оказывает влияния на предел обнаружения хлорфенолов и ведет к перерасходу веществ. В примерах 1 и 2 заявляемый предел обнаружения не достигается, поскольку йодпроизводные хлорфенолов при этих условиях образуются с полуколичественным выходом.
По сравнению с прототипом предлагаемое техническое решение имеет следующие преимущества:
1. Более низкий предел обнаружения хлорфенолов в воде: 0.01 мкг/дм3; по прототипу - 0.1 мкг/дм3.
2. Достигается полное разделение изомерных йодпроизводных хлорфенолов (рис.2), поскольку они сильнее различаются хроматографическими свойствами, чем аналогичные бромпроизводные. При бромировании хлорфенолов степень разделения изомеров составляет 80-85%, что осложняет проведение их количественного анализа.
3. Применяемый модифицирующий агент (йод) менее токсичен, более доступен и устойчив при хранении.
Способ определения хлорзамещенных фенолов в водных средах, включающий их химическую модификацию, экстракционное концентрирование и газохроматографическое детектирование, отличающийся тем, что на стадии химической модификации в качестве реагента-модификатора применяют йод в количестве 0,01-0,03% в присутствии бета-аланина и аммиака в количестве 0,5-2,0% и 0,005-0,02% от массы водной пробы соответственно.