Антибактериальное средство и способ его получения
Иллюстрации
Показать всеНастоящее изобретение относится к области фармакологии и медицины и касается антибактериального средства, представляющего собой конъюгат наноалмаза с амикацином с размером частиц 2-10 нм при содержании амикацина до 40 мас.%, а также способа его получения. 2 н. и 1 з.п. ф-лы, 5 ил., 1 табл., 1 пр.
Реферат
Настоящее изобретение относится к области фармацевтики и медицины, в частности к антибактериальному средству, представляющему собой конъюгат наноалмаза с антибиотиком аминогликозидного ряда амикацином, обладающему повышенной антибактериальной активностью, а также способа его получения.
Одним из основных элементов этиопатогенетического лечения бактериальных инфекций является рациональная антибиотикотерапия. Для выбора наиболее эффективного препарата из большого арсенала современных антибактериальных лекарственных средств необходимо учитывать их степень антибактериальной активности против конкретных возбудителей. К антибиотикам аминогликозидного ряда относятся наиболее значимые, разрешенные к медицинской практике антибактериальные вещества: канамицин, гентамицина сульфат, сизомицина сульфат, тобрамицин и амикацина сульфат.
Все аминогликозиды содержат амино- и гидроксильные группы, играющие важную роль в противобактериальной активности и служащие местом осуществляемой бактериальными ферментами инактивации. Механизм действия этой группы антибиотиков обусловлен необратимым связыванием со специфическими рецепторами бактериальных рибосом и нарушением синтеза цитоплазматических мембран, приводящим к гибели бактериальных клеток. Типичным представителем аминогликозидных антибиотиков в настоящее время является синтезированный в 1973 г. N-[4-амино-2-(S)-гидроксибутирил]-O-6-амино-6-дезокси-α-D-глюкопиранозил(1→4)]-O-[3-амино-3дезокси-α-D-глюкопиранозил(1→6)]-2-дезокси-D-стрептамина дисульфат (амикацина сульфат) C22H43N5O13·2H2SO4. Этот антибиотик III поколения обладает самой высокой активностью и широким спектром антибактериального действия. Однако амикацина сульфат, как и другие антибиотики этого ряда, обладает рядом существенных недостатков, в частности, сниженной эффективностью в отношении грамположительных бактерий и выраженным токсическим действием.
Известен способ повышения эффективности амикацина в виде как свободного основания, так и сульфата и его варианты путем введения антибиотика в липосомы с размерами частиц от 100 нм до 1 мкм с применением различных липидов [1-4]. Было показано, что в малой дозе (4 мкг/мл) липосомальный амикацин был в 8 раз эффективнее свободного амикацина, а в большой дозе (16 мкг/мл) - в 130 раз эффективнее свободного амикацина, при этом убивал M. Tuberculosis, в то время как свободный антибиотик лишь ингибировал их развитие [2].
Известен способ повышения эффективности аминогликозидных антибиотиков, в частности, амикацина сульфата путем их связывания с наночастицами биодеградируемых полимеров [5-6]. Однако конкретные данные об изменении активности антибиотиков, в частности амикацина, в патентах не приводятся.
Хотя липосомальные формы аминогликозидных антибиотиков, в частности, амикацина авторами изобретений предлагаются для использования в пероральных лекарственных формах, однако, липосомы в большинстве случаев для этого не подходят из-за их восприимчивости к рН желудка и пищеварительным ферментам кишечника [7]. Полимерные наночастицы также могут обладать рядом существенных недостатков. Большинство мономеров, способных к мицеллярной полимеризации в водной системе, образуют медленно биоразлагаемые или даже бионеразлагаемые полимеры. При этом молекулярная масса полимера полностью не может контролироваться. Остатки в среде полимеризации (такие как мономеры, олигомеры, органические растворители, ПАВ или катализаторы) могут быть токсичны, что требует дополнительной очистки коллоидной системы. Во время процесса полимеризации активированные молекулы мономера также могут взаимодействовать с молекулой лекарственного вещества, что в свою очередь может приводить к его инактивации или неконтролируемым изменениям свойств [8].
В связи с вышеизложенным чрезвычайно актуальным является разработка способов повышения эффективности антибиотиков аминогликозидного ряда, в том числе амикацина сульфата.
Известно применение наноалмазов для повышения эффективности действия ряда лекарственных средств антимикробного действия, таких как: фторохинолон, амоксициллин, 2-бром-2-нитропропан-1,3-диол, 3,5-диметилтетрагидро-1,3,5-2Н-тиазин-2-тион, N-(3-хлорометил)-тиофталемид, бутил-п-гидроксибензоат, дийодометил-п-толилсульфон, тетрахлороизофталонитрил, азитромицин, пенициллин и кларитромицин [9].
Также известно применение наноалмазов, содержащих на своей поверхности атомы фтора, для повышения эффективности ряда опиоидов, алкалоидов, каннабиоидов и нестероидных противовоспалительных веществ [10].
Известно повышение эффективности и снижение токсичности противоопухолевого антибиотика доксорубицина при его связывании с наноалмазом [11].
Известно применение наноалмаза для повышения противоопухолевой активности дитерпеноида таксола при их химическом связывании [12].
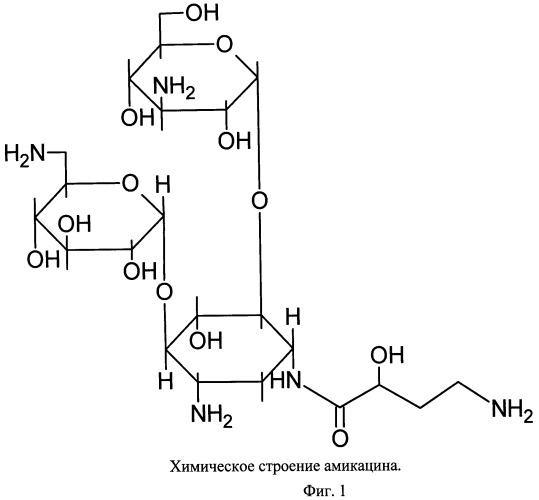
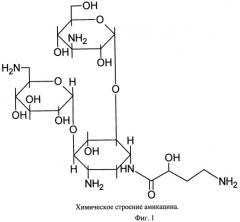
В основу настоящего изобретения положена задача поиска нового антибактериального средства, представляющего собой связанный с наноалмазом амикацин (Фиг.1), характеризующейся повышенной антибактериальной активностью, превосходящей активность фармакопейного препарата.
Задача решена тем, что в качестве антибактериального средства получен конъюгат наноалмаза с амикацином.
Разработан также способ получения конъюгата наноалмаза с амикацином.
Конъюгат наноалмаза с амикацином обладает повышенной антибактериальной активностью в отношении грамположительных бактерий по сравнению с фармакопейным амикацином сульфатом и легко проникает через клеточные мембраны внутрь клетки.
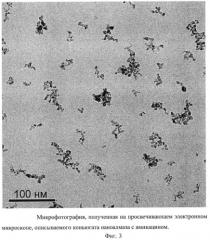
В соответствии с изобретением описывается конъюгат наноалмаза с амикацином, представляющий собой ультрадисперсный порошок (Фиг.2) серого или темно-серого цвета с размером частиц 2-10 нм (Фиг.3), содержащий от 0,1 до 40 мас.% амикацина, и размером агрегатов в водной суспензии от 10 до 100 нм (Фиг.4).
На Фиг.2 отчетливо видно наличие у заявляемого конъюгата наноалмаза с амикацином ультрадисперсной структуры из частиц с размером, меньшим разрешающей способности использованного прибора (от 20 нм).
Микрофотография частиц конъюгата наноалмаза с амикацином получена на автоэмиссионном сканирующем электронном микроскопе (СЭМ) сверхвысокого разрешения Zeiss Ultra Plus (Carl Zeiss, Германия).
На Фиг.3 видно, что среднее распределение по размерам частиц конъюгата наноалмаза с амикацином составляет 2-10 нм.
Микрофотография частиц конъюгата наноалмаза с амикацином получена на просвечивающем электронном микроскопе (ПЭМ) Jeol 1011 (JEOL, Япония).
На Фиг.4 приведена кривая распределения размеров частиц в суспензии описываемого конъюгата наноалмаза с амикацином для среднего размера частиц 15 нм с распределением 10-30 нм.
Измерение распределения размера частиц в суспензии конъюгата проводили методом динамического лазерного светорассеяния на приборе ZetaSizer (Malvem Instruments, США).
На Фиг.5 приведен ПК-спектр описываемого конъюгата в диапазоне 400-1800 см-1. На спектре присутствуют два сильных сигнала при частоте 1630 и 1120 см-1, одна полоса средней интенсивности с максимум 620 см-1 и слабые сигналы при 1458, 1406, 1318, 1046 см-1.
ИК-спектры регистрировали на приборе FTIRS IR200 Thermonicolet (Thermo Scientific, США). Разрешение 2 см-1, количество сканов 64. Для анализа навеску образца смешивали с порошком KBr и прессовали в таблетку.
Описывается также на примере амикацина способ получения конъюгата наноалмаза с аминогликозидным антибиотиком с размером частиц 2-10 нм, содержащие до 40 мас.% антибиотика, заключающийся в том, что частицы наноалмаза с размером частиц 2-10 нм, модифицированные хлором, растворяют в полярном растворителе с образованием суспензии, добавляют третичный амин и амикацина сульфат, полученную смесь выдерживают при температуре 0-70°C при постоянной ультразвуковой обработке, центрифугируют, промывают растворителем и высушивают. Реагенты берут из расчета наноалмаз: амикацина сульфат = 1:1 по массе. Третичный амин берут с избытком из расчета связывания всех образующихся в растворе сульфат-анионов от амикацина сульфата. Удаление сульфата третичным амином необходимо для связывания свободного амикацина с наноалмазом.
В качестве третичного амина используют триэтиламин, в качестве полярного растворителя используют низшие алифатические спирты, водно-спиртовую смесь или воду. Выдерживание при температуре 0-70°C осуществляют в течение от 1 до 72 ч.
Количество антибиотика в конъюгате наноалмаза с амикацином определяют по способу, заключающимся в следующем. Готовят смеси наноалмаза с разным содержанием амикацина сульфата. Берут навески каждой смеси и определяемого образца равной массы. Регистрируют их ИК-спектры, выбирают на них наиболее интенсивные характеристические сигналы, которые соотносят с полосами ИК-спектра исходного амикацина сульфата. Затем строят калибровочные кривые зависимости интенсивности сигнала в ИК-спектре от содержания амикацина в навеске. Далее, по интенсивности выбранных характеристических полос исследуемого конъюгата наноалмаза с амикацином по калибровочным кривым определяют количественное содержание в нем амикацина. По полученным данным определяют среднее значение величины содержания амикацина в конъюгате наноалмаза с амикацином.
В результате проведенных исследований нами выявлены свойства конъюгата наноалмаза с амикацином, дающие возможность применить его в качестве антибактериального средства с повышенной антибактериальной активностью, превосходящей активность фармакопейного амикацина сульфата.
Антибактериальную активность конъюгата определяли микробиологическим способом in vitro. Культура микроорганизмов Bacillus subtilis засевалась в количестве 0,1 мл 5·105 клеток, пробирки инкубировались при температуре 37°C с последующим высеванием.
Результаты определения активности антибиотика по оценке минимальной ингибирующей концентрации (МИК) исследуемых препаратов представлены в таблице.
Значения МИК амикацина сульфата и конъюгата наноалмаза с амикацином.
| Вид микроорганизма | Антибактериальное вещество, мг/мл | |
| Амикацина сульфат (субстанция) | Конъюгат наноалмаза с амикацином | |
| Bacillus subtilis | 0,15 | 0,024 |
Из данных таблицы видно, что антибактериальная активность конъюгата наноалмаза с амикацином превышает антибактериальную активность амикацина сульфата в 6,25 раза для культуры микроорганизмов Bacillus subtilis.
Способ получения заявляемого конъюгата наноалмаза с аминогликозидным антибиотиком, например с амикацином, заключается в получении хлорированного наноалмаза, при взаимодействии которого с аминогруппой антибиотика образуется химическая связь C-N между поверхностью наноалмаза и аминогруппой антибиотика, в результате которой получается конъюгат наноалмаза с антибиотиком.
Используемые в способе получения модифицированные хлором частицы наноалмаза получают путем отжига наноалмаза в токе газообразного водорода и последующего жидкофазного хлорирования молекулярным хлором. Отжиг ведут при температуре от 500 до 1200°C в течение 1-8 ч. Затем отожженный наноалмаз подвергают жидкофазному хлорированию при фотохимическом воздействии видимым светом в течение 36-60 ч при температуре 50-70°C. Затем образец промывают, центрифугируют и высушивают под вакуумом до постоянного веса.
Из хлорированного наноалмаза готовят суспензию в полярном органическом, водно-органическом растворителе или в воде и вносят в нее амикацин с добавлением третичного амина. В качестве органического растворителя предпочтительно использовать те, в которых растворяется антибиотик, например, низшие алифатические спирты, воду или их смеси. Полученную смесь подвергают постоянной ультразвуковой обработке и выдерживании при температуре от 0 до 70°C в течение 1-72 ч. Полученный продукт промывают соответствующим растворителем, центрифугируют и осадок высушивают под вакуумом при 70°C в течение всей ночи.
Полученный по заявляемому способу конъюгат наноалмаза с амикацином может найти широкое применение в медицине в качестве системы доставки амикацина в организм. С этой целью используют электронно-микроскопическое изучение взаимодействия полученного конъюгата с культурами клеток методами клеточной биологии.
Срезы клеток, инкубированных с полученным конъюгатом, получали на ультрамикротоме Leica Ultracut UCT (Leica, Германия). Микрофотографии срезов клеток получали на просвечивающем электронном микроскопе JEM 1230 (JEOL, Япония).
Краткое описание графических материалов.
Фиг.1. Химическое строение амикацина.
Фиг.2. Микрофотография, полученная на сканирующем электронном микроскопе, описываемого коньюгата наноалмаза с амикацином.
Фиг.3. Микрофотография, полученная на просвечивающем электронном микроскопе, описываемого коньюгата наноалмаза с амикацином.
Фиг.4. Распределение размеров частиц описываемого конъюгата наноалмаза с амикацином в суспензии.
Фиг.5. ИК-спектр описываемого конъюгата наноалмаза с амикацином.
Фиг.6. Микрофотография клетки HeLa после инкубации в течение 15 мин с конъюгатом наноалмаза с амикацином, частицы которого проникли в клетку.
Изобретение иллюстрируется следующим примером.
Пример
200 мг исходного наноалмаза отжигают в токе газообразного водорода при температуре 1000°C в течение 6 ч. Затем отожженный наноалмаз подвергают жидкофазному хлорированию молекулярным хлором, растворенном в 40 мл CCl4 до 5,6 мас.% Cl2. Реакцию хлорирования проводят при фотохимическом воздействии видимым светом в течение 48 ч при температуре 60°C. Затем образец промывают CCl4 с центрифугированием суспензии при 6000 об/мин и высушивают под давлением до постоянного веса. Затем из хлорированного наноалмаза получают суспензию, используя 40 мл спиртовой смеси (метанол: изопропанол = 1:1), в которую вносят 200 мг амикацина сульфата с добавлением 3 мл триэтиламина. Полученную смесь выдерживают при постоянной ультразвуковой обработке при температуре при 60°C в течение 48 ч. Полученный продукт промывают большим количеством этанола, затем воды, центрифугируют и высушивают под вакуумом при 60°C в течение всей ночи. Остаточная влажность продукта составляет 1,5%. Выход целевого продукта 184 мг (92%).
Полученный продукт представляет собой темно-серый ультрадисперсный порошок с размерами первичных частиц 2-10 нм с содержанием амикацина 40 мас.% и характеризующийся ИК-спектром в диапазоне 400-1800 см-1: два сильных сигнала при частоте 1630 и 1120 см-1, одна полоса средней интенсивности с максимум 620 см-1 и слабые сигналы при 1458, 1406, 1318, 1046 см-1. Средний размер частиц в суспензии полученного продукта составил 15 нм с распределением по размеру 10-30 нм.
Выдерживание при температуре 30-70°C в течение 1-72 ч и использование в качестве полярного растворителя смеси низших алифатических спиртов и воды приводит к получению конъюгата с аналогичными характеристиками и содержанием амикацина в интервале 18-39 мас.%.
Выдерживание при температуре 0-30°C в течение 4-72 ч и использование в качестве полярного растворителя смеси низших алифатических спиртов и воды приводит к получению конъюгата с аналогичными характеристиками и содержанием амикацина в интервале 1-25,5 мас.%.
Выдерживание при температуре 2-10°C в течение 1-4 ч и использование в качестве полярного растворителя воды приводит к получению конъюгата с аналогичными характеристиками и содержанием амикацина 0,1-0,7 мас.%.
Антибактериальную активность конъюгата определяют микробиологическим способом in vitro. Конъюгат наноалмаза с амикацином и амикацина сульфат растворяют предварительно в стерильной воде для инъекций, затем доводят до рабочей концентрации изотоническим раствором натрия хлорида. Далее готовят серийные двойные разведения испытуемых веществ в питательном бульоне. Питательный мясо-пептонный бульон приготавливливают контролируя рН 7,2-7,4 в течение 18-20 ч. На полученную питательную среду засевают культуры микроорганизмов Bacillus subtilis в количестве 0,1 мл 5·105 клеток. Опытные пробирки инкубируют при температуре 37°C 18-20 часов, после чего проводят контрольные высевы на питательный агар. Чашки с питательным агаром просматривают на отсутствие роста культур микроорганизмов.
Результаты определения активности заявляемого антибактериального средства по оценке минимальной ингибирующей концентрации исследуемых препаратов представлены в таблице.
Полученный конъюгат наноалмаза с амикацином в качестве системы доставки антибиотика аминогликозидного ряда можно использовать для доставки амикацина в организм. Проникновение конъюгата наноалмаза с амикацином в организм подтверждается электронно-микроскопическими исследованиями его взаимодействия с культурой клеток HeLa. Конъюгат наноалмаза с амикацином проникает в клетку уже после времени инкубации 15 мин (Фиг.6). На Фиг.6 изображены проникшие внутрь клетки частицы конъюгата наноалмаза с амикацином. На микрофотографии также видна ультрадисперсная структура частиц наноалмаза, которые выраженно отличаются от клеточных органелл из-за дополнительного контрастирования ионами тяжелых металлов.
Список литературы
1. Cynamon M.., Swenson C.E., Palmer G.S. et al. Liposome-encapsulated-amikacin therapy of Mycobacterium avium complex infection in beige mice. // Antimicrob. Agents Chemother., 1989. V.33. №8. P.1179-1183.
2. USPat 5759571, 1998, E.V.Hersch et al.
3. USPat 2010/0260829 A1, 2010, L.Boni et al.
4. USPat 7879351 B2, 2011, Z.Li et al.
5. USPat 2004/0247682 A1, 2004, C.Popescu et al.
6. USPat 2009/0169635 A1, 2009, J.Schwarz et al.
7. Нанолекарства. Концепции доставки лекарств в нанонауке. / Ред. Алф Лампрехт. - M.: Научный Мир, 2010. С.23.
8. Grangier J.L., Puygrenier M., Gauthier J.C., Couvreur P. Nanoparticles as carriers for growth hormone releasing factors (GRF). // J. Control. Rel., 1991. V.15, P. 3-13.
9. USPat 2009/0226495 A1, 2009, S.C.Picardi, A.Razavi.
10. USPat 2010/0129457 A1, 2010, A.Razavi.
11. USPat 2010/0040672 A1, 2010, D.Ho et al.
12. USPat 2011/0008447 A1, 2011, J.-I.Chao et al.
1. Антибактериальное средство, представляющее собой конъюгат наноалмаза с амикацином с размером частиц 2-10 нм при содержании амикацина от 0,1 до 40 мас.%.
2. Способ получения конъюгата наноалмаза с амикацином по п.1, характеризующийся тем, что модифицированные хлором частицы наноалмаза растворяют в полярном растворителе с образованием суспензии, добавляют амикацина сульфат и третичный амин, полученную смесь обрабатывают ультразвуком с выдерживанием при 0-70°С с последующей промывкой растворителем, центрифугированием и сушкой.
3. Способ по п.2, отличающийся тем, что в качестве третичного амина используют триэтиламин, и в качестве полярного растворителя используют низшие алифатические спирты, водно-спиртовые смеси или воду, и обработку ультразвуком при температуре 0-70°С ведут в течение от 1 до 72 ч.