Ферментный электрод
Иллюстрации
Показать всеИзобретение относится к ферментному электроду, включающему частицы углерода, несущие глюкозодегидрогеназу (GDH) с флавинадениндинуклеотидом (FAD) в качестве кофермента; и электродный слой, контактирующий с указанными частицами углерода, причем частицы углерода и электродный слой состоят из частиц углерода с диаметром частицы не более 100 нм и удельной поверхностью по меньшей мере 200 м2/г. Также изобретение относится к способу получения указанного электрода, а также датчику глюкозы и ферментной топливной батарее, использующим данный электрод. Электрод не требует использования медиатора электронов, позволяя получать высокую величину тока отклика и широкий динамический спектр при использовании в качестве датчика глюкозы. 4 н. и 8 з.п. ф-лы, 9 пр., 14 ил.
Реферат
Область техники
Настоящее изобретение относится к ферментному электроду, на котором помещаются чернила, содержащие глюкозодегидрогеназу, в частности к ферментному электроду, используемому в качестве сенсора глюкозы, чернилам, используемым для изготовления ферментного электрода, и способу изготовления ферментного электрода.
Уровень техники
Ферментный электрод обычно относится к электроду, на поверхности которого фиксирован фермент, такому как золотой электрод, платиновый электрод или углеродный электрод. Обладая преимуществом реакционной специфичности фермента, ферментный электрод широко использовался в качестве биологического датчика для специфичного обнаружения различных физиологически активных веществ. В частности, ферментный электрод можно использовать в качестве датчика глюкозы для измерения концентрации глюкозы в крови как важного маркера при диабете.
Примеры оксидоредуктаз, используемых для ферментного электрода, включают в себя дегидрогеназы, представленные глюкозодегидрогеназой (GDH), и оксигеназы, представленные пиранозооксидазой (GOD). GOD обладает высокой субстратной специфичностью в отношении глюкозы и отличной устойчивостью к нагреванию. Поскольку массовое производство указанного фермента является возможным, затраты на его производство ниже, чем для других ферментов, что является преимуществом. Также маловероятно, что на систему, использующую GDH, будет влиять кислород, растворенный в исследуемом образце. Таким образом, даже когда измерение осуществляется в условиях низкого парциального давления кислорода или даже когда измерение осуществляется при высокой концентрации образца, требующей большого количества фермента, измерение глюкозы может быть точным.
В случаях, когда указанные оксидоредуктазы наносят на ферментный электрод, существует проблема, что величина тока отклика электрода является низкой. Таким образом, авторы настоящего изобретения предложили, для того чтобы улучшить величину тока отклика электрода, ферментный электрод, содержащий белок переноса электронов вместе с медиатором электронов (см. патентный документ 2, ниже).
Медиатор электронов относится к окислительно-восстановительному веществу, такому как небелковый металлический комплекс или органическое соединение, веществу, способному опосредовать перенос электронов с оксидоредуктазы на электрод. Примеры включают в себя феррицианид калия, метосульфат феназина, ферроцен и его производные.
Белок переноса электронов относится к белку, способному восстанавливаться, получая электроны от донора электронов, а затем окисляться, отдавая электроны акцептору электронов в окислительно-восстановительной системе организма. Примеры белка переноса электронов включают в себя цитохром b и цитохром С, и, предпочтительно, цитохром b562 или тому подобное.
В патентном документе 1 белок переноса электронов, вместе с оксидоредуктазой, иммобилизован на электроде, и, таким образом, может осуществляться перенос электронов с оксидоредуктазы на электрод или медиатор электронов, в результате чего получают ферментный электрод с высокой величиной тока отклика.
Для измерения концентрации глюкозы с использованием указанных ферментных электродов, в общих чертах, буфер помещают в термостатную ячейку, и в нее добавляют кофермент, CaCl2 и медиатор электронов. Смесь затем содержат при постоянной температуре. После этого в качестве рабочего электрода используют ферментный электрод, на котором иммобилизован фермент. Используют противоэлектрод (например, платиновый электрод) и электрод сравнения (например, электрод Ag/AgCl). Постоянное напряжение подают на упомянутый выше углеродный электрод, и после достижения электрическим током устойчивого состояния добавляют образец, содержащий глюкозу, а затем измеряют увеличение электрического тока.
Таким образом, указанные обычные способы требуют включения в электрод медиатора электронов или добавления медиатора электронов в термостатную ячейку в виде водного раствора. Также необходимо обеспечивать медиатор электронов отдельно от оксидоредуктазы. Следовательно, процесс был усложненным, и существовали проблемы стоимости массового производства.
Патентный документ 1: JP 2003-121407 A
Патентный документ 2: WO 02/73181
Патентный документ 3: WO 2005/023111
Описание изобретения
Проблемы, которые должны быть решены изобретением
Целью настоящего изобретения является создание ферментного электрода, который не требует использования медиатора электронов и не уступает электродам, в котором используется медиатор электронов, позволяя получать высокую величину тока отклика и широкий динамический спектр при использовании в качестве датчика глюкозы.
Средства решения поставленных задач
В настоящем изобретении было установлено, что когда ферментный электрод состоит из частиц углерода, на которых закреплена глюкозодегидрогеназа, а электродный слой, контактирующий с указанными частицами углерода, используется в качестве датчика для измерения глюкозы, в котором диаметр указанных частиц углерода и/или частиц углерода, составляющих указанный электродный слой, не превышает 10 нм, а его удельная поверхность составляет по меньшей мере 200 м2/г, электроны беспрепятственно перемещаются между упомянутым электродным слоем и частицами углерода, на которых закреплена глюкозодегидрогеназа, или между частицами углерода, составляющими электродный слой, и частицами углерода, на которых закреплена глюкозодегидрогеназа, и, таким образом, можно добиться его функционирования в качестве ферментного электрода.
Таким образом, настоящее изобретение делает возможным усиление тока отклика в ферментном электроде, составленном, как описано выше, путем подбора диаметра частиц и удельной поверхности частиц углерода, на которых закреплена глюкозодегидрогеназа, независимо от формы или размера электродного материала, контактирующего с частицами углерода, на которых закреплена глюкозодегидрогеназа.
Также настоящее изобретение делает возможным дополнительное усиление тока отклика в ферментном электроде, составленном, как описано выше, путем использования частиц углерода в качестве электронного материала, контактирующего с частицами углерода, на которых закреплена глюкозодегидрогеназа, а также подбора диаметра и удельной поверхности частиц.
Точная структура настоящего изобретения следующая:
(1) Ферментный электрод, включающий в себя частицы углерода, несущие глюкозодегидрогеназу (GDH) с флавинадениндинуклеотидом (FAD) в качестве кофермента; и электродный слой, контактирующий с указанными частицами углерода, в котором частицы углерода и/или электродный слой состоят (состоит) из частиц углерода с диаметром частиц не более 100 нм и удельной поверхностью по меньшей мере 200 м2/г.
(2) Ферментный электрод по п. (1), в котором глюкозодегидрогеназа (GDH) представляет собой каталитическую субъединицу оксидоредуктазы или комплекс каталитической субъединицы оксидоредуктазы и субъединицы переноса электронов.
(3) Ферментный электрод по п. (1) или (2), в котором электродный слой состоит из металла.
(4) Ферментный электрод по п. (3), в котором электродный слой состоит из металлической проволоки.
(5) Ферментный электрод по любому из п.п. (1)-(4), который применяют в качестве датчика глюкозы.
(6) Чернильный материал для применения в ферментном электроде, включающий в себя глюкозодегидрогеназу (GDH) с флавинадениндинуклеотидом (FAD) в качестве кофермента; и частицы углерода, имеющие диаметр не более 100 нм и удельную поверхность по меньшей мере 200 м2/г.
(7) Чернильный материал по п. (6), в котором глюкозодегидрогеназа (GDH) представляет собой каталитическую субъединицу оксидоредуктазы или комплекс каталитической субъединицы оксидоредуктазы и субъединицы переноса электронов.
(8) Способ изготовления ферментного электрода, включающий в себя нанесение на поверхность электродного слоя чернильного материала по п. (6) или (7) с последующей сушкой.
Частица углерода, используемая в настоящем изобретении, на которой закреплена глюкозодегидрогеназа (GDH) с флавинадениндинуклеотидом (FAD) в качестве кофермента, характеризуется малым диаметром и большой удельной поверхностью. Предпочтительной является частица углерода, имеющая диаметр не более 100 нм и удельную поверхность по меньшей мере 200 м2/г, и более предпочтительной является частица углерода, имеющая диаметр не более 50 нм и удельную поверхность по меньшей мере 200 м2/г. Примеры указанной частицы углерода включают в себя имеющиеся в продаже сажу Ketchen (диаметр частицы 34 нм, удельная поверхность 1400 м2/г), VULCAN (диаметр частицы 30 нм, удельная поверхность 254 м2/г) и Lion Paste (товарный знак Lion Corporation), содержащую сажу Ketchen.
В настоящем изобретении упомянутые выше частицы углерода смешивают с глюкозодегидрогеназой (GDH), используя флавинадениндинуклеотид (FAD) в качестве кофермента (в настоящем описании “FADGDH”), для изготовления чернильного материала, из которого состоит ферментный электрод. Чернильный материал можно изготавливать добавлением растворителя, например водного раствора пропанола, к частицам углерода, например саже Ketchen, и тщательным перемешиванием смеси.
В настоящем изобретении ферментный электрод, в общих чертах, изготавливают нанесением на электродный слой упомянутого выше чернильного материала.
Для электродного слоя, используемого в настоящем изобретении, можно использовать частицу углерода или металл. Частица углерода с малым диаметром и большой удельной поверхностью является предпочтительной, но специальным образом не ограничивается. Более предпочтительно, частица углерода имеет диаметр не более 100 нм, еще более предпочтительно не более 50 нм, и удельную поверхность по меньшей мере 200 м2/г. Примеры указанной частицы углерода включают в себя имеющиеся в продаже сажу Ketchen (диаметр частицы 34 нм, удельная поверхность 1400 м2/г), VULCAN (диаметр частицы 30 нм, удельная поверхность 254 м2/г) и Lion Paste (товарный знак Lion Corporation), содержащую сажу Ketchen. В тех случаях, когда используется металл, предпочтительно использовать металлическую проволоку, более предпочтительно золотую проволоку или проволоку из нержавеющего металла.
Глюкозодегидрогеназа, используемая в настоящем изобретении, может представлять собой модифицированную оксидоредуктазу, в которой часть натуральной оксидоредуктазы химически модифицирована. Указанный модифицированный фермент можно получать, например, заменой одного или более аминокислотных остатков в белке на другие встречающиеся в естественных условиях или не встречающиеся в естественных условиях аминокислотные остатки, или делецией или добавлением одной или более аминокислот.
Как описано выше, ферментный электрод по настоящему изобретению не требует медиатора электронов для переноса электронов на электродный слой, благодаря подбору диаметра частиц и удельной поверхности частиц углерода, на которых закреплена глюкозодегидрогеназа. Глюкозодегидрогеназа, используемая в настоящем изобретении, с точки зрения функций, состоит из каталитически активной субъединицы, обладающей активностью дегидрогенизации глюкозы, и субъединицы переноса электронов, включающей в себя белок переноса электронов для предоставления электронов с упомянутой выше каталитической субъединицы электродному слою. В данном случае в настоящем изобретении можно использовать одну только каталитическую субъединицу в качестве оксидоредуктазы, или можно использовать комплекс каталитической субъединицы и субъединицы переноса электронов.
Каталитическая субъединица обладает функциями отбора электрона от глюкозы в образце и передачи указанного электрона на субъединицу переноса электронов. Предпочтительно, используют каталитическую субъединицу FADGDH с флавинадениндинуклеотидом (FAD) в качестве кофермента. Таким образом, электрон передается с каталитической субъединицы на субъединицу переноса электронов через восстановленный FAD.
Содержание каталитической субъединицы устанавливается, например, в количестве, соответствующем от 5 до 100 ЕД активности. В данном случае определение единицы фермента (1 ЕД) известно для каждого фермента. Например, в случае GDH, когда обесцвечивание, основанное на восстановлении DCIP (2,6-дихлориндофенола) при обычных условиях проведения теста (рН 6,0, 37°С), измеряют с течением времени на длине волны поглощения 600 нм, которая представляет собой длину волны поглощения DCIP, 1 единица определяется как количество фермента, которое окисляет 1 мкМ глюкозы каждую 1 минуту (коэффициент молярной экстинкции составляет 4,76×1000 мкМ/см).
FADGDH особым образом не ограничивается до тех пор, пока он представляет собой каталитическую субъединицу, обладающую активностью дегидрогенизации глюкозы, или комплекс FADGDH, в котором субъединица переноса электронов связана с упомянутой выше каталитической субъединицей. Из них предпочтительно использовать Burkholderia, в частности штамм Burkholderia cepacia KS1 (в данном описании называемый «штаммом KS1»).
Штамм KS1 представляет собой новый штамм, выделенный из почвы поблизости от горячего источника и идентифицированный как Burkholderia cepacia на основании его микологических свойств. Он был передан на хранение в депозитарий International Patent Organism Depositary, National Institute of Avanced Industrial Science and Technology (AIST Tsukuba Central 6, 1-1-1 Higashi, Tsukuba, Ibaraki, Japan, 305-8566), под инвентарным номером FERM BP-7306, с 25 сентября 2000 г. Подробности о штамме KS1 описаны в WO 02/36779. Он может продуцировать GDH, содержащую субъединицу α (с молекулярной массой приблизительно 60 кДа), которая представляет собой каталитическую субъединицу, субъединицу β (с молекулярной массой приблизительно 43 кДа), соответствующую цитохрому с, который представляет собой субъединицу переноса электронов, и субъединицу γ (с молекулярной массой приблизительно 14 кДа). Молекулярную массу измеряли с использованием электрофореза в SDS-полиакриламидном геле в условиях восстановления.
Для того чтобы изготовить ферментный электрод по настоящему изобретению, глюкозодегидрогеназу или ее комплекс тщательно смешивают с порошками углерода, а полученную смесь помещают на электрод. Для того чтобы иммобилизовать глюкозодегидрогеназу или ее комплекс на частице углерода, после помещения на электрод, как описано выше, например, осуществляют поперечное связывание с использованием бинарного поперечносвязывающего агента, такого как глутаровый альдегид. Альтернативно, также можно осуществлять иммобилизацию с использованием твердого полиэлектролита. В большинстве случаев в качестве твердого полиэлектролита используют Nafion. Пленку из иммобилизованного фермента можно изготовить растворением твердого полиэлектролита, включая Nafion, в растворителе, таком как изопропанол, и добавлением указанной смеси по каплям к ферментной пленке, в которой абсорбирован фермент, или нанесен в форме покрытия и высушен; или смешиванием раствора Nafion с ферментом и сушкой.
Ферментный электрод по настоящему изобретению, в принципе, работает без медиатора электронов. Однако использование медиатора электронов не исключено. В тех случаях, когда используется медиатор электронов, он особым образом не ограничивается, и можно использовать, например, феррицианид калия, метосульфат феназина, комплексы рутения и т.п.
В тех случаях, когда ферментный электрод по настоящему изобретению используется как датчик глюкозы, упомянутый выше ферментный электрод используется как рабочий электрод. Можно использовать противоэлектрод, например платиновый электрод, и электрод сравнения, например электрод Ag/AgCl. Буфер помещают в термостатную ячейку и устанавливают указанные электроды. Затем подают постоянное напряжение на рабочий электрод, и после достижения электрическим током устойчивого состояния в термостатную ячейку помещают образец, содержащий глюкозу, и измеряют увеличение электрического тока. В соответствии с калибровочной кривой, полученной с использованием раствора глюкозы стандартных концентраций, можно рассчитать концентрацию глюкозы в образце.
Помимо этого, при использовании в качестве датчика глюкозы, ферментный электрод можно составить таким образом, чтобы, например, непрерывно измерять концентрацию глюкозы, и несколько измерений глюкозы можно было осуществлять без перерыва. В данном случае датчик глюкозы дополнительно включает в себя коллекторный элемент для сбора крови или интерстициальной жидкости из подкожных тканей, и составлен таким образом, чтобы кровь или интерстициальная жидкость, собранная коллекторным элементом, могла контактировать с электродом.
Упомянутый выше датчик глюкозы можно составить таким образом, чтобы по меньшей мере часть электрода была внедрена в подкожные ткани и использовалась. В данном случае электрод формируют на изолирующем субстрате.
Ферментный электрод по настоящему изобретению можно использовать в качестве анода в ферментной топливной батарее. В данном случае в качестве топлива можно использовать субстрат, соответствующий субстратной специфичности фермента. В качестве катода можно использовать углеродный электрод с подложкой из платины, платиновый электрод и т.п., и можно сконструировать ферментную топливную батарею без разделительной перегородки. В качестве реакционного раствора можно использовать обычный буфер, такой как фосфатный буфер. Его можно в дальнейшем использовать в жидкостях организма. Электродвижущую силу можно подобрать изменением величины сопротивления, приложенного к цепи внешней нагрузки.
Краткое описание чертежей
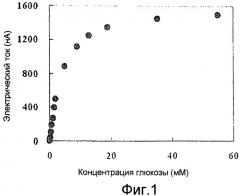
Фиг. 1 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании сажи Ketchen в ферментном FADGDH иммобилизованном слое и при использовании сажи Ketchen в электродном слое.
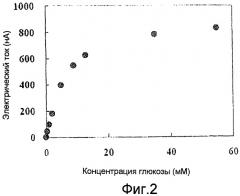
Фиг. 2 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании углеродной пасты в ферментном FADGDH иммобилизованном слое и при использовании сажи Ketchen в электродном материале.
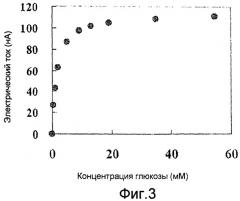
Фиг. 3 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании сажи Ketchen в ферментном FADGDH иммобилизованном слое и при использовании углеродной пасты в электродном материале.
Фиг. 4 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании углеродной пасты в ферментном FADGDH иммобилизованном слое и при использовании углеродной пасты в электродном материале.
Фиг. 5 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании сажи Ketchen, Lion Paste, VULCAN и Denka Black в ферментном FADGDH иммобилизованном слое и при использовании стекловидного углерода в электродном материале.
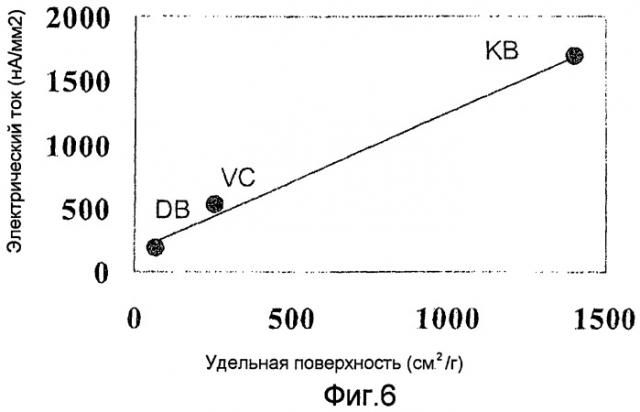
Фиг. 6 показывает корреляцию между удельной поверхностью углеродной частицы ферментного иммобилизованного слоя и величиной тока отклика.
Фиг. 7 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании Lion Paste (W-311N, W-370) в ферментном FADGDH иммобилизованном слое и при использовании стекловидного углерода в электродном материале.
Фиг. 8 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании VULCAN в ферментном FADGDH иммобилизованном слое и при использовании VULCAN в электродном материале.
Фиг. 9 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании Lion Paste (W-311N) в ферментном FADGDH иммобилизованном слое и при использовании золотой проволоки в электродном материале.
Фиг. 10 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании Lion Paste (W-311N) в ферментном FADGDH иммобилизованном слое и при использовании нержавеющей проволоки в электродном материале.
Фиг. 11 показывает корреляцию между концентрацией глюкозы и величиной электрического тока при использовании Lion Paste (W-311N) в ферментном FADGDH иммобилизованном слое и при использовании нержавеющего интегрального электрода в электродном материале.
Фиг. 12 показывает имеющийся в продаже электрод, изготовленный закреплением частиц углерода на полимерном субстрате.
Фиг. 13 показывает кривую отклика после добавления по каплям образцов, содержавших глюкозу, к ферментному электроду, изготовленному нанесением ферментных чернил на электрод, показанный на фиг. 12, и приложения электрического потенциала.
Фиг. 14 показывает, на кривой отклика, показанной на фиг. 13, корреляцию между концентрацией глюкозы в образце и величиной электрического тока через 5 секунд после приложения электрического потенциала.
Лучший способ осуществления настоящего изобретения
Настоящее изобретение далее будет описано подробно с использованием примеров; однако настоящее изобретение ими не ограничивается.
Примеры в случае использования частицы углерода в качестве электродного слоя
Сначала показаны примеры в случаях использования частиц углерода как в электродном слое, так и в ферментном слое.
Пример 1
Сажу Ketchen (далее - КВ) с диаметром частиц 34 нм, удельной поверхностью 1400 м2/г и порозностью 78 об.% использовали в качестве частицы углерода. К КВ (100 мг) добавляли воду Milli Q (400 мкл) и 5% Nafion (48% водный раствор 1-пропанола) (1 мл). Смесь тщательно перемешивали и оставляли стоять в течение 3 дней для получения чернил КВ. Смесь 100 мМ p.p.b. (pH 7,0) (10 мкл) и 8,4 ЕД/мл FADGDH (40 мкл) с чернилами КВ (10 мкл) использовали в качестве чернил FADGDH/КВ. К интегральному электроду (φ0,4 мм), заполненному КВ в качестве электродного материала, по каплям добавляли чернила FADGDH/КВ таким образом, чтобы получить 25 ЕД/мм2, и сушили при 4°С в течение 2 часов. Изготовленный ферментный электрод использовали в качестве рабочего электрода, Pt использовали в качестве противоэлектрода и Ag/AgCl электрод сравнения использовали в качестве электрода сравнения. Фиг. 1 показывает результаты измерений величины тока отклика после добавления глюкозы, при электрическом потенциале +250 мВ, по сравнению с Ag/AgCl, с использованием 100 мМ p.p.b. (pH 7,0) (10 мкл) в качестве реакционного раствора в системе трех электродов. Измерение осуществляли при 37°С, при перемешивании реакционного раствора со скоростью 250 об/мин. Величину тока отклика определяли как разницу, полученную вычитанием величины электрического тока, полученного при концентрации глюкозы 0 мМ, из величины, измеренной для каждой концентрации глюкозы.
Как показано на фиг. 1, при постепенном повышении концентрации глюкозы, наблюдавшаяся величина электрического тока возрастала. При конечной концентрации глюкозы 55 мМ величина тока отклика составляла приблизительно 1500 нА. При концентрации глюкозы 5 мМ плотность тока составляла 6998 нА/мм2. Было подтверждено, что при использовании углеродной частицы КВ с диаметром не более 100 нм и удельной поверхностью по меньшей мере 200 м2/г была получена удовлетворительная величина тока отклика.
Сравнительный пример 1
Изготавливали ферментный электрод, как описано в примере 1, за исключением того, что в качестве частицы углерода вместо КВ использовали СР с диаметром частиц 7000 нм и удельной поверхностью 1 м2/г. То есть к СР (100 мг) добавляли воду Milli Q (400 мкл) и 5% Nafion (48% водный раствор 1-пропанола) (1 мл). Смесь тщательно перемешивали и оставляли стоять в течение 3 дней для получения чернил СР. Смесь 100 мМ p.p.b. (pH 7,0) (10 мкл) и 8,4 ЕД/мл FADGDH (40 мкл) с чернилами СР (10 мкл) использовали в качестве чернил FADGDH/СР. К интегральному электроду (φ0,4 мм), заполненному КВ в качестве электродного материала, по каплям добавляли чернила FADGDH/СР таким образом, чтобы получить 25 ЕД/мм2, и сушили при 4°С в течение 2 часов. Изготовленный ферментный электрод использовали в качестве рабочего электрода, Pt использовали в качестве противоэлектрода и Ag/AgCl электрод сравнения использовали в качестве электрода сравнения. Фиг. 2 показывает результаты измерений величины тока отклика после добавления глюкозы, при электрическом потенциале +250 мВ, по сравнению с Ag/AgCl, с использованием 100 мМ p.p.b. (pH 7,0) (10 мкл) в качестве реакционного раствора в системе трех электродов. Измерение осуществляли при 37°С, при перемешивании реакционного раствора со скоростью 250 об/мин. Величину тока отклика определяли как разницу, полученную вычитанием величины электрического тока, полученного при концентрации глюкозы 0 мМ, из величины, измеренной для каждой концентрации глюкозы.
Как показано на фиг. 2, при постепенном повышении концентрации глюкозы, наблюдавшаяся величина электрического тока возрастала. При конечной концентрации глюкозы 55 мМ величина тока отклика составляла приблизительно 800 нА. При концентрации глюкозы 5 мМ плотность тока составляла 3160 нА/мм2. Было подтверждено, путем сравнения фиг. 1 и фиг. 2, что при использовании интегрального электрода, заполненного тем же КВ в качестве электродного слоя, величина тока отклика уменьшалась с 1500 нА до приблизительно 800 нА, из-за замены чернильного материала, которым был покрыт указанный электрод, чернил FADGDH/КВ на чернила FADGDH/СР. То есть было подтверждено, что при использовании одного и того же электродного слоя, чем меньше диаметр частицы углерода, на которой закреплен фермент, и чем больше ее удельная поверхность, тем выше становится величина тока отклика.
Пример 2
К КВ (100 мг) добавляли воду Milli Q (400 мкл) и 5% Nafion (48% водный раствор 1-пропанола) (1 мл). Смесь тщательно перемешивали и оставляли стоять в течение 3 дней для получения чернил КВ. Смесь 100 мМ p.p.b. (pH 7,0) (10 мкл) и 8,4 ЕД/мл FADGDH (40 мкл) с чернилами КВ (10 мкл) использовали в качестве чернил FADGDH/КВ. К интегральному электроду (φ0,4 мм), заполненному углеродной пастой (СР) в качестве электродного материала, по каплям добавляли чернила FADGDH/КВ таким образом, чтобы получить 25 ЕД/мм2, и сушили при 4°С в течение 2 часов. Фиг. 3 показывает корреляцию между величиной установившегося электрического тока и концентрацией глюкозы в реакционном растворе. Как показано на фиг. 3, в случае настоящего фермента, величина электрического тока при 55 мМ составляла приблизительно 110 нА, несмотря на то что использовалась та же площадь электрода и то же количество фермента. Плотность тока настоящего ферментного электрода при концентрации глюкозы 5 мМ составляла 690 нА/мм2.
Сравнительный пример 2
Изготавливали ферментный электрод, как описано в примере 1, за исключением того, что в качестве частицы углерода вместо КВ использовали углеродную пасту (далее - СР) с диаметром частиц 7000 нм и удельной поверхностью 1 м2/г. К СР (100 мг) добавляли воду Milli Q (400 мкл) и 5% Nafion (48% водный раствор 1-пропанола) (1 мл). Смесь тщательно перемешивали и оставляли стоять в течение 3 дней для получения чернил СР. Смесь 100 мМ p.p.b. (pH 7,0) (10 мкл) и 8,4 ЕД/мл FADGDH (40 мкл) с чернилами СР (10 мкл) использовали в качестве чернил FADGDH/СР. К интегральному электроду (φ0,4 мм), заполненному СР в качестве электродного материала, по каплям добавляли чернила FADGDH/СР таким образом, чтобы получить 25 ЕД/мм2, и сушили при 4°С в течение 2 часов. Фиг. 4 показывает корреляцию между величиной установившегося электрического тока и концентрацией глюкозы в реакционном растворе. Как показано на фиг. 4, в случае электрода FADGDH+СР, величина электрического тока при 55 мМ составляла приблизительно 55 нА, несмотря на то что использовалась та же площадь электрода и то же количество фермента. Плотность тока настоящего ферментного электрода при концентрации глюкозы 5 мМ составляла 330 нА/мм2.
Было подтверждено, сравнением фиг. 3 и фиг. 4, что в случаях, когда использовали интегральный электрод, заполненный той же СР в качестве электродного слоя, величина тока отклика уменьшалась с 690 нА до приблизительно 55 нА, из-за замены чернильного материала, которым был покрыт указанный электрод, чернил FADGDH/КВ на чернила FADGDH/СР. То есть было подтверждено, что при использовании одного и того же электродного слоя, чем меньше диаметр частицы углерода, на которой закреплен фермент, и чем больше ее удельная поверхность, тем выше становится величина тока отклика.
Пример 3
Для того чтобы изучить влияние удельной поверхности частицы углерода, на которой закреплен фермент, с использованием того же электрода из стекловидного углерода (GC) в качестве электродного слоя, измеряли ток отклика, с использованием частицы углерода, помимо КВ, использовавшегося выше, VULCAN (VC, товарный знак Cabot), имеющий диаметр частиц 30 нм и удельную поверхность 254 м2/г, Lion Paste (LP, товарный знак Lion Corporation), которая представляет собой пасту, состоящую из ацетиленовой сажи (Denka Black, DB, Denki Kagaku Kogyo Kabushiki Kaisha), имеющей диаметр частиц 35 нм и удельную поверхность 68 м2/г, и КВ.
Сначала смешивали КВ (100 мг), Milli Q (200 мкл) и 5% Nafion (1200 мкл) для получения чернил КВ. VC (100 мг), Milli Q (200 мкл) и 5% Nafion (1200 мкл) для получения чернил VC. Чернила КВ и чернила VC, 100 мМ p.p.b. (рН 7,0) и 4,6 ЕД/мкл FADGDH смешивали в объемном соотношении 1:3,8:3,2 для получения ферментных чернил КВ и ферментных чернил VC, соответственно. Затем смешивали DB (50 мг), Milli Q (850 мкл) и 5% Nafion (600 мкл) для получения чернил DB. Чернила DB, 100 мМ p.p.b. (рН 7,0) и 4,6 ЕД/мкл FADGDH смешивали в объемном соотношении 1:1,4:1,6 для получения ферментных чернил DB. Также, Lion Paste с КВ в качестве главного компонента, Lion Paste W-311N, 5% Nafion, 100 мМ p.p.b. (рН 7,0) и 4,6 ЕД/мкл FADGDH смешивали в объемном соотношении 1:1:4:4 для получения ферментных чернил LP. Далее, без использования частиц углерода, 5% Nafion, 100 мМ p.p.b. (рН 7,0) и 4,6 ЕД/мкл FADGDH смешивали в объемном соотношении 1:5:4 для получения ферментных чернил.
Ферментные чернила КВ (чернила КВ на фиг. 5), ферментные чернила VC (чернила VC на фиг. 5), ферментные чернила DB (чернила DB на фиг. 5), ферментные чернила Lion Paste (чернила LP на фиг. 5) или ферментные чернила (чернила на фиг. 5) (5 мкл) по каплям добавляли к электроду из полированного стекловидного углерода (GC) (φ3 мм), и сушили при 4°С в течение 2 часов. Указанный электрод подвергали поперечной сшивке с использованием паров 25% раствора глутарового альдегида в течение 30 минут, а затем погружали в 10 мМ Tris-HCl (рН 7,0) на 20 минут. Указанный электрод погружали в 100 мМ p.p.b. (рН 7,0) при 4°C на ночь для уравновешивания. В трехэлектродной системе с использованием изготовленного ферментного электрода в качестве рабочего электрода, Pt в качестве противоэлектрода и Ag/AgCl в качестве электрода сравнения, а также с использованием 100 мМ p.p.b. (рН 7,0) (10 мл) в качестве реакционного раствора, измеряли величину тока отклика после добавления глюкозы, при электрическом потенциале +250 мВ, по сравнению с Ag/AgCl, и получали калибровочную кривую (150 об/мин., 37°С).
Результаты измерений глюкозы с использованием полученного описанным способом ферментного электрода показаны на фиг. 5. По мере возрастания концентрации глюкозы наблюдалось увеличение электрического тока на каждом из ферментных электродов. Из них в случаях, когда использовались ферментные чернила КВ или ферментные чернила Lion Paste, был получен сходный отклик, который был чрезвычайно высоким по сравнению с откликом при использовании других чернил. В случаях, когда использовались ферментные чернила VC, был получен отклик, достаточно высокий, чтобы быть практически приемлемым, в то же время более низкий, чем отклик при использовании двух чернил, указанных выше. Напротив, в случаях, когда использовались ферментные чернила DB, был получен лишь низкий сигнал, как в случае использования ферментных чернил без частиц углерода. Корреляция между величиной тока отклика указанных датчиков при концентрации глюкозы 5 мМ и удельной поверхностью частицы углерода в чернилах показана на фиг. 6. При использовании VULCAN (VC), имеющего удельную поверхность 254 м2/г, был получен фактически удовлетворительный ток отклика, в то время как при использовании ацетиленовой сажи, имеющей удельную поверхность 68 м2/г, удовлетворительный ток отклика получен не был. Таким образом, было показано, что имеет место высокая корреляция между величиной тока отклика и удельной поверхностью используемой частицы углерода, и требуется использовать частицы углерода, имеющие удельную поверхность по меньшей мере 200 м2/г. Также требовался диаметр частицы, не превышающий 100 нм.
Пример 4
Nafion (5%), Lion Paste W-311N или W-370C, 100 мМ p.p.b. (рН 7,0) и 8,4 ЕД/мкл FADGDH смешивали в объемном соотношении 1:1:4:4 для получения ферментных чернил. Каждые ферментные чернила по каплям добавляли к электроду из полированного стекловидного углерода (GC) (φ3 мм) таким образом, чтобы количество FADGDH составляло 17 ЕД (2,4 ЕД/мм2), и сушили при 4°С в течение 2 часов. Указанный электрод подвергали поперечной сшивке с использованием паров 25% раствора глутарового альдегида в течение 30 минут, а затем погружали в 10 мМ Tris-HCl (рН 7,0) при комнатной температуре на 20 минут для удаления непрореагировавшего глутарового альдегида. Указанный дополнительно электрод погружали в 100 мМ p.p.b. (рН 7,0) на 30 минут для уравновешивания. Используя указанные электроды в качестве рабочего электрода, платиновую проволоку в качестве противоэлектрода и Ag/AgCl в качестве электрода сравнения, а также используя 100 мМ p.p.b. (рН 7,0) (10 мл) в качестве реакционного раствора, измеряли величину тока отклика после добавления глюкозы, при электрическом потенциале +250 мВ, по сравнению с Ag/AgCl. Измерение осуществляли при 37°С, при перемешивании реакционного раствора со скоростью 250 об/мин. Величину тока отклика определяли как разницу, полученную вычитанием величины установившегося электрического тока, полученного при концентрации глюкозы 0 мМ, из величины установившегося электрического тока, измеренной для каждой концентрации глюкозы.
Результаты измерений глюкозы с использованием полученного описанным способом ферментного электрода показаны на фиг. 7. По мере повышения концентрации глюкозы наблюдавшаяся величина электрического тока возрастала. В случаях использования в ферментном слое Lion Paste W-311N или W-370C, при концентрации глюкозы 5 мМ, плотность тока составляла 1684 нА/мм2 или 1452 нА/мм2, соответственно. Было подтверждено, что при использовании Lion Paste, имевшей КВ в качестве главного компонента, был получен высокий ток отклика, независимо от типов продуктов.
Пример 5
В качестве частицы углерода использовали VULCAN (VC), имеющий диаметр частиц 30 нм и удельную поверхность 254 м2/г. К VC (100 мг) добавляли Milli Q (400 мкл) и 5% Nafion (48% водный раствор 1-пропанола) (1 мл). Смесь тщательно перемешивали и оставляли стоять в течение 3 дней для получения чернил VC. Смесь 100 мМ p.p.b. (рН 7,0) (10 мкл) и 8,4 ЕД/мкл FADGDH (40 мкл) с чернилами VC (10 мкл) использовали в качестве чернил FADGDH/VUL. К интегральному электроду (φ0,75 мм), заполненному VC в качестве электродного материала, по каплям добавляли чернила FADGDH/VC таким образом, чтобы получить 25 ЕД/мм2, и сушили при 4°С в течение 2 часов. Изготовленный ферментный электрод использовали в качестве рабочего электрода, Pt использовали в качестве противоэлектрода и Ag/AgCl электрод сравнения использовали в качестве электрода сравнения. Фиг. 5 показывает результаты измерений величины тока отклика после добавления глюкозы, при электрическом потенциале +250 мВ, по сравнению с Ag/AgCl, с использованием 100 мМ p.p.b. (pH 7,0) (10 мкл) в качестве реакционного раствора в системе трех электродов. Измерение осуществляли при 37°С, при перемешивании реакционного раствора со скоростью 250 об/мин. Величину тока отклика определяли как разницу, полученную вычитанием величины электрического тока, полученного при концентрации глюкозы 0 мМ, из величины, измеренной для каждой концентрации глюкозы.
Как показано на фиг. 8, при постепенном повышении концентрации глюкозы, наблюдавшаяся величина электрического тока возрастала. При конечной концентрации глюкозы 55 мМ величина тока отклика составляла приблизительно 3500 нА. При концентрации глюкозы 5 мМ плотность тока составляла 2327 нА/мм2. Как описано выше, было подтверждено, что при использовании чернил VC с VC, имеющим диаметр частиц 30 нм и удельную поверхность 254 м2/г, была получена удовлетворительная величина тока отклика как при использовании стекловидного электрода для электродного слоя, как показано в примере 3, так и при использовании VC для электродного слоя, как показано в настоящем примере.
Как описано выше, было подтверждено, что при использовании частицы углерода как для электродного слоя, так и для ферментного слоя, если тот же тип частицы углерода использовали в электродном слое, чем меньше диаметр частицы углерода,