Иммуностимулирующие олигонуклеотиды
Иллюстрации
Показать всеИзобретение относится к области иммунологии. Предложен иммуностимулирующий олигонуклеотид 5' TCGTCGTTTTTCGGTGCTTTT 3'. Описаны варианты применения олигонуклеотида для получения иммуностимулирующего олигонуклеотида с такой же иммуностимулирующей активностью с по меньшей мере одним липофильным замещенным нуклеотидным аналогом или в качестве адъюванта в вакцине для индукции антиген-специфического иммунного ответа. Использование изобретения обеспечивает иммуностимулирующие олигонуклеотид, который вызывает в популяции CD4+ Т-клеток выработку большего количества Т-клеток, секретирующих IFN-гамма и больше полифункциональных Т-клеток, чем ODN 5' TCGTCGTTTTTCGGTCGTTTT 3', что может найти применение в медицине. 3 н. и 22 з.п. ф-лы, 21 ил., 3 табл., 4 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к иммуностимулирующим олигонуклеотидам и способам применения иммуностимулирующих олигонуклеотидов для индукции антиген-специфического иммунного ответа.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Бактериальная ДНК, в отличие от ДНК позвоночных, оказывает иммуностимулирующие эффекты для активации В-клеток и естественных клеток-киллеров (Tokunaga, Т., et al., 1988. Jpn. J. Cancer Res. 79:682-686; Tokunaga, Т., et al., 1984, JNCI 72:955-962; Messina, J.P., et al., 1991, J.Immunol. 147:1759-1764; и обзор в Krieg, 1998, In: Applied Oligonucleotide Technology, C.A.Stein and A.M.Krieg, (Eds.), John Wiley and Sons, Inc., New York, N.Y., pp.431-448). В настоящее время понятно, что такие иммуностимулирующие эффекты бактериальной ДНК являются результатом присутствия неметилированных CpG-динуклеотидов в окружении конкретных оснований (CpG-мотивов), обычных в бактериальной ДНК, но метилированных и редко присутствующих в ДНК позвоночных (Krieg et al, 1995 Nature 374:546-549; Krieg, 1999 Biochim. Biophys. Acta 1489:107-116). Иммуностимулирующие эффекты бактериальной ДНК можно имитировать синтетическими олигодезоксинуклеотидами (ODN), содержащими эти CpG-мотивы. Такие CpG ODN оказывают сильные стимулирующие эффекты на человеческие и мышиные лейкоциты, включая пролиферацию В-клеток; секрецию цитокинов и иммуноглобулинов;
цитолитическую активность естественных клеток-киллеров (NK) и секрецию интерферона-гамма (IFN-гамма); и активацию дендритных клеток (DC) и других антиген-представляющих клеток для экспрессии костимулирующих молекул и секреции цитокинов, особенно цитокинов Th1-типа, которые важны для стимуляции развития Т-клеточных ответов ТМ-типа. Эти иммуностимулирующие эффекты нативного фосфодиэфирного скелета CpG ODN высоко специфичны в отношении CpG, поскольку данные эффекты значительно уменьшаются, если CpG-мотив метилирован, заменен на GpC, или иным образом удален или изменен (Krieg et al., 1995 Nature 374:546-549; Hartmann et al., 1999 Proc. Natl. Acad. Sci. USA 96:9305-10).
Ранее сообщалось о том, что иммуностимулирующая активность CpG-олигонуклеотидов зависит от количества CpG-мотивов, последовательностей, фланкирующих CG-динуклеотид, расположения CpG-мотива(ов) и расстояния между CpG-мотивами (Ballas et al., 1996, J. Immunol. 157(5): 1840-5; Hartmann et al., 2000, J. Immunol., 164(3): 1617-24; Klinman et al., 2003, Clin. Exp. Immunol., 133(2): 227-32). В данной заявке описан иммуностимулирующий олигонуклеотид, в котором удален 3' CpG-мотив и который неожиданно сохраняет свою иммуностимулирующую активность. Также описана вакцина, содержащая иммуностимулирующий олигонуклеотид и антиген, и способы применения такой вакцины.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В аспектах изобретения предложен иммуностимулирующий олигонуклеотид, содержащий нуклеотидную последовательность 5' TCGTCGTTTTTCGGTGCTTTT 3' (SEQ ID NO:1). В некоторых воплощениях иммуностимулирующий олигонуклеотид содержит одну или более модифицированных связей. В некоторых воплощениях иммуностимулирующий олигонуклеотид содержит одну или более фосфоротиоатных связей. В некоторых воплощениях все межнуклетидные связи в олигонуклеотиде представляют собой фосфоротиоатные связи. В некоторых воплощениях иммуностимулирующий олигонуклеотид содержит по меньшей мере один липофильный замещенный нуклеотидный аналог и пиримидин-пуриновый динуклеотид.
В аспектах изобретения предложена вакцина, содержащая антиген и иммуностимулирующий олигонуклеотид, содержащий нуклеотидную последовательность SEQ ID NO:1, дополнительно содержащая фармацевтически приемлемый носитель. В некоторых воплощениях иммуностимулирующий олигонуклеотид присутствует в количестве, эффективном для индукции антиген-специфического иммунного ответа. В других воплощениях индуцируемый антиген-специфический иммунный ответ представляет собой Th1-иммунный ответ. В некоторых воплощениях антиген представляет собой микробный антиген, аутоантиген или вещество, вызывающее привыкание. В других воплощениях бактериальный антиген ассоциирован с Staphylococcus aureus, или бактериальный антиген ассоциирован с бактерией, вызывающей кариес зубов. В других воплощениях бактерия представляет собой Streptococcus mutans, Streptococcus sobrinus, Streptococcus sanguis, Lactobacillus acidophilis или Actinomyces viscosus. В других воплощениях бактериальный антиген ассоциирован с бактерией, вызывающей периодонтальное заболевание. В других воплощениях бактерия представляет собой Porphyromonas gingivalis или Actinobacillus actinomycetemcomitans. В некоторых воплощениях вирусный антиген ассоциирован с респираторно-синцитиальным вирусом (RSV), вирусом простого герпеса 1, вирусом простого герпеса 2, вирусом иммунодефицита человека-1 (HIV-1) или HIV-2. В других воплощениях паразитарный антиген ассоциирован с паразитом, вызывающим малярию. В некоторых воплощениях аутоантиген представляет собой опухолевый антиген, антиген, ассоциированный с болезнью Альцгеймера, антиген против человеческого антитела, или антиген, который экспрессируется из человеческих эндогенных ретровирусных элементов. В других воплощениях опухолевый антиген представляет собой HER2 (рецептор человеческого эпидермального фактора роста 2), MAGE (антиген, ассоциированный с меланомой), NY-ESO (раково-тестикулярный антиген), PSA (простатспецифический антиген), СЕА (карциноэмбриональный антиген) или вариант EGFR (рецептор эпидермального фактора роста). В других воплощениях, где антиген ассоциирован с болезнью Альцгеймера, антиген представляет собой tau или β-амилоид. В некоторых воплощениях антиген представляет собой IgE. В некоторых воплощениях антиген представляет собой никотиновый гаптен, конъюгированный с носителем. В других воплощениях носитель, с которым конъюгирован никотиновый гаптен, представляет собой дифтерийный токсин (DT). В других воплощениях антиген представляет собой пептид, рекомбинантный белок, очищенный белок, цельный убитый патоген, живой ослабленный вирус или вирусный вектор, живую ослабленную бактерию или бактериальный вектор, полисахарид, гаптен или кодируется плазмидной ДНК.
В некоторых воплощениях антиген конъюгирован с носителем. В других воплощениях носитель представляет собой дифтерийный токсин (DT). В других воплощениях носитель представляет собой вирусоподобную частицу. В других воплощениях вирусоподобная частица представляет собой РНК-фаг Q-β, поверхностный антиген гепатита В (HBsAg) или коровый антиген гепатита В (HBcAg). В некоторых воплощениях вакцина дополнительно содержит один или более адъювантов. В других воплощениях адъювант представляет собой агонист Toll-подобного рецептора (TLR), который не является TLR9. В других воплощениях агонист представляет собой агонист TLR3. В других воплощениях агонист TLR3 представляет собой стабилизированную poly I:C (полиинозиновая-полицитидиловая кислота). В некоторых воплощениях агонист представляет собой агонист TLR4. В других воплощениях агонист TLR4 представляет собой производное липополисахарида (LPS). В других воплощениях производное LPS представляет собой MPL (монофосфориллипид А) или GLA (гамма-линоленовая кислота). В других воплощениях агонист представляет собой агонист TLR5. В других воплощениях агонист TLR5 педставляет собой флагеллин. В некоторых воплощениях агонист представляет собой агонист TLR7 или 8. В других воплощениях агонист TLR7 или 8 представляет собой небольшую молекулу имидазохинолинового семейства. В других воплощениях адъювант представляет собой соль алюминия. В других воплощениях соль алюминия представляет собой гидрат окиси алюминия. В некоторых воплощениях адъювант представляет собой иммуностимулирующий комплекс (ISCOM). В других воплощениях адъювант представляет собой эмульсию масло-в-воде или вода-в-масле. В некоторых воплощениях адъювант представляет собой липосому. В других воплощениях адъювант представляет собой систему доставки. В других воплощениях система доставки представляет собой наночастицу или микрочастицу.
В некоторых воплощениях иммуностимулирующий олигонуклеотид содержит одну или более модифицированных связей. В других воплощениях иммуностимулирующий олигонуклеотид содержит одну или более фосфоротиоатных связей. В некоторых воплощениях все междуклеотидные связи в олигонуклеотиде представляют собой фосфоротиоатные связи. В других воплощениях иммуностимулирующий олигонуклеотид содержит по меньшей мере один липофильный замещенный нуклеотидный аналог и пиримидин-пуриновый динуклеотид. В некоторых воплощениях вакцина приготовлена для введения. В других воплощениях вакцина приготовлена для введения парентеральным путем, где парентеральный путь представляет собой внутримышечный, подкожный, интрадермальный, внутривенный или интраперитонеальный путь. В дополнительных воплощениях вакцина приготовлена для введения местным путем, где местный путь представляет собой кожный, трансдермальный пути или путь через поверхность слизистой оболочки. В других воплощениях путь через поверхность слизистой оболочки представляет собой пероральный, интраназальный, интравагинальный, интраректальный, интрабуккальный или внутриглазной путь.
В некоторых аспектах изобретения способ индукции антиген-специфического иммунного ответа у субъекта, нуждающемся в этом, включает введение субъекту антигена и иммуностимулирующего олигонуклеотида, содержащего нуклеотидную последовательность SEQ ID NO:1 в количестве, эффективном для индукции у указанного субъекта антиген-специфического иммунного ответа. В некоторых воплощениях антиген представляет собой микробный антиген, аутоантиген или вещество, вызывающее привыкание. В других воплощениях микробный антиген представляет собой бактериальный антиген, вирусный антиген или паразитарный антиген. В других воплощениях бактериальный антиген ассоциирован с Staphylococcus aureus, или бактериальный антиген ассоциирован с бактерией, вызывающей кариес зубов. В других воплощениях бактерия представляет собой Streptococcus mutans, Streptococcus sobrinus, Streptococcus sanguis, Lactobacillus acidophilis или Actinomyces viscosus. В других воплощениях бактериальный антиген ассоциирован с бактерией, вызывающей периодонтальное заболевание. В других воплощениях бактерия представляет собой Porphyromonas gingivalis или Actinobacillus actinomycetemcomitans. В некоторых воплощениях вирусный антиген ассоциирован с респираторно-синцитиальным вирусом (RSV), вирусом простого герпеса 1, вирусом простого герпеса 2, вирусом иммунодефицита человека-1 (HIV-1) или HIV-2. В других воплощениях паразитарный антиген ассоциирован с паразитом, вызывающим малярию. В некоторых воплощениях аутоантиген представляет собой опухолевый антиген, антиген, ассоциированный с болезнью Альцгеймера, антиген против человеческого антитела или антиген, который экспрессируется из человеческих эндогенных ретровирусных элементов. В других воплощениях опухолевый антиген представляет собой HER2, MAGE, NY-ESO, PSA, СЕА или вариант EGFR. В других воплощениях, где антиген ассоциирован с болезнью Альцгеймера, антиген представляет собой tau или β-амилоид. В некоторых воплощениях антиген представляет собой IgE. В некоторых воплощениях антиген представляет собой никотиновый гаптен, конъюгированный с носителем. В других воплощениях носитель, с которым конъюгирован никотиновый гаптен, представляет собой дифтерийный токсин (DT). В других воплощениях антиген представляет собой пептид, рекомбинантный белок, очищенный белок, цельный убитый патоген, живой ослабленный вирус или вирусный вектор, живую ослабленную бактерию или бактериальный вектор, полисахарид, гаптен или кодируется плазмидной ДНК.
В некоторых воплощениях антиген конъюгирован с носителем. В других воплощениях носитель представляет собой дифтерийный токсин (DT). В других воплощениях носитель представляет собой вирусоподобную частицу. В других воплощениях вирусоподобная частица представляет собой РНК-фаг Q-β, поверхностный антиген гепатита В (HBsAg) или коровый антиген гепатита В (HBcAg). В некоторых воплощениях вакцина дополнительно содержит один или более адъювантов. В других воплощениях адъювант представляет собой агонист Toll-подобного рецептора (TLR), который не является TLR9. В других воплощениях агонист представляет собой агонист TLR3. В других воплощениях агонист TLR3 представляет собой стабилизированную poly I:C. В некоторых воплощениях агонист представляет собой агонист TLR4. В других воплощениях агонист TLR4 представляет собой производное липополисахарида (LPS). В дополнительных воплощениях производное LPS представляет собой MPL или GLA. В других воплощениях агонист представляет собой агонист TLR5. В других воплощениях агонист TLR5 представляет собой флагеллин. В некоторых воплощениях агонист представляет собой агонист TLR7 или 8. В других воплощениях агонист TLR7 или 8 представляет собой небольшую молекулу имидазохинолинового семейства. В других воплощениях адъювант представляет собой соль алюминия. В других воплощениях соль алюминия представляет собой гидрат окиси алюминия. В некоторых воплощениях адъювант представляет собой иммуностимулирующий комплекс (ISCOM). В других воплощениях адъювант представляет собой эмульсию масло-в-воде или вода-в-масле. В некоторых воплощениях адъювант представляет собой липосому. В других воплощениях адъювант представляет собой систему доставки. В других воплощениях система доставки представляет собой наночастицу или микрочастицу.
В некоторых воплощениях иммуностимулирующий олигонуклеотид содержит одну или более модифицированных связей. В других воплощениях иммуностимулирующий олигонуклеотид содержит одну или более фосфоротиоатных связей. В некоторых воплощениях все межнуклетидные связи в олигонуклеотиде представляют собой фосфоротиоатные связи. В других воплощениях иммуностимулирующий олигонуклеотид содержит по меньшей мере один липофильный замещенный нуклеотидный аналог и пиримидин-пуриновый динуклеотид. В некоторых воплощениях антиген и/или иммуностимулирующий олигонуклеотид готовят для введения. В других воплощениях антиген и/или иммуностимулирующий олигонуклеотид готовят для введения парентеральным путем, где парентеральный путь представляет собой внутримышечный, подкожный, интрадермальный, внутривенный или интраперитонеальный путь. В дополнительных воплощениях антиген и/или иммуностимулирующий олигонуклеотид готовят для введения местным путем, где местный путь представляет собой кожный, трансдермальный пути или путь через поверхность слизистой оболочки. В других воплощениях путь через поверхность слизистой оболочки представляет собой пероральный, интраназальный, интравагинальный, интраректальный, интрабуккальный или внутриглазной путь. В некоторых воплощениях антиген и иммуностимулирующий олигонуклеотид вводят таким же, похожим или другим путем. В других воплощениях антиген и иммуностимулирующий олигонуклеотид вводят вместе, одновременно или раздельно. В других воплощениях антиген и иммуностимулирующий олигонуклеотид вводят в течение 24 часов относительно друг друга. В некоторых воплощениях субъект представляет собой вид, которого лечит ветеринарный врач. В других воплощениях субъект представляет собой субъекта, отличного от грызуна. В некоторых воплощениях субъект представляет собой человека.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
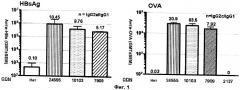
Фиг.1: Усиление гуморальных иммунных ответов у мышей. Взрослых (6-8 недель; n=10/группу) мышей иммунизировали 1 мкг HBsAg (левая панель) или 20 мкг OVA (овальбумин) (правая панель) без адъюванта или в комбинации с CPG 24555, 10103 или 7909 (10 мкг) или не-CpG контрольным ODN 2137 (10 мкг; только с OVA). Плазму через 2 недели (для HBsAg) или 1 неделю (для OVA) после последней иммунизации анализировали в отношении антиген-специфических общих уровней IgG, IgG1 и IgG2a/c (антитела против HBs или антитела против OVA). Каждая горизонтальная черта представляет среднее геометрическое (±SEM (стандартная ошибка среднего)) титров общего IgG. Титры определяли как наибольшее разведение, дающее в результате значение абсорбции, вдвое превышающее абсорбцию для неиммунизированной плазмы с величиной отсечения 0,05. Числа, указанные над каждой горизонтальной чертой, представляют отношение антиген-специфический IgG2a(или 2c)/IgG1.
Фиг.2: Природа гуморального иммунного ответа, индуцируемого у мышей. Взрослых (6-8 недель; n=10/группу) мышей иммунизировали 1 мкг HBsAg (левая панель) или 20 мкг OVA (правая панель без адъюванта или в комбинации с CPG 24555, 10103 или 7909 (10 мкг) или не-CpG контрольным ODN 2137 (10 мкг; только с OVA). Плазму через 2 недели (для HBsAg) или 1 неделю (для OVA) после последней иммунизации анализировали в отношении уровней IgG1 (неокрашенные столбики) и IgG2a или IgG2c (черные столбики) против HBsAg (антитела против HBs) или OVA (антитела против OVA). Каждая горизонтальная черта представляет среднее геометрическое (±SEM) титра разведения для конечной точки согласно ELISA (иммуноферментный анализ) для всей группы (n=10). Титры определяли как наибольшее разведение, дающее в результате значение абсорбции, вдвое превышающее абсорбцию для неиммунизированной плазмы с величиной отсечения 0,05.
Фиг.3: Цитотоксические Т-лимфоцитарные ответы, индуцированные у мышей. Взрослых (6-8 недель; n=5/группу) мышей иммунизировали 1 мкг HBsAg (левая панель) или 20 мкг OVA (правая панель без адъюванта или в комбинации с CPG 24555, 10103 или 7909 (10 мкг) или не-CpG контрольным ODN 2137 (10 мкг; только с OVA). Спленоциты через 2 недели (для HBsAg) или 1 неделю (для OVA) после последней иммунизации анализировали в отношении антиген-специфических CTL ответов с использованием стандартного анализа высвобождения 51Cr.
Фиг.4: Отсутствие CpG-опосредованного усиления CTL ответов у мышей, дефектных по TLR9. Дефектных по TLR9 взрослых (6-8 недель; n=5 группу) мышей иммунизировали 20 мкг OVA без адъюванта или в комбинации с CPG 24555, 10103 или 7909 (10 мкг), или не-CpG контрольным ODN 2137 (10 мкг). Спленоциты через 1 неделю после последней иммунизации анализировали в отношении OVA-специфических CTL ответов с использованием стандартного анализа высвобождения 51Cr.
Фиг.5: OVA-специфические CD8 Т-клетки у дикого типа по сравнению с дефектными по TLR9 мышами. Взрослых (6-8 недель; n=5/группу) мышей дикого типа и дефектных по TLR9 иммунизировали 20 мкг OVA без адъюванта или в комбинации с CPG 24555, 10103 или 7909 (10 мкг) или не-CpG контрольным ODN 2137 (10 мкг). Спленоциты через 1 неделю после последней иммунизации анализировали в отношении OVA-специфических CD8 Т-клеток с использованием тетрамеров МНС класс I Н-2 т.п.н. - SIINFEKL.
Фиг.6: Антиген-специфическая секреция IFN-g у мышей. Взрослых (6-8 недель; n=5/группу) мышей иммунизировали 1 мкг HBsAg (левая панель) или 20 мкг OVA (правая панель без адъюванта или в комбинации с CPG 24555, 10103 или 7909 (10 мкг), или не-CpG контрольным ODN 2137 (10 мкг; только с OVA). Спленоциты через 2 недели (для HBsAg) или 1 неделю (для OVA) после последней иммунизации стимулировали соответствующим антигеном, как представлено на чертежах, в течение 72 ч, и культуральные супернатанты анализировали в отношении IFN-γ с помощью ELISA.
Фиг.7: Отсутствие CpG-опосредованного увеличения антиген-специфической секреции IFN-g у дефектных по TLR9 мышей. Дефектных по TLR9 взрослых (6-8 недель; n=5/группу) мышей иммунизировали 20 мкг OVA без адъюванта или в комбинации с CPG 24555, 10103 или 7909 (10 мкг), или не-CpG контрольным ODN 2137 (10 мкг). Спленоциты через 1 неделю после последней иммунизации стимулировали OVA в концентрациях 0, 0,5 и 1 мг/мл в течение 72 ч, и культуральные супернатанты анализировали в отношении IFN-γ с помощью ELISA.
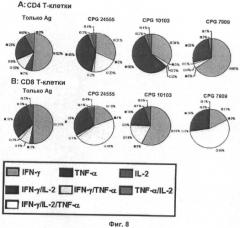
Фиг.8: Антиген-специфические популяции Т-клеток, секретирующих множество цитокинов, у мышей. Взрослых (6-8 недель; n=5/группу) мышей иммунизировали 1 мкг HBsAg только с антигеном или в комбинации с CPG 24555, 10103 или 7909 (10 мкг). Спленоциты через 2 недели после иммунизации повторно стимулировали антигеном HBsAg (для CD4) или пептидом HBs класса I (для CD8), и CD4 (панель А) и CD8 (панель В) Т-клеточные популяции, секретирующие IFN-γ, TNF-α и/или IL-2, количественно оценивали с использованием проточной цитометрии.
Фиг.9: Врожденный иммунитет у человеческих РВМС (мононуклеарные клетки периферической крови). Человеческие РВМС (5×106/мл) инкубировали с различными концентрациями CPG 10103, CPG 24555 или не-CpG контрольным ODN 22881 в течение 24 или 48 ч. Клеточные супернатанты собирали и анализировали в отношении секреции цитокинов/хемокинов с использованием имеющегося в продаже набора для ELISA. На Фиг.9А представлена секреция IFN-α, МСР-1 и IP-10. На Фиг.9В представлена секреция IL-6, IL-10 и IL-2R.
Фиг.10: Врожденный иммунитет in vivo у мышей BALB/c. Мышам BALB/c (n=5/группу) подкожно инъецировали PBS (забуференный фосфатами физиологический раствор) (контроль плацебо), CPG 24555, CPG 10103 или не-CpG контрольный ODN 2137 в дозе 100 мкг. У животных брали кровь через 3 часа после инъекции и плазму анализировали в отношении IP-10 (Фиг.10А) и IL-12 (Фиг.10В) или IL-6 (Фиг.10С) с использованием имеющегося в продаже ELISA.
Фиг.11: Гуморальный иммунитет in vivo у мышей BALB/c. Мышей BALB/c иммунизировали внутримышечно HBsAg (1 мкг) ±CPG 24555 или 10103 (10 мкг), OVA (20 мкг)±CPG 24555 или 10103 (10 мкг), или НА вируса гриппа А Texas 1/77, H3N2 (1 мкг) ± квасцы (Alum) (25 мкг Al3+), ±CPG 24555 или 10103 (10 мкг). Мышей иммунизировали на 0 и 14 сутки (HBsAg), на 0, 7 и 21 сутки (OVA) или только на 0 сутки (НА). На Фиг.11А представлены HBsAg-специфические общие титры IgG через 2 недели после иммунизации, измеренные с помощью ELISA в конечной точке. На Фиг.11В представлены OVA-специфические общие титры IgG через 1 неделю после последней иммунизации. На Фиг.11С представлена кинетика НА-специфического общего IgG в различные моменты времени после иммунизации, измеренные с помощью ELISA в конечной точке.
Фиг.12: Т-клеточные ответы у мышей BALB/c. Мышам BALB/c инъецировали внутримышечно HBsAg (1 мкг) с CPG ODN 2455, CPG 10103 или не-CpG контрольным ODN 2137 в дозе 10 мкг или без них. Мышей инъецировали на 0 и 14 сутки. На Фиг.12А продемонстрированы HBsAg-специфические CTL, измеренные по высвобождению 51Cr через 2 недели после иммунизации. Мышам C57bl/6 инъецировали внутримышечно OVA (20 мкг) с CPG ODN 2455, CPG 10103 или не-CpG контрольным ODN 2137 в дозе 10 мкг или без них. Мышей инъецировали на 0, 7 и 21 сутки. На Фиг.12В представлены OVA-специфические CTL, измеренные по высвобождению 51Cr через 1 неделю после последней иммунизации.
Фиг.13: Т-клеточные ответы у мышей BALB/c. Мышам BALB/c инъецировали внутримышечно HBsAg (1 мкг) с CPG ODN 2455, CPG 10103 или не-CpG контрольным ODN 2137 в дозе 10 мкг или без них. Мышей инъецировали на 0 и 14 сутки. Спленоциты, собранные через 2 недели после последней иммунизации, инкубировали с соответствующим антигеном в течение 72 часов, и культуральные супернатанты тестировали в отношении IFN-γ с помощью ELISA (Фиг.13А). Мышам C57bl/6 инъецировали внутримышечно OVA (20 мкг) с CPG ODN 2455, CPG 10103 или не-CpG контрольным ODN 2137 в дозе 10 мкг или без них. Мышей инъецировали на 0,7 и 21 сутки. Спленоциты через 1 неделю после последней иммунизации инкубировали с соответствующим антигеном в течение 72 часов, и культуральные супернатанты тестировали в отношении IFN-γ с помощью ELISA (Фиг.13В).
Фиг.14: Антитела против HA через 6 недель после иммунизации. Самок мышей BALB/c иммунизировали НА (1 мкг) ± CpG или контрольным ODN (10 мкг) ± квасцы (25 мкг Al3+) в общем объеме 50 мкл. Количество анти-НА измеряли через 6 недель после иммунизации.
Фиг.15: Титры ингибирования гемагглютинации (HIA) через 4 недели после иммунизации. Функциональную активность антител оценивали с использованием анализа ингибирования гемагглютинации (HIA). Измеряли способность увеличивать титры только HIA или в комбинации с квасцами.
Фиг.16: HA-специфическая секреция IFN-γ. Самок мышей BALB/c иммунизировали НА (1 мкг) ± CpG или контрольным ODN (10 мкг) ± квасцы (25 мкг Al3+) в общем объеме 50 мкл. Спленоциты, собранные через 6 недель после иммунизации, использовали для анализа антиген-специфической секреции IFN-γ.
Фиг.17: Гуморальные ответы у приматов, отличных от человека. Яванских макак (Cynomolgus monkeys) (возраст 3-5 лет; n=5 на группу) иммунизировали только Engerix-B (10 мкг HBsAg; 250 мкг Al3+) или в комбинации с 0,5 мг CPG 7909 или CPG 24555 посредством внутримышечной инъекции на 0, 4 и 8 неделю. У животных брали кровь через регулярные интервалы времени и титр HBsAg-специфического антитела измеряли с использованием имеющихся в продаже наборов (MONOLIS™ анти-HBs).
Фиг.18: Гуморальные ответы у приматов, отличных от человека. Яванских макак (возраст 3-5 лет; n=5 на группу) иммунизировали только Engerix-B (10 мкг HBsAg; 250 мкг Al3) или в комбинации с 0,5 мг CPG 7909 или CPG 24555 посредством внутримышечной инъекции на 0, 4 и 8 неделю. Плазму через 4 недели после 2-й иммунизации и 2 недели после 3-й иммунизации анализировали в отношении авидности антитела с использованием способа вытеснения тиоцианата натрия.
Фиг.19: Т-клеточные ответы у приматов, отличных от человека: Яванских макак (возраст 3-5 лет; n=5 на группу) иммунизировали только Engerix-B (10 мкг HBsAg; 250 мкг Al3) или в комбинации с 0,5 мг CPG 7909 или CPG 24555 посредством внутримышечной инъекции на 0, 4 и 8 неделю. Мононуклеарные клетки периферической крови (РВМС) до вакцинации и в некоторые временные точки после вакцинации тестировали в отношении HBsAg-специфической, опосредованной CD4 Т-клетками внутриклеточной секреции цитокинов с помощью проточной цитометрии. На Фиг.19А представлена секреция IFN-γ. На Фиг.19В представлена секреция IL-2. На Фиг.19С представлена секреция TNF-α.
Фиг.20: Т-клеточные ответы: Полифункциональные CD4 Т-клетки; Количественный анализ. Яванских макак (возраст 3-5 лет; n=5 на группу) иммунизировали только Engerix-B (10 мкг HBsAg; 250 мкг Al3) или в комбинации с 0,5 мг CPG 7909 или CPG 24555 посредством внутримышечной инъекции на 0, 4 и 8 неделю. Мононуклеарные клетки периферической крови (РВМС) через 2 недели после 3-й иммунизации тестировали в отношении HBsAg-специфических CD4 Т-клеток, секретирующих один, два или три цитокина, с помощью проточной цитометрии. На Фиг.20А представлено количество HBsAg-специфических CD4 Т-клеток, секретирующих один, два или три цитокина на один миллион проанализированных CD4 Т-клеток. На Фиг.20В представлена доля Т-клеток, продуцирующих один, два или три цитокина, в общей популяции HBsAg-специфических CD4 Т-клеток.
Фиг.21: Т-клеточные ответы: полифункциональные CD4 Т-клетки; Количественный анализ. Измеряли количество клеток, секретирующих IL-2, IFN-γ и TNF-α, или комбинации этих цитокинов. Яванских макак (возраст 3-5 лет; n=5 на группу) иммунизировали только Engerix-B (10 мкг HBsAg; 250 мкг Al3+) или в комбинации с 0,5 мг CPG 7909 или CPG 24555 посредством внутримышечной инъекции на 0, 4 и 8 неделю. Мононуклеарные клетки периферической крови (РВМС) через 2 недели после 3-й иммунизации тестировали в отношении количества HBsAg-специфических CD4 Т-клеток, секретирующих IL-2, IFN-γ и TNF-α или комбинации этих цитокинов, с помощью проточной цитометрии.
ОПИСАНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO:1 - Нуклеотидная последовательность иммуностимулирующего олигонуклеотида ODN CPG 24555.
SEQ ID NO:2 - Нуклеотидная последовательность иммуностимулирующего олигонуклеотида CPG 10103.
SEQ ID NO:3 - Нуклеотидная последовательность иммуностимулирующего олигонуклеотида CPG 7909.
SEQ ID NO:4 - Нуклеотидная последовательность не-CpG олигонуклеотида 22881.
SEQ ID NO:5 - Нуклеотидная последовательность не-CpG олигонуклеотида 2137.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Аспекты изобретения основаны частично на неожиданном обнаружении того, что удаление CpG-мотива из иммуностимулирующего олигонуклеотида не оказывало отрицательного влияния на способность иммуностимулирующего олигонуклеотида усиливать антиген-специфические иммунные ответы. Также неожиданно обнаружили, что удаление указанного CpG-мотива обеспечивает продукцию популяции антиген-специфических Т-клеток, которая отличается. В частности, было обнаружено, что указанная популяция антиген-специфических Т-клеток содержит больше Т-клеток, секретирующих IFN-гамма, и больше полифункциональных Т-клеток.
В аспектах изобретения иммуностимулирующий олигонуклеотид имеет последовательность нуклеиновой кислоты 5' TCGTCGTTTTTCGGTGCTTTT 3' (ODN CPG 24555; SEQ ID NO:1). Последовательность нуклеиновой кислоты иммуностимулирующего олигонуклеотида SEQ ID NO:1 отличается от ранее приведенной последовательности 5' TCGTCGTTTTTCGGTCGTTTT 3' (SEQ ID NO:2) иммуностимулирующего олигонуклеотида (ODN 10103) путем обращения 3'-ближайшего CG-динуклеотида. Сходство активности между двумя иммуностимулирующими олигонуклеотидами является неожиданным, поскольку ранее сообщалось о том, что иммуностимулирующая активность CpG-олигонуклеотидов зависит от количества CpG-мотивов, последовательностей, фланкирующих CG-динуклеотид, расположения CpG-мотива(ов) и расстояния между мотивами CpG (Ballas et al., 1996,, J. Immunol. 157(5): 1840-5; Hartmann et al., 2000, J. Immunol., 164(3): 1617-24; Klinman et al., 2003, Clin. Exp.Immunol., 133(2): 227-32). Удаление 3'-ближайшего CG-динуклеотида из иммуностимулирующего олигонуклеотида CPG ODN 24555 (SEQ ID NO:1) не приводило к отрицательному эффекту на способность этого иммуностимулирующего олигонуклеотида усиливать антиген-специфические иммунные ответы, как можно было бы ожидать из предшествующего описания. CPG ODN 24555 демонстрировал сходную и в некоторых случаях повышенную иммуностимулирующую активность по сравнению с CPG ODN 10103.
Кроме того, было обнаружено, что CPG ODN 24555 индуцирует другую популяцию антиген-специфических Т-клеток по сравнению с CPG ODN 10103 (см. Фиг.8, таблица 1 и таблица 2). В частности, неожиданно обнаружили, что популяция антиген-специфических Т-клеток (в частности, популяция антиген-специфических CD4+ Т-клеток), полученная с использованием CPG ODN 24555 в качестве адъюванта, содержит больше Т-клеток, секретирующих IFN-гамма, и больше полифункциональных Т-клеток по сравнению с популяцией антиген-специфических Т-клеток, полученной с использованием CPG ODN 10103 или CPG ODN 7909.
Например, получали более высокую долю антиген-специфических CD4+ Т-клеток, продуцирующих IFN-γ, по сравнению с популяцией антиген-специфических CD4+ Т-клеток, полученной с CpG ODN 10103. Кроме того, получали более высокую долю полифункциональных антиген-специфических CD4+ Т-клеток, продуцирующих IFN-γ и TNF-α, как IFN-γ, так и IL-2, или как TNF-α, так и IL-2, или даже тройных продуцентов, секретирующих IFN-γ, TNF-α и IL-2, по сравнению с популяцией антиген-специфических CD4+ Т-клеток, полученной с CPG ODN 10103 или CPG ODN 7909. Кроме того, получали более высокую долю антиген-специфических CD8+ Т-клеток, продуцирующих TNF-α, по сравнению с популяцией антиген-специфических CD8+ Т-клеток, полученной с CPG ODN 10103. Также получали более высокую долю антиген-специфических CD8+ Т-клеток, продуцирующих как IFN-γ, так и IL-2, как TNF-α, так и IL-2, или даже тройных продуцентов IFN-γ, TNF-α и IL-2, по сравнению с популяцией антиген-специфических CD8+ Т-клеток, полученной с CPG ODN 10103 или CPG ODN 7909.
Недавно продемонстрировали важность полифункциональности Т-клеток для иммуногенности. В частности, полифункциональность антиген-специфических Т-клеток в отношении продукции хемокинов (таких как IFN-γ, TNF-α и IL-2) коррелирует в некоторых случаях с их защитным потенциалом (см., например, Harari A, et al., Immunol Rev. 2006:211:236-54, Makedonas G and Betts MR. Springer Semin Immunopathol. 2006; 28(3):209-19, Precopio ML et al., J Exp Med. 2007 204(6):1405-16, Xu R et al. Vaccine. 2008; 26(37):4819-29), как полагают, благодаря их более хорошей эффекторной функции по сравнению с Т-клетками, которые секретируют только один цитокин.
CPG ODN 24555 преимущественно обеспечивает продукцию популяций полифункциональных антиген-специфических Т-клеток при использовании в качестве адъюванта, что может быть важным при назначении вакцины.
Иммуностимулирующие нуклеиновые кислоты могут быть двухцепочечными или одноцепочечными. Как правило, двухцепочечные молекулы являются более стабильными in vivo, тогда как одноцепочечные молекулы обладают повышенной иммунной активностью. В некоторых аспектах изобретения предпочтительно, чтобы нуклеиновая кислота была одноцепочечной, а в других аспектах предпочтительно, чтобы нуклеиновая кислота была двухцепочечной.
Термины "нуклеиновая кислота" и "олигонуклеотид" используются в данной заявке взаимозаменяемо для обозначения множества нуклеотидов (т.е. молекул, содержащих сахар (например, рибозу или дезоксирибозу), связанный с фосфатной группой и с заменяемым органическим основанием, представляющим собой либо замещенный пиримидин (например, цитозин (С), тимидин (Т) или урацил (U)), либо замещенный пурин (например, аденин (А) или гуанин (G)). Используемые в данной заявке термины относятся к олигодезоксирибонуклеотидам, олигорибонуклеотидам (т.е. полинуклеотид минус фосфат) и любому другому органическому основанию, содержащему полимер. Молекулы нуклеиновой кислоты могут быть получены из существующих источников нуклеиновой кислоты (например, геномной или кДНК), но предпочтительно являются синтетическими (например, получены путем синтеза нуклеиновой кислоты).
В аспектах изобретения иммуностимулирующие олигонуклеотиды могут охватывать различные химические модификации и замены по сравнению с природными РНК и ДНК, включающие фосфодиэфирный межнуклеозидный мостик, β-D-рибозную единицу и/или природное нуклеозидное основание (аденин, гуанин, цитозин, тимин, урацил). Примеры химических модификаций известны специалистам в данной области техники и описаны, например, в Uhlmann E. et al. (1990), Chem. Rev. 90:543; "Protocols for Oligonucleotides and Analogs" Synthesis and Properties & Synthesis and Analytical Techniques, S. Agrawal, Ed., Humana Press, Totowa, USA 1993; Crooke, S.T. et al. (1996) Annu. Rev. Pharmacol. Toxicol. 36:107-129; и Hunziker J. et al., (1995), Mod. Synth. Methods 7:331-417. Олигонуклеотид по изобретению может иметь одну или более модификаций, где каждая модификация располагается по конкретному фосфодиэфирному межнуклеозидному мостику и/или по конкретной β-D-рибозной единице, и/или по конкретному положению природного нуклеозидного основания по сравнению с олигонуклеотидом с такой же последовательностью, которая состоит из природной ДНК или РНК.
В аспектах изобретения олигонуклеотиды могут содержать одну или более модификаций. Такие модификации могут быть выбраны из: а) замены фосфодиэфирного межнуклеозидного мостика, расположенного на 3'- и/или 5'-конце нуклеозида, на модифицированный межнуклеозидный мостик, б) замены фосфодиэфирного мостика, расположенного на 3'- и/или 5'-конце нуклеозида, на дефосфомостик, в) замены сахарной фосфатной единицы из сахарофосфатного скелета на другую единицу, г) замены β-D-рибозной единицы на модифицированную сахарную единицу, и д) замены природного нуклеозидного основания.
Нуклеиновые кислоты также включают замещенные пурины и пиримидины, такие как С-5 пропинпиримидин и 7-деаза-7-замещенные пурин-модифицированные основания (Wagner et al., 1996, Nat. Biotechnol. 14:840-4). Пурины и пиримидины включают, но не ограничиваются этим, аденин, цитозин, гуанин, тимидин, 5-метилцитозин, 2-аминопурин, 2-амино-6-хлорпурин, 2,6-диаминоаурин, гипоксантин и другие природные и неприродные нуклеозидные основания, замещенные и незамещенные ароматические группировки. Другие такие модификации хорошо известны специалистам в данной области техники.
Модифицированное основание представляет собой любое основание, которое химически отличается от встречающихся в природе оснований, обычно обнаруживаемых в ДНК и РНК, таких как Т, С, G, А и U, но которое имеет общие химические структуры с этими встречающимися в природе основаниями. Модифицированное нуклеозидное основание может быть выбрано, например, из гипоксантина, дигидроурацила, псевдоурацила, 2-тиоурацила, 4-тиоурацила, 5-аминоурацила, 5-(С1-С6)-алкилурацила, 5-(С2-С6)-алкенилурацила, 5-(С2-С6)-алкинилурацила, 5-(гидроксиметил)урацила, 5-хлорурацила, 5-фторурацила, 5-бромурацила, 5-гидроксицитозина, 5-(С1-С6)-алкилцитозина, 5-(С3-С6)-алкенилцитозина, 5-(С2-С6)-алкинилцитозина, 5-хлорцитозина, 5-фторцитозина, 5-бромцитозина, N2-диметилгуанина, 2,4-диаминопурина, 8-азапурина, замещенного 7-деазапурина, предпочтительно 7-деаза-7-замещенного и/или 7-деаза-8-замещенного пурина, 5-гидроксиметилцитозина, N4-алкилцитозина (например, N4-этилцитозина), 5-гидроксидезоксицитидина, 5-гидроксиметилдезоксицитидина, N4-алкилдезоксицитидина (например, N4-этилдезоксицитидина), 6-тиодезоксигуанозина, дезоксирибонуклеозидов нитропиррола, С5-пропинилпиримизина, диаминопурина (например, 2,6-диаминопурина), инозина, 5-метилцитозина, 2-аминопурина, 2-амино-6-хлорпурина, гипоксантина или других модификаций природного нуклеозидного основания. Подразумевается, что этот перечень является примерным, и его не следует интерпретировать как ограничивающий объем изобретения.
В некоторых аспектах изобретения CpG-динуклеотид описанных в данной заявке иммуностимулирующих олигонуклеотидов предпочтительно неметилирован. Неметилированный CpG-мотив представляет собой неметилированную цитозин-гуаниновую динуклеотидную последовательность (т.е. неметилированный 5'-цитозин с последующим 3'-гуанозином и связанные фосфатной связью). В других аспектах CpG-мотив метилирован. Метилированный CpG-мотив представляет собой метилированную цитозин-гуаниновую динуклеотидную последовательность (т.е. метилированный 5'-цитозин, затем 3'-гуанозин, и связанные фосфатной связью).
В некоторых аспектах изобретения иммуностимулирующий олигонуклеотид может соде