Устройство и способ доставки физиологического датчика
Иллюстрации
Показать всеГруппа изобретений относится к медицинской технике. Внутрисосудистое устройство для доставки датчика содержит дистальный рукав, датчик и проксимальный участок. Дистальный рукав имеет просвет для приема отдельного медицинского проволочного направителя и скольжения по нему. Датчик измеряет физиологический параметр пациента и генерирует сигнал, используемый для расчета фракционного резерва кровотока. Проксимальный участок имеет основную секцию и дистальный переходный участок, соединяющий основную секцию с наружной поверхностью дистального рукава. Проксимальный участок содержит канал связи для передачи сигнала с датчика в местоположение вне пациента и содействует позиционированию датчика в анатомической структуре пациента. Внутрисосудистое устройство для доставки датчика может содержать мультипросветный стержень с просветами для проволочного направителя и для датчика, а также два датчика, первый из которых соединен со стержнем датчика, а второй - с наружным участком мультипросветного стержня. При этом датчики могут быть разнесены друг от друга на варьируемое расстояние за счет скольжения стержня датчика относительно мультипросветного стержня. Система инжекции текучей среды содержит трубку для подачи текучей среды, панель управления и процессор, который может принимать сигнал, отражающий кровяное давление, от устройства для доставки датчика. Применение группы изобретений позволит повысить точность позиционирования устройства. 3 н. и 12 з.п. ф-лы, 17 ил.
Реферат
Перекрестная ссылка на родственные заявки
По настоящей заявке испрашивается приоритет по предварительной патентной заявке US № 61/096216, зарегистрированной 11 сентября 2008, содержание которой в полном объеме включено в настоящее описание путем ссылки.
Область техники, к которой относится изобретение
Данная заявка, в общем, относится к области медицинских технологий и, в частности, к устройствам и способам позиционирования и применения физиологических датчиков в анатомических (например, сосудистых) структурах пациентов, например в кровеносных сосудах или клапанах сердца.
Уровень техники
Определенные физиологические измерения могут быть выполнены путем размещения датчика в организме пациента. Такие физиологические измерения могут включать в себя, например, измерения параметров крови, таких как кровяное давление, уровень насыщения кислородом, pH крови и т.д. Некоторые из таких измерений могут иметь диагностическую ценность и/или могут создавать основу для принятия решений о стратегии лечения.
Технология оценки того, в какой степени патологическое изменение, связанное со стенозом, нарушает кровоток через кровеносный сосуд, называется измерением фракционного резерва кровотока (FFR). Для расчета величины FFR для заданного стеноза берутся два показания кровяного давления. Одно показание давления снимают на дистальной стороне стеноза (например, ниже по потоку от стеноза), а другой показатель давления снимают на проксимальной стороне стеноза (например, выше по потоку относительно стеноза, по направлению к аорте). Величину FFR определяют как отношение максимального кровотока в стенозированной артерии, измеренного дистально от места патологического изменения, к нормальному максимальному кровотоку, при этом расчет обычно производят на основе измеренного градиента давления, который выражается отношением дистального давления к проксимальному давлению. Таким образом, величина FFR - безразмерное отношение дистального давления к проксимальному давлению. Градиент давления или перепад давления на участке патологического изменения, связанного со стенозом, является индикатором степени тяжести стеноза, при этом величина FFR - полезный инструмент в оценке перепада давления. Чем больше сужение, вызванное стенозом, тем больше падение давления и тем меньше величина FFR. Измерение величины FFR может быть полезным инструментом в плане диагностики. Например, клинические исследования показали, что величина FFR, составляющая менее чем примерно 0,75, может использоваться в качестве критерия, на основе которого принимаются решения о стратегии лечения. Pijls, DeBruyne и др., Measurement of Fractional Flow Reserve to Assess the Functional Severity of Coronary-Artery Stenoses, 334:1703-1708, New England Journal of Medicine, June 27, 1996. Врач может принять решение, например, о проведении интервенционной процедуры (например, ангиопластики или стентирования), если значение FFR для данного патологического изменения, связанного со стенозом, ниже 0,75, или может решить воздержаться от проведения такого лечения патологических изменений, если значение FFR выше 0,75. Таким образом, FFR-измерение может стать моментом принятия решения для выбора стратегии лечения.
Один из способов измерения градиента давления на участке патологического изменения заключается в использовании небольшого катетера, присоединенного к датчику измерения кровяного давления. Катетер проводят по проволочному направителю, помещенному на участке патологического изменения. Катетер продвигают по проволочному направителю, пока наконечник катетера не пересечет участок патологического изменения. Регистрируют кровяное давление на дистальной стороне участка патологического изменения. Это значение давления делят на значение давления, зарегистрированное в аорте. Недостатком такого способа является то, что может привноситься некоторая ошибка, связанная с размером сечения катетера. Когда катетер пересекает участок патологического изменения, катетер сам по себе блокирует проход, в дополнение к тому сужению, которое вызвано стенозом. Таким образом, измеренное дистальное давление будет несколько ниже, чем оно было бы без дополнительного блокирования кровотока, что может завысить измеренный градиент давления на участке патологического изменения.
Перепад давления можно также измерить на клапане сердца. Если клапан пропускает кровь в обратном направлении, обычно наблюдают перепад давления меньше оптимального. Применение катетера для измерения перепада давления на клапане сердца - часто используемый прием. Однако в силу размера катетера клапан сердца может не обеспечивать должного уплотнения вокруг катетера. Протечка также может быть связана с присутствием катетера и может вносить свой вклад в неточные показания перепада давления. Примером того, где это может происходить, является митральный клапан (например, регургитация митрального клапана).
Один из способов измерения кровяного давления в организме пациента заключается в использовании проволочного направителя с функцией определения давления. В таком устройстве имеется датчик давления, встроенный в сам проволочный направитель. Проволочный направитель с функцией определения давления может использоваться для размещения интервенционных устройств, таких как ангиопластические баллоны или стенты. До проведения интервенции проволочный направитель с функцией определения давления проводят через участок патологического изменения, связанного со стенозом, так чтобы чувствительный элемент находился на дистальной стороне участка патологического изменения, и регистрируют дистальное кровяное давление. После этого проволочный направитель может отводиться назад, так чтобы чувствительный элемент находился на проксимальной стороне участка патологического изменения. Далее можно рассчитать градиент давления на участке стеноза и получаемую в итоге величину FFR.
Для того чтобы в определенных случаях применения использовать датчик давления на основе проволочного направителя, проволочный направитель должен быть репозиционирован, так чтобы чувствительный элемент проволочного направителя был правильно размещен, например, в отношении участка патологического изменения, связанного со стенозом. Измерения кровяного давления для расчета величины FFR, например, обычно выполняют на обеих сторонах данного стеноза, так что проволочный направитель обычно отводят назад через участок стеноза, чтобы выполнить измерение выше по потоку. После отвода назад проволочного направителя для выполнения измерения проксимального давления (аортального давления или коронарного давления выше по потоку) проволочный направитель может снова быть репозиционирован ниже по потоку от участка патологического изменения, например, если будет определено (к примеру, на основе расчета FFR), что требуется разместить интервенционное устройство. В случае существования множества участков патологического изменения чувствительный элемент проволочного направителя с функцией определения давления потребуется продвигать и отводить назад через множество участков патологического изменения, причем потенциально потребуется продвигать и снова репозиционировать для каждого такого участка патологического изменения. Продвижение проволочного направителя с функцией определения давления и манипулирование им на участках патологического изменения, связанного со стенозом, и в сосудистой системе, например, может быть сложной задачей и/или потребовать много времени.
Предпочтения врача - еще один фактор, который может повлиять на выбор диагностических инструментов или технологических приемов в определенных практических случаях. Например, для некоторых врачей может войти в привычку использовать конкретные проволочные направители для определенных случаев применения. «Стандартные» (например, имеющиеся на рынке) медицинские проволочные направители могут иметь различные размеры, показатели гибкости и моментные характеристики. Врач может предпочесть использовать различные проволочные направители для решения различных задач, например для получения доступа в труднодоступные анатомические области, либо когда в артериях встречаются бифуркации. Определенные проволочные направители, таким образом, могут лучше подходить для решения конкретных задач в силу их моментных или изгибных характеристик, и врач может отдать существенное предпочтение использованию определенного проволочного направителя, исходя из конкретной задачи (или задач), которая перед ним стоит. Проволочный направитель с функцией определения давления может иметь моментные и изгибные характеристики, которые либо неизвестны врачу, либо непригодны для решения определенной задачи, поскольку такой проволочный направитель специально выполнен с возможностью содержания датчика давления как составной части самого проволочного направителя. В итоге врач может испытывать трудности при манипулировании проволочным направителем с функцией определения давления в целевом анатомическом местоположении по сравнению со «стандартным» (например, не определяющим давление) медицинским проволочным направителем.
Привыкнув к эксплуатационным характеристикам определенного проволочного направителя, не определяющего давление, врач может воспротивиться применению проволочного направителя с функцией определения давления, который может увеличить время и повысить сложность позиционирования и репозиционирования проволочного направителя с функцией определения давления, например, по участку патологического изменения, связанного со стенозом. В таких случаях врач может предпочесть отказаться от преимуществ диагностического измерения, такого как измерение величины FFR, и просто выбрать проведение какого-либо интервенционного лечения в качестве консервативного подхода в принятии таких решений. Если бы технологии диагностических измерений и соответствующие устройства были достаточно просты в использовании, большее число врачей смогли бы их применять и тем самым принимали бы более взвешенные решения по лечению.
Сущность изобретения
Устройства и способы доставки физиологического датчика согласно вариантам осуществления изобретения могут использоваться для диагностического применения, такого как кардиоваскулярные процедуры в коронарных артериях, в области интервенционной радиологии применительно к периферийным артериям, а также в области кардиологии применительно к клапанам сердца.
Внутрисосудистое устройство для доставки датчика согласно некоторым вариантам осуществления изобретения содержит дистальный рукав с просветом для проволочного направителя для скольжения по медицинскому проволочному направителю, датчик, соединенный с дистальным рукавом, при этом датчик выполнен с возможностью измерения физиологического параметра пациента и генерирования сигнала, отражающего этот физиологический параметр. Проксимальный участок соединен с дистальным рукавом. Проксимальный участок содержит канал связи для передачи сигнала с датчика в местоположение вне пациента (такое как монитор устройства отображения информации или другое медицинское устройство и т.д.). Проксимальный участок устройства для доставки датчика выполнен с возможностью содействия позиционированию датчика в сосудистой структуре пациента.
Способ оценки степени опасности патологического изменения, связанного со стенозом, в кровеносном сосуде пациента согласно некоторым вариантам осуществления изобретения содержит размещение внутрисосудистого устройства для доставки датчика по проволочному направителю в положение, при котором датчик располагается дистально от участка патологического изменения, и измерение дистального давления. В некоторых вариантах осуществления способ может дополнительно содержать использование устройства для доставки датчика в целях перемещения датчика в положение, проксимальное по отношению к участку патологического изменения, и измерение проксимального (например, аортального) давления, а далее вычисление отношения (либо какое-либо иное количественное сравнение) этих двух результатов измерений давления. В некоторых вариантах осуществления проксимальное давление может быть получено от отдельного устройства определения давления (например, датчика давления, соединенного с системой инжекции текучей среды), при этом измерения дистального и проксимального давления могут выполняться по существу одновременно (например, для уменьшения ошибок отсчета времени), прежде чем произвести количественное сравнение этих двух величин.
Краткое описание чертежей
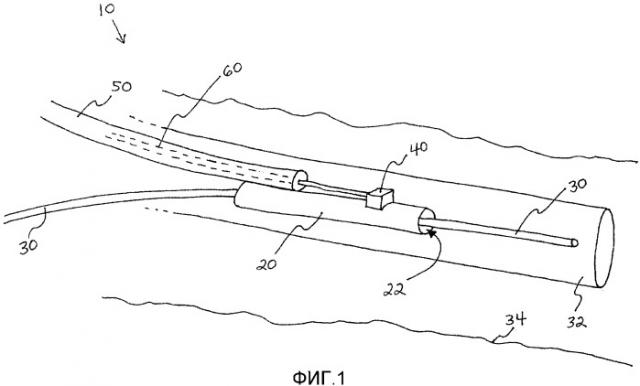
На Фигуре 1 показан вид в перспективе устройства для доставки датчика согласно одному варианту осуществления изобретения.
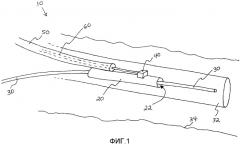
На Фигуре 2 показан концептуальный вид в перспективе устройства для доставки датчика для выполнения физиологических измерений согласно одному варианту осуществления изобретения.
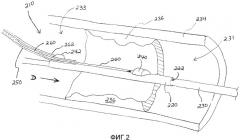
На Фигуре 3 показан концептуальный график зависимости кровяного давления пациента от времени.
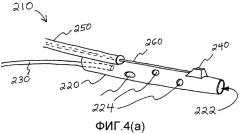
На Фигуре 4(а) показан вид сбоку устройства для доставки датчика согласно одному варианту осуществления изобретения, имеющего одно или несколько проточных отверстий, расположенных вдоль бокового участка.
На Фигуре 4(b) показан вид в разрезе устройства для доставки датчика согласно одному варианту осуществления изобретения, имеющего одно или несколько проточных отверстий.
На Фигуре 5(а) показан вид сбоку, в разрезе, устройства для доставки датчика с корпусом датчика согласно одному варианту осуществления изобретения.
На Фигуре 5(b) показан вид сбоку, в разрезе, устройства для доставки датчика с корпусом датчика согласно одному варианту осуществления изобретения.
На Фигурах 5(c) и 5(d) показаны виды сбоку устройства для доставки датчика с рентгеноконтрастной маркировочной полосой согласно одному варианту осуществления изобретения.
На Фигуре 5(e) показан вид сбоку, в разрезе, устройства для доставки датчика с распоркой для разгрузки от натяжения согласно одному варианту осуществления изобретения.
На Фигурах 6(a)-6(g) показаны увеличенные виды сбоку дистального перемещения устройства для доставки датчика согласно некоторым вариантам осуществления изобретения.
На Фигурах 7(a) и 7(b) показаны виды в перспективе устройства для доставки датчика, имеющего второй датчик, расположенный на проксимальном рукаве согласно одному варианту осуществления изобретения.
На Фигуре 8 показан вид в перспективе устройства для доставки датчика, имеющего разветвительную трубку согласно одному варианту осуществления изобретения.
На Фигуре 9 показан вид сбоку, в сечении, устройства для доставки датчика, которое имеет двухпросветную конфигурацию согласно одному варианту осуществления изобретения.
На Фигуре 10 показан вид сбоку устройства для доставки датчика, имеющего конфигурацию «расположения по проволоке» согласно одному варианту осуществления изобретения.
На Фигуре 11 показана блок-схема последовательности операций, представляющая способ использования устройства для доставки датчика согласно некоторым вариантам осуществления изобретения.
На Фигуре 12 показан вид в перспективе системы инжекции текучей среды, которая может быть использована для взаимодействия с устройством для доставки датчика согласно одному варианту осуществления изобретения.
На Фигуре 13 показан вид в перспективе системы инжекции текучей среды, которая может быть использована для взаимодействия с устройством для доставки датчика согласно одному варианту осуществления изобретения.
На Фигуре 14 показана блок-схема последовательности операций способа использования устройства для доставки датчика в сочетании с системой инжекции текучей среды согласно некоторым вариантам осуществления изобретения.
На Фигуре 15 показана блок-схема последовательности операций способа использования устройства для доставки датчика согласно одному варианту осуществления изобретения.
На Фигуре 16 показан вид в перспективе механизированной инжекционной системы, выполненной с возможностью соединения с устройством для доставки физиологического датчика согласно некоторым вариантам осуществления изобретения.
На Фигуре 17 показан схематичный вид экрана интерфейса пользователя, содержащий информацию, которая может быть отображена для оператора согласно некоторым вариантам осуществления изобретения.
Подробное описание
Последующее подробное описание сопровождается ссылками на прилагаемые чертежи, на которых одинаковые номера позиций соответствуют одинаковым элементам. На чертежах, которые не обязательно выполнены в масштабе, изображены отобранные варианты осуществления изобретения; другие возможные варианты осуществления могут стать очевидны средним специалистам в данной области техники на основе представленных идей. Таким образом, варианты осуществления, показанные на прилагаемых чертежах и описанные ниже, даны в иллюстративных целях и не направлены на ограничение объема изобретения, определяемого прилагаемой формулой изобретения.
Пример устройства для доставки датчика согласно некоторым вариантам осуществления изобретения показан на Фигуре 1. Устройство 10 для доставки датчика на Фигуре 1 включает в себя дистальный рукав 20, имеющий просвет 22 для проволочного направителя, предназначенный для приема медицинского проволочного направителя 30 с возможностью скольжения. Датчик 40 соединен с дистальным рукавом 20, при этом датчик 40 способен определять и/или измерять физиологический параметр пациента, а также генерировать сигнал, отражающий этот физиологический параметр. Таким образом, дистальный рукав 20, а значит и датчик 40, могут располагаться в организме пациента (например, в анатомической структуре пациента, такой как вена, артерия или другой кровеносный сосуд, либо, например, в клапане сердца) путем обеспечения скольжения дистального рукава 20 по медицинскому проволочному направителю 30 до требуемого местоположения.
Устройство 10 для доставки датчика на Фигуре 1 также включает в себя проксимальный участок 50, который соединен с дистальным рукавом 20. Проксимальный участок 50 включает в себя канал 60 связи для передачи сигнала с датчика 40 в некоторое местоположение вне пациента (например, в процессор, на устройство отображения, компьютер, монитор или на другое медицинское устройство). Канал 60 связи может содержать волоконно-оптический канал связи в некоторых предпочтительных вариантах осуществления, таких, где датчик 40 представляет собой волоконно-оптический датчик давления. Согласно альтернативному варианту канал 60 связи может содержать электропроводящую среду, например один или несколько электропроводящих проводов. Разумеется, многие другие виды сред передачи данных могут быть пригодны для передачи сигналов, сгенерированных датчиком 40, в некоторое местоположение вне пациента. В некоторых вариантах осуществления изобретения канал 60 связи может содержать любую из множества текучих и/или не обладающих текучестью сред передачи данных, такую как беспроводная линия передачи данных или связь в ИК диапазоне, либо звуковая связь, например ультразвуковая связь, которые можно привести в качестве примеров.
Проксимальный участок 50 также выполнен с возможностью содействия оператору (например, врачу или другому медицинскому персоналу) в позиционировании дистального рукава 20 и датчика 40 в пределах анатомической (например, сосудистой) структуры пациента. Обычно это осуществляется путем того, что оператор сначала вводит «стандартный» медицинский проволочный направитель 30 в сосудистую систему пациента и продвигает его за пределы целевой области. Устройство 10 для доставки датчика далее размещается путем «насаживания» дистального рукава 20 на проволочный направитель 30, так чтобы просвет 22 скользил по проволочному направителю 30, и продвижения дистального рукава 20 (и связанного с ним датчика 40) путем перемещения (например, проталкивания и/или подтягивания на себя) проксимального участка 50, пока датчик 40 не займет требуемое положение.
Устройством 10 и проволочным направителем 30 обычно манипулируют внутри направляющего катетера 32, который помещен в целевую анатомическую (например, сосудистую) структуру. В некоторых предпочтительных вариантах осуществления изобретения просвет 22 для проволочного направителя может быть выполнен с возможностью скольжения по медицинским проволочным направителям «стандартного» размера. Например, многие производители выпускают медицинские проволочные направители, размеры которых варьируется менее чем от примерно 0,014 дюйма в наружном диаметре до более примерно 0,038 дюйма в наружном диаметре, имея при этом конечное число принятых размеров в пределах этого диапазона. Медицинские проволочные направители «стандартного» размера могут, например, иметь наружные диаметры 0,010, 0,014, 0,018, 0,021, 0,025, 0,028, 0,032, 0,035 и 0,038 дюйма. Таким образом, в некоторых предпочтительных вариантах осуществления изобретения просвет 22 для проволочного направителя может иметь соответствующий размер, чтобы скользить по медицинскому проволочному направителю определенного стандартного размера. Устройство согласно предпочтительным вариантам осуществления, таким образом, может иметь некоторый диапазон размеров, соответствующих стандартным размерам медицинского проволочного направителя.
Одно из потенциальных преимуществ устройства 10 для доставки датчика согласно вариантам осуществления изобретения заключается в том, что оно позволяет врачу использовать проволочный направитель по своему выбору. Устройство 10 для доставки датчика может иметь размер, допускающий возможность использования с любым проволочным направителем. Врач, например, может выбрать определенный проволочный направитель на основе его особых изгибных и моментных характеристик для определенных процедур. Устройство 10 для доставки согласно различным вариантам осуществления изобретения предоставляет врачу возможность использовать такой проволочный направитель, который наилучшим образом пригоден для конкретного применения.
Еще одно потенциальное преимущество устройства 10 для доставки датчика заключается в том, что оно не требует репозиционирования проволочного направителя для того чтобы снять показания датчика. После того как проволочный направитель, например, размещен на участке патологического изменения, связанного со стенозом, устройство 10 для доставки датчика может быть установлено (например, продвинуто и/или отведено назад) по проволочному направителю, и датчик 40, следовательно, может быть продвинут или отведен назад через участки патологического изменения, например для снятия показаний давления, не прибегая при этом к перемещению проволочного направителя. Врач также может сэкономить время благодаря тому, что ему не приходится репозиционировать проволочный направитель по участку или участкам патологического изменения для того чтобы выполнить такие измерения.
В примере, показанном на Фигуре 1, устройство 10 размещают с использованием направляющего катетера 32, который помещен в целевую сосудистую структуру (в данном примере - в кровеносный сосуд 34, который, например, может представлять собой коронарную артерию пациента). В некоторых вариантах осуществления изобретения размер или «площадь» (например, ширина и/или площадь сечения) устройства 10 могут позволить ему вмещаться в направляющие катетеры определенных стандартных размеров. Например, для определенных диагностических целей желательно иметь устройство 10, размещаемое в направляющем катетере определенных стандартных размеров (например, менее чем примерно 4-5 единиц по шкале Шаррьера (FR)).
В некоторых вариантах осуществления изобретения дистальный рукав 20 устройства может быть по существу концентричен с проволочным направителем 30. Соединение проксимального участка 50 с дистальным рукавом 20 позволяет проволочному направителю 30 быть отдельным от остальной части устройства 10 (например, в «монорельсовой» конфигурации катетера, как ее иногда называют); это обычно происходит внутри направляющего катетера 32. Проволочный направитель 30 и устройство 10 оба выводятся из пациента на проксимальном конце направляющего катетера 32 как отдельные устройства. Отделение устройства 10 и проволочного направителя 30 друг от друга позволяет врачу в необходимых случаях независимо контролировать устройство 10 и проволочный направитель 30. Это может также позволить врачу использовать более короткий проволочный направитель для замены катетера. Например, монорельсовая конфигурация может предусматривать использование проволочного направителя, длина которого составляет примерно 170-200 см, в то время как конфигурация «по всей проволоке» может потребовать использования значительно более длинного (например, до 300 см и более) проволочного направителя. Отделение друг от друга устройства 10 и проволочного направителя 30 (кроме как на дистальном рукаве 20) может также привести к снижению трения (например, в направляющем катетере 32) по сравнению со случаем, когда устройство 10 и проволочный направитель 30 должны перемещаться вместе как единый блок. В некоторых вариантах осуществления на различные участки устройства может наноситься гидрофильное покрытие, чтобы дополнительно снизить величину трения, преодолеваемого, например, при продвижении или отведении назад устройства 10.
Одно из диагностических приложений, в которых могут с успехом использоваться различные варианты осуществления настоящего изобретения, - измерение фракционного резерва кровотока (FRR). Как отмечалось выше, FRR-измерения дают количественную оценку того, в какой степени патологическое изменение, связанное со стенозом, например, нарушает кровоток через кровеносный сосуд. Для расчета величины FRR для данного стеноза требуются два измерения кровяного давления: одно показание давления снимается на дистальной стороне стеноза (стороне ниже по потоку), а другое показание давления снимается на проксимальной стороне стеноза (стороне выше по потоку). Величина FRR, таким образом, представляет собой безразмерное отношение дистального давления к проксимальному давлению. Градиент давления на участке патологического изменения, связанного со стенозом - индикатор степени тяжести стеноза. Чем большее сопротивление оказывает стеноз, тем выше перепад давления и тем ниже величина FRR.
Чтобы сделать раскрытие более ясным, ниже будут описаны некоторые варианты осуществления изобретения в контексте выполнения измерений величины FRR. Однако следует понимать, что существуют и другие применения, в которых описанные здесь устройства и способы могут способствовать измерению физиологических параметров.
На Фигуре 2 показан вид в перспективе устройства для доставки датчика, предназначенного для измерения физиологического параметра пациента согласно одному варианту осуществления изобретения. Вариант осуществления, показанный на Фигуре 2, может быть, например, использован для выполнения FRR-измерения в кровеносном сосуде пациента. На Фигуре 2 показано устройство 210 для доставки датчика, размещаемое в кровеносном сосуде пациента (например, коронарной артерии 234) через стеноз (например, участок 236 патологического изменения, связанного со стенозом). Для проведения FRR-измерения, например, первый датчик 240 может быть расположен для измерения дистального (ниже по потоку) кровяного давления Pd в местоположении 231 ниже по потоку от целевого местоположения (например, участка 236 патологического изменения, связанного со стенозом). Первый датчик 240 после этого можно расположить для измерения проксимального (выше по потоку) кровяного давления Pp в местоположении 233 выше по потоку относительно целевого местоположения (например, участка 236 патологического изменения, связанного со стенозом). Величина FRR просто рассчитывается как отношение дистального давления к проксимальному давлению, или FRR=(Pd/Pp). Термины «ниже по потоку» и «выше по потоку» используются по отношению к нормальному направлению кровотока, «D», как показано на Фигуре 2.
На Фигуре 2 первый датчик 240 соединен с дистальным рукавом 220. В варианте осуществления, показанном на Фигуре 2, первый датчик 240 соединен с наружной поверхностью дистального рукава 220. Первый датчик 240 выполнен с возможностью измерения физиологического параметра пациента, такого как параметр крови (например, кровяного давления, температуры, pH, степени насыщения кислородом и т.д.), и генерирования сигнала, отражающего этот физиологический параметр. В некоторых предпочтительных вариантах осуществления изобретения первый датчик 240 представляет собой волоконно-оптический датчик давления, выполненный с возможностью измерения кровяного давления. Примером волоконно-оптического датчика давления служит волоконно-оптический датчик давления Fabry-Perot, который является коммерчески доступным датчиком. В качестве примеров волоконно-оптических датчиков давления Fabry-Perot можно привести волоконно-оптический датчик давления на основе микроэлектромеханической системы (MEMS) «OPP-M» (размером 400 микрон), изготавливаемый компанией Opsens (Квебек, Канада), и датчик «FOP-MIV» (размером 515 микрон), изготавливаемый компанией Fiso Technologies, Inc. (Квебек, Канада). В некоторых альтернативных вариантах осуществления первый датчик 240 может представлять собой пьезорезистивный датчик давления (например, пьезорезистивный датчик давления на основе микроэлектромеханической системы (MEMS)), а в других вариантах осуществления первый датчик 240 может представлять собой емкостный датчик давления (например, емкостный датчик давления на основе микроэлектромеханической системы (MEMS)). Для выполнения большинства физиологических измерений с помощью датчика 240, например, требуется диапазон определения давления от около -50 мм рт. ст. до около +300 мм рт. ст. (относительно атмосферного давления).
В вариантах осуществления изобретения с использованием волоконно-оптического датчика давления Fabry-Perot, применяемого в качестве датчика 240, такой датчик имеет отражающую диафрагму, которая изменяет результаты измерения длины полости в соответствии с давлением, приложенным к диафрагме. Когерентный свет от светового источника проходит по волокну и пересекает малую полость на конце датчика. Отражающая диафрагма отражает часть светового сигнала обратно в волокно. Отраженный свет проходит обратно через волокно в детектор на конце волокна, где расположен световой источник. Две световые волны, свет от источника и отраженный свет проходят в противоположных направлениях и интерферируют друг с другом. Степень интерференции изменяется в зависимости от длины полости. Длина полости изменяется по мере того как диафрагма смещается под давлением. Степень интерференции регистрируется интерференционным детектором.
На Фигуре 2 показан проксимальный участок 250, соединенный с дистальным рукавом 220. Проксимальный участок 250 включает в себя канал 260 связи для передачи физиологического сигнала с датчика 240 в местоположение вне пациента (например, в процессор, устройство отображения, на компьютер, монитор или другое медицинское устройство). Проксимальный участок 250 предпочтительно может быть выполнен из материала, обладающего существенной жесткостью, чтобы содействовать оператору (например, врачу или другому медицинскому персоналу) в позиционировании дистального рукава 220 и датчика 240 в пределах анатомической (например, сосудистой) структуры пациента.
Одним из пригодных материалов для проксимального участка 250, например, может быть гипотрубка из нержавеющей стали. В зависимости от области применения, проксимальный участок 250 (который иногда называют «доставочной трубкой») обычно должен быть более жестким и сопротивляющимся деформациям, чем дистальный рукав 220, чтобы обеспечить достаточный контроль над устройством при его проталкивании, подтягивании и иными действиями над ним, выполняемыми при размещении в целевом местоположении пациента. При интервенционных кардиологических процедурах, например, по меньшей мере, часть проксимального участка 250 будет подвержена манипулированию в направляющем катетере, расположенном в аорте. Проксимальный участок 250 в данном случае применения, таким образом, должен обладать достаточной гибкостью, чтобы соответствовать дуге аорты, и при этом быть достаточно жестким, чтобы проталкивать и оттягивать устройство. Соответственно пригодные материалы для проксимального участка 250 могут также включать в себя (в дополнение к вышеупомянутой гипотрубке из нержавеющей стали) такие материалы, как нитинол, нейлон и пластик или, например, композиции из множества материалов.
Канал 260 связи может располагаться вдоль наружной поверхности проксимального участка 250 или может быть образован в проксимальном участке 250, как показано на Фигуре 2. Например, канал 260 связи может содержать соединительный просвет, который в некоторых вариантах осуществления продолжается продольно по проксимальному участку 250. Канал 260 связи в некоторых вариантах осуществления может содержать волоконно-оптический канал связи, как в случае, когда датчик 240 является волоконно-оптическим датчиком давления. В альтернативном варианте канал 260 связи может содержать электропроводную среду, такую как электропроводящие провода, или иные среды передачи данных, пригодные для передачи сигнала, сгенерированного датчиком 240. В предпочтительных вариантах осуществления изобретения канал 260 связи содержит нетекучую среду передачи данных. В варианте осуществления, показанном на Фигуре 2, канал 260 связи (например, волоконно-оптический кабель) продолжается дистально за пределы проксимального участка 250 и соединен с датчиком 240. Канал 260 связи в таком варианте осуществления, по меньшей мере, частично размещен в соединительном просвете проксимального участка 250 (например, гипотрубке из нержавеющей стали).
На Фигуре 2 также показан возможный вариант осуществления изобретения, в котором с устройством 210 может быть соединен второй датчик 242. Например, второй датчик 242 может быть соединен с проксимальным участком 250, так что первый и второй датчики 240, 242 существенно разнесены друг от друга (например, на фиксированное расстояние), чтобы перекрыть участок патологического изменения, связанного со стенозом. Данный вариант осуществления может предоставить возможность измерить величину FRR без необходимости репозиционировать устройство 210, поскольку первый датчик 240 может быть помещен дистально от участка 236 патологического изменения, связанного со стенозом, для измерения величины Pd, а второй датчик 242 может быть помещен проксимально по отношению к участку 236 патологического изменения, связанного со стенозом, для измерения величины Pp. Второй датчик 242 может иметь канал 262 связи, который может быть размещен в проксимальном участке 250 или, например, может быть расположен вдоль наружной поверхности проксимального участка 250, как показано на Фигуре 2. Кроме того, возможность измерять величины Pd и Pp по существу одновременно может повысить точность и/или снизить влияние различного типа ошибок, представленных и описанных ниже со ссылкой на Фигуру 3.
Следует заметить, что в некоторых вариантах осуществления может присутствовать более двух датчиков, и что расстояние между смежными датчиками в таких вариантах осуществления может варьироваться, чтобы обеспечить возможность их распределения в пространстве. В некоторых альтернативных вариантах осуществления изобретения один или несколько датчиков могут быть размещены на проксимальном участке 250, при этом, например, на дистальном рукаве 220 датчики могут отсутствовать. В некоторых альтернативных вариантах осуществления может потребоваться иметь множество датчиков (два, три, четыре или более), разнесенных на известное фиксированное расстояние, расположенных вдоль проксимального участка 250. Это может, например, обеспечить возможность измерять величины Pd и Pp по существу одновременно, вне зависимости от длины участка патологического изменения, путем отбора соответствующей пары датчиков (из имеющегося множества датчиков), помещенных на уч