Вакцина ассоциированная против ньюкаслской болезни, реовирусного теносиновита и метапневмовирусной инфекции птиц инактивированная эмульсионная
Иллюстрации
Показать всеИзобретение относится к ветеринарии и касается вакцины ассоциированной против ньюкаслской болезни (НБ), реовирусного теносиновита (РВТ) и метапневмовирусной инфекции (МПВИ) птиц инактивированной эмульсионной, содержащей активное вещество и целевую добавку. В качестве целевой добавки вакцина содержит масляный адъювант марки Montanide ISA-70 VG. Изобретение обеспечивает индукцию у привитой птицы высокого уровня антител к возбудителям НБ, РВТ и МПВИ через 28 суток после применения, который сохраняется в течение 12 месяцев и трансовариально передается потомству. 6 з.п. ф-лы, 7 пр., 7 ил., 5 табл.
Реферат
Изобретение относится к области ветеринарной вирусологии и биотехнологии, касается ассоциированной вакцины инактивированной эмульсионной, которая может быть использована для специфической профилактики болезней птиц, индуцируемых вирусами ньюкаслской болезни (НБ), реовирусного теносиновита (РВТ) и метапневмовирусной инфекции (МПВИ) птиц.
Мировая тенденция конца XX, начала XXI в.в. в птицеводстве - это эпоха превращения домашних мелкотоварных хозяйств в крупномасштабное высокопродуктивное производство. Такая ситуация породила уникальные изменения биоэкологической ниши, окружающей выращиваемое поголовье, и, в частности, привела к чрезвычайно спрессованной во времени трансформации спектра вирусных инфекций, повсеместно поражающих домашнюю птицу. За этот период появились вновь, антигенно обновились или существенно усилили вирулентность более десяти возбудителей, став причиной весьма опасных инфекционных болезней птиц. Среди хорошо известных, например, вирусов НБ или болезни Марека (БМ) особое место заняли возбудители РВТ и МПВИ. Именно эти этиологические агенты, действуя порознь, или, как правило, в ассоциации наносят катастрофический с экономической точки зрения ущерб промышленному птицеводству. При этом ущерб становится более ощутимым, когда эти заболевания поражают племенное ядро или стада кур - несушек (1-6).
Эффективность предупреждения указанных заболеваний во всем мире связывают главным образом с применением живых и инактивированных вакцин. При этом вакцинопрофилактика до последнего времени остается единственным фундаментально проработанным методическим приемом для эффективного противостояния инфекционным болезням при крупномасштабном выращивании птицы.
Однако каждый тип вакцин, используемых для специфической профилактики вышеуказанных заболеваний у птиц, имеет преимущества и недостатки. Преимущество живых вакцин состоит в технологичности и в возможности использования массовых методов применения при вакцинации. К недостаткам живых вакцин относятся формирование нестабильной иммунной реакции у птиц, развитие различного рода осложнений, таких как повышенная реактогенность, развитие иммуносупрессии, а иногда и гибели птиц при воздействии неблагоприятных условий содержания и наличия сопутствующих инфекций, а также возможны проблемы воспроизводства, длительная персистенция и выделение вакцинного вируса во внешнюю среду.
В промышленном птицеводстве широкое применение нашли сорбированные на гидроокиси алюминия (ГОА) или масляные на основе эмульсии обратного типа инактивированные вакцины, обладающие существенными преимуществами по сравнению с живыми вакцинными препаратами. Прежде всего следует отметить их высокую безопасность и безвредность, возможность стандартизации дозированного введения специфического антигена, стабильность основных биологических свойств, возможность создания системного, напряженного и продолжительного иммунологического эффекта (7).
Известна вакцина против НБ птиц инактивированная эмульсионная, содержащая в качестве активного вещества авирулентный очищенный антигенный материал из штамма "Ла Сота" вируса НБ, полученного в 9÷12 -суточных эмбрионах SPF - кур с инфекционной активностью не ниже 8,0 Ig ЭИД50/см3 до инактивации и титром гемагглютинирующей активности (ГА - активность) в экстраэмбриональной жидкости не ниже 1:256, и в качестве целевой добавки масляный адъювант в эффективном соотношении (8, 9).
Известна вакцина против РВТ птиц инактивированная эмульсионная, содержащая в качестве активного вещества авирулентный очищенный антигенный материал из штамма "1133" реовируса птиц, полученного в культуре клеток фибробластов эмбрионов SPF - кур (ФЭК) с инфекционной активностью не ниже 7,0 Ig ТЦД50/см3 до инактивации, и в качестве целевой добавки масляный адъювант в эффективном соотношении (10÷13).
Известна вакцина против МПВИ птиц инактивированная эмульсионная, содержащая в качестве активного вещества авирулентный очищенный антигенный материал из метапневмовируса птиц серотипа А, полученного в перевиваемой культуре клеток почки зеленой африканской мартышки (Vero) с инфекционной активностью не ниже 6,0 Ig ТЦД50/см3 до инактивации, и в качестве целевой добавки масляный адъювант в соотношении, мас.%: 70,0:30,0 соответственно (14).
Известна вакцина против МПВИ птиц инактивированная эмульсионная, содержащая в качестве активного вещества авирулентный очищенный антигенный материал из штамма "PVO3-B №-127 ДЕП" метапневмовируса птиц, полученного в перевиваемой культуре клеток Vero, с инфекционной активностью не ниже 7,0 Ig ТЦД50/см3 до инактивации, и в качестве целевой добавки масляный адъювант в соотношении мас.%: 70,0:30,0 соответственно (15, 16).
Применение моновалентных инактивированных вакцин в птицеводстве ограничено необходимостью одновременной вакцинации против нескольких инфекций в короткий промежуток времени (как правило, в пределах 80÷100 - суточного возраста), коротким производственным сроком использования птицы, а также ограниченным мышечным пространством для одновременной инъекции нескольких препаратов. Кроме того, многократное повторение индивидуального способа вакцинации приводит к повышению трудовых затрат, увеличению сроков образования иммунитета у птиц, способствует возникновению стрессовых явлений и осложнений.
Указанные недостатки частично устранены разработкой и применением в птицеводстве ассоциированных инактивированных вакцин, имеющих в составе разнообразное количественное и качественное соотношение антигенов.
Известна вакцина ассоциированная против НБ и МПВИ птиц инактивированная сорбированная, содержащая смесь авирулентных очищенных антигенных материалов из штамма "Ла Сота" вируса НБ и из штамма "PVO3-B" вируса МПВИ птиц, полученных культивированием в чувствительных биологических системах, и в качестве целевой добавки адъювант-сорбент ГОА в эффективном соотношении (16, 17).
Известна вакцина ассоциированная против НБ и РВТ птиц инактивированная эмульсионная, содержащая смесь авирулентных очищенных антигенных материалов из штамма "Ла Сота" вируса НБ и из штамма "1133" вируса РВТ птиц, полученных культивированием в чувствительных биологических системах, и масляный адъювант в эффективном соотношении (2, 18, 19).
Известна вакцина ассоциированная против НБ и МПВИ птиц инактивированная эмульсионная, содержащая смесь авирулентных очищенных антигенных материалов из штамма "Ла Сота" вируса НБ и из штамма "PVO3-B" вируса МПВИ птиц, полученных культивированием в чувствительных биологических системах, и масляный адъювант в эффективном соотношении (16, 17, 20, 21).
Наиболее близкой к предлагаемому изобретению по совокупности существенных признаков является вакцина ассоциированная против НБ и МПВИ птиц инактивированная эмульсионная, содержащая смесь авирулентных очищенных антигенных материалов из штамма "Ла Сота" вируса НБ и из штамма "PVO3-B" вируса МПВИ птиц, полученных культивированием в чувствительных биологических системах, и масляный адъювант в эффективном соотношении (16, 17, 20, 21).
Общим существенным недостатком известных бивалентных инактивированных вакцин, в том числе вакцины - прототипа, является их недостаточно высокая эффективность вследствие ограниченности одновременной вакцинации против нескольких инфекций в короткий промежуток времени (как правило, в пределах 80÷100 - суточного возраста), коротким производственным сроком использования птицы, а также ограниченного мышечного пространства для одновременной инъекции нескольких препаратов. Кроме того, многократное повторение индивидуального способа вакцинации приводит к повышению трудовых затрат, увеличивает сроки образования иммунитета у птиц, способствует возникновению стрессовых явлений и осложнений.
Известно так же, что при изготовлении ассоциированных инактивированных вакцин с валентностью выше трех происходит значительное взаимное разведение содержащихся в них антигенных компонентов. В результате снижается их концентрация в прививном объеме препарата. При этом возможность повышения концентрации вирусов при помощи культивирования ограничена. В связи с этим одним из наиболее важных технологических показателей является определение минимальной концентрации антигенов и их оптимального соотношения в прививном объеме вакцины, что обеспечивало бы формирование напряженного иммунитета у кур. Немаловажным в производстве эмульсионных вакцин является выбор адъюванта, который обеспечивал бы стабильность вакцинной эмульсии, индукцию и персистенцию высоких титров антител у привитых птиц при отсутствии побочных эффектов в местах своего введения, а также удобство применения вакцины в производственных условиях. Поэтому проблема получения высокоэффективной ассоциированной вакцины инактивированной эмульсионной против основных возбудителей вирусных заболеваний птиц продолжает оставаться актуальной и является основным направлением исследований по созданию искомого препарата.
Задача, на решение которой направлено настоящее изобретение, заключается в получении вакцины ассоциированной инактивированной эмульсионной, создающей эффективную защиту восприимчивых птиц от заражения возбудителями НБ, РВТ и МПВИ. Основными показателями эффективности применения препарата являются защита племенных стад кур от НБ, а также создание ранней защиты цыплят с помощью материнского иммунитета от РВТ и МПВИ.
Технический результат от использования предложенного изобретения заключается в расширении арсенала высокоиммуногенных безвредных и ареактогенных ассоциированных вакцин инактивированных эмульсионных против возбудителей НБ, РВТ и МПВИ птиц, циркулирующих на территории Российской Федерации. Технический результат достигнут благодаря определению минимальной концентрации каждого антигена в прививном объеме препарата, минимальной инфекционной активности вирусов, входящих в состав предлагаемой вакцины, до инактивации и оптимального соотношения антигенных компонентов в вакцине, а также благодаря нахождению эффективного, удобного в технологическом плане и безопасного адъюванта.
Указанный технический результат достигнут созданием вакцины ассоциированной против НБ, РВТ и МПВИ птиц инактивированной эмульсионной, охарактеризованной следующей совокупностью признаков.
Согласно изобретению предлагаемая вакцина содержит в качестве активного вещества смесь из авирулентного очищенного антигенного материала из штамма «Ла Сота» вируса НБ птиц, полученного в 9÷12 - суточных эмбрионах SPF - кур с инфекционной активностью не ниже 10,0 Ig ЭИД50/см3 до инактивации, из авирулентного очищенного антигенного материала из штамма "1133" вируса РВТ птиц, полученного в культуре клеток ФЭК с инфекционной активностью не ниже 7,5 Ig ТЦД50/см3 до инактивации, из авирулентного очищенного антигенного материала из штамма "1733" вируса РВТ птиц, полученного в культуре клеток ФЭК с инфекционной активностью не ниже 7,5 Ig ТЦД50/см3 до инактивации, и авирулентного очищенного антигенного материала из штамма "PVO3-B" метапневмовируса птиц, полученного в перевиваемой культуре клеток Vero, с инфекционной активностью не ниже 7,0 Ig ТЦД50/см3 до инактивации, взятых в объемном соотношении 0,3:0,6:0,6:1,5 соответственно и в количествах, обеспечивающих протективную иммуногенную активность каждого антигена в организме птицы после введения ей целевого препарата.
В качестве целевой добавки предлагаемая вакцина содержит масляный адъювант марки Montanide ISA-70 VG производства "Seppic" (Франция, стандарт ИСО 9001).
В предлагаемой вакцине активное вещество и целевая добавка объединены в соотношении, мас.%: 30,0:70,0 соответственно.
Предлагаемое изобретение включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается правовая охрана:
1. Вакцина ассоциированная против НБ, РВТ и МПВИ птиц инактивированная эмульсионная.
2. Активное вещество.
3. В качестве активного вещества смесь из авирулентного очищенного антигенного материала из штамма "Ла Сота" вируса НБ птиц, сем. Paramyxoridae, подсемейства Parmyxovirinae, рода Avulavirus, серотипа 1, из авирулентного очищенного антигенного материала из штамма "1133" вируса РВТ птиц сем. Reoviridae, рода Orthoreovirus, коллекция ФГУ "ВГНКИ" "1133-ДЕП", из авирулентного очищенного антигенного материала из штамма "1733" вируса РВТ птиц сем. Reoviridae, рода Orthoreovirus, коллекция ФГУ "ВГНКИ" "1733"-116-ДЕП", и из авирулентного очищенного материала из штамма "PVO3-B №127-ДЕП" вируса МПВИ птиц, сем. Paramyxoviridae, подсемейства Pneumovirinae, рода Metapneumovirus, подтипа В, коллекция ФГУ "ВГНКИ" "PVO3-B №127-ДЕП", взятых в объемном соотношении 0,3:0,6:0,6:1,5 соответственно и в количествах, обеспечивающих протективную иммунногенную активность каждого антигена в организме птиц после введения им целевого препарата.
4. Целевая добавка.
5. В качестве целевой добавки масляный адъювант.
Признаками изобретения, характеризующими предлагаемую вакцину и совпадающими с признаками прототипа, в том числе родовое понятие, отражающее назначение, являются:
1. Вакцина ассоциированная против НБ и МПВИ птиц инактивированная эмульсионная.
2. Активное вещество.
3. Целевая добавка.
По сравнению с вакциной-прототипом существенные отличительные признаки предлагаемой вакцины заключаются в том, что в качестве активного вещества она содержит смесь из авирулентного очищенного антигенного материала из штамма "Ла Сота" вируса НБ птиц сем. Paramyxoviridae, подсем. Paramyxovirinae, рода Avulavirus, серотипа 1, из авирулентного очищенного антигенного материала из штамма "1133" вируса РВТ птиц сем. Reoviridae, рода Orthoreovirus, коллекция ФГУ "ВГНКИ " "1133-ДЕП", из авирулентного очищенного антигенного материала из штамма "1733" вируса РВТ птиц сем. Reoviridae, рода Orthoreovirus, коллекция ФГУ "ВГНКИ" "1733"-116-ДЕП", и из авирулентного очищенного материала из штамма "PV03-B" вируса МПВИ птиц сем. Paramyxoviridae, подсемейства Pneumovirinae, рода Metapneumovirus, подтипа В, коллекция ФГУ "ВГНКИ" "PVO3-B №127-ДЕП", взятых в объемном соотношении 0,3:0,6:0,6:1,5 соответственно и в количествах, обеспечивающих иммуногенную активность каждого антигена в организме птицы после введения ей целевого препарата.
Предлагаемое изобретение характеризуется другими отличительными признаками, выражающими конкретные формы выполнения или особые условия его использования:
1. Авирулентный очищенный антигенный материал из штамма "Ла Сота" вируса НБ птиц, полученного в 9÷12 - суточных эмбрионах SPF-кур с инфекционной активностью не ниже 10,0 Ig ЭИД50/см3 до инактивации, в количестве 3,0 мас.%.
2. Авирулентный очищенный антигенный материал из штамма "1133" вируса РТВ птиц, полученного в культуре клеток ФЭК с инфекционной активностью не ниже 7,5 Ig ТЦД50/см3 до инактивации, в количестве 6,0 мас.%.
3. Авирулентный очищенный антигенный материал из штамма "1733" вируса РТВ птиц, полученного в культуре клеток ФЭК с инфекционной активностью не ниже 7,5 Ig ТЦД50/см3 до инактивации, в количестве 6,0 мас.%.
4. Авирулентный очищенный антигенный материал из штамма "PVO3-B" метапневмовируса птиц, полученного в перевиваемой культуре клеток Vero с инфекционной активностью не ниже 7,0 Ig ТЦД50/см3 до инактивации, в количестве 15,0 мас.%.
5. Масляный адъювант в количестве не менее 70,0 мас.%.
6. Смесь из авирулентного очищенного антигенного материала из штамма "Ла Сота" вируса НБ птиц, полученного в 9÷12 - суточных эмбрионах SPF-кур с инфекционной активностью не ниже 10,0 Ig ЭИД50/см3 до инактивации, из авирулентного очищенного антигенного материала из штамма "1133" вируса РТВ птиц, полученного в культуре клеток ФЭК с инфекционной активностью не ниже 7,5 Ig ТЦД50/см3 до инактивации, из авирулентного очищенного антигенного материала из штамма "1733" вируса РТВ птиц, полученного в культуре клеток ФЭК с инфекционной активностью не ниже 7,5 Ig ТЦД50/см3 до инактивации, из авирулентного очищенного антигенного материала из штамма "PVO3-B" метапневмовируса птиц, полученного в перевиваемой культуре клеток Vero, с инфекционной активностью не ниже 7,0 Ig ТЦД50/см3 до инактивации, и масляный адъювант в соотношении, мас.%.
| Антигенный материал из штамма "Ла Сота" вируса НБ птиц | 3,0 |
| Антигенный материал из штамма "1133" вируса РВТ птиц | 6,0 |
| Антигенный материал из штамма "1733" вируса РВТ птиц | 6,0 |
| Антигенный материал из штамма "PVO3-B" вируса МПВИ птиц | 15,0 |
| Масляный адъювант | до 100,0 |
Входящие в предлагаемую вакцину штаммы вирусов известны и являются производственными при изготовлении моновакцин (8÷16).
В результате проведенных исследований авторы определили важнейшие технологические показатели, позволившие создать препарат, в котором отсутствует конкуренция между антигенами, входящими в состав предлагаемой вакцины, а его иммуногенные свойства были сравнимы с таковыми после применения монопрепаратов.
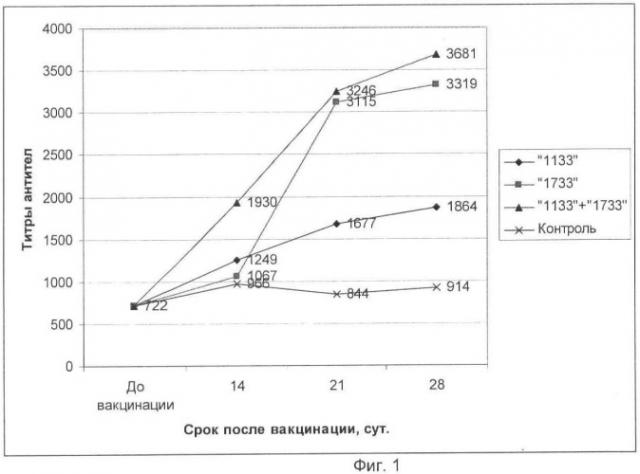
В результате проведенной НИР и анализа литературы было решено в компонентном составе предлагаемой вакцины использовать два штамма вируса РВТ - «1133» и «1733». Это было сделано по нескольким причинам. Во-первых, было доказано, что совместное применение данных штаммов вызывает выработку более напряженного иммунитета у птиц против возбудителя РВТ, на что указывают результаты серологических исследований опытных сывороток крови (табл.3, фиг.1). Во-вторых, в результате использования в предлагаемой вакцине в качестве компонента РВТ двух антиген отличающихся штаммов РВТ повышается эффективность применяемой вакцины в отношении различных штаммов полевых возбудителей реовирусной инфекции (7).
Дополнительный технический результат от использования предлагаемого изобретения достигается за счет того, что для инактивации вирусосодержащих материалов используют аминоэтилэтиленимин (АЭЭИ), что позволяет значительно снизить трудо- и энергозатраты на изготовление вакцины и повысить качество антигенных материалов.
Дополнительный технический результат от использования предлагаемого изобретения в части повышения антигенной и иммуногенной активности целевого продукта достигается также за счет использования в его составе масляного адъюванта Montanide ISA - 70 VG производства фирмы " SEPPIC" (Франция, стандарт ИСО 9001).
Сущность изобретения пояснена на графических материалах, на которых на:
фиг.1 представлено графическое изображение динамики образования поствакцинальных антител на антигенный компонент РВТ образцов предлагаемой вакцины, содержащих в своем составе различные комбинации штаммов вируса РВТ птиц;
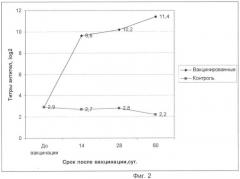
фиг.2 представлено графическое изображение динамики образования поствакцинальных антител на антигенный компонент НБ птиц серии №1 предлагаемой вакцины;
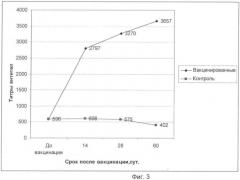
фиг.3 - графическое изображение динамики образования поствакцинальных антител на антигенный компонент РВТ птиц серии №1 предлагаемой вакцины;
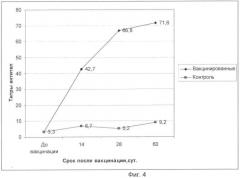
фиг.4 - графическое изображение динамики образования поствакцинальных антител на антигенный компонент МПВИ птиц серии №1 предлагаемой вакцины;
фиг.5 - графическое изображение динамики образования
поствакцинальных антител на антигенный компонент НБ птиц серии №2 предлагаемой вакцины;
фиг.6 - графическое изображение динамики образования поствакцинальных антител на антигенный компонент РВТ птиц серии №2 предлагаемой вакцины;
фиг.7 - графическое изображение динамики образования поствакцинальных антител на антигенный компонент МПВИ птиц серии №2 предлагаемой вакцины.
Используемый для изготовления предлагаемой вакцины штамм "Ла Сота" вируса НБ птиц характеризуется следующими признаками и свойствами.
Морфологические признаки
Вирус НБ птиц штамма " Ла Сота" относится к сем. Paramyxoviridae, подсем. Paramyxovirinae, роду Avulavirus, серотипу 1 и обладает одноцепочечным несегментированным РНК-геномом негативной полярности, состоящим более чем из 15000 нуклеотидов. Сферические, покрытые оболочкой вирионы имеют диаметр 150 нм и более с характерными поверхностными выступами длиной 8 нм. Есть филаментозные формы диаметром 60÷100 нм и варьирующей длины до нескольких микрометров. Нуклеокапсид имеет спиральный тип симметрии, РНП 12÷17 нм, длину до 1 мкм и жестко упорядоченную структуру. Встречаются вирионы, содержащие несколько нуклеокапсидов.
Антигенные свойства
Антигенная структура стабильна: 5÷7 полипептидов с молекулярной массой 35÷200 килодальтон, один или более поверхностных антигенов; один нуклеокапсидный антиген. Реплицируются в цитоплазме. Обладают геммагглютинирующими свойствами. Некоторые члены семейства имеют нейраминидазу и РНК-зависимую РНК-полимеразу. При вакцинации вирус индуцирует образование специфических антител. Титр гемагглютининов в экстраэмбриональной жидкости при культивировании в эмбрионах кур не ниже 1:256.
Биотехнологические характеристики
Вирус НБ проявляет высокую биологическую, иммуногенную и антигенную активность, культивируется в 9÷12 - суточных эмбрионах SPF-кур. Инфекционная активность в лиофилизованном виде не ниже 8,0 Ig ЭИД50/см3.
Устойчивость к внешним факторам
Штамм "Ла Сота" вируса НБ птиц чувствителен к эфиру, инактивируется при рН 3,0. Лиофилизованный вирус хранится при температуре минус 2÷40°С в течение 12 месяцев.
Дополнительные признаки и свойства
Свободен от бактериальной и грибной контаминации. Сохраняет инфекционную активность при температуре минус 20÷40°С в течение 12 месяцев, а в лиофилизованном виде при титровании в эмбрионах или в трахеальной органной культуре эмбрионов кур не ниже 6,5 Ig ЭИД50/см3.
Для получения антигенного материала из штамма "Ла Сота" вируса НБ птиц в качестве чувствительной биологической системы культивирования используют преимущественно 9÷12 - суточные эмбрионы SPF-кур. Полученный вирусосодержащий материал очищают от балластных примесей центрифугированием или любым другим известным методом.
Для инактивации вируса НБ птиц используют АЭЭИ, который добавляют в очищенную вирусосодержащую суспензию до концентрации 0,05-0,1%. Инактивацию вируса проводят при температуре 37±0,5°С и рН в пределах 7,0-7,6 в течение 24 часов. По окончании инактивации АЭЭИ нейтрализуют внесением в антигенный материал тиосульфата натрия. Для этого в охлажденную суспензию антигена добавляют 1М раствор тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Полученный антиген подвергают контролю на антигенную активность, авирулентность, стерильность и pH.
Для изготовления предлагаемой вакцины используют авирулентный очищенный антигенный материал из штамма "Ла Сота" вируса НБ птиц, полученного в 9÷12 - суточных эмбрионах SPF-кур с инфекционной активностью не ниже 9,0 Ig ЭИД50/см3 до инактивации и ГА-активностью не ниже 1: 512, в количестве 3,0 мас.%.
Используемые для изготовления предлагаемой вакцины штаммы "1133" и "1733" вируса РВТ птиц относятся к семейству Reoviridae, роду Orthoreovirus, депонированы 14.07.1998 г. и 13.12.2001 г. соответственно в коллекцию штаммов микроорганизмов ФГУ "ВГНКИ" под регистрационными номерами "1133-ДЕП" и "1733"-116ДЕП" и характеризуются следующими признаками и свойствами.
Морфологические признаки
Реовирус не имеет оболочки, обладает икосаэдральной симметрией и двухкапсидной структурой. Вирусные частицы имеют диаметр около 75 нм и плотность в хлориде цезия 1,36÷1,37 г/см3. Вирусный геном состоит из 2-спиральной РНК и имеет фрагментарную структуру. По размеру геном можно разделить на три класса с 10 дискретными молекулярными видами.
Антигенные свойства
Реовирусы птиц обладают группоспецифическим антигеном. Его можно наблюдать в реакции диффузионной преципитации. Специфичность антигена серотипа можно определить в реакции нейтрализации. Нейтрализующие антитела определяются уже спустя 70 дней после инфицирования, а преципитирующие - приблизительно на вторую неделю. Исследованиями ин vivo и ин vitro была доказана способность реовирусов птиц вырабатывать интерферон.
Биотехнологические характеристики
Реовирусы хорошо растут в эмбрионах SPF-кур после инфицирования через желточный мешок или на хориоаллантоисную оболочку, при этом, гибель эмбрионов наступает через 3÷5 или 8 дней соответственно. Вирус способен расти в первичных куриных клеточных культурах легких, почек, печени, макрофагов и семенников эмбриона. Фибробласты куриного эмбриона также являются подходящей средой для роста вируса, но для этого часто приходится проводить адаптацию вируса. Доказано, что реовирус растет в таких клеточных линиях, как Vero, ВНК-21/13, почек кроликов, почек свиней, в клеточной линии японских перепелов и лимфобластоидных клетках кур.
Устойчивость к внешним факторам
Реовирусы не чувствительны к эфиру, слабо чувствительны к хлороформу. Они устойчивы к действию pH 3, перекиси водорода в течение 1 часа при комнатной температуре, 2% лизолу и 3% формалину. Кроме того, они устойчивы к метаболическим ингибиторам ДНК: актиномицину. Д, цитозинарабиноозиду и 5-фтор-2-дезоксиридину. Реовирусы устойчивы к нагреванию и способны находиться при температуре 60°С в течение 8÷10 часов. Инактивируются 70% этанолом, 0,5% органическим йодом и 5% раствором перекиси водорода.
Дополнительные признаки и свойства
Обладает антигенной активностью в составе инактивированной вакцины.
Патогенность - выражена.
Вирулентность - выражена.
Контагиозность - выражена.
Онкогенность - отсутствует.
Штаммы "1133" и "1733" реовируса свободны от контаминации бактериями, микоплазмами и другими гемагглютинирующими вирусами.
Для получения антигенных материалов из штаммов "1133" и "1733" вируса РВТ в качестве чувствительной системы культивирования используют преимущественно первичную культуру клеток ФЭК. Полученные вирусосодержащие материалы очищают от балластных примесей центрифугированием или любым другим известным методом.
Для инактивации вируса РВТ птиц используют АЭЭИ, который добавляют в очищенные вирусосодержащие суспензии до концентрации 0,1%. Инактивацию вируса проводят при температуре 37±0,5°С и pH 7,4÷7,6 в течение 24 часов. По окончании инактивации АЭЭИ нейтрализуют внесением в антигенный материал тиосульфата натрия. Для этого в охлажденные суспензии каждого антигена добавляют 2М раствора тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Полученные антигены подвергают контролю на антигенную активность, авирулентность, стерильность и pH.
Для изготовления предлагаемой вакцины используют авирулентные очищенные антигенные материалы из штаммов "1133"и "1733" вируса РВТ птиц, полученные в культуре клеток ФЭК с инфекционной активностью не ниже 7,5 Ig ТЦД50/см3 до инактивации в количестве не ниже 6,0 мас.% для каждого из штаммов.
Используемый для изготовления предлагаемой вакцины штамм "PVO3-B" вируса МПВИ птиц относится к семейству Paramixoviridae, роду Metapneumovirus, депонирован 22.11.2006 г. в коллекцию штаммов микроорганизмов ФГУ "ВГНКИ" под регистрационным номером "PVO3-B №127-ДЕП" и характеризуется следующими признаками и свойствами.
Морфологические признаки
Метапневмовирус птиц - это РНК-содержащий вирус, с несегментированным одноцепочечным негативным геномом (17÷20).
Вирус сложный, имеет комплексную структуру и покрыт липопротеиновой оболочкой, образующейся при выходе вириона. Образует сферические частицы, симметричные по спиральному типу, которые имеют размеры 80-200 нм. Оболочка напоминает бахрому, равномерно покрытую поверхностными выступами длиной 13÷15 нм, которые представляют собой шипы, их ширина равна 2÷3 нм у основания, максимальная - 3÷5 нм, расстояние между шипами равно 2÷3 нм.
Антигенные свойства
ГА-активность по отношению к эритроцитам кур, индеек, уток, свиней, крупного рогатого скота, мышей и морских свинок отсутствует. Метапневмовирусы обладают группоспецифичным антигеном. Специфичность антигена можно определить в реакции нейтрализации вируса в культурах органов или в культуре клеток Vero.
Биотехнологические характеристики
Вирус МПВИ размножается в культурах клеток 18 первичных и 11 перевиваемых линий, вызывая цитопатические изменения. Репродукция его в культуре тканей сопровождается уплотнением цитоплазмы клеток, появлением в них вакуолей и вирусных частиц. Через 40 часов в цитоплазме некоторых клеток обнаруживается множество малых аморфных эозинофильных включений, окруженных прозрачной зоной. В одной клетке может быть до 12 (и более) таких включений. Через 2 дня в зараженных культурах увеличивается количество клеток с пикнотическим ядром, а через 7 дней поражаются все клетки.
Согласно литературным данным субкультуры клеток по чувствительности к вирусам не уступают первичным культурам и являются более экономичными.
Устойчивость к внешним факторам
Вирус МПВИ птиц активен в пределах pH 4,5÷9, не устойчив к действию высоких температур. Так, при температуре 37°С через 24 часа титр инфекционности понижался до 1 Ig, а через 72 часа вирус полностью инактивировался. При температуре 50°С вирус разрушался через 6 часов. Вирус термочувствителен (к заморозке и оттаиванию), неустойчив при pH 3,0. При температуре 20°С инфекционная активность вируса снижалась до нуля за 4 недели, при 4°С - через 20 недель, а при минус 20°С и минус 70°С не снижалась и через 58 недель. При хранении сухого вируссодержащего материала при комнатной температуре в течение 7 суток вирус сохранял жизнеспособность и размножался в культуре клеток Vero. Большинство дезинфицирующих растворов при температуре 20°С в течение 10 мин полностью не разрушают вирус, кроме органических растворителей таких, как хлороформ и этиловый спирт концентрацией 30÷40%. Препараты, в состав которых входят различные органические кислоты, и препараты, содержащие разные альдегиды, были способны инактивировать вирус in vitro в пределах 15 мин при концентрации 0,5%. Дезинфектанты, такие, как соединения четырехзамещенного аммония, этанол, йодоформ, производные фенола, бигуанид и хлорная известь активно снижали жизнеспособность вируса. По последним данным, метапневмовирус птиц выживает до 72 часов на большинстве поверхностей разных предметов.
Дополнительные признаки и свойства
Обладает антигенной активностью в составе инактивированной вакцины.
Патогенность - выражена.
Вирулентность - выражена.
Контагиозность - выражена.
Онкогенность - отсутствует.
Штамм "PVO3-B" метапневмовируса птиц свободен от контаминации бактериями, микоплазмами и другими гемагглютинирующими вирусами.
Для получения антигенного материала из штамма "PVO3-B" вируса МПВИ в качестве чувствительной системы культивирования используют культуру клеток Vero. Полученный вирусосодержащий материал очищают от балластных примесей центрифугированием или любым другим известным методом.
Для инактивации вируса МПВИ используют АЭЭИ, который добавляют в очищенную вирусосодержащую суспензию до концентрации 0,1%. Инактивацию вируса проводят при температуре +37±0,5°С и pH 7,4÷7,6 в течение 24 часов. По окончании инактивации АЭЭИ нейтрализуют внесением в антигенный материал тиосульфата натрия. Для этого в охлажденную суспензию антигена добавляют 2М раствор тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Полученный антиген подвергают контролю на антигенную активность, авирулентность, стерильность и pH.
Для изготовления предлагаемой вакцины используют авирулентный очищенный антигенный материал из штамма "PVO3-B" вируса МПВИ, полученного в культуре клеток Vero с инфекционной активностью не ниже 7,0 Ig ТЦД50/см3 до инактивации, в количестве не ниже 15,0 мас.%.
Для изготовления предлагаемой вакцины полученные антигенные материалы из штамма "Ла Сота" вируса НБ птиц, из штамма "1133" вируса РВТ, из штамма "1733" вируса РВТ и из штамма "PVO3-B" вируса МПВИ птиц смешивают в объемном соотношении 0,3:0,6:0,6:1,5 соответственно и смесь тщательно эмульгируют с масляным адъювантом в весовом соотношении, мас.%: 30,0:70,0 соответственно. При этом для получения антигенной фазы препарата используют метод смешивания неодинаковых весовых объемов полученных антигенных материалов в соотношении, мас.%:
| Авирулентный очищенный антигенный материал | 3,0 |
| из штамма "Ла Сота" вируса НБ птиц, полученного | |
| в 9÷12- суточных эмбрионах SPF-кур | |
| с инфекционной активностью | |
| не ниже 10,0 Ig ЭИД50/см3 до инактивации | |
| Авирулентный очищенный антигенный материал | 6,0 |
| из штамма "1133 " вируса РВТ птиц, полученного в культуре | |
| клеток ФЭК с инфекционной активностью | |
| не ниже 7,5 Ig ТЦД50/см3 до инактивации | |
| Авирулентный очищенный антигенный материал | 6,0 |
| из штамма "1733 " вируса РВТ птиц, полученного в культуре | |
| клеток ФЭК с инфекционной активностью | |
| не ниже 7,5 Ig ТЦД50/см3 до инактивации | |
| Авирулентный очищенный антигенный материал | 15,0 |
| из штамма "PVO3-B" метапневмовируса птиц, | |
| полученного в перевиваемой культуре клеток | |
| Vero, с инфекционной активностью не ниже | |
| 7,0 Ig ТЦД50/см3 до инактивации |
Из масляных адъювантов целесообразно использовать масляный адъювант марки Montanide ISA-70 VG производства фирмы "SEPPIC" (Франция, стандарт ИСО 9001).
Содержание антигенов в предлагаемой вакцине в указанном выше соотношении является их эффективным количеством в препарате, обеспечивающим достижение технического результата.
Использование предлагаемого изобретения расширяет арсенал высокоиммуногенных безвредных и ареактогенных эмульсионных инактивированных ассоциированных вакцин против НБ, РВТ и МПВИ птиц, способных защищать взрослое поголовье птиц от заражения возбудителем НБ, а также индуцировать высокий уровень материнских антител у молодняка птиц и соответственно защитить его от заражения вирусами НБ, РВТ и МПВИ в первые дни жизни.
Сущность предлагаемого изобретения пояснена примерами его исполнения и использования.
Пример 1
Получение антигенного материала из штамма " Ла Сота" вируса НБ.
Для получения производственной расплодки вируса НБ птиц используют вирус производственного штамма "Ла Сота", репродуцированный в 9÷12 - суточных эмбрионах SPF-кур с титром инфекционной и ГА-активности не ниже 8,0 Ig ЭИД50/м3 и 1:1024 соответственно и хранившийся при температуре не выше минус 40°С в течение не более 90 суток. Посевной вирус размораживают при температуре (+18°С)÷(+24°С) и центрифугируют при 2500 об/мин в течение 10 минут. Надосадочную жидкость отбирают, разводят стерильным физиологическим раствором pH 7,2 из расчета 100000-200000 ЭИД50/см3 (1:10000).
Приготовленный таким образом вирусосодержащий материал используют для заражения 9÷10 - суточных эмбрионов SPF-кур. Вирусосодержащий материал вносят в аллантоисную полость в объеме 0,2 см3. Зараженные куриные эмбрионы инкубируют 72÷96 часов при температуре (+36°С)÷(+37°С) и относительной влажности 60÷70%. Овоскопию зараженных эмбрионов проводят ежедневно в течение 96 часов инкубации. По окончании инкубации эмбрионы помещают в холодильную камеру при температуре (+2°С)÷(+6°С) на 16÷18 часов для того, чтобы при вскрытии исключить попадание эритроцитов в алантоисно-эмбриональную жидкость. Перед вскрытием эмбрионы выдерживают 2÷3 часа при комнатной температуре до испарения конденсата (влаги) на скорлупе. После охлаждения куриные эмбрионы вскрывают, соблюдая правила асептики. ЭЭЖ от каждых 20÷30 эмбрионов собирают в стерильные флаконы вместимостью 200÷500 см3. Затем ЭЭЖ центрифугируют при 1000 об/мин в течение 10÷15 минут для удаления эритроцитов. После центрифугирования вирусный материал сливают в 15÷20 - литровые бутыли. Из каждой бутыли берут пробу в количестве 1,0 см3 для определения титра гемагглютинина и биологической активности вируса НБ. Инфекционная активность вирусосодержащего материала, идущего на составление предлагаемой вакцины, должна быть не ниже 9,0 Ig ЭИД50/см3, а ГА-активность не ниже 1:512.
Полученный вирусный материал подвергают инактивации рабочим раствором АЭЭИ. Для этого предварительно вирусную суспензию нагревают в реакторе до температуры +37,0±0,5°С, а затем в нее добавляют 10%-ный раствор АЭЭИ (рабочий ра