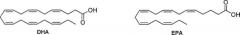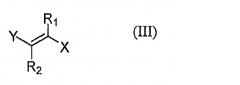Конъюгированные липидные производные
Иллюстрации
Показать всеИзобретение относится к новому липидному соединению общей формулы (I), в которой n=0; R1 и R2 являются одинаковыми или различными и могут быть выбраны из группы заместителей, состоящей из атома водорода, С1-С7алкильной группы, атома галогена и С1-С7алкокси группы; Х представляет собой COR3 или CH2OR4, где R3 выбран из группы, состоящей из водорода, гидрокси, С1-С7алкокси и амино; и R4 выбран из группы, состоящей из водорода, С1-С7алкила или С1-С7ацила, Y представляет собой С9-С21алкен с одной или несколькими двойными связями в Е- или Z-конфигурации, при этом цепь Y является незамещенной и содержит двойную связь в ω-3 положении; при условии, что R1 и R2 не могут одновременно представлять собой атом водорода. Изобретение также относится к фармацевтическим композициям, содержащим липидные соединения, которые используются для лечения и/или предотвращения состояния, связанного с повышенными функциями NFkB, лечения и/или предотвращения воспалительного заболевания или состояния, понижения уровней инсулина в плазме и/или глюкозы в крови, лечения резистентности к инсулину и лечения и/или предотвращения резистентности периферических тканей к инсулину и/или диабетического состояния, например диабета 2 типа.
6 н. и 39 з.п. ф-лы, 1 табл., 1 ил., 31 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым α,β-ненасыщенным производным жирных кислот, к ненасыщенным жирным кислотам, к способам получения таких соединений, фармацевтическим и липидным композициям, содержащим эти соединения, и к применениям этих соединений и композиций в медицине.
Уровень техники
Пищевые полиненасыщенные жирные кислоты (PUFA) оказывают воздействие на различные физиологические процессы, влияющие на нормальное состояние здоровья и хронические заболевания, такие как регуляция уровней липидов в плазме, сердечно-сосудистые и иммунные функции, действие инсулина и развитие нейронов и зрительная функция. Усвоение PUFA (как правило, в сложноэфирной форме, например, в составе глицеридов или фосфолипидов) будет приводить к их распределению по существу в каждой клетке организма, воздействуя на состав и функцию мембран, синтез эйкозаноидов, передачу клеточных сигналов и регуляцию экспрессии генов. Вариации в распределении различных жирных кислот/липидов в различных тканях, в дополнение к специфичному клеточному метаболизму липидов, а также регулируемая жирными кислотами экспрессия факторов транскрипции, вероятно, играют важную роль в определении того, как именно клетки реагируют на изменения композиции PUFA (Benatti, P. et al., J. Am. Coll. Nutr. 2004, 23, 281).
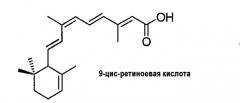
PUFA или их метаболиты, как показано, модулируют транскрипцию генов посредством взаимодействия с несколькими ядерными рецепторами. Они представляют собой активируемые пероксисомальным пролифератором рецепторы (PPAR), ядерный рецептор гепатоцитов (HNF-4), X рецептор печени (LXR) и рецептор 9-цис-ретиноевой кислоты (ретиноевый X рецептор, RXR). Лечение с помощью PUFA может также регулировать множество факторов транскрипции в ядре, включая SREBP, NFκB, c/EBPβ и HIF-1α. Эти эффекты не связаны с прямым связыванием жирной кислоты с фактором транскрипции, но включают механизмы, которые влияют на ядерное содержание факторов транскрипции.
Регуляция транскрипции генов с помощью PUFA оказывает выраженное воздействие на метаболизм клеток и тканей и дает надежное объяснение вовлечения взаимодействий питательное вещество-ген в инициирование и предотвращение или облегчение заболеваний, таких как ожирение, диабет, сердечно-сосудистые расстройства, иммунные воспалительные заболевания и раковые заболевания (Wahle, J., et al., Proceedings of Nutrition Society, 2003, 349).
Рыбий жир, обогащенный ω-3 полиненасыщенными жирными кислотами, эйкозапентаеновой кислотой (EPA) и докозагексаеновой кислотой (DHA), как показано, уменьшают риск сердечно-сосудистых заболеваний, частично посредством понижения концентрации триглицеридов в крови. Этот благоприятный эффект возникает в основном благодаря объединенным воздействиям ингибирования липогенеза посредством уменьшения содержания SPEBP-1 и стимулирования окисления жирных кислот посредством активирования PPAR-α в печени.
ω-3 Полиненасыщенные жирные кислоты в рыбьем жире, как сообщается, улучшают прогноз нескольких хронических воспалительных заболеваний, характеризуемых аккумуляцией лейкоцитов, и опосредуемых лейкоцитами повреждений тканей, включая атеросклероз, IgA нефропатию, воспалительное заболевание желудка, ревматоидный артрит, псориаз и тому подобное (Mishra, A., Arterioscler. Thromb. Vasc. Biol., 2004, 1621).
DHA представляет собой наиболее распространенную ω-3 PUFA в большинстве тканей и содержится в большом количестве в нейронных мембранах, составляя приблизительно 30-40% фосфолипидов серого вещества церебрального кортекса и фоторецепторных клеток в сетчатке. DHA аккумулируется при высоких уровнях в постнатальной CNS млекопитающих, показывая, что DHA вовлечена в созревание CNS. У нескольких различных видов пониженные уровни DHA в мозгу и в сетчатке связываются с ослаблением нейронных и зрительных функций. Добавление DHA может быть полезным при лечении депрессии, шизофрении, гиперактивности, рассеянного склероза, болезни Альцгеймера, дегенеративных заболеваний сетчатки и пероксисомальных расстройств (Horrocks and Farooqui, Prostaglandins, Leukotrienes and Essential Fatty acids, 2004, 70, 361). Пищевые DHA могут также быть полезными при лечении атеросклероза, воспаления и рака (Horrocks et al., Pharmacol. Res. 1999, 40: 211; Rose, et al., 1999, 83, 217).
Хотя ω-3 PUFA обладают многими положительными биологическими воздействиями, их терапевтическая ценность является ограниченной, и терапевтическая область, где ω-3 PUFA являются наиболее перспективными, представляет собой сердечно-сосудистую область, в качестве агента, понижающего уровни триглицеридов. Однако для того, чтобы вызвать гиполипидемию, необходимы высокие дозы полиненасыщенных жирных кислот. Одна из причин этого представляет собой деградацию полиненасыщенных жирных кислот в печени посредством окисления.
Ядерные рецепторы (NR) составляют большое и очень консервативное семейство активируемых лигандами факторов транскрипции, которые регулируют разнообразные биологические процессы, такие как развитие, метаболизм и репродукция. Замечено, что лиганды к этим рецепторам могут использоваться при лечении распространенных заболеваний, таких как атеросклероз, диабет, ожирение и воспалительные заболевания. В этом качестве NR становятся важными мишенями для лекарственных средств, и идентификация новых лигандов NR вызывает большой интерес. Активность множества ядерных рецепторов контролируется посредством связывания малых липофильных лигандов, которые включают гормоны, метаболиты, такие как жирные кислоты, желчные кислоты, оксистерины и ксено- и эндобиотики. Ядерные рецепторы могут связываться как мономеры, гомодимеры или гетеродимеры RXR с ДНК. Существует три типа гетеродимерных комплексов: незанятые гетеродимеры, непермиссивные гетеродимеры, которые могут активироваться только лигандами-партнерами, но не одним лишь лигандом RXR, и пермиссивные гетеродимеры, которые могут активироваться с помощью либо лигандов RXR, либо его рецептора-партнера, и активируются синергетически в присутствии обоих лигандов (Aranda and Pascual, Physiological Reviews, 2001, 81, 1269). В качестве обязательного гетеродимерного партнера для множества ядерных рецепторов (включая рецептор витамина D (VDR), рецептор тироидного гормона (TR), рецептор полностью транс-ретиноевой кислоты (RAR), активируемый пероксисомальным пролифератором рецептор (PPAR), X рецептор печени (LXR) и другие) RXR играет роль главного координатора множества путей ядерных рецепторов.
Лиганды, которые регулируют гетеродимерные партнеры RXR, могут грубо разделяться на два подмножества. Одно подмножество содержит обладающие высоким сродством, сильно специфичные лиганды стероидов/гормонов (VDR и TR) и действуют как эндокринные модуляторы. Другое подмножество связывается с имеющимися в избытке липидными лигандами, обладающими более низким сродством (PPAR, LXR), и, видимо, действуют частично как липидные биосенсоры. Гены, регулируемые гетеродимерами RXR, включают гены, вовлеченные в разнообразные клеточные процессы, включая регуляцию клеточного цикла и дифференциацию. Они также регулируют гены, вовлеченные в перенос, биосинтез и метаболизм липидов (Goldstein, J.T. et al., Arch. Biochem. and Biophys., 2003, 420, 185).
Родственный лиганд RXR представляет собой 9-цис-ретиноевую кислоту, молекулу, которая также связывается с RAR и трансактивирует их с очень сходным сродством и эффективностью. С другой стороны, полностью транс-ретиноевая кислота, родственный лиганд RAR, не связывается с рецептором RXR.
Имеются доказательства, что лиганды RXR могут функционировать как сенсибилизаторы инсулина и могут уменьшать гипергликемию, гиперинсулинемию и гипертриглицеридемию у мышей ob/ob и db/db (Mukherjee et al., Nature, 1997, 386, 407). Сообщается также, что хроническое введение агонистов RXR крысам Zucker fa/fa уменьшает потребление пищи и увеличение массы тела, понижает концентрации инсулина в плазме, в то же время поддерживая нормогликемию (Liu, et al., Int. J. Obesity., 2000, 997; Ogilvie, K. et al., Endocrinology, 2004, 145, 565).
В 2000 году сообщалось, что DHA, выделенная из мозга мышей, селективно активирует RXR в анализах на основе клеток (Urquiza et al., Science 2000, 290, 2140, WO 01/73439). В этих исследованиях DHA не активирует RAR. После этого сообщалось, что несколько ненасыщенных жирных кислот, включая DHA, арахидоновую кислоту и олеиновую кислоту, могут специфично связывать и активировать LBD (домен связывания лиганда) RXRα и по этой причине действуют как лиганды in vivo этого рецептора (Lengquist J., et. al. Molecular & Cellular Proteomics 3, 2004, 692). В исследованиях, опубликованных Fan et al., показано, что DHA служит в качестве специфичного лиганда для активирования RXRα по отношению к n-6 PUFA в колоноцитах (Carcinogenesis, 2003, 24, 1541).
Хотя агонисты RXR известны, и эти соединения исследованы на различных биологических системах, литература не описывает использование модифицированных PUFA в качестве сильнодействующих лигандов для RXR.
Фактор транскрипции NF-κB представляет собой индуцируемый эукариотический фактор транскрипции семейства rel. Он представляет собой главный компонент каскада стрессовых реакций, который регулирует активирование генов раннего отклика, вовлеченных в экспрессию воспалительных цитокинов, молекул адгезии, белков теплового шока, циклооксигеназ, липоксигеназ и окислительно-восстановительных ферментов. Zhao, G. et al. (Biochemical and Biophysical Research. Comm., 2005, 909) предполагают, что противовоспалительные воздействия PUFA в клетках моноцитов человека THP-1 частично опосредуются посредством ингибирования активирования NF-κB через активирование PPAR-γ. Другие предполагают, что противовоспалительное воздействие PUFA опосредуется через зависимое от PPAR-α ингибирование активирования NF-κB.
Рецептор-селективные лиганды являются высокоприоритетными при поиске промежуточных продуктов для лекарственных средств на основе NR, поскольку нативные лиганды NR дают системные побочные воздействия и токсичность из-за отсутствия у них специфичности связывания.
9-цис-ретиноевая кислота регулирует разнообразные биологические функции через механизм, который включает связывание как RXR, так и RAR. Эти рецепторы вовлечены во множество различных функций. Их далеко идущие биологические воздействия мотивируют поиск RAR- или RXR-селективных лигандов. Неселективные ретиноидные лиганды при использовании в качестве лекарственных средств имеют побочные воздействия, такие как тератогенность и токсичность для кожи и слизистых, которые значительно уменьшаются, когда используются специфичные к RXR агонисты. Кроме того, показано, что под действием RXR-селективных агонистов может осуществляться опухолеспецифичный апоптоз. Селективные агонисты RXR могут предложить альтернативный подход для лечения метаболических расстройств. Таким образом, имеется необходимость в легкодоступных RXR-селективных лигандах, которые могут обеспечить рассмотренные выше преимущества без побочных воздействий неселективных лигандов.
Поскольку многие ядерные рецепторы распределяются по-разному в различных тканях, является важным получение лигандов, которые способны in vivo нацеливаться на указанные клетки, чтобы связывать и активировать целевой рецептор.
Сущность изобретения
Одной из целей настоящего изобретения является создание липидных соединений, имеющих фармацевтическую активность.
Эта цель достигается с помощью липидного соединения в соответствии с формулой (I):
где
- R1 и R2 являются одинаковыми или различными и могут быть выбраны из группы заместителей, состоящей из атома водорода, алкильной группы, атома галогена и алкокси группы;
- X представляет собой COR3 или CH2OR4, где
- R3 выбран из группы, состоящей из водорода, гидрокси, алкокси и амино,
- где Х дополнительно включает производные карбоновой кислоты, когда R3 представляет собой гидрокси; и
- R4 выбран из группы, состоящей из водорода, алкила или ацила,
- Y представляет собой C9-C21 алкен с одной или несколькими двойными связями с E- или Z-конфигурацией;
или любого его фармацевтически приемлемого комплекса, сольвата или пролекарства.
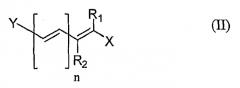
В частности, настоящее изобретение относится к липидным соединениям с E-конфигурацией в соответствии с формулой (II):
Когда X представлен формулой COR3 и R3 представляет собой гидрокси, настоящее изобретение также относится к производным карбоновых кислот. Например, такие производные карбоновой кислоты могут быть выбраны из группы, состоящей из фосфолипида или моно-, ди- или триглицерида.
В липидном соединении по настоящему изобретению R1 и R2 в формуле (I) являются одинаковыми или различными и могут быть выбраны из группы заместителей, состоящей из атома водорода, C1-C7 алкильной группы, C1-C7 алкокси группы и атома галогена.
Предпочтительно, R1 и R2 являются одинаковыми или различными и выбраны из группы заместителей, состоящей из атома водорода, C1-C3 алкильной группы, C1-C3 алкокси группы и атома галогена. Более предпочтительно, R1 и R2 являются одинаковыми или различными и выбраны из метильной группы, этильной группы и атома водорода.
Когда R1 и/или R2 представляют собой атомы галогена, предпочтительным является атом фтора. В липидном соединении по настоящему изобретению X может быть представлен формулой COR3. В таких случаях R3 может представлять собой C1-C7-алкокси группу, или, более конкретно, C1-C3-алкокси группу. Альтернативно, R3 представляет собой гидрокси группу.
В альтернативных вариантах осуществления X представлен формулой CH2OR4. В таких вариантах осуществления R4 может представлять собой C1-C7-алкильную группу или, более конкретно, C1-C3-алкильную группу. Альтернативно, R4 представляет собой C1-C7 ацильную группу, в частности C1-C3 ацильную группу.
В липидном соединении в соответствии с настоящим изобретением двойная связь между атомами углерода 2 и 3 предпочтительно находится в E-конфигурации.
В вариантах осуществления настоящего изобретения, где R1 и R2 являются различными и один из них представляет собой C1-C3 алкокси, а другой представляет собой водород, двойная связь между атомами углерода 2 и 3 может находиться в Z-конфигурации.
Как определено в общей формуле (I), Y может представлять собой C9-C21 алкен с одной или несколькими двойными связями с E- или Z-конфигурацией. В частности, Y представляет собой C14-C19 алкен с 2-6 двойными связями. В вариантах осуществления Y представляет собой C14-C19 алкен с 2-6 двойными связями в Z- конфигурации, чередующимися с метиленовыми группами. Альтернативно, Y является незамещенным. В предпочтительных вариантах осуществления настоящего изобретения липидное соединение содержит двойную связь углерод-углерод в ω-3 положении Y.
Липидные соединения по настоящему изобретению могут разделяться на категории в соответствии с количеством конъюгированных систем, представленных с помощью целого числа n в скобках в формуле (I) или (II). Как определено, n может изменяться в пределах между 0 и 2.
Когда n=0, липидное соединение по настоящему изобретению относится к формуле (III):
Кроме того, липидные соединения, представленные формулой (III) по настоящему изобретению, могут разделяться на подкатегории в виде следующих предпочтительных групп:
IIIa: X=COR 3
• X=COR3, где R3 представляет собой гидрокси группу или C1-C3 алкокси группу;
• R1 и R2 являются одинаковыми или различными и выбраны из атома водорода, C1-C3 алкильной группы, C1-C3 алкокси группы и атома галогена и
• Y представляет собой C13-C19 алкен, имеющий 2-6 двойных связей.
IIIb: X=COR 3 , R 1 ≠ R 2
• X=COR3, где R3 представляет собой гидрокси группу или C1-C2 алкокси группу;
• R1 и R2 являются различными, и один из них представляет собой атом водорода, а другой C1-C2 алкильную группу или C1-C2 алкокси группу; и
• Y представляет собой C17-C19 алкен, имеющий 3-5 двойных связей.
Предпочтительные соединения формулы (III) и подгрупп IIIa или IIIb представляют собой следующие липидные соединения 1-4, 6-8 и 26:
IIIc: X=CH 2 OR 4
• X=CH2OR4, где R4 представляет собой водород или C1-C3 ацильную группу;
• R1 и R2 являются одинаковыми или различными и выбраны из атома водорода, C1-C3 алкильной группы, C1-C3 алкокси группы и атома галогена и
• Y представляет собой C13-C19 алкен, имеющий 2-6 двойных связей.
IIId: X=CH 2 OR 4 , R 1 ≠ R 2
• X=CH2OR4, где R4 представляет собой водород; и
• R1 и R2 являются различными, и один из них представляет собой атом водорода, а другой C1-C2 алкильную группу или C1-C2 алкокси группу;
• Y представляет собой C17-C19 алкен, имеющий 3-5 двойных связей.
Предпочтительные соединения формулы (III) и подгрупп IIIc и IIId представляют собой следующие липидные соединения 5, 9 и 27:
Когда n=1, липидное соединение по настоящему изобретению относится к формуле (IV):
Кроме того, липидные соединения, представленные формулой (IV) по настоящему изобретению, могут разделяться на подкатегории в виде следующих предпочтительных групп:
IVa: X=COR 3
• X=COR3, где R3 представляет собой гидрокси группу или C1-C3 алкокси группу;
• R1 и R2 являются одинаковыми или различными и выбраны из атома водорода, C1-C3 алкильной группы и атома галогена; и
• Y представляет собой C11-C17 алкен, имеющий 2-6 двойных связей.
IVb: X=COR 3 , R 1 ≠ R 2
• X=COR3, где R3 представляет собой гидрокси группу или C1-C2 алкокси группу; и
• R1 и R2 являются различными, и один из них представляет собой атом водорода, а другой C1-C2 алкильную группу;
• Y представляет собой C15-C17 алкен, имеющий 3-5 двойных связей.
Предпочтительные соединения формулы (IV) и подгрупп IVa и IVb представляют собой следующие липидные соединения 10-11, 17-18, 20 и 22.
IVc: X=COR 3 , R 1 =R 2
• X=COR3, где R3 представляет собой гидрокси группу или C1-C2 алкокси группу;
• R1 и R2 представляют собой водород; и
• Y представляет собой C11-C17 алкен, имеющий 2-6 двойных связей.
IVd: X=COR 3 , R 1 =R 2
• X=COR3, где R3 представляет собой гидрокси группу или C1-C2 алкокси группу;
• R1 и R2 представляют собой водород; и
• Y представляет собой C15-C17 алкен, имеющий 4-5 двойных связей.
Предпочтительные соединения формулы (IV) и подгрупп IVc и IVd представляют собой следующие липидные соединения 12-15:
IVe: X=CH 2 OR 4
• X=CH2OR4, где R4 представляет собой атом водорода или C1-C3 ацильную группу;
• R1 и R2 являются одинаковыми или различными и выбраны из атома водорода, C1-C3 алкильной группы и атома галогена; и
• Y представляет собой C11-C17 алкен, имеющий 2-6 двойных связей.
IVf: X=CH 2 OR 4 , R 1 ≠ R 2
• X=CH2OR4, где R4 представляет собой водород;
• R1 и R2 являются различными, и один из них представляет собой атом водорода, а другой C1-C2 алкильную группу; и
• Y представляет собой C15-C17 алкен, имеющий 3-5 двойных связей.
Предпочтительные соединения формулы (IV) и подгрупп IVe и IVf представляют собой следующие липидные соединения 19, 21 и 23:
IVg: X=CH 2 OR 4 , R 1 =R 2
• X=CH2OR4, где R4 представляет собой водород;
• R1 и R2 являются одинаковыми и представляют собой атомы водорода; и
• Y представляет собой C11-C17 алкен, имеющий 2-6 двойных связей.
IVh: X=CH 2 OR 4 , R 1 =R 2
• X=CH2OR4, где R4 представляет собой водород;
• R1 и R2 являются одинаковыми и представляют собой атомы водорода; и
• Y представляет собой C17 алкен, имеющий 5 двойных связей.
Предпочтительное соединение формулы (IV) и подгрупп IVg и IVh представляет собой следующее липидное соединение 16:
Когда n=2, липидное соединение по настоящему изобретению относится к формуле (V)
Кроме того, липидные соединения, представленные формулой (V) по настоящему изобретению, могут разделяться на подкатегории в виде следующих предпочтительных групп:
Va: X=COR 3
• X=COR3, где R3 представляет собой гидрокси группу или C1-C3 алкокси группу;
• R1 и R2 являются одинаковыми или различными и выбраны из атома водорода, C1-C3 алкильной группы и атома галогена; и
• Y представляет собой C9-C16 алкен, имеющий 1-4 двойных связи.
Vb: X-COR 3 , R 1 ≠ R 2
• X=COR3, где R3 представляет собой гидрокси группу или C1-C2 алкокси группу;
• R1 и R2 являются различными, и один из них представляет собой атом водорода, а другой C1-C2 алкильную группу; и
• Y представляет собой C15 алкен, имеющий 4 двойных связи.
Предпочтительные соединения формулы (V) и подгрупп Va и Vb представляют собой следующие липидные соединения 24 и 25:
Настоящее изобретение также относится к способу получения липидного соединения в соответствии с любой из формул (I)-(V) настоящего изобретения.
Кроме того, настоящее изобретение относится к липидному соединению в соответствии с любой из формул (I)-(V) для применения в качестве лекарственного средства или для диагностических целей, например, для позитронной эмиссионной томографии (ПЭТ).
Настоящее изобретение также относится к фармацевтической композиции, содержащей липидное соединение в соответствии с любой из общих формул (I)-(V). Фармацевтическая композиция может содержать фармацевтически приемлемый носитель, наполнитель или разбавитель или любое их сочетание, и соответствующим образом предназначается для перорального введения. Соответствующая ежедневная доза липидного соединения в соответствии с любой из формул (I)-(V) составляет от 5 мг до 10 г указанного липидного соединения; от 50 мг до 1 г указанного липидного соединения или от 50 мг до 200 мг указанного липидного соединения.
Настоящее изобретение также относится к липидной композиции, содержащей липидное соединение в соответствии с любой из формул (I)-(V). Соответственно, по меньшей мере, 80% масс., или, по меньшей мере, 90% масс., или, по меньшей мере, 95% масс. липидной композиции состоит из указанного липидного соединения. Липидная композиция может дополнительно содержать фармацевтически приемлемый антиоксидант, например токоферол.
Кроме того, настоящее изобретение относится к применению липидного соединения в соответствии с любой из формул (I)-(V) для получения лекарственного средства для
• активирования или модулирования, по меньшей мере, одной из изоформ α, γ и/или δ активируемого пероксисомальным пролифератором рецептора (PPAR) человека;
• активирования или модулирования RXR;
• ингибирования или регулирования NF-ΚB;
• лечения и/или предотвращения воспалительного заболевания или состояния;
• понижения уровня инсулина в плазме, глюкозы в крови и/или триглицеридов в сыворотке;
• предотвращения и/или лечения повышенных уровней триглицеридов, уровней холестерина LDL (липопротеинов низкой плотности) и/или уровней холестерина VLDL (липопротеинов сверхнизкой плотности);
• предотвращения и/или лечения гиперлипидемического состояния, например гипертриглицеридемии (HTG);
• лечения и/или предотвращения ожирения или состояния с избыточной массой тела;
• лечения и/или предотвращения резистентности периферических тканей к инсулину и/или диабетического состояния;
• уменьшения массы тела и/или для предотвращения увеличения массы тела;
• лечения и/или предотвращения жирового заболевания печени, например неалкогольного жирового заболевания печени (NAFLD);
• лечения резистентности к инсулину, гиперлипидемии и/или ожирения или состояния с избыточной массой тела; и
• лечения и/или предотвращения диабета типа 2.
Настоящее изобретение также относится к липидным соединениям в соответствии с любой из формул (I)-(V) для лечения и/или предотвращения состояний, перечисленных выше.
Кроме того, настоящее изобретение относится к способам лечения и/или предотвращения состояний, перечисленных выше, включающих введение млекопитающему, нуждающемуся в этом, фармацевтически активного количества липидного соединения в соответствии с любой из формул (I)-(V).
Подробное описание настоящего изобретения
Неожиданно обнаружили, что новые полиненасыщенные производные, представленные общими формулами (I)-(V), имеют большее сродство к ядерным рецепторам семейства PPAR по сравнению с DHA и EPA. Производные дают агонисты RXR, более сильнодействующие, чем DHA.
RXR/PPAR представляет собой пермиссивный гетеродимер, который синергически активируются в присутствии обоих лигандов. Поскольку новые соединения по настоящему изобретению являются лигандами как для PPAR, так и для RXR, они могут действовать как агонисты двойного действия. Поскольку различные PUFA аккумулируются по-разному в различных тканях, эти модифицированные PUFA имеют потенциал для того, чтобы быть тканеспецифичными лигандами для ядерных рецепторов.
В дополнение к тому, что они являются лучшими лигандами для рецепторов PPAR и RXR, производные по настоящему изобретению не деградируются легко с помощью путей α- и β-окисления, как природные PUFA, из-за заместителя в α- или β-положении.
Новые соединения могут использоваться в терапии либо по одному, либо в сочетании с другими лигандами к PPAR с высоким сродством. В этом случае производное PUFA будет действовать как лиганд для RXR, синергически увеличивая влияние лиганда PPAR на транскрипцию гена.
В дополнение к этому предусматриваются новые соединения, которые приобретают функциональность ретиноидов: ретинола и ретиналя. Эти соединения представляют собой пролекарста, которые активируются in vivo с помощью путей окисления.
Номенклатура и терминология
Липидные соединения по настоящему изобретению являются замещенными по атому углерода 2 и/или 3, отсчитывая от функциональной группы, обозначенной X в формулах (I)-(V). Такие замещения могут называться "альфа-замещение" или "бета-замещение". В липидных соединениях по настоящему изобретению существует двойная связь между атомами углерода 2 и 3, которая предпочтительно находится в E-конфигурации.
Как здесь используется, термин "положение ω-3" означает, что первая двойная связь существует как третья связь углерод-углерод от конца конечной CH3 (ω) углеродной цепи.
В химии нумерация атомов углерода начинается с α-конца. Жирные кислоты представляют собой углеводороды с прямой цепью, имеющие карбоксильную (COOH) группу на одном конце (α) и (обычно) метильную группу на другом (ω) конце.
Как здесь используется, выражение "двойные связи, чередующиеся с метиленовой группой" относится к случаю, когда метиленовая группа располагается между отдельными двойными связями углеродной цепи в липидном соединении.
В соединении в соответствии с настоящим изобретением указанная алкильная группа может быть выбрана из группы, состоящей из метила, этила, н-пропила, изопропила, н-бутила, изобутила, втор-бутила и н-гексила; указанный атом галогена может представлять собой фтор; указанная алкокси группа может быть выбрана из группы, состоящей из метокси, этокси, пропокси, изопропокси, втор-бутокси, OCH2CF3 и OCH2CH2OCH3;
Здесь, указанная ацильная группа представляет собой соединение формулы:
где A представляет собой C1-C7 алкил.
Основной объект настоящего изобретения представляет собой липидное соединение формулы (I):
где
- R1 и R2 являются одинаковыми или различными и могут быть выбраны из группы заместителей, состоящей из атома водорода, алкильной группы, атома галогена и алкокси группы;
- X представляет собой COR3 или CH2OR4, где
- R3 выбран из группы, состоящей из водорода, гидрокси, алкокси и амино,
- где Х дополнительно включает производные карбоновой кислоты, когда R3 представляет собой гидрокси; и
- R4 выбран из группы, состоящей из водорода, алкила или ацила,
- Y представляет собой C9-С21алкен с одной или несколькими двойными связями с E- или Z-конфигурацией;
или любой его фармацевтически приемлемый комплекс, сольват или пролекарство.
Предпочтительно, липидное соединение по настоящему изобретению представляет собой E-изомер и представлено формулой (II):
Когда n=0, липидное соединение по настоящему изобретению представлено формулой (III):
Когда n=1, липидное соединение по настоящему изобретению представлено формулой (IV):
Когда n=2, липидное соединение по настоящему изобретению представлено формулой (V):
Соединения, указанные выше, могут разделяться на подкатегории на основе того, представляет ли собой X COR3 или CH2OR4, на основе заместителей R1 и R2, и того, являются ли R1 и R2 различными или одинаковыми, а также на основе длины и количества двойных связей цепи Y. Особенно предпочтительные соединения представляют собой соединения (1)-(27), перечисленные выше.
Предпочтительные липидные соединения в соответствии с настоящим изобретением могут также разделяться на следующие категории A-1, A-2, B-1 и B-2.
Категория A-Z- и/или E-изомеры
Общая формула (I)
Z- и E-изомеры соединений, описанных общей формулой (I), могут выделяться из смесей с помощью различных технологий разделения. Флэш-хроматография (силикагель) представляет собой распространенную технологию разделения. Z- и E-изомеры соединений, описанных общей формулой, выше, могут выделяться в форме сложных эфиров карбоновых кислот, другие, как карбоновые кислоты или как спирты, с помощью флэш-хроматографии. Карбоновые кислоты могут повторно этерифицироваться посредством использования первичных спиртов и кислотного катализатора (H2SO4, HCl, BF3). Спирты могут окисляться с получением карбоновой кислоты.
Категория A-1, Z- и/или E-изомеры, n=0, X=COR 3
Для всех примеров в этой категории, (30), (32) и (33): n=0
X = этилкарбоксилат
Этил (2Z/E,11E,14E,17E)-2-этил-эйкоза-2,11,14,17-тетраеноат (30)
Этил (2Z/E,7Z,10Z,13Z,16Z,19Z)-2-этокси-докоза-2,7,10,13,16,19-гексаеновая кислота (32)
Этил (2Z,7Z,10Z,13Z,16Z,19Z)-2-этокси-докоза-2,7,10,13,16,19-гексаеновая кислота (33)
Категория A-2, Z- и/или E-изомеры, n=0, X=CH 2 OR 4
Для всех примеров в этой категории, (29), (31) и (34):
n=0
R4=H
(полностью Z)-2-этил-эйкоза-2,11,14,17-тетраен-1-ол (31)
(полностью Z)-3-метил-докоза-2,7,10,13,16,19-гексаен-1-ол (29)
(полностью Z)-2-этокси-докоза-2,7,10,13,16,19-гексаен-1-ол (34)
Категория A-1, n=1, X=COR 3 и X=CH 2 OR 4
Для всех примеров в этой категории, (35), (36), (37), (38), (39) и (40): n=1
Этил (2Z,4E,8Z,11Z,14Z,17Z)-2-этил-эйкоза-2,4,8,11,14,17-гексаноат (35)
(2Z,4E,8Z,11Z,14Z,17Z)-2-этил-эйкоза-2,4,8,11,14,17-гексаен-1-ол (36)
Этил (2E/Z,4E,13Z,16Z,19Z)-3-метил-докоза-2,4,13,16,19-пентаеноат (37)
(2Z,4E,13Z,16Z,19Z)-3-метил-докоза-2,4,13,16,19-пентаен-1-ол (38)
(2Z,4E,7Z,10Z,13Z,16Z,19Z)-2-этил-докоза-2,4,7,10,13,16,19-пентаен-1-ол (39)
Этил (2Z/2E,4E,13Z,16Z,19Z)-2-этил-докоза-2,4,13,16,19-гептаеноат (40)
Категория B: E-изомеры
Общая формула (II), где предпочтительно
Y=C9-С21алкен с одной или несколькими двойными связями с E- или Z-конфигурацией. X = гидроксиметил (-CH2OH), карбальдегид (-C(O)H), или карбоновая кислота, или ее производное, карбоксилат, ангидрид карбоновой кислоты или карбоксамид. Каждый из R1 и R2, которые могут быть одинаковыми или различными, представляет собой атом водорода, атом фтора, алкокси группу или алкильную группу.
Категория B-1; E-изомеры, n=0-2 и X=COR 3
Категория B-2; E-изомеры, n=0-2 и X=CH 2 OR 4
Категория B-1; n=0, X=COR 3 и R=OCH 2 CH 3
Для всех примеров в этой категории, (1), (3), (6) и (8):
n=0
X = этилкарбоксилат
Этил (2E,7Z,10Z,13Z,16Z,19Z)-2-метил-докоза-2,7,10,13,16,19-гексаеноат (1)
Этил (2E,7Z,10Z,13Z,16Z,19Z)-3-метил-докоза-2,7,10,13,16,19-гексаеноат (3)
Этил (2E,11Z,14Z,17Z)-2-метил-эйкоза-2,11,14,17-тетраеноат (6)
Этил (2E,5Z,8Z,11Z,14Z,17Z)-2-метил-икоза-2,5,8,11,14,17-гексаеноат (8)
Категория B-1: n=0, X=COR 3 и R 3 =OH
Для всех примеров в этой категории, (2), (4), (7) и (26):
n=0
R3 = гидрокси (OH)
(2E,7Z,10Z,13Z,16Z,19Z)-2-метил-докоза-2,7,10,13,16,19-гексаеновая кислота (2)
(2E,7Z,10Z,13Z,16Z,19Z)-3-метил-докоза-2,7,10,13,16,19-гексаеновая кислота (4)
(2E,11E,14E,17E)-2-метил-эйкоза-2,11,14,17-тетраеновая кислота (7)
(2Z,7Z,10Z,13Z,16Z,19Z)-2-этокси-докоза-2,7,10,13,16,19-гексаеновая кислота (26)
Категория В-2, n=0, X=CH 2 OR 4 и R 4 =H
Для всех примеров в этой категории; (5), (9) и (27):
n=0
Заместитель представляет собой алкил или этокси.
(2E,7Z,10Z,13Z,16Z,19Z)-3-метил-докоза-2,7,10,13,16,19-гексаен-1-ол (5)
(2E,11Z,14Z,17Z)-2-этил-эйкоза-2,11,14,17-тетраен-1-ол (9)
2E,7Z,10Z,13Z,16Z,19Z)-2-этокси-докоза-2,7,10,13,16,19