Способ демеркуризации поверхностей, загрязненных металлической ртутью
Иллюстрации
Показать всеИзобретение относится к области технической химии, в частности к способам демеркуризации поверхностей, загрязненных металлической ртутью при ее проливе при температурах от 0 до -30°С. Сущность изобретения заключается в удаления ртути с поверхностей в течение более короткого времени с более высокой эффективностью, чем при использовании типовых демеркуризирующих растворов. Способ демеркуризации поверхностей, загрязненных металлической ртутью, включает нанесение водного раствора демеркуризатора, выдержку демеркуризатора на поверхности и удаление образовавшихся нерастворимых в воде продуктов окисления ртути механическим путем. С целью сокращения времени демеркуризации и уменьшения повреждения поверхностей, демеркуризацию проводят растворами жидкого хлора в четыреххлористом углероде с концентрацией от 5 мг/мл до 170 мг/мл с временем демеркуризации не менее 5 минут в интервале температур от 0°С до -30°С. 8 ил., 2 пр.
Реферат
Изобретение относится к области технической химии, в частности к способам демеркуризации поверхностей, загрязненных металлической ртутью при ее проливе.
Наиболее распространенными способами демеркуризации поверхностей - аналогами настоящего изобретения являются способы нанесения на поверхности растворов различных демеркуризаторов [1]:
- мыльно-содовый раствор (4% раствор мыла в 5% водном растворе соды);
- 20% раствор хлорного железа (FeCl3);
- 5-10% водный раствор сульфита натрия;
- 4-5% водный раствор полисульфида натрия;
- 20% водный раствор хлорной извести;
- 5-10 % соляная кислота;
- 2-3% раствор йода в водном растворе йодида калия;
- 0,2% водный раствор марганцовокислого калия, подкисленного соляной кислотой;
- пиролюзит (паста двуокиси марганца);
- 4-5% растворы моно-, дихлорамина.
Из приведенного перечня демеркуризаторов наилучшими демеркуризирующими свойствами обладают: 20% водный раствор хлорного железа, 0,2% водный раствор марганцовокислого калия, подкисленного соляной кислотой. При взаимодействии с перечисленными растворами ртуть превращается в нерастворимую в воде форму (Hg2Cl2; HgO и др.) и удаляется с поверхности механическим способом. При этом время взаимодействия ртути в молекулярной форме и демеркуризатора составляет 1,5÷2 суток с расходом 0,4÷1 литр на 1 м2. Другим существенным недостатком приведенных демеркуризаторов является их полная неспособность выполнять свое предназначение при низких температурах (-10 ÷ -30°С).
Известны способы термической демеркуризации поверхностей, заключающиеся в нагреве поверхностей до 200÷250°С с одновременным отсосом воздуха через фильтр, поглощающий пары ртути. Поглощение паров ртути осуществляется на йодированном активированном угле [2, 3].
Известен способ обработки поверхностей [4] 4÷5 % раствором моно-дихлорамина в четыреххлористом углероде. При этом время контакта поверхности с раствором должно составлять 8÷10 часов. После этого поверхность дополнительно обрабатывается 4÷5% раствором полисульфида натрия с временем контакта в течение 8÷10 часов. Обработка поверхности получается двухступенчатой: в процессе первой обработки образуются сульфамид ртути и каломель, а в процессе второй обработки - сульфид ртути.
Известен способ демеркуризации поверхностей с помощью перекиси водорода [5]. Способ не обеспечивает надежной демеркуризации из-за низкой стойкости перекиси водорода в сравнении с временем, необходимым для проведения демеркуризации.
Прототипом изобретения является способ обработки поверхностей [6] раствором оксида хлора (I) в четыреххлористом углероде.
Недостатками способа-прототипа являются:
- Высокая стоимость получения оксида хлора (I), приводящая к большим затратам при демеркуризации.
- Более высокая токсичность оксида хлора (I) по сравнению с хлором.
- Образование продуктов превращения ртути в неустойчивых оксидных формах, способных впоследствии восстанавливаться до металлической ртути в присутствии восстановителей.
Сущность изобретения заключается в использовании в качестве демеркуризатора раствора жидкого хлора Cl2 в четыреххлористом углероде, что обеспечивает достижение заявляемого результата: удаления ртути с поверхностей в течение сопоставимого времени с окисью хлора - до 5 минут - с образованием только каломели и сулемы в диапазоне температур от 0 до минус 30°С.
Технический результат заключается в быстром уничтожении ртути в любой форме на поверхности при недавних проливах при отрицательных температурах до -30°С. По данному параметру хлор превосходит раствор окиси хлора (I).
Существенными признаками изобретения являются:
- использование в качестве демеркуризаторов растворов жидкого хлора Cl2 в четыреххлористом углероде. В ходе экспериментов, результаты которых приведены ниже, было выяснено, что растворы жидкого хлора Cl2 в четыреххлористом углероде обладают высокой, превращающей ртуть в хлоридные формы способностью, которая значительно превосходит реакционную способность демеркуризаторов, приведенных в [1], и несколько уступает в скорости реакции аналогично приготовленным растворам оксида хлора (I). Перевод растворов абсорбированного хлора в ЧХУ в раствор жидкого хлора в ЧХУ осуществляется комбинацией давления и понижения температуры;
- использование концентрации этих растворов от 5 мг/мл до 170 мг/мл для уничтожения капельной формы ртути. Указанные значения концентраций обеспечивают демеркуризацию поверхности в широком интервале величин поверхностных загрязнений и масс капельной ртути. Если загрязненность ртутью сформировалась за счет пролива ртути, то следует использовать раствор указанных концентраций. Если загрязненность ртутью сформирована за счет адсорбции паров ртути, то достаточно раствора 5 мг/мл. Промежуточные значения концентрации позволяют подобрать оптимальное значение концентрации хлора в четыреххлористом углероде в зависимости от величины загрязненности вплоть до наличия капель ртути различных размеров;
- возможность использования данного раствора при низких температурах до минус 30°С (Температура замерзания ртути минус 38,87°С). Температура замерзания (плавления) чистого ЧХУ составляет минус 23°С. Температура замерзания (плавления) чистого хлора составляет минус 101°С. Экспериментально установлено, что при температуре минус 30°С растворы хлора в ЧХУ концентрацией от 5 мг/мл до 170 мг/мл не замерзают. Однако по мере долгого нахождения раствора в указанных условиях при нормальном давлении и покидании хлором ЧХУ, последний может замерзнуть;
- меньшее время демеркуризации, чем у всех основных демеркуризаторов, и сопоставимое с раствором окиси хлора (I) (около 5 минут при использовании растворов от 50 мг/мл до 170 мг/мл) при температуре в диапазоне (0÷ -30 )°С и около 10 минут при использовании растворов от 5 мг/мл до 50 мг/мл;
- необходимость легкого механического воздействия на ртуть (растирание капель в демеркуризаторе (через пленку, например, мягкой щеткой) в капельной форме для ее уничтожения в течение 5÷6 минут. При выполнении этой процедуры следует иметь в виду, что при температурах до минус 34 С° хлор начинает интенсивно покидать раствор, с ухудшением демеркуризирующих свойств последнего. Выраженные демеркуризирующие свойства при 0÷ -15 °С сохраняются некоторое время, которое составляет около 10÷15 минут;
- высокая эффективность демеркуризации, достигающая 100% при однократной обработке капельной формы ртути при избытке демеркуризатора;
- дешевизна проведения демеркуризации по сравнению с данными патента № 2356654 из-за очень низкой стоимости хлора (50-литровый баллон с жидким хлором стоит около 2000 рублей, в ценах 2011 г.);
- удаление продуктов демеркуризации механическим путем, а паров демеркуризатора вентилированием (проветриванием).
Эффективность демеркуризации при проведении экспериментов проверялась по разработанному нами способу отбора и обработки проб ртути с поверхностей [7], в основе которого лежит метод Полежаева.
Хлор получали по реакции взаимодействия соляной кислоты с марганцовокислым калием:
2KMnO4+ 16HCl= 2KCl +2MnCl2 +5Cl2 + 8Н2О
Для получения 7,1 г Cl2 брали навеску 12,7 г KMnO4 и воздействовали на нее 75 мл 37% соляной кислоты (плотность 1,19 г/см3).
Для получения тока хлора в колбу с марганцовокислым калием приливали по каплям соляную кислоту (Фиг.1). Для исключения попадания в склянку Дрекселя паров хлористого водорода ток хлора пропускали через склянку с водой. От паров воды хлор очищали пропусканием над пятиокисью фосфора. На заключительной стадии реакции необходимо подать весь образовавшийся хлор в склянку Дрекселя из колбы. Для этого использовали резиновый насос, подающий воздух в колбу и вытесняющий хлор в склянку. Для проведения реакции подавали в колбу с марганцовокислым калием соляную кислоту с расходом 1 капля в 2 секунды. Это обеспечивало равномерное образование хлора и его проход через склянку Дрекселя. После проведения реакции четыреххлористый углерод изменил цвет на желто-зеленый (Фиг.2).
Склянку отсоединяли и сливали раствор в герметично закрывающуюся емкость. Склянка Дрекселя с ЧХУ взвешивалась до и после проведения синтеза. Получаемые привесы хлора в ЧХУ составили от (4÷12) грамм Cl2, которые растворялись в 70 мл четыреххлористого углерода. Полученные растворы Cl2 в CCl4, таким образом, имели концентрацию около 57÷171 мг/мл. Для проверки их демеркуризирующих свойств, при не видимой глазом загрязненности, использовались растворы концентрацией 5 мг/мл.
Для обеспечения безопасности все работы проводили с соблюдением мер безопасности при работе с хлором, под тягой при наличии противогазов, готовых к использованию.
Свойства хлора в ЧХУ по уничтожению ртути превосходят все известные демеркуризаторы, кроме окиси хлора. Хлор, растворенный в четыреххлористом углероде, способен за очень короткое время уничтожать капли ртути при легком механическом воздействии, что демонстрируется примерами, приведенными ниже. Заявляемая авторами новизна подчеркивается также и тем, что в процессе приготовления заявляемого авторами демеркуризатора была выявлена научная новизна: растворы хлора в ЧХУ не обладают заметной активностью по отношению к ртути до тех пор, пока хлор из абсорбированного состояния не будет переведен в жидкое состояние. Данный факт, как установлено авторами, не упоминается в химической и патентной литературе.
Более того, нами показано, что все попытки воздействовать на капельную ртуть полученным раствором абсорбированного в ЧХУ хлора были отрицательными (Фиг.3).
Аналогичный результат виден на видеозаписи, свидетельствующей о невозможности воздействия на ртуть абсорбированным в ЧХУ хлором (Видеофайл «Отсутствие взаимодействия»).
Перевод хлора в жидкое состояние осуществляется сочетанным воздействием на него отрицательных температур и давления.
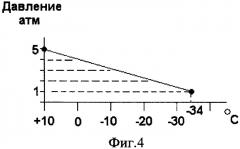
При температуре минус 34°С сжижение происходит при нормальном атмосферном давлении. При давлении 5 атм (5·105 Па) сжижение происходит при +10°С. Промежуточные значения можно выбрать из графика, приведенного на фиг.4.
Так, при получении абсорбированного хлора его температура составляет около 0°С. Данные растворы с ртутью не взаимодействуют. После сливания этого раствора в герметично закрывающуюся емкость с минимальным воздушным пространством и охлаждении до температур ниже -25°С и выдержке его в герметично закрытом состоянии около суток раствор приобретал выраженную способность к быстрому превращению ртути в каломель и сулему (Фиг.5). После переливания раствора в герметичную емкость происходило достаточно сильное увеличение давления (до 2 атм ) за счет испаряющегося хлора, которое понижало температуру его сжижения от минус 34°С до минус (20 ÷ 25)°С. При образовании жидкого хлора раствор приобретал демеркуризирующие свойства.
Это обстоятельство делает Cl2 в CCl4 незаменимым дешевым демеркуризатором при низких отрицательных (до минус 30°С) температурах.
Разбавление исходного раствора Cl2 в CCl4 в дальнейшем четыреххлористым углеродом приводит к понижению реакционной способности и уменьшению повреждающей способности раствора.
Пример 1
Капля ртути массой около 6 грамм при комнатной температуре (Фиг.6) заливалась 5 мл раствора жидкого Cl2 в CCl4 концентрацией 50 мг/мл, который хранился при минус 25°С.
Сразу же после приливания раствора, капля ртути чернела, с образованием слегка вытянутой формы.
Спустя 5 минут при встряхивании стакана практически вся металлическая ртуть превращается в серый порошок (Фиг.7). Высушенный в нейтральной газовой среде гелия осадок имеет белый цвет, что указывает на ее переход в смесь каломели и сулемы. В течение этого времени ртуть уничтожается полностью (Фиг.8).
Осадок был плохо растворим в воде и при анализе в нем были обнаружены только сулема и каломель.
Пример 2
Капля ртути весом около 9 грамм при комнатной температуре заливалась 5 мл раствора жидкого Cl2 в CCl4 концентрацией 170 мг/мл, взятого из холодильника, при температуре минус 25°С. Сразу после приливания капля чернела и при легком взбалтывании раствора быстро превращалась в черно-серый порошок.
Данный процесс записан в режиме реального времени на цифровую фотокамеру и представлен в качестве демонстрационного материала на CD-диске. На видеозаписи отсутствует только сам момент приливания раствора жидкого хлора в ЧХУ, который проводился под тягой (Видеофайл «Уничтожение ртути хлором»). При проведении демеркуризации данным раствором необходимо при наличии капельных форм соблюдать условия небольшого избытка демеркуризатора по отношению к массе капельной ртути.
Предлагаемый способ может найти широкое применение в промышленности, в ВС РФ, МЧС, в быту, так как отличается простотой реализации и высокой эффективностью демеркуризации. Особую ценность способ имеет для уничтожения капель ртути при отрицательных температурах. При -10 ÷ -30°С ни один из известных демеркуризаторов (кроме окиси хлора в ЧХУ) уничтожить ртуть не в состоянии. Способ изначально создавался для уничтожения ртути при очень больших «свежих» проливах из систем дифферентовки глубоководных аппаратов (десятки кг), базирующихся на Севере, где температуры в -20 - -30°С обычное явление (Температура замерзания ртути минус 38,87°С).
Недостатком способа является повреждение поверхностей, которое при кратковременном контакте 5 минут для металлов, пластиков, резин минимально, однако с течением времени возможно огрубление структуры пластиков и резины и появление следов коррозии на некоторых металлах и сплавах. Повреждения можно свести к минимуму подбором соответствующих величин концентраций хлора. Предлагаемый способ демеркуризации не является универсальным и не обеспечивает удаления ртути при застарелых загрязнениях с возникновением ртутных «депо», амальгам, а также объектов, абсорбировавших ртуть (штукатурка, дерево, бетон и др.). При проведении демеркуризации имеется необходимость использования средств защиты органов дыхания.
Краткое описание чертежей
Фиг.1- установка получения хлора без примеси хлористого водорода.
Фиг.2 - общий вид раствора хлора в ЧХУ.
Фиг.3 - отсутствие воздействия раствора абсорбированного хлора на ртуть в течение 5 минут.
Фиг.4 - значение температур и давления, при которых происходит снижение хлора.
Фиг.5 - результат воздействия охлажденного до -25°С под повышенным давлением раствора абсорбированного хлора с ртутью. Серый осадок - каломель и сулема. Оставшиеся капли ртути - результат неэквимолярного соотношения реагирующих компонентов. Исходная капля ртути имела массу около 25 грамм.
Фиг.6 - исходная капля ртути массой около 6 грамм.
Фиг.7 - общий вид колбы с продуктами демеркуризации после уничтожения в ней ртути.
Фиг.8 - внешний вид полученного продукта после слива остатков демеркуризатора и высушивания в струе гелия.
Литература
1. Ртуть. Нормативные и методические документы. Справочник - С-Пб. 1999 г. «Методические рекомендации по контролю за организацией текущей и заключительной демеркуризации и оценке ее эффективности», стр.44.
2. Яворская С.Ф. «Новости медицины», вып.26, 72 (1952).
3. Яворская С.Ф. «Гигиена и санитария» №2.38, 1965 г.
4. «Гигиена и санитария» №4.48, 1953 г.
5. А.С. №266727 Бюл. Изобр.№12 (1970 г.).
6. Патент РФ №2356654.
7. Патент РФ №2229109.
Способ демеркуризации поверхностей, загрязненных металлической ртутью, включающий нанесение раствора демеркуризатора, выдержку демеркуризатора на поверхности, при этом для удешевления процесса демеркуризации ее проводят растворами жидкого хлора в четыреххлористом углероде с концентрацией хлора от 5 мг/мл до 170 мг/мл, в интервале температур от 0°С до -30°С, под пленкой, закрывающей демеркуризируемую поверхность, при небольшом механическом воздействии на капельную ртуть щеткой в течение 5-6 мин с удалением остатков демеркуризатора путем вентилирования (проветривания) демеркуризируемых помещений, а продуктов демеркуризации - механическим путем.