Способ получения бензимидазолов
Иллюстрации
Показать всеИзобретение относится к области основного органического синтеза, а именно к способу получения N,N'-бис и N,N,N,N-тeтpaкис-бензимидазолилметил N,N'-бис (пиперазиноэтил) этилендиаминов, N,N'-бис и N,N,N,N-тетракис-бензимидазолилэтил-N,N'-бис(пиперазиноэтил)этилендиаминов, которые получают путем взаимодействия карбоновых кислот: N,N'-бис и N,N,N,N-тетракис-карбоксиэтил и N,N'-бис и N,N,N,N-тетракис-карбоксиэтил N,N'-бис (пиперазиноэтил) этилендиамина с орто-фенилендиамином при нагревании сначала при температуре 100-125°С в течение 0,6-1,5 ч, затем при 130-150°С в течение 2,5-3,4 ч в среде ароматического органического растворителя при мольном соотношении гексаминодикислота:фенилендиамин = 1:2,1-2,15 и гексаминотетракислота:фенилендиамин = 1:4,1-4,15. Выделение целевого продукта проводят путем перегонки реакционной массы. В качестве ароматического органического растворителя используют орто, мета и пара-ксилолы или смесь орто, мета и пара-ксилолов. Технический результат: повышение выхода целевых продуктов, усовершенствование способа получения бензимидазолов. 1 з.п. ф-лы, 1 табл., 6 пр.
Реферат
Изобретение относится к области основного органического синтеза, а именно к способу получения N,N'-бис и N,N,N,N-тетракис-бензимидазолилметил N,N'-бис (пиперазиноэтил) этилендиаминов, N,N'-бис и N,N,N,N-тетракис-бензимидазолилэтил-N,N'-бис (пиперазиноэтил) этилендиаминов (1-4), которые могут найти применение в химикофармацевтической промышленности в качестве лекарственных и антигельминтных препаратов.
Известен способ получения гидрохлоридов 2-бензил- или 2-стерил-бензимидазола конденсацией о-фенилендиамина (о-ФДА) с карбоновыми кислотами в присутствии хлорокиси фосфора при температуре 80-90°С с выходом 83-95% [патент РФ №2054421, кл. С07D 235/18, опубл. 20.02.1996]. Недостатком известного способа является применение сильно ядовитой хлорокиси фосфора РОCl3 и дефицитных карбоновых кислот - коричной, феруловой, 4-метоксикоричной, 2,4-диметоксикоричной, 4-нитро-коричной кислот и др.
Наиболее близким способом по технической сущности и достигаемому результату является получение бензимидазолов путем взаимодействия карбоновых кислот с орто-фемилендиамином при нагревании и выделения целевого продукта, при этом температуру процесса поддерживают в пределах 170-190°С, в качестве карбоновых кислот используют N-карбоксиметил-N1-[(β-2,5-диметил-1-пиролил)этил]пиперазин (пирроло кислота) и N-карбоксиметил-N1-[(β-пиперазиноэтил)имиды) (имидопиперазино кислота), выделение продукта проводят путем кристаллизации из смеси ацетона и гексана, взятых в соотношении 2:1 [Загидуллин Р.Н. О некоторых реакциях N(β-аминоэтил) пиперазина и его производных // Журнал «Химия гетероциклических соединений. 1991. №3. С.381-384]. Кристаллизация осуществляется в течение 8-12 часов. Выход целевых продуктов составляет 52-73%.
Недостатками известного способа получения бензимидазолов являются низкий выход целевых продуктов (52-73%), применение легковоспламеняющихся горючих растворителей (ацетон - гексан) и продолжительность процесса выделения целевого продукта.
Технический результат при использовании заявляемого способа выражается в усовершенствовании технологического процесса получения соединений бензимидазолов (1-4), повышении выхода целевых продуктов.
Технический результат достигается способом получения бензимидазолов путем взаимодействия карбоновых кислот с орто-фенилендиамином при нагревании и выделения целевого продукта, при этом в качестве карбоновых кислот используют N,N'-бис и N,N,N,N-тетракис-карбоксиэтил и N,N'-бис и N,N,N,N-тетракис-карбоксиэтил N,N'-бис (пиперазиноэтил) этилендиамины, а взаимодействие карбоновых кислот с орто-фенилдиамином проводят сначала при температуре 100-125°С в течение 0,6-1,5 ч, затем при 130-150°C в течение 2,5-3,4 ч в среде ароматического органического растворителя при мольном соотношении гексаминодикислота:фенилендиамин = 1:2,1-2,15 и гексаминотетракислота:фенилендиамин = 1:4,1-4,15, выделение целевого продукта проводят путем перегонки реакционной массы. В качестве ароматического органического растворителя используют орто, мета и пара-ксилолы или смесь орто, мета и пара-ксилолов. Получают N,N'-бис и N,N,N,N-тетракис-бензимидазолилметил N,N'-бис (пиперазиноэтил) этилендиамины, N,N'-бис и N,N,N,N-тетракис-бензимидазолилэтил- N,N'-бис (пиперазиноэтил) этилендиамины (1-4) с выходом 83,4-87,3%.
где
где R=H(5), CH2COOH(6), R=H(1), ;
R=H (7), CH2CH2COOH (8), R=H(3) ;
Преимуществом заявляемого изобретения является высокие выходы целевых продуктов, усовершенствование технологического процесса синтеза бензимидазолов путем снижения продолжительности процесса выделения целевого продукта, обеспечения безопасности процесса за счет использования в качестве органического растворителя ксилолов - невзрывоопасного вещества. Кроме того, в заявляемом способе представлены соединения, имеющие необычные структуры, которые состоят из этилендиаминного пиперазинового цикла и фрагмента бензимидазола.
Сущность изобретения иллюстрируется следующими примерами.
Пример 1. В реактор, снабженный мешалкой, термометром, капельной воронкой и обратным холодильником, загружают 40 г соединения (5) (0,1 моль) в 80 мл пара-ксилола и 23,76 г орто-фенилдиамина (0,22 моль о-ФДА). Мольное соотношение гексаминодикислота (5): о-ФДА=1:2,2. Реакционную смесь нагревают сначала при температуре 110°C в течение 1,0 ч, затем при 140°С в течение 3 ч. Выделение целевого продукта проводят путем перегонки реакционной массы в течение 1,5 часов, при этом сначала отгоняется азеотроп пара-ксилола с водой. Получают 45,96 г целевого продукта (1) в виде вязкой жидкости. Выход продукта 84,5%. Найдено, %: С 66,63; Н 8,46; N 25,31. C30H44N10. Вычислено, %: С 66,17; Н 8,08; N 25,73.
Пример 2. В условиях примера 1 в реактор загружают 51,6 г (0,1 моль) соединения (6) в 150 мл орто-ксилола и 44,28 г (0,41 моль) о-ФДА. Мольное соотношение гексаминотетракислота (6): о-ФДА=1:4,15. Реакционную смесь нагревают сначала при температуре 120°С в течение 1 ч, затем при температуре 140°С в течение 3 ч. Выделение целевого продукта проводят путем перегонки реакционной массы в течение 1,5 часов, при этом сначала отгоняется азеотроп орто-ксилола с водой. Получают 67,37 г продукта (2) в виде вязкой массы. Выход целевого продукта 83,8%. Найдено, %: С 69,04; Н 7,32; N 23,96. C46H56N14. Вычислено, %: С 68,65; Н 6,96; N 24,37.
Пример 3. В условиях примера 1 в реактор загружают 42,8 г (0,1 моль) соединения (7) в 100 мл мета-ксилола и 23,76 г (0,22 моль) о-ФДА. Мольное соотношение гексаминодикислота (7): о-ФДА=1:2,2. Реакционную смесь нагревают сначала при 120°С в течение 1,5 ч, затем при 145°С в течение 2,5 ч.
Выделение целевого продукта проводят путем перегонки реакционной массы в течение 1,5 часов, при этом сначала отгоняется азеотроп мета-ксилола с водой. Получают 49,3 г продукта (3) в виде вязкой массы. Выход целевого продукта 86,2%. Найдено, %: С 67,56; H 8,80; N 24,08. C32H48N10. Вычислено, %: С 67,13; H 8,39; N 24,47.
Пример 4. В условиях примера 1 в реактор загружают 57,2 г (0,1 моль) соединения (8) в 150 мл пара-ксилола и 44,82 г (0,415 моль) о-ФДА. Мольное соотношение гексаминотетракислота (8): о-ФДА=1:4,15. Реакционную смесь нагревают при температуре 125°С в течение 0,6 ч, затем при температуре 150°С в течение 3,4 ч. Выделение целевого продукта проводят путем перегонки реакционной массы в течение 2 часов, при этом сначала отгоняется азеотроп пара-ксилола с водой. Получают 75,0 г продукта (4) в виде густой массы. Выход целевого продукта 87,3%. Найдено, %: С 70,15; Н 7,80; N 22,37. C50H64N14. Вычислено, %: С 69,76; H 7,44; N 22,79.
Пример 5. В условиях примера 1 в реактор загружают 42,8 г (0,1 моль) соединения (5) в 120 мл пара-ксилола 21,6 г (0,2 моль) о-ФДA. Мольное соотношение гексаминодикислота (5): о-ФДА=1:2,0. Реакционную смесь нагревают при температуре 110°C в течение 8 ч. Выделение целевого продукта проводят путем перегонки реакционной массы в течение 1,5 часов, при этом сначала отгоняется азеотроп пара-ксилола с водой. Получают 36,6 г продукта (1). Выход целевого продукта 67,4%. Найдено, %: С 66,97; Н 8,76; N 25,11. C30H44N10. Вычислено, %: С 66,17; Н 8,08; N 25,73.
Пример 6. В условиях примера 1 к реактор загружают 57,2 г (0,1 моль) соединения (8) в 200 мл пара - ксилола и 43,2 г (0,4 моль) о-ФДА. Мольное соотношение гексаминотетракислота (8): о-ФДА=1:4,0. Реакционную смесь нагревают при температуре 160-180°C в течение 3 ч. Выделение целевого продукта проводят путем перегонки реакционной массы в течение 1,5 часов. Получают 56,6 г продукта (4) в виде густой массы. Выход целевого продукта 65,9%. Найдено, %: С 69,09; H 8,07; N 22,14. C50H64N14. Вычислено, %: С 69,76; Н 7,44; N 22,79.
При условии выдерживания заявляемых параметров процесса по температуре и мольному соотношению реагентов достигаются высокие выходы целевых соединений (примеры 1-4). Повышение температуры процесса сначала выше 125С, далее выше 150°С, или понижение температуры процесса на первой стадии ниже 100°С, второй стадии ниже 130°С приводит к снижению выхода целевого продукта. При снижении мольного соотношения гексаминодикислота: фенилендиамин менее, чем 1:2,1 и гексаминотетракислота:фенилендиамин менее чем 1:4,1 также снижается выход целевого продукта из-за недостаточности орто-фенилендиамина. Повышение расхода орто-фенилендиамина выше мольного соотношения гексаминодикислота: фенилендиамин более чем 1:2,2 и гексаминотетракислота:фенилендиамин более чем 1:4,15 не приводит к росту выхода целевого продукта, при этом допускается перерасход данного реагента. Ведение процесса взаимодействия карбоновых кислот с орто-фенилендиамином в одну стадию также приводит к снижению выхода целевого продукта. Проведение стадии выделения целевого продукта путем перегонки реакционной массы в течение 1,5-2 часов значительно сокращает продолжительность процесса.
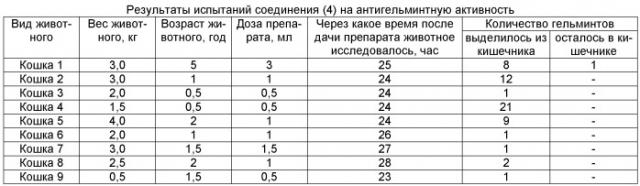
Известно, что ряд производных бензимидазола обладает поразительно высокой антигельминтной активностью (Денисова Л.И. «Труд Всес. Института гельминтол.». 1969. Т. 15. С.97-101; Бехли А.Ф. «Журнал Всес. Химического общества им. Д.И.Менделеева». 1961. Т. 10. №6). В связи с этим полученные производные бензимидазола были испытаны на антигельминтную активность. Испытания показали, что производные бензимидазола проявляют антигельминтную активность. Особенно высокую активность показало соединение (4). Результаты испытаний соединения (4) на антигельминтную активность представлены в таблице (Загидуллин Р.П. Многоосновные амины. Пиперазины. Уфа, изд-во «Гилем», 2010, с.106, табл.3.3).
1. Способ получения бензимидазолов путем взаимодействия карбоновых кислот с орто-фенилендиамином при нагревании и выделения целевого продукта, отличающийся тем, что в качестве карбоновых кислот используют N,N'-бис и N,N,N,N-тетракис-карбоксиметил и N,N'-бис и N,N,N,N-тетракис-карбоксиметил N,N'-бис (пиперазиноэтил) этилендиамины, а взаимодействие карбоновых кислот с орто-фенилдиамином проводят сначала при температуре 100-125°С в течение 0,6-1,5 ч, затем при 130-150°С в течение 2,5-3,4 ч в среде ароматического органического растворителя при мольном соотношении гексаминодикислота:фенилендиамин=1:2,1-2,15 и гексаминотетракислота:фенилендиамин=1:4,1-4,15, выделение целевого продукта проводят путем перегонки реакционной массы.
2. Способ по п.1, отличающийся тем, что в качестве ароматического органического растворителя используют орто, мета и пара-ксилолы или смесь орто, мета и пара-ксилолов.