Токосъемник для вторичной батареи и вторичная батарея с его использованием
Иллюстрации
Показать всеИзобретение относится к токосъемнику для вторичной батареи блока питания, используемого на транспортных средствах, в частности электромобилях. Изобретение предназначено для увеличения емкости батареи. Токосъемник для вторичной батареи (1) по настоящему изобретению включает в себя слой (2) смолы, обладающий электрической проводимостью, и слой (3) ионного барьера, имеющийся на поверхности слоя (2) смолы. Слой (3) ионного барьера содержит захватывающие ионы частицы (6), в которых на поверхностях металлосодержащих частиц (4) имеются соединения (5) металлов. Захватывающие ионы частицы (6) предусмотрены непрерывно от границы (7) раздела между слоем (2) смолы и слоем (3) ионного барьера до поверхности (3а) слоя (3) ионного барьера. Таким образом, слой (3) ионного барьера предотвращает поступление ионов, так что может быть снижена адсорбция ионов в токосъемнике (1). 2 н. и 15 з.п. ф-лы, 9 ил., 5 табл.
Реферат
Область техники
[0001] Настоящее изобретение относится к токосъемнику для вторичной батареи и вторичной батарее с его использованием. Более конкретно, настоящее изобретение относится к токосъемнику для вторичной батареи, включающему в себя слой смолы, обладающий электрической проводимостью, который способен эффективно предотвращать ионную проницаемость и обеспечивать снижение веса, а также относится к вторичной батарее с его использованием.
Уровень техники
[0002] В последние годы достигнуты успехи в разработке гибридного электромобиля (HEV), электромобиля (EV), а также транспортного средства на топливных элементах. В этих видах так называемых электромобилей необходимо использовать блок питания, допускающий повторяющуюся зарядку и разрядку. Примеры блока питания включают в себя вторичную батарею, такую как литий-ионная батарея и никель-водородная батарея, и конденсатор с двойным электрическим слоем. В частности, литий-ионная вторичная батарея рассматривается как выгодная для электромобиля вследствие высокой плотности энергии и высокой долговечности в отношении повторной зарядки и разрядки. Поэтому стимулируются разработки относительно различных типов вторичных батарей. Следует отметить, что для того, чтобы применять вторичную батарею в источнике питания для приведения в действие электромотора, используемого в вышеуказанных различных типах транспортных средств, требуется множество соединенных последовательно вторичных батарей, чтобы обеспечивать высокую выходную мощность.
[0003] Тем не менее, когда батареи подключаются друг к другу посредством соединителя, выходная мощность снижается вследствие электрического сопротивления соединителя. Помимо этого, батареи с соединителем являются невыгодными в пространственном отношении. Другими словами, соединитель вызывает снижение плотности выходной мощности или плотности энергии в батареях.
[0004] Для решения такой проблемы достигнуты успехи в разработке биполярной вторичной батареи, такой как биполярная литий-ионная вторичная батарея. Биполярная вторичная батарея имеет конфигурацию, в которой множество биполярных электродов, каждый из которых снабжен слоем активного материала положительного электрода, сформированным на одной стороне токосъемника, и слоем активного материала отрицательного электрода, сформированным на другой его стороне, уложены поверх друг друга через слой электролита или сепаратор.
[0005] Токосъемник, используемый в описанной выше биполярной вторичной батарее, предпочтительно изготавливается из материала, который является более легким по весу и имеет превосходную электрическую проводимость, чтобы обеспечивать большую плотность выходной мощности. Поэтому в последние годы вместо традиционной металлической фольги был предложен токосъемник, который состоит из полимерного материала, в который добавлен электропроводящий материал. Например, патентный документ 1 раскрывает токосъемник, в котором в полимерный материал в качестве электропроводящего материала подмешаны частицы металла или частицы углерода и содержится смола, обладающая электрической проводимостью.
Список ссылок
Патентная литература
[0006] Патентный документ 1: публикация не прошедшей экспертизу заявки на патент Японии №2006-190649
Сущность изобретения
[0007] Тем не менее, токосъемник, описанный в патентном документе 1, имеет в электролитическом растворе низкие свойства барьера ионам лития по сравнению с токосъемником из металлической фольги. Таким образом, признано, что когда такой токосъемник применяется к биполярной литий-ионной вторичной батарее, ионы лития могут проникать в токосъемник биполярной батареи и оставаться адсорбированными в токосъемнике. Адсорбированные ионы лития не высвобождаются легко. Как результат, емкость батареи может снижаться.
[0008] Настоящее изобретение было создано с учетом такой традиционной проблемы. Задача настоящего изобретения заключается в том, чтобы предоставить токосъемник для вторичной батареи, включающий в себя слой смолы, обладающий электрической проводимостью, который может подавлять адсорбцию ионов в токосъемнике.
[0009] Токосъемник для вторичной батареи согласно одному аспекту настоящего изобретения включает в себя слой смолы, обладающий электрической проводимостью, и слой ионного барьера, имеющийся на поверхности слоя смолы. Слой ионного барьера содержит захватывающие ионы частицы, в которых на поверхностях металлосодержащих частиц имеются соединения металлов. Захватывающие ионы частицы предусмотрены непрерывно от границы раздела между слоем смолы и слоем ионного барьера до поверхности слоя ионного барьера.
[0010] Краткое описание чертежей
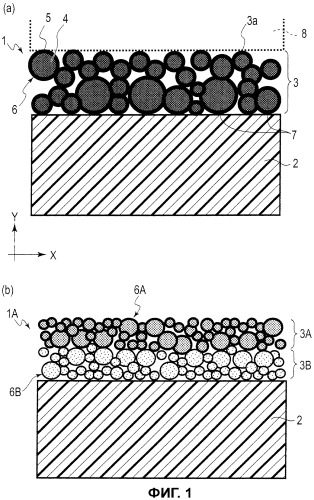
Фиг.1(a) является схематичным видом в поперечном сечении, показывающим один пример токосъемника согласно варианту осуществления настоящего изобретения. Фиг.1(b) является схематичным видом в поперечном сечении, показывающим другой пример токосъемника согласно варианту осуществления настоящего изобретения.
Фиг.2(a) является рентгеновским фотоэлектронным спектром атомов титана в нитриде титана перед приложением напряжения. Фиг.2(b) является рентгеновским фотоэлектронным спектром атомов титана в нитриде титана после приложения напряжения.
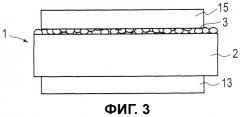
Фиг.3 является схематичным видом в поперечном сечении биполярного электрода, включающего в себя токосъемник, положительный электрод и отрицательный электрод, согласно варианту осуществления настоящего изобретения.
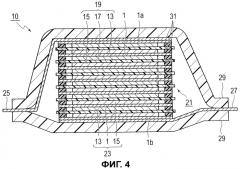
Фиг.4 является схематичным видом в поперечном сечении, типично показывающим всю структуру биполярной литий-ионной вторичной батареи.
Фиг.5 является видом в перспективе, показывающим внешний вид биполярной литий-ионной вторичной батареи.
Фиг.6 является графиком, показывающим взаимосвязь между числом циклов и коэффициентом сохранения емкости каждой батареи в примерах III-1, III-2, III-3 и III-5 и батареи с использованием только слоя смолы в качестве токосъемника.
Фиг.7 является графиком, показывающим взаимосвязь между коэффициентом сохранения емкости и толщиной слоя ионного барьера в примере IV.
Фиг.8 является графиком, показывающим взаимосвязь между относительной температурой и временем у каждой батареи в примерах V-1, V-2 и V-3 и сравнительном примере V-1 и батареи с использованием только слоя смолы в качестве токосъемника.
Фиг.9 является видом в перспективе, показывающим структуру собранной батареи в примере V.
Описание вариантов осуществления
[0011] Ниже приводится подробное описание токосъемника для вторичной батареи и вторичной батареи с использованием такого токосъемника согласно настоящему изобретению со ссылкой на чертежи. Следует отметить, что соотношения размеров на чертежах чрезмерно увеличены для удобства пояснения и могут отличаться от фактических соотношений. Помимо этого, для удобства пояснения описание будет главным образом приведено для случая, когда токосъемник для вторичной батареи согласно настоящему изобретению используется для литий-ионной вторичной батареи.
Токосъемник для вторичной батареи
[0012] Токосъемник 1 для вторичной батареи согласно варианту осуществления настоящего изобретения включает в себя слой 2 смолы, обладающий электрической проводимостью, и слой 3 ионного барьера, имеющийся на поверхности слоя 2 смолы, как показано на фиг.1. Слой 3 ионного барьера включает в себя захватывающие ионы частицы 6, каждая из которых включает в себя соединение 5 металла, имеющееся на поверхности металлосодержащей частицы 4. Захватывающие ионы частицы 6 предусмотрены непрерывно от границы 7 раздела между слоем 2 смолы и слоем 3 ионного барьера до поверхности 3a слоя 3 ионного барьера.
[0013] Более конкретно, как показано на фиг.1, слой 3 ионного барьера включает в себя множество захватывающих ионы частиц 6. Захватывающие ионы частицы 6 непрерывно соединяются друг с другом от границы 7 раздела, на которой слой 2 смолы контактирует со слоем 3 ионного барьера, до поверхности 3a слоя 3 ионного барьера на противоположной от границы 7 раздела стороне. В варианте осуществления, показанном на фиг.1, поверхность 3a на противоположной от границы 7 раздела стороне находится в контакте с электродом (положительным электродом или отрицательным электродом) 8. Вследствие такой конфигурации образуется электропроводящий путь от границы 7 раздела к поверхности 3a, так что обеспечивается электрическая проводимость от электрода 8 к слою 2 смолы. Помимо этого, захватывающие ионы частицы 6 в слое 3 ионного барьера предотвращают проникновение ионов (например, ионов лития), перемещающихся между положительным электродом и отрицательным электродом через слой электролита, внутрь слоя 2 смолы. Следовательно, вследствие наличия слоя 3 ионного барьера предотвращается адсорбция ионов к внутренности токосъемника 1.
[0014] Захватывающие ионы частицы 6, составляющие слой 3 ионного барьера, включают в себя металлосодержащие частицы 4, каждая из которых находится в центральной части соответствующих захватывающих ионы частиц, и снабжены соединениями 5 металлов на поверхностях металлосодержащих частиц 4. Соединения 5 металлов взаимодействуют с ионами лития, адсорбируя ионы лития во время зарядки. Поэтому ионы лития, проникающие в слой 3 ионного барьера из электрода 8, не достигают легко слоя 2 смолы. Помимо этого, склонность к ионизации в соединениях 5 металлов становится высокой во время разрядки, так что соединения 5 металлов высвобождают ионы лития. Следовательно, поскольку соединения 5 металлов обратимо адсорбируют и высвобождают ионы, и ионы, относящиеся к реакции в батарее, по существу не уменьшаются, может быть сохранена разрядная емкость.
[0015] В случае литий-ионной батареи, когда в сепаратор подмешивают инородные вещества, такие как порошок железа, вызывается внутреннее короткое замыкание. Другими словами, подмешанные в сепаратор инородные вещества выделяют тепло, когда энергия химической реакции в положительном электроде и отрицательном электроде преобразуется в электроэнергию. Как результат, сепаратор расплавляется. Когда сепаратор расплавился, изоляция между положительным электродом и отрицательным электродом не может поддерживаться, и, следовательно, выделяется дополнительное тепло. В случае, если слой ионного барьера состоит из частиц металла, обладающих высокой электрической проводимостью, электрический ток протекает в направлении плоскости (направлении X на фиг.1). Соответственно, внутри батареи дополнительно стимулируется тепловыделение.
[0016] Тем не менее, поскольку электрическое сопротивление соединений 5 металлов в захватывающих ионы частицах 6 выше, чем у чистого металла, электрическое сопротивление токосъемника в направлении плоскости (направлении X на фиг.1) становится высоким. Поэтому, даже когда вызывается внутреннее короткое замыкание, концентрирование электрического тока в месте короткого замыкания вдоль направления плоскости токосъемника предотвращается, и может быть предотвращено увеличение температуры внутри батареи. Как описано ниже, толщина слоя 3 ионного барьера предпочтительно находится в пределах диапазона от 50 нм до 1000 нм. Таким образом, даже когда электрическое сопротивление соединений 5 металлов выше, чем у чистого металла, обеспечивается электрическая проводимость в направлении Y, и имеется меньшее влияние на свойства батареи. Таким образом, хотя во время зарядки и разрядки электрический ток протекает в направлении Y, электрический ток не протекает легко в направлении плоскости. Соответственно, могут быть достигнуты как электрическая проводимость, так и безопасность во время короткого замыкания.
[0017] В дальнейшем будут пояснены слой ионного барьера и слой смолы, составляющие токосъемник согласно настоящему варианту осуществления.
Слой ионного барьера
[0018] Как описано выше, слой 3 ионного барьера включает в себя захватывающие ионы частицы 6, в которых на поверхностях металлосодержащих частиц 4 имеются соединения 5 металлов. Слой 3 ионного барьера может быть осажден так, чтобы он покрывал всю поверхность слоя 2 смолы, или же он может покрывать часть поверхности слоя 2 смолы. Слой 3 ионного барьера также может быть предусмотрен на одной поверхности слоя 2 смолы или может быть предусмотрен на обеих поверхностях слоя 2 смолы. Дополнительно, слой 3 ионного барьера может содержать другие вещества, в дополнение к захватывающим ионы частицам 6, для предотвращения проникновения ионов лития внутрь слоя 2 смолы, или же может содержать только захватывающие ионы частицы 6.
[0019] Каждое соединение 5 металла должно иметься по меньшей мере на части поверхности металлосодержащей частицы 4. Тем не менее, с точки зрения обеспечения электрического сопротивления в направлении плоскости слоя 3 ионного барьера, соединения 5 металлов предпочтительно покрывают полностью все поверхности металлосодержащих частиц 4. Предпочтительные примеры металлосодержащих частиц 4 внутри захватывающих ионы частиц 6 включают в себя частицы чистого металла, состоящие из одного единственного металлического элемента, частицы сплава, состоящие из нескольких металлических элементов, или частицы соединения металла, состоящие из металлического элемента и неметаллического элемента. Металлосодержащие частицы предпочтительно содержат по меньшей мере один металлический элемент, выбранный из группы, состоящей из меди (Cu), никеля (Ni), титана (Ti), хрома (Cr), платины (Pt) и золота (Au). Другими словами, металлосодержащие частицы 4 могут быть частицами чистого металла, состоящими из по меньшей мере одного металлического элемента, выбранного из группы, состоящей из меди, никеля, титана, хрома, платины и золота, или могут быть частицами сплава, содержащими эти металлические элементы. Металлосодержащие частицы 4 также могут быть частицами соединения металла, содержащими эти частицы металла и неметаллические элементы. Вышеуказанные металлические элементы имеют высокую стабильность напряжения даже при условии низкого напряжения, такого как несколько десятков мВ, в случае, когда в качестве активного материала отрицательного электрода используется углеродный материал. Поэтому, поскольку вымывание металла в слое 3 ионного барьера подавляется, может быть предотвращено обнажение слоя 2 смолы. Как результат, предотвращается проникновение ионов лития в смолу, и, следовательно, может быть предотвращено ухудшение свойств батареи.
[0020] Когда металлосодержащие частицы 4 являются частицами соединения металла, частицы соединения металла предпочтительно содержат по меньшей мере одно соединение, выбранное из группы, состоящей из оксида металла, нитрида металла, карбида металла, сульфата металла, фосфата металла и фосфорного соединения металла. Более конкретно, для частиц соединения металла может использоваться оксид, нитрид, карбид, сульфат, фосфат или фосфорное соединение по меньшей мере одного металлического элемента, выбранного из группы, состоящей из меди, никеля, титана, хрома, платины и золота.
[0021] Что касается соединений 5 металлов, то используется соединение, которое адсорбирует ионы лития во время зарядки и высвобождает ионы лития во время разрядки. Поэтому соединения 5 металлов предпочтительно содержат по меньшей мере одно соединение, выбранное из группы, состоящей из оксида металла, нитрида металла, карбида металла, сульфата металла, фосфата металла и фосфорного соединения металла. Более конкретно, в качестве соединений 5 металлов могут использоваться оксид, нитрид, карбид, сульфат, фосфат или фосфорное соединение по меньшей мере одного металлического элемента, выбранного из группы, состоящей из меди, никеля, титана, хрома, платины и золота. Эти соединения металлов взаимодействуют с ионами лития и адсорбируют ионы лития во время зарядки. Поэтому ионы лития не достигают легко слоя смолы. То есть, неспаренные электроны или неразделенная электронная пара атомов кислорода (O), атомов азота (N) или атомов фосфора (P), присутствующих в оксиде, нитриде или фосфиде этих металлических элементов, имеет отрицательный электрический заряд, а ионы лития имеют положительный электрический заряд. Таким образом, когда оксид, нитрид или фосфид используются в качестве соединений 5 металлов, электрическое взаимодействие с ионами лития, в частности, становится сильным. Поэтому считается, что ионы лития могут быть адсорбированы эффективно.
[0022] В частности, в качестве соединений 5 металлов предпочтительно используется оксид металла. Более конкретно, предпочтительно использовать оксид по меньшей мере одного металлического элемента, выбранного из группы, состоящей из меди, никеля, титана, хрома, платины и золота. Такой оксид металла легко взаимодействует с ионами лития. Поэтому считается, что ионы лития притягиваются и стабилизируются в соединениях 5 металлов.
[0023] Помимо этого, особо предпочтительно, чтобы металлосодержащие частицы 4 были частицами, состоящими из меди, титана или хрома, а соединения 5 металлов состояли из оксида металлического элемента, составляющего металлосодержащие частицы 4. Более конкретно, металлосодержащими частицами 4 предпочтительно является медь (Cu), а соединениями 5 металлов предпочтительно является оксид меди (оксид меди(I) (Cu2O), оксид меди(II) (CuO)). Оксид меди(I) (Cu2O) в субнанометровом оксидном слое (соединениях 5 металлов), присутствующем на поверхностном слое медных частиц металлосодержащих частиц 4, взаимодействует с ионами лития, образуя стабильный средний слой. Таким образом, считается, что ионы лития не достигают легко слоя 2 смолы.
[0024] Кроме того, металлосодержащими частицами 4 предпочтительно является титан (Ti), а соединениями 5 металлов предпочтительно является оксид титана (TiO2). 2p-орбиталь атомов кислорода в оксиде титана является свободной орбиталью, либо на 2p-орбитали имеются неспаренные электроны с отрицательным электрическим зарядом. Поэтому считается, что свободная орбиталь или неспаренные электроны притягивают ионы лития, стабилизируя ионы лития на соединениях 5 металлов. Помимо этого, как представлено титанатом лития (LiTiO2, Li4Ti5O12), который может быть активным материалом отрицательного электрода, оксид титана имеет хорошую стабильность с литием. Поэтому считается, что оксид титана, присутствующий на самой верхней поверхности, образует вместе с ионами лития сложное соединение, не давая ионам лития достигать слоя 2 смолы.
[0025] Дополнительно, металлосодержащими частицами 4 предпочтительно является хром (Cr), а соединениями 5 металлов предпочтительно является оксид хрома (Cr2O3). Также считается, что оксид хрома адсорбирует ионы лития по идентичному механизму, как и в случае описанных выше оксида меди и оксида титана.
[0026] Помимо этого, металлосодержащие частицы 4 могут быть частицами соединения металла, и частицы соединения металла и соединения 5 металлов в захватывающих ионы частицах 6 могут быть образованы из идентичного материала. Другими словами, полностью все захватывающие ионы частицы 6 могут быть образованы из вышеописанного оксида металла, нитрида металла, карбида металла, сульфата металла, фосфата металла или фосфорного соединения металла. Даже такие захватывающие ионы частицы 6 могут обеспечивать адсорбционную емкость по ионам лития на своих поверхностях. Помимо этого, даже когда полностью все металлосодержащие частицы являются оксидом металла или нитридом металла, может быть сохранена электрическая проводимость в направлении укладки, поскольку толщина слоя 3 ионного барьера является очень небольшой. Как результат, практически отсутствует влияние на свойства батареи.
[0027] Конкретные примеры захватывающих ионы частиц 6, в которых полностью все металлосодержащие частицы являются соединениями металлов, включают в себя частицы оксида меди (Cu2O), оксида титана (TiO2) и оксида хрома (Cr2O3). Другие примеры включают в себя частицы нитрида меди (Cu3N), нитрида титана (TiN) и нитрида хрома (CrN). Помимо этого, могут использоваться частицы фосфида меди (Cu3P), фосфида титана (TiP) и фосфида хрома (CrP). Дополнительно, также являются предпочтительными частицы оксида никеля (NiO), нитрида никеля (NiN) и фосфида никеля (такого как Ni3P).
[0028] Кроме того, соединения 5 металлов в захватывающих ионы частицах 6 предпочтительно являются соединениями, которые могут иметь смешанную валентность. А именно, предпочтительно, чтобы соединения 5 металлов были соединениями, содержащими два или более элемента идентичного типа, имеющих различные атомные валентности. Такие соединения, имеющие смешанную валентность, превращаются в электрический изолятор, когда внутри батареи выделяется тепло со скоростью, к примеру, 10-100°C/мин. Вследствие функции превращения в электрический изолятор электрическое сопротивление слоя 3 ионного барьера во время тепловыделения увеличивается, так что может быть предотвращено выделение джоулева тепла.
[0029] Например, нитрид титана обычно имеет смешанную валентность, обусловленную нестехиометрическим составом, представленным как TiNx. Когда внутри батареи выделяется тепло, нитрид титана испытывает реакцию денитрификации. В частности, в случае, если на отрицательном электроде предусмотрен слой ионного барьера, содержащий частицы нитрида титана, вызываются реакция денитрификации и реакция окисления нитрида титана, так что образуется оксид титана (TiOx) - электрический изолятор. Соответственно, оксид титана увеличивает электрическое сопротивление на отрицательном электроде, тем самым предотвращая выделение джоулева тепла.
[0030] Фиг.2(a) показывает рентгеновский фотоэлектронный спектр (XPS) атомов титана перед приложением напряжения в нитриде титана и спектр после разделения по форме сигналов. Фиг.2(b) показывает рентгеновский фотоэлектронный спектр атомов титана после приложения напряжения в нитриде титана и спектр после разделения по форме сигналов. Как показано на фиг.2(a), титан обычно является двухвалентным, трехвалентным и четырехвалентным на самой верхней поверхности в нитриде титана (TiNx). Тем не менее, когда на отрицательном электроде предусмотрен слой ионного барьера, содержащий нитрид титана и подвергающийся восстановлению во время зарядки, титан на самой верхней поверхности изменяется на нульвалентный, двухвалентный и трехвалентный, как показано на фиг.2(b). Дополнительно, когда внутри батареи выделяется тепло, титан становится четырехвалентным в связи как с реакцией денитрификации, так и с реакцией окисления. Такой четырехвалентный титан превращается в являющийся электрическим изолятором оксид титана (TiO2) и тем самым стабилизируется вследствие кислорода в воздухе или кислорода, высвобожденного из активного материала положительного электрода.
[0031] Как описано выше, предпочтительно, чтобы по меньшей мере соединения 5 металлов были соединениями, которые могут иметь смешанную валентность. Тем не менее, полностью все захватывающие ионы частицы 6 могут быть соединениями, которые могут иметь смешанную валентность. Примеры тех соединений, которые имеют смешанную валентность, включают в себя нитрид переходного 3d-металла и нитрид переходного 4d-металла. Примеры переходного 3d-металла включают в себя скандий (Sc), титан (Ti), ванадий (V), хром (Cr), марганец (Mn), железо (Fe), кобальт (Co), никель (Ni), медь (Cu) и цинк (Zn). Примеры переходного 4d-металла включают в себя иттрий (Y), цирконий (Zr), ниобий (Nb), молибден (Mo), технеций (Tc), рутений (Ru), палладий (Pd), серебро (Ag) и кадмий (Cd). Из них предпочтительными являются нитрид Ti, V, Cr, Mn, Fe или Co при переходном 3d-металле и нитрид Zr при переходном 4d-металле. В частности, нитрид титана (TiNx), нитрид циркония (ZrNx) и нитрид хрома (CrNx) являются предпочтительными, поскольку эти соединения обладают стабильностью напряжения в отрицательном электроде в дополнение к вышеописанным характеристикам.
[0032] Слой 3 ионного барьера может состоять из нескольких типов слоев, которые уложены поверх друг друга. Альтернативно, слой 3 ионного барьера имеет слоистую структуру, включающую в себя: слой, содержащий первые захватывающие ионы частицы, в которых на поверхностях металлосодержащих частиц имеются соединения металлов, состоящие из металлического элемента и неметаллического элемента; и слой, содержащий вторые захватывающие ионы частицы, в которых на поверхностях металлосодержащих частиц имеются соединения, которые могут иметь смешанную валентность. Например, как показано на фиг.1(b), захватывающий ионы слой 3A в токосъемнике 1A является слоем, состоящим из первых захватывающих ионы частиц 6A, в которых на поверхностях металлосодержащих частиц имеются соединения, которые могут иметь смешанную валентность. Аналогично, захватывающий ионы слой 3B является слоем, состоящим из вторых захватывающих ионы частиц 6B, в которых на поверхностях металлосодержащих частиц имеются соединения металлов, состоящие из металлического элемента и неметаллического элемента. Таким образом, слой ионного барьера может состоять из нескольких типов слоев, которые уложены поверх друг друга.
[0033] Захватывающие ионы частицы 6 могут быть образованы с произвольной формой. Примеры формы захватывающих ионы частиц 6 включают в себя сферическую форму, кубическую форму, столбчатую форму, пластинчатую форму, чешуйчатую форму, стержнеобразную форму, игольчатую форму, волокнистую форму, пластинчатую форму, кластерную форму и аморфную форму, которая может выбираться в зависимости от ситуации. Помимо этого, захватывающие ионы частицы 6 могут быть в состоянии наночастиц или нанокластера. Отсутствуют конкретные ограничения на диаметр частицы у захватывающих ионы частиц, но диаметр первичных частиц у захватывающих ионы частиц предпочтительно составляет в пределах диапазона от 0,1 нм до 500 нм, более предпочтительно - от 0,1 нм до 200 нм, еще более предпочтительно - от 0,1 нм до 50 нм. Когда диаметр первичных частиц у захватывающих ионы частиц 6 составляет 0,1 нм или более, частицы 6 могут быть легко обеспечены на слое 2 смолы. Дополнительно, когда диаметр первичных частиц у частиц 6 составляет 500 нм или менее, может быть обеспечена достаточная удельная площадь поверхности, так что достигается высокий эффект адсорбирования ионов лития. Помимо этого, поскольку электролитический раствор не проникает легко через этот слой из зазоров между смежными друг с другом частицами 6, захватывающие ионы частицы 6 эффективно функционируют в качестве разделительной перегородки. Диаметр первичных частиц может быть получен в результате изучения приготовленного токосъемника с использованием сканирующего электронного микроскопа (SEM) или просвечивающего электронного микроскопа (TEM). Следует отметить, что "диаметр частицы" в настоящем описании представляет собой максимальное расстояние L из расстояний между соответствующими произвольными двумя точками на контуре соответствующих частиц.
[0034] Как описано выше, слой ионного барьера содержит электропроводящий материал, содержащий неметаллический элемент и обладающий свойством предотвращения проникновения вышеописанных ионов или растворителя. Электропроводящий материал, содержащий неметаллический элемент, имеет небольшую плотность по сравнению с материалом, состоящим из металла. Поэтому может быть достигнуто снижение веса токосъемника. Неметаллический элемент, содержащийся в электропроводящем материале, предпочтительно имеет 5 атом.% или более, более предпочтительно 50 атом.% или более, с учетом снижения веса.
[0035] Электропроводящий материал, используемый в слое ионного барьера в настоящем варианте осуществления, имеет большое объемное удельное сопротивление по сравнению с электропроводящим материалом, состоящим из металла, поскольку электропроводящий материал по настоящему варианту осуществления содержит неметаллический элемент. Следовательно, даже когда вызывается внутреннее короткое замыкание, концентрирование электрического тока в месте короткого замыкания не возникает легко. Соответственно, может быть предотвращено тепловыделение в токосъемнике. Следует отметить, что электрическая проводимость в направлении толщины токосъемника не может быть получена, когда объемное удельное сопротивление чрезмерно большое. С учетом вышеописанного, объемное удельное сопротивление слоя ионного барьера предпочтительно составляет от 7,2×10-5 до 10 Ом·см, более предпочтительно - от 1×10-4 до 5 Ом·см, еще более предпочтительно - от 1×10-3 до 1 Ом·см.
[0036] Толщина слоя 3 ионного барьера предпочтительно составляет в пределах диапазона от 50 нм до 1000 нм. Помимо этого, как показано на фиг.1(b), в случае наличия в токосъемнике нескольких слоев ионного барьера, полная толщина слоев ионного барьера предпочтительно составляет в пределах диапазона от 50 нм до 1000 нм. Как описано выше, слой ионного барьера содержит соединение металла, состоящее из оксида металла или нитрида металла, обладающего способностью к адсорбции и высвобождению ионов. Следовательно, даже когда его толщина составляет приблизительно от 50 нм до 1000 нм, слой ионного барьера может предотвращать проникновение ионов. Толщина слоя 3 ионного барьера более предпочтительно находится в пределах диапазона от 50 нм до 200 нм, особенно предпочтительно - в пределах диапазона от 50 нм до 100 нм. Толщина слоя 3 ионного барьера и толщина слоя 2 смолы, описанных ниже, может быть измерена в результате изучения приготовленного токосъемника с использованием SEM или TEM.
[0037] Фиг.3 является схематичным видом в поперечном сечении биполярной батареи 23, включающей в себя токосъемник 1 для вторичной батареи, слой 13 активного материала положительного электрода (положительный электрод), имеющийся на одной поверхности токосъемника, и слой 15 активного материала отрицательного электрода (отрицательный электрод), имеющийся на другой поверхности токосъемника. Как показано на фиг.3, слой 3 ионного барьера в токосъемнике 1 предпочтительно сформирован на всей поверхности слоя 2 смолы, находясь в контакте со слоем 15 активного материала отрицательного электрода. Ионы лития в электролитическом растворе обычно проникают внутрь слоя 2 смолы от поверхности стыка между слоем 15 активного материала отрицательного электрода и слоем 2 смолы. Следовательно, вследствие наличия слоя 3 ионного барьера на слое 15 активного материала отрицательного электрода, как показано на фиг.3, эффект предотвращения проникновения ионов лития в электролитический раствор повышается, тем самым улучшая коэффициент сохранения емкости батареи.
Слой смолы
[0038] Слой 2 смолы содержит полимерный материал в качестве основного компонента. Слой 2 смолы способствует снижению веса токосъемника, а также функционирует в качестве среды переноса электронов. Чтобы получать слой смолы, обладающий электрической проводимостью, может использоваться электропроводящий полимер, или же к слою смолы может быть добавлен электропроводящий материал. В токосъемнике согласно настоящему варианту осуществления электропроводящий материал может использоваться при необходимости, поскольку захватывающие ионы частицы обеспечивают электрическую проводимость.
[0039] Отсутствуют конкретные ограничения на смолу, используемую в слое смолы, и может использоваться традиционно известный электрически непроводящий полимер или электропроводящий полимер. Предпочтительные примеры электрически непроводящего полимера включают в себя полиэтилен (PE), полиэтилен высокой плотности (HDPE), полиэтилен низкой плотности (LDPE)), полипропилен (PP), полиэтилентерефталат (PET), полибутилентерефталат (PBT), полиэфирнитрил (PEN), полиимид (PI), полиамидимид (PAI), полиамид (PA), политетрафторэтилен (PTFE), каучук на основе сополимера бутадиена и стирола (SBR), полиакрилонитрил (PAN), полиметилакрилат (PMA), полиметилметакрилат (PMMA), поливинилхлорид (PVC), поливинилиденфторид (PVdF), полистирол (PS), силиконовая смола, целлюлоза и эпоксидная смола. Эти электрически непроводящие полимеры обладают превосходной стабильностью напряжения или стойкостью к растворителям. Помимо этого, предпочтительные примеры электропроводящего полимера включают в себя полианилин, полипиррол, политиофен, полиацетилен, полипарафенилен, полифениленвинилен, полиакрилонитрил и полиоксадиазол. Эти электропроводящие полимеры обладают достаточной электрической проводимостью без добавления электропроводящего материала. Следовательно, электропроводящий полимер имеет преимущество ввиду простоты процесса производства и снижения веса токосъемника. Вышеописанные электрически непроводящие полимеры и электропроводящие полимеры могут использоваться независимо в виде одного единственного материала, или же два или более их вида могут использоваться в комбинации в виде смеси.
[0040] Токосъемник согласно настоящему варианту осуществления особенно предпочтительно содержит полиимид в качестве полимерного материала, используемого в слое смолы. Поскольку полиимид не адсорбирует легко ионы лития, эффект в качестве полимерного материала может достигаться в значительной степени.
[0041] Слой смолы может содержать другие полимерные материалы в дополнение к полиимиду. Предпочтительные примеры других полимерных материалов включают в себя материал, имеющий функциональную группу, такую как амид, аминогруппа, тиоамид, имид, иминогруппа, кетон, кетен, изоцианат, ацильная группа, ацетильная группа, карбоксильная группа, карбонильная группа, альдегидная группа, ацеталь, полуацеталь, сложный эфир, сложный тиоэфир, сложный фосфатный эфир, простой эфир, энон, энол, ангидрид кислоты, гидразин кислоты, азид кислоты и сульфонильная группа. Вышеуказанные функциональные группы не разлагаются легко при использовании в токосъемнике для вторичной батареи. Примеры полимерных материалов, имеющих такую функциональную группу и являющихся стабильными относительно электролитического раствора, напряжений и ионов лития, включают в себя полиамид (PA), полиамидимид (PAI), полиэтилентерефталат (PET), полибутилентерефталат (PBT), модифицированный простой эфир полифенилена (m-PPE, модифицированный PPE, PPO), акриловую смолу, полисульфон (PSF), полиэфирсульфон (PES), аморфный полиарилат (PAR), жидкокристаллический полимер (LCP) и полиэфирэфиркетон.
[0042] Слой смолы при необходимости содержит электропроводящий материал для того, чтобы обеспечивать электрическую проводимость в направлении укладки. Отсутствуют конкретные ограничения на используемый электропроводящий материал при условии, что этот материал является веществом, обладающим электрической проводимостью. Примеры материала, обладающего превосходной электрической проводимостью, стабильностью напряжения или свойствами барьера для ионов лития, включают в себя металл и углеродный материал. В частности, углеродный материал имеет довольно большой интервал напряжений, является стабильным в широком диапазоне относительно как напряжения положительного электрода, так и напряжения отрицательного электрода, и обладает превосходной электрической проводимостью. Помимо этого, углеродный материал имеет небольшую плотность по сравнению с электропроводящим материалом, содержащим металл. Следовательно, целесообразно использовать углеродный материал, поскольку может достигаться снижение веса токосъемника.
[0043] Отсутствуют конкретные ограничения на металл, содержащийся в слое смолы, но слой смолы предпочтительно содержит один металл или сплав металла, или оксид металла, в котором металл выбирается из группы, состоящей из никеля (Ni), титана (Ti), алюминия (Al), платины (Pt), золота (Au), железа (Fe), хрома (Cr), олова (Sn), цинка (Zn), индия (In), сурьмы (Sb) и калия (K). Эти металлы обладают стабильностью напряжения в положительном электроде или отрицательном электроде, сформированном на поверхности токосъемника. Из этих металлов особенно предпочтительно используются Ni, Pt, Au и Cr.
[0044] Конкретные примеры сплава, содержащегося в слое смолы, включают в себя нержавеющую сталь (SUS), инконель (зарегистрированный товарный знак), хастелой (зарегистрированный товарный знак), сплав Fe-Cr и сплав Ni-Cr. Когда используются эти сплавы, может достигаться высокая стабильность напряжения.
[0045] Отсутствуют конкретные ограничения на углеродный материал, содержащийся в слое смолы, но слой смолы предпочтительно содержит по меньшей мере один м