Способ получения безводного комплекса тиоцианата иттрия
Иллюстрации
Показать всеИзобретение относится к области координационной химии, конкретно к приготовлению исходных реагентов для синтезов, исключающих присутствие молекул воды. Способ получения безводного комплекса тиоцианата иттрия, характеризующегося химической формулой [Y(18-crown-6)(NCS)3], либо [Y(18-crown-6)(NCS)3]-nSol, где Sol - молекула растворителя, заключается в том, что проводят взаимодействие гексагидрата тиоцианата иттрия Y(NCS)3·6H2O с краун-эфиром номенклатурного обозначения 18-crown-6 в растворителях, выбранных из ряда: ацетонитрил, тетрагидрофуран, этилацетат, изопропанол при мольном соотношении 18-crown-6:иттрий=1.0÷2.0, при этом взаимодействие проводят в атмосфере воздуха при температуре 15÷30°С. Изобретение позволяет получать полностью дегидратировнные комплексы тиоцианата иттрия в одну стадию, использовать в качестве растворителей доступные и недорогие органические растворители, сократить энергозатраты, а также дает возможность получения новых соединений, пригодных для замены дорогостоящих металлорганических реагентов. 2 ил., 4 пр.
Реферат
Изобретение относится к области координационной химии, конкретно к приготовлению исходных реагентов для синтезов, исключающих присутствие молекул воды.
Известен способ обезвоживания YCl3·nH2O тионилхлоридом в растворе ацетонитрила (MeCN), в результате которого получали частично дегидратированный сольват [YCl3(H2O)2(MeCN)2] [G.A. Willey, P.R. Meehan, P.A. Salter, W. Errington. Yttrium(lll) chloride solvates: Synthesis and structural characterisation of YCl2(H2O)2(MeCN)2. // Polyhedron. 1996, V.15, P.3193-3196].
Недостатком известного метода является собственно неполная дегидратация.
В известном способе синтеза безводных метанольных сольватов бромида и хлорида лантана [T.J.Boyle, L.A.M.Ottley, T.M.Alam, M.A.Rodriguez, P.Yang, S.K.Mcintyre. Structural characterization of methanol substituted lanthanum halides. // Polyhedron. 2010, V.29, P.1784-1795] получены комплексы LnX3(MeOH)x.
Недостатком является то, что полученные комплексы крайне неустойчивы в атмосфере влажного воздуха.
Известен способ получения ансамбля комплекса иттрия Y(NCS)3·6H2O с краун-эфиром 18-crown-6 [A.Ilyukhin, Zh.Dobrokhotova, S.Petrosyants, V.Novotortsev. Yttrium tiocyanate-based supramolecular architectures: Synthesis, crystal structures, and thermal properties. // Polyhedron. 2011, V.30, P.2654-2660], который выбран в качестве прототипа. Данный способ получения включает в себя взаимодействие гексагидрата тиоцианата иттрия Y(NCS)3·6H2O с краун-эфиром 18-crown-6 в простых первичных алифатических спиртах таких, как МеОН и ЕtOН. В результате реакции получают ассоциат [Y(H2O)4(NCS)3]·1.5(18-crown-6), в котором молекула краун-эфира находится во внешней сфере комплекса и в котором прошла частичная дегидратация координационной сферы иттрия. Супрамолекулярный ансамбль по прототипу вполне устойчив на воздухе и полностью дегидратируется при дополнительном нагреве до температуры свыше 100°С.
Недостатком прототипа является то, что в выбранных условиях не удается провести одностадийное замещение всех координированных молекул воды в координационной сфере иттрия на молекулу краун-эфира.
Вторым недостатком прототипа является дополнительная стадия нагрева для полного удаления молекул воды.
Изобретение направлено на изыскание способа получения безводного комплекса тиоционата иттрия в одну стадию, на воздухе, влажности 50-90% и при температуре 15÷30°С.
Технический результат достигается тем, что предложен способ получения безводного комплекса тиоцианата иттрия, характеризующегося химической формулой [Y(18-crown-6)(NCS)3], либо [Y(18-crown-6)(NCS)3]·nSol, где Sol - молекула растворителя, заключающийся в том, что проводят взаимодействие гексагидрата тиоцианата иттрия Y(NCS)3·6H2O с краун-эфиром номенклатурного обозначения 18-crown-6 в растворителях, выбранных из ряда: ацетонитрил, тетрагидрофуран, этилацетат, изопропанол при мольном соотношении 18-crown-6:иттрий = 1.0÷2.0; при этом взаимодействие проводят в атмосфере воздуха при температуре 15÷30°С.
Для синтеза безводных тиоцианатов иттрия используют следующие исходные реагенты: иттрия тиоцианат гексагидрат (Y(NCS)3·6H2O, ч., Новосибирский завод редких металлов), краун-эфир 4,7,10,13,16-гексаоксоциклооктадекан (18-crown-6, C12H24O6, 99%, Aldrich), и растворители: ацетонитрил (C2H3N, ч., Химмед), тетрагидрофуран (C4H8O, ч., Химмед), этилацетат или этиловый эфир уксусной кислоты (C4H8O2, ч., Химмед), изопропиловый спирт (C3H8O, ч., Химмед). Синтез проводят в атмосфере воздуха, влажности 50÷90%, в стеклянном стакане, который помещают на магнитную мешалку для перемешивания. Для синтеза заданные количества краун-эфира и тиоцианата иттрия последовательно растворяют в выбранном растворителе на воздухе при температуре 15÷30°С. В зависимости от растворителя безводные тиоцианаты иттрия выделяют из реакционной смеси либо сразу в виде донной фазы, либо после изотермического испарения полученного гомогенного раствора. Осадки отделяют на стеклянном фильтре, подключенном к водоструйному насосу, после чего высушивают в эксикаторе над силикагелем до постоянной массы.
Анализ полученных безводных тиоцианатов иттрия проводят с использованием элементного анализа на углерод, водород, азот на анализаторе Carlo Erba, метода ИК-спектроскопии на приборе ИК-Фурье спектрометре Nexus фирмы Nicolet, а также метода рентгенофазового анализа на дифрактометре STOE STADI Р и рентгеноструктурного анализа (при наличии монокристаллов) на дифрактометре Bruker SMART APEX2. Термическое поведение соединений изучают методами дифференциальной сканирующей калориметрии (ДСК) и термогравиметрического анализа (ТГА) на приборе NETZSCH TG 209 F1.
Было установлено, что синтез при температуре <15°С не целесообразен из-за понижения растворимости реагентов, повышение температуры выше 30°С не допускается, так как синтез проходит в открытом сосуде с использованием легколетучих растворителей.
Мольное соотношении 18-crown-6:иттрий=1.0÷2.0 выбирают из тех соображений, что при соотношении меньше 1.0 существенно уменьшается выход продукта, а при соотношении свыше 2.0 избыточное содержание краун-эфира не оказывает существенного влияния на процесс комплексообразования.
Исследование влияния концентрации неорганической соли и краун-эфира показало, что оптимальным соотношением, обеспечивающим максимальный выход безводного продукта, является соотношение 1.5.
Сущность заявляемого изобретения поясняется следующими прилагаемыми иллюстрациями.
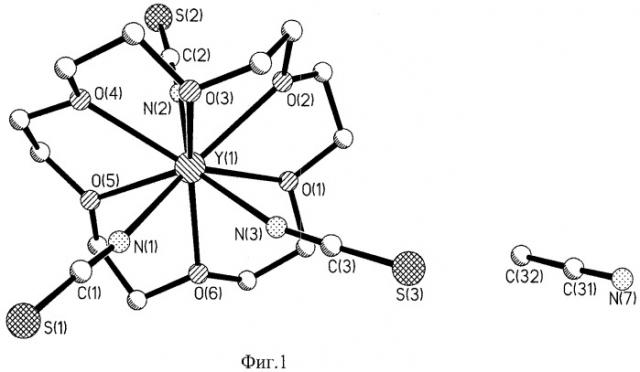
Фиг.1. Молекулярная структура безводного сольвата [Y(18-crown-6)(NCS)3]·CH3CN.
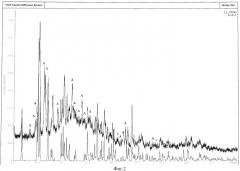
Фиг.2. Рентгенограмма смеси безводных комплексов, полученных из раствора изопропанола. Нижняя кривая - теоретическая рентгенограмма [Y(18-crown-6)(NCS)3]·0.5(18-crown-6), пики А отвечают комплексу [Y(18-crown-6)(NCS)3].
Исследование влияния растворителя на дегидратацию тиоцианата иттрия при взаимодействии с 18-crown-6 показало, что замещение молекул воды в координационной сфере иттрия можно связать с особенностями формирования водородных связей краун-эфиром и молекулами растворителя. В растворителях, которые выступают преимущественно как акцепторы при формировании водородной связи - ацетонитрил, тетрагидрофуран, этилацетат - у краун-эфира нет возможности реализовать свои акцепторные возможности в объеме растворителя, так как в комплексах РЗМ связи преимущественно ионные, координированные O-донорные молекулы воды легко вытесняются O-донорами макроцикла, чему способствует макроциклический эффект и энтропийный характер подобных реакций.
Что касается изопропанола, то его попадание в ряд с акцепторными растворителями связано со стерическими особенностями вторичного спирта [P.Huyskens. Molecular structure of liquid alcohols. // J. Molec. Structure. 1983, v.100, P.403-414], поведение вторичных спиртов резко отличается от первичных, каковыми являются метанол и этанол по прототипу.
Ниже приведены примеры реализации заявляемого изобретения. Примеры иллюстрируют, но не ограничивают предложенный способ.
Пример 1
Для приготовления безводного комплекса тиоцианата иттрия 0.38 г (1.44 ммоля) 18-crown-6 и 0.36 г (0.97 ммоля) гексагидрата тиоцианата иттрия последовательно помещали в стеклянный стакан с 10 мл тетрагидрофурана. Перемешивали на магнитной мешалке до получения гомогенного кремового раствора. Через 2 суток изотермического испарения выпали кристаллы желтого цвета. Всю массу кристаллов откачивали на фильтре Шотта. Высушивали в эксикаторе над силикагелем, получали 0.31 г порошка ярко-желтого цвета.
Для [Y(C12H24O6)(NCS)3]=C15H24N3O6S3Y (формульная масса=527.42) найдено, %: С 34.14; Н 4.70; N 7.74; S 17.56, вычислено, %: С 34.15, Н 4.58, N7.96, S 18.23.
Пример 2
Для приготовления безводного комплекса тиоцианата иттрия, 0.37 г (1.42 ммоля) 18-crown-6 и 0.35 г (0.94 ммоля) гексагидрата тиоцианата иттрия последовательно растворяли в стеклянном стакане в 10 мл ацетонитрила. Перемешивали на магнитной мешалке до получения гомогенного кремового раствора. Через 2 суток изотермического испарения образовалась твердая фаза желтоватого цвета, после отделения которой получили бесцветный раствор. Через 2 суток изотермического концентрирования этого раствора выпали бесцветные кристаллы, выход 0,40 г. Отделяли на стеклянном фильтре, высушивали в эксикаторе над силикагелем.
Рентгеноструктурный анализ показал образование безводного сольвата [Y(18-crown-6)(NCS)3]·CH3CN (см. Фиг.1).
Пример 3
Для приготовления безводного комплекса тиоцианата иттрия, 0.40 г (1.54 ммоля) 18-crown-6 и 0.37 г (0.98 ммоля) гексагидрата тиоцианата иттрия последовательно растворяли в стеклянном стакане в 40 мл этилацетата. После перемешивания получили розовый раствор с белой донной фазой. Твердую фазу отделяли на стеклянном фильтре, высушивали в эксикаторе над силикагелем.
Выход 0.48 г.
Для [Y(C12H24O6)(NCS)3]=C15H24N3O6S3Y (формульная масса=527.42) найдено, %: С 34.27; Н 4.62; N 7.77; S 17.89; вычислено, %: С 34.15, Н 4.58, N 7.96, S 18.23.
Пример 4
Для приготовления безводного комплекса тиоцианата иттрия, 0.44 г (1.66 ммоля) 18-crown-6 растворяли в 10 мл изопропанола, после добавления 0.39 г (1.04 ммоля) гексагидрата тиоцианата иттрия сразу выделялся нерастворимый продукт, который переносили на стеклянный фильтр, откачивали и высушивали в эксикаторе над силикагелем. Получили 0.52 г кристаллического порошка розового цвета.
По данным РФА образуется смесь безводных комплексов 50% [Y(C12H24O6)(NCS)3]+50%[Y(C12H24O6)(NCS)3]·0,5(C12H24O6) (см. Фиг.2). Для смеси 50% [Y(C12H24O6)(NCS)3]+50%[Y(C12H24O6)(NCS)3]·0,5(C12H24O6) найдено, %: С 36.13; Н 5.00; N 7.32; S 16.75; вычислено, %: С 36.42; Н 5.09; N 7.07; S 16.20.
Таким образом, предлагаемый метод синтеза позволяет получать полностью дегидратировнные комплексы тиоцианата иттрия из коммерческих не дегитратированных растворителей. Преимуществами настоящего изобретения являются: устойчивость на воздухе получаемых соединений, отсутствие их гидратации и гидролиза при температуре 15÷30°С и влажности воздуха 50÷90%; использование в качестве растворителей доступных и недорогих органических растворителей; заметное сокращение энергозатрат при проведении синтеза; возможность получения новых соединений, пригодных для замены дорогостоящих металлорганических реагентов.
Способ получения безводного комплекса тиоцианата иттрия, характеризующегося химической формулой [Y(18-crown-6)(NCS)3], либо [Y(18-crown-6)(NCS)3]·nSol, где Sol - молекула растворителя, заключающийся в том, что проводят взаимодействие гексагидрата тиоцианата иттрия Y(NCS)3·6H2O с краун-эфиром номенклатурного обозначения 18-crown-6 в растворителях, выбранных из ряда: ацетонитрил, тетрагидрофуран, этилацетат, изопропанол при мольном соотношении 18-crown-6:иттрий=1.0÷2.0; при этом взаимодействие проводят в атмосфере воздуха при температуре 15÷30°С.