5-галогензамещенные производные оксиндола и их применение для лечения вазопрессинзависимых заболеваний
Иллюстрации
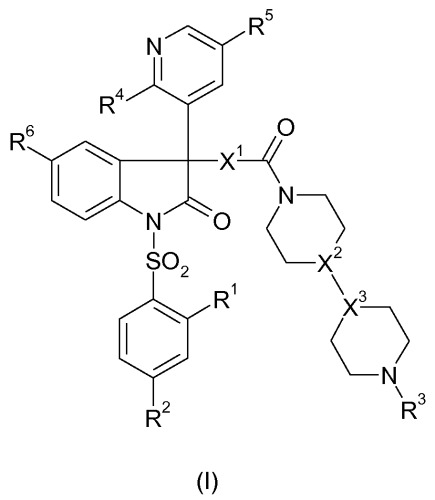
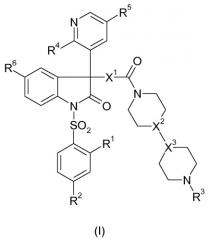
Показать всеИзобретение относится к новым 5-галогензамещенным производным оксиндола формулы I: где: R1 означает водород, метокси- или этоксигруппу; R2 означает водород или метоксигруппу; R3 означает водород, метил, этил, н-пропил или изопропил; R4 означает этокси- или изопропоксигруппу; R5 означает Н или метил; R6 означает Сl или F; X1 означает О, NH или СН2; X2 и X3 означают N или СН при условии, что X2 и X3 одновременно не представляют собой N; а также их фармацевтически приемлемые соли. Кроме того, изобретение относится к фармацевтическим композициям для лечения и/или профилактики вазопрессинзависимых заболеваний, содержащим производные формулы I, и к их применению для лечения вазопрессинзависимых заболеваний. 5 н. и 20 з.п. ф-лы, 8 пр., 2 табл.
Реферат
Настоящее изобретение относится к новым замещенным производным оксиндола, фармацевтическим композициям, содержащим такие производные, и их применению для лечения вазопрессинзависимых заболеваний.
Вазопрессин представляет собой эндогенный гормон, оказывающий самое разное действие на органы и ткани. Предполагают, что вазопрессиновая система играет роль в случае различных болезненных состояний, таких как, например, сердечная недостаточность и артериальная гипертония. В настоящее время известны три рецептора (V1a, V1b, или V3, и V2), через которые вазопрессин опосредует свои многочисленные воздействия. Поэтому антагонисты данных рецепторов исследуют как возможные новые терапевтически активные исходные вещества для лечения болезней (M. Thibonnier, Exp. Opin. Invest. Drugs, 1998, 7(5), 729-740).
В данной заявке описаны новые замещенные оксиндолы, содержащие в положении 1 фенилсульфонильную группу. 1-Фенилсульфонил-1,3-дигидро-2H-индол-2-он был описан в качестве лиганда рецепторов вазопрессина. В WO 93/15051, WO 95/18105, WO 98/25901, WO 01/55130, WO 01/55134, WO 01/164668 и WO 01/98295 также описаны производные, которые в положении 1 радикала оксиндола содержат арилсульфонильные группы. Данные соединения отличаются от соединений по настоящему изобретению в основном заместителями в положении 3.
Так, в WO 93/15051 и WO 98/25901 описаны 1-фенилсульфонил-1,3-дигидро-2H-индол-2-оны в качестве лигандов рецепторов вазопрессина, в которых радикал оксиндола в положении 3 содержит в качестве заместителей два алкила, которые совместно могут образовывать также циклоалкил (спиросоединение). В качестве альтернативы спироцикл может содержать гетероатомы, такие как кислород и азот (которые при необходимости связаны с заместителями).
В WO 95/18105 описаны 1-фенилсульфонил-1,3-дигидро-2H-индол-2-оны в качестве лигандов рецепторов вазопрессина, которые в положении 3 содержат атом азота. Дополнительно в положении 3 присоединены радикалы, которые при необходимости выбирают из замещенных алкилов, циклоалкилов, фенила или бензила.
В WO 03/008407 описаны 1-фенилсульфонилоксиндолы, в которых в положении 3 через мочевинную, карбаматную или 2-оксоэтильную группу к оксиндолу присоединены пиридилпиперазины.
В WO 2005/030755 в качестве примера 105 описан 5-хлор-1-(2,4-диметоксифенилсульфонил)-3-(2-метоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(1-метилпиперидин-4-ил)пиперазин-1-карбоновой кислоты.
В WO 2006/005609 в качестве примера 66 описан дигидрохлорид [5-хлор-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксифенил)-2-оксо-2,3-дигидро-1H-индол-3-ил]амида 4-(1-метилпиперидин-4-ил)пиперазин-1-карбоновой кислоты.
Наряду со сродством связывания с V1b-рецептором вазопрессина для лечения и/или профилактики вазопрессинзависимых заболеваний могут быть полезными другие свойства, такие как, например:
1) селективность к V1b-рецептору вазопрессина по сравнению с V1a-рецептором вазопрессина, т.е. отношение сродства связывания с V1a-рецептором (Ki(V1a) (определенного в единицах "наномолярности", нМ)), и сродства связывания с V1b-рецептором (Ki(V1b) (определенного в единицах "наномолярности", нМ)). Чем больше отношение Ki(V1a)/Ki(V1b), тем больше V1b-селективность;
2) селективность к V1b-рецептору вазопрессина по сравнению с V2-рецептором вазопрессина, т.е. отношение сродства связывания с V2-рецептором (Ki(V2) (определенного в единицах "наномолярности", нМ)) и сродства связывания с V1b-рецептором (Ki(V1b) (определенного в единицах "наномолярности", нМ). Чем больше отношение Ki(V2)/Ki(V1b), тем больше V1b-селективность;
3) селективность к V1b-рецептору вазопрессина по сравнению с OT-рецептором окситоцина, т.е. отношение сродства связывания с OT-рецептором окситоцина (Ki(OT) (определенного в единицах "наномолярности", нМ)) и сродства связывания с V1b-рецептором (Ki(V1b) (определенного в единицах "наномолярности", нМ). Чем больше отношение Ki(OT)/Ki(V1b), тем больше V1b-селективность;
4) метаболическая стабильность, например, определенная по измеренному in vitro времени полувыведения в микросомах печени различных видов (например, крысы или человека);
5) отсутствие или только незначительная степень ингибирования ферментов типа цитохром P450 (CYP): цитохром P450 (CYP) представляет собой обозначение суперсемейства гемопротеинов с ферментативной активностью (типа оксидазы). Они имеют особое значение также при разложении (метаболизме) инородных веществ, таких как лекарственные средства или ксенобиотики, в организмах млекопитающих. Важнейшими представителями типов и подтипов CYP в организме человека являются CYP 1A2, CYP 2C9, CYP 2D6 и CYP 3A4. При одновременном применении ингибиторов CYP 3A4 (например, грейпфрутового сока, циметидина, эритромицина) и лекарственных средств, которые данной ферментативной системой разлагаются и, таким образом, конкурируют за тот же сайт связывания с ферментом, их разложение может быть замедлено и вследствие этого может быть нежелательно усилено основное и побочное действие примененного лекарственного средства;
6) приемлемая растворимость в воде (мг/мл);
7) приемлемая фармакокинетика (изменение во времени концентрации соединения по настоящему изобретению в плазме или в тканях, например, головного мозга). Фармакокинетика может быть описана следующими параметрами: время полувыведения (ч), объем распределения (л·кг-1), клиренс плазмы (л·ч-1·кг-1), AUC ("площадь под кривой", т.е. площадь под кривой зависимости "концентрация-время", нг·ч·л-1), оральная биодоступность (соотношение AUC после перорального введения и AUC после внутривенного введения, нормализующее дозу), так называемое отношение "мозг-плазма" (соотношение AUC в ткани головного мозга и AUC в плазме);
8) отсутствие или только незначительная степень блокады hERG-канала: соединения, блокирующие hERG-канал, могут обуславливать удлинение QT-интервала и вследствие этого могут вести к серьезным нарушениям ритма сердца (например, к так называемой аритмии типа "torsade de pointes" ("пируэт")). Посредством испытаний, описанных в литературе, на замещение дофетилидом с радиоактивной меткой (G.J. Diaz et al., Journal of Pharmacological and Toxicological Methods, 50 (2004), 187-199) может быть определен потенциал соединений, блокирующих hERG-канал. Чем меньше IC50 в данном "испытании с дофетилидом", тем вероятнее мощная hERG-блокада. Кроме того, блокада hERG-канала может быть измерена в электрофизиологических экспериментах с клетками, трансфицированных hERG-каналом, посредством так называемого метода "whole-cell patch clamping" (метод локальной фиксации потенциала в конфигурации "целая клетка") (G.J. Diaz et al., Journal of Pharmacological and Toxicological Methods, 50 (2004), 187-199).
Задачей данного изобретения являлось получение соединений для лечения или профилактики различных вазопрессинзависимых заболеваний. Соединения должны были обладать высокой активностью и селективностью и, прежде всего, высоким сродством и селективностью в отношении V1b-рецептора вазопрессина. Дополнительно соединение по настоящему изобретению должно было обладать одним или несколькими упомянутыми ранее преимуществами по пунктам с 1) по 8).
Задача решена за счет соединений формулы I:
где:
R1 означает водород, метокси- или этоксигруппу;
R2 означает водород или метоксигруппу;
R3 означает водород, метил, этил, н-пропил или изопропил;
R4 означает этокси- или изопропоксигруппу;
R5 означает H или метил;
R6 означает Cl или F;
X1 означает O, NH или CH2;
X2 и X3 означают N или CH при условии, что X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемых солей и пролекарств.
В соответствии с этим настоящее изобретение относится к соединениям формулы I (далее называемым также "соединения I"), а также к фармацевтически приемлемым солям соединений I и пролекарствам соединений I.
Фармацевтически приемлемые соли соединений формулы I, которые обозначаются также, как физиологически приемлемые соли, получают, как правило, по реакции свободного основания соединений I по настоящему изобретению (т.е. соединений I структурной формулы I) с приемлемыми кислотами. Приемлемые кислоты приведены, например, в "Fortschritte der Arzneimittelforschung", 1966, Birkhäuser Verlag, Bd. 10, S. 224-285. В их число входят, например, соляная, лимонная, винная, молочная, фосфорная, метансульфоновая, уксусная, муравьиная, малеиновая и фумаровая кислоты.
Под термином "пролекарства" понимают такие соединения, которые in vivo метаболизируются до соединений I по настоящему изобретению. Типичные примеры пролекарств описаны в C.G. Wermeth (Hrsg.): The Practice of Medicinal Chemistry, Academic Press, San Diego, 1996, Seiten 671-715. В их число входят, например, фосфаты, карбаматы, аминокислоты, сложные эфиры, амиды, пептиды, мочевины и тому подобное. В данном случае приемлемыми пролекарствами могут быть, например, такие соединения I, в которых внешний атом азота внешнего пиперидин/пиперазинового кольца образует амидную/пептидную группировку благодаря тому‚ что данный атом азота связан с C1-C4-алкилкарбонилом, например, таким как ацетил, пропионил, н-пропилкарбонил, изопропилкарбонил, н-бутилкарбонил или трет-бутилкарбонил (пивалоил), с бензоилом или с аминокислотным остатком, присоединенным через группу CO, например с глицином, аланином, серином, фенилаланином, присоединенными через группу CO, и т.п., в качестве заместителя в положении R3. В качестве пролекарств приемлемыми являются также алкилкарбонилоксиалкилкарбаматы, в которых внешний атом азота внешнего пиперидин/пиперазинового кольца связан с группировкой формулы -C(=O)-O-CHRa-O-C(=O)-Rb в положении R3, где Ra и Rb независимо друг от друга означают C1-C4-алкилы. Такие карбаматы описаны, например, в J. Alexander, R. Cargill, S.R. Michelson, H. Schwam, J. Medicinal Chem. 1988, 31(2), 318-322. Затем такие группы вследствие метаболизма могут отщепляться и превращаться в соединения I, в которых R3 означает H.
C1-C4-алкил в рамках данного изобретения представляет собой линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, такой как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил.
C1-C3-алкоксигруппа в рамках данного изобретения представляет собой линейный или разветвленный алкил, содержащий от 1 до 3 атомов углерода и связанный через атом кислорода. Примеры таких групп представляют собой метокси-, этокси-, н-пропокси- и изопропоксигруппы.
Соединения формулы I по настоящему изобретению, их фармакологически приемлемые соли и пролекарства могут существовать также в виде сольватов или гидратов. Под сольватами в рамках данного изобретения понимают кристаллические формы соединений I или их фармацевтически приемлемых солей или пролекарств, в кристаллическую решетку которых встроены молекулы растворителя. Молекулы растворителя встроены предпочтительно в стехиометрическом соотношении. Гидраты представляют собой особую форму сольватов; в данном случае растворителем является вода.
Приведенные далее данные касательно основных и предпочтительных отличительных признаков настоящего изобретения, в частности, относительно R1, R2, R3, R4, R5, R6, X1, X2 и X3 соединения I, а также касательно отличительных признаков способа по настоящему изобретению и применения по настоящему изобретению, относятся как к непосредственно упомянутым значениям, так и предпочтительно к их любой возможной комбинации.
Соединения I получают предпочтительно в виде свободных оснований (т.е. согласно структурной формуле I) или в виде их кислотно-аддитивных солей.
В предпочтительном варианте осуществления R1 означает водород или метоксигруппу.
В более предпочтительном варианте осуществления R1 и R2 означают метоксигруппу.
В предпочтительном варианте осуществления R3 означает водород, метил или этил, предпочтительно водород или метил и более предпочтительно метил.
В предпочтительном варианте осуществления R4 означает этоксигруппу, а R5 означает H.
В альтернативном предпочтительном варианте осуществления R4 означает этоксигруппу, а R5 означает метил.
В альтернативном предпочтительном варианте осуществления R4 означает изопропоксигруппу, а R5 означает H.
Более предпочтительно R4 означает этоксигруппу, а R5 означает H.
В предпочтительном варианте осуществления R6 означает Cl.
В альтернативном предпочтительном варианте осуществления R6 означает F.
Более предпочтительно R6 означает Cl.
В предпочтительном варианте осуществления X1 означает NH.
В альтернативном предпочтительном варианте осуществления X1 означает O.
В альтернативном предпочтительном варианте осуществления X1 означает CH2.
Более предпочтительно X1 означает NH или CH2 и предпочтительно NH.
В предпочтительном варианте осуществления один из радикалов X2 и X3 означает N, а другой означает CH.
В более предпочтительном варианте осуществления X2 означает N, а X3 означает CH.
В альтернативном более предпочтительном варианте осуществления X2 означает CH, а X3 означает N.
В альтернативном предпочтительном варианте осуществления X2 и X3 означают CH.
Предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает водород или метоксигруппу;
R2 означает водород или метоксигруппу;
R3 означает водород, метил, этил, н-пропил или изопропил и предпочтительно водород, метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH, O или CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Более предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает водород или метоксигруппу;
R2 означает водород или метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH, O или CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Значительно более предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R1 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH, O или CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Наиболее предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Альтернативно наиболее предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH;
X2 означает N;
X3 означает CH;
а также их фармацевтически приемлемые соли и пролекарства.
Предпочтительными объектами настоящего изобретения являются также соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH;
X2 означает CH;
X3 означает N;
а также их фармацевтически приемлемые соли и пролекарства.
Предпочтительными объектами настоящего изобретения являются также соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH;
X2 означает CH;
X3 означает CH;
а также их фармацевтически приемлемые соли и пролекарства.
Альтернативно предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает водород или метоксигруппу;
R2 означает водород или метоксигруппу;
R3 означает водород, метил, этил, н-пропил или изопропил и предпочтительно водород, метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает NH, O или CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Альтернативно более предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает водород или метоксигруппу;
R2 означает водород или метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает NH, O или CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Альтернативно значительно более предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает NH, O или CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Альтернативно наиболее предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает NH;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Альтернативно наиболее предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает CH2;
X2 означает N или CH;
X3 означает N или CH;
причем X2 и X3 одновременно не представляют собой N;
а также их фармацевтически приемлемые соли и пролекарства.
Предпочтительными объектами настоящего изобретения являются соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает NH;
X2 означает N;
X3 означает CH;
а также их фармацевтически приемлемые соли и пролекарства.
Предпочтительными объектами настоящего изобретения являются также соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает NH;
X2 означает CH;
X3 означает N;
а также их фармацевтически приемлемые соли и пролекарства.
Предпочтительными объектами настоящего изобретения являются также соединения формулы I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил или этил;
R4 означает этоксигруппу;
R5 означает метил;
R6 означает Cl;
X1 означает NH;
X2 означает CH;
X3 означает CH;
а также их фармацевтически приемлемые соли и пролекарства.
Особенно предпочтительными являются соединения I, где:
R1 означает метоксигруппу;
R2 означает метоксигруппу;
R3 означает метил;
R4 означает этоксигруппу;
R5 означает водород;
R6 означает Cl;
X1 означает NH;
X2 означает N;
X3 означает CH;
а также их фармацевтически приемлемые соли и пролекарства.
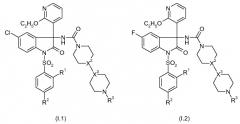
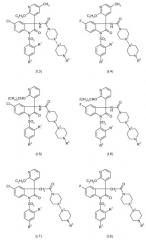
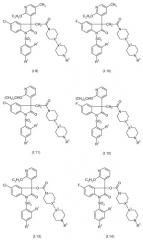
Примеры предпочтительных вариантов осуществления настоящего изобретения представляют собой соединения формул с I.1 по I.18, а также их фармацевтически приемлемые соли и пролекарства, в которых X2, X3, R1, R2 и R3 имеют значения, указанные в соответствующих строках таблицы 1.
| Таблица 1 | |||||
| № примера | X2 | X3 | R1 | R2 | R3 |
| A-1 | N | CH | метокси | метокси | метил |
| A-2 | N | CH | метокси | H | метил |
| A-3 | N | CH | этокси | H | метил |
| A-4 | N | CH | H | H | метил |
| A-5 | N | CH | H | метокси | метил |
| A-6 | N | CH | этокси | метокси | метил |
| A-7 | N | CH | метокси | метокси | этил |
| A-8 | N | CH | метокси | H | этил |
| A-9 | N | CH | этокси | H | этил |
| A-10 | N | CH | H | H | этил |
| A-11 | N | CH | H | метокси | этил |
| A-12 | N | CH | этокси | метокси | этил |
| A-13 | N | CH | метокси | метокси | н-пропил |
| A-14 | N | CH | метокси | H | н-пропил |
| A-15 | N | CH | этокси | H | н-пропил |
| A-16 | N | CH | H | H | н-пропил |
| A-17 | N | CH | H | метокси | н-пропил |
| A-18 | N | CH | этокси | метокси | н-пропил |
| A-19 | N | CH | метокси | метокси | изопропил |
| A-20 | N | CH | метокси | H | изопропил |
| A-21 | N | CH | этокси | H | изопропил |
| A-22 | N | CH | H | H | изопропил |
| A-23 | N | CH | H | метокси | изопропил |
| A-24 | N | CH | этокси | метокси | изопропил |
| A-25 | N | CH | метокси | метокси | H |
| A-26 | N | CH | метокси | H | H |
| A-27 | N | CH | этокси | H | H |
| A-28 | N | CH | H | H | H |
| A-29 | N | CH | H | метокси | H |
| A-30 | N | CH | этокси | метокси | H |
| A-31 | CH | N | метокси | метокси | метил |
| A-32 | CH | N | метокси | H | метил |
| A-33 | CH | N | этокси | H | метил |
| A-34 | CH | N | H | H | метил |
| A-35 | CH | N | H | метокси | метил |
| A-36 | CH | N | этокси | метокси | метил |
| A-37 | CH | N | метокси | метокси | этил |
| A-38 | CH | N | метокси | H | этил |
| A-39 | CH | N | этокси | H | этил |
| A-40 | CH | N | H | H | этил |
| A-41 | CH | N | H | метокси | этил |
| A-42 | CH | N | этокси | метокси | этил |
| A-43 | CH | N | метокси | метокси | н-пропил |
| A-44 | CH | N | метокси | H | н-пропил |
| A-45 | CH | N | этокси | H | н-пропил |
| A-46 | CH | N | H | H | н-пропил |
| A-47 | CH | N | H | метокси | н-пропил |
| A-48 | CH | N | этокси | метокси | н-пропил |
| A-49 | CH | N | метокси | метокси | изопропил |
| A-50 | CH | N | метокси | H | изопропил |
| A-51 | CH | N | этокси | H | изопропил |
| A-52 | CH | N | H | H | изопропил |
| A-53 | CH | N | H | метокси | изопропил |
| A-54 | CH | N | этокси | метокси | изопропил |
| A-55 | CH | N | метокси | метокси | H |
| A-56 | CH | N | метокси | H | H |
| A-57 | CH | N | этокси | H | H |
| A-58 | CH | N | H | H | H |
| A-59 | CH | N | H | метокси | H |
| A-60 | CH | N | этокси | метокси | H |
| A-61 | CH | CH | метокси | метокси | метил |
| A-62 | CH | CH | метокси | H | метил |
| A-63 | CH | CH | этокси | H | метил |
| A-64 | CH | CH | H | H | метил |
| A-65 | CH | CH | H | метокси | метил |
| A-66 | CH | CH | этокси | метокси | метил |
| A-67 | CH | CH | метокси | метокси | этил |
| A-68 | CH | CH | метокси | H | этил |
| A-69 | CH | CH | этокси | H | этил |
| A-70 | CH | CH | H | H | этил |
| A-71 | CH | CH | H | метокси | этил |
| A-72 | CH | CH | этокси | метокси | этил |
| A-73 | CH | CH | метокси | метокси | н-пропил |
| A-74 | CH | CH | метокси | H | н-пропил |
| A-75 | CH | CH | этокси | H | н-пропил |
| A-76 | CH | CH | H | H | н-пропил |
| A-77 | CH | CH | H | метокси | н-пропил |
| A-78 | CH | CH | этокси | метокси | н-пропил |
| A-79 | CH | CH | метокси | метокси | изопропил |
| A-80 | CH | CH | метокси | H | изопропил |
| A-81 | CH | CH | этокси | H | изопропил |
| A-82 | CH | CH | H | H | изопропил |
| A-83 | CH | CH | H | метокси | изопропил |
| A-84 | CH | CH | этокси | метокси | изопропил |
| A-85 | CH | CH | метокси | метокси | H |
| A-86 | CH | CH | метокси | H | H |
| A-87 | CH | CH | этокси | H | H |
| A-88 | CH | CH | H | H | H |
| A-89 | CH | CH | H | метокси | H |
| A-90 | CH | CH | этокси | метокси | H |
Среди упомянутых ранее соединений с I.1 по I.18 предпочтительными являются соединения формул I.1, I.3, I.5, I.7, I.9, I.11, I.13, I.15 и I.17, в которых X2, X3, R1, R2 и R3 имеют значения, указанные в соответствующих строках таблицы 1. Среди последних упомянутых соединений в свою очередь предпочтительными являются соединения формул I.1, I.3, I.5, I.7 и I.13, в которых X2, X3, R1, R2 и R3 имеют значения, указанные в соответствующих строках таблицы 1.
Более предпочтительными являются соединения формулы I.1, в которой X2, X3, R1, R2 и R3 имеют значения, указанные в таблице 1 в строках A-1, A-2, A-4, A-7, A-31, A-32, A-34, A-37, A-38, A-40, A-61, A-67 и A-85, предпочтительно в строках A-1, A-2, A-4, A-7, A-31, A-37, A-38, A-61 и A-67, и более предпочтительно в строках A-1, A-4, A-7, A-31, A-37, A-61 и A-67.
Более предпочтительными являются также соединения формулы I.3, в которой X2, X3, R1, R2 и R3 имеют значения, указанные в таблице 1 в строках A-1, A-7, A-31 и A-37 и предпочтительно в строках A-1 и A-7.
Более предпочтительными являются также соединения формулы I.5, в которой X2, X3, R1, R2 и R3 имеют значения, указанные в таблице 1 в строках A-1, A-7, A-31 и A-37 и предпочтительно в строках A-1 и A-7.
Более предпочтительными являются также соединения формулы I.7, в которой X2, X3, R1, R2 и R3 имеют значения, указанные в таблице 1 в строках A-1, A-4, A-31, A-34, A-37 и A-40 и предпочтительно в строке A-1.
Более предпочтительными являются также соединения формулы I.13, в которой X2, X3, R1, R2 и R3 имеют значения, указанные в таблице 1 в строках A-1, A-2, A-4, A-31, A-32 и A-34 и предпочтительно в строке A-2.
Среди упомянутых более предпочтительных соединений в свою очередь предпочтительными являются соединения I.1, I.3, I.5 и I.7, причем X2, X3, R1, R2 и R3 имеют значения, указанные для соответствующих соединений. Среди последних упомянутых соединений более предпочтительными являются соединения формул I.1, I.3 и I.5 и предпочтительно формул I.1 и I.3, причем соединения формулы I.1 являются наиболее предпочтительными.
В соединениях I по настоящему изобретению в положении 3 2-оксиндольного кольца находится центр хиральности. Поэтому соединения по настоящему изобретению могут существовать в виде смеси 1:1 энантиомеров (рацемата) или в виде нерацемической смеси энантиомеров, которая обогащена одним из энантиомеров, т.е. энантиомером, вращающим плоскость колебаний линейно-поляризованного света влево (т.е. вращающим против часовой стрелки) (далее обозначается как (-)-энантиомер), или энантиомером, вращающим плоскость колебаний линейно-поляризованного света вправо (т.е. вращающим по часовой стрелке) (далее обозначается как (+)-энантиомер), или в виде по существу энантиомерно чистых соединений, т.е. в виде по существу энантиомерно чистых (-)-энантиомеров или (+)-энантиомеров. Так как в случае соединений по настоящему изобретению имеется только один центр асимметрии и отсутствует ось/плоскость хиральности, то нерацемическую смесь можно охарактеризовать также как смесь энантиомеров, в которой преобладает или R- или S-энантиомер. В соответствии с этим по существу энантиомерно чистые соединения могут быть охарактеризованы также, как по существу энантиомерно чистый R-энантиомер или по существу энантиомерно чистый S-энантиомер.
Под выражением "по существу энантиомерно чистые соединения" в рамках данного изобретения понимают такие соединения, в которых энантиомерный избыток (enantiomeric excess, ee; % ee=(R-S)/(R+S)×100 или (S-R)/(S+R)×100) составляет по меньшей мере 80% ee, предпочтительно по меньшей мере 85% ee, более предпочтительно по меньшей мере 90% ee, наиболее предпочтительно по меньшей мере 95% ee и, в частности, по меньшей мере 98% ee.
В одном из вариантов осуществления настоящего изобретения соединения по настоящему изобретению находятся в виде по существу энантиомерно чистых соединений. Более предпочтительными являются соединения, в которых энантиомерный избыток составляет по меньшей мере 85% ee, более предпочтительно по меньшей мере 90% ee, наиболее предпочтительно по меньшей мере 95% ee и, в частности, по меньшей мере 98% ee.
Таким образом, объектами настоящего изобретения являются как чистые энантиомеры, так и их смеси, например смеси, в которых один из энантиомеров содержится в преобладающем количестве, а также рацематы. Объектом настоящего изобретения являются также фармацевтически приемлемые соли и пролекарства чистых энантиомеров соединений I, а также смеси энантиомеров в виде фармацевтически приемлемых солей и пролекарств соединений I.
Предпочтительные варианты осуществления настоящего изобретения относятся к упомянутым ранее соединениям формулы I, отличающимся тем, что они существуют в оптически активной форме и представляют собой вращающие вправо (т.е. вращающие по часовой стрелке) плоскость колебаний поляризованного света энантиомеры соответствующих соединений формулы I в виде свободного основания или их фармацевтически приемлемой соли или пролекарства. Правовращающие или вращающие по часовой стрелке энантиомеры соединений I далее обозначаются как (+)-энантиомеры.
Более предпочтительными являются соединения общей формулы I, их фармацевтически приемлемые соли и пролекарства, упомянутые ранее и содержащие соответствующий (+)-энантиомер по оптической чистоте (enantiomeric excess (энантиомерный избыток)), ee) в количестве больше 50% ee, преимущественно по меньшей мере 80% ee, более предпочтительно по меньшей мере 90% ee, наиболее предпочтительно по меньшей мере 95% ee и, в частности, по меньшей мере 98% ee.
Предпочтительные варианты осуществления настоящего изобретения относятся также к упомянутым ранее соединениям общей формулы I, отличающимся тем, что они существуют в оптически неактивной форме, т.е. в виде рацематов или в виде фармацевтически приемлемых солей или пролекарств рацематов.
В рамках данного изобретения указания по направлению вращения поляризованного света преимущественно даны в виде знака (+) или (-) соответственно результату определения в хлороформе в качестве растворителя или в хлороформсодержащих смесях растворителей и предпочтительно в хлороформе.
Далее описаны примерные пути синтеза для получения производных оксиндола по настоящему изобретению.
Получение соединений по настоящему изобретению может быть осуществлено согласно методикам синтеза аналогичных соединений, описанным в WO 2005/030755 и WO 2006/005609, и в качестве примера отображено в общих чертах на схемах синтеза 1-3. На данных схемах синтеза приняты обозначения соответственно формуле I.
3-Гидрокси-1,3-дигидроиндол-2-оны IV могут быть получены присоединением металлсодержащего гетероцикла III к кетогруппе в положении 3 изатинов II. Металлсодержащие гетероциклы, такие как, например, соответствующий реактив Гриньяра (Mg) или литийорганическое соединение, могут быть получены традиционным способом из галогенсодержащих или углеводородных соединений. Примерные методики представлены в Houben-Weyl, Methoden der Organischen Chemie, Bd. 13, 1-2, Kap. Mg- bzw. Li-Verbindungen. Изатины II имеются в продаже или могут быть получены аналогично способам, описанным в литературе (Advances in Heterocyclic Chemistry, A.R. Katritzky and A.J. Boulton, Academic Press, New York, 1975, 18, 2-58; J. Brazil. Chem. Soc. 12, 273-324, 2001).
3-Гидроксиоксиндолы IV могут быть превращены в соединения V, содержащие в положении 3 уходящую группу LG', причем уходящая группа LG' представляет собой традиционную уходящую группу, такую как, например, хлорид- или бромид-ион. Промежуточное соединение V, в котором, например, LG'=хлор, может быть получено обработкой спирта IV тионилхлоридом в присутствии основания, такого как, например, пиридин, в приемлемом растворителе, таком как, например, дихлорметан.
Затем соединения V могут быть превращены в амины VI по реакции замещения с амином, таким как, например, аммиак. Далее соединения VI могут быть превращены обработкой сульфонилхлоридом VII после депротонирования сильным основанием, таким как, например, трет-бутилат калия или гидрид натрия в ДМФА, в сульфонилированное соединение VIII. Применяемые сульфонилхлориды VII могут быть приобретены в торговой сети или получены известными способами (см., например, J. Med. Chem. 40, 1149 (1997)).
Получение соединений общей формулы I по настоящему изобретению, в которых в положении 3 находится мочевинная группа, может быть осуществлено двухстадийным способом, описанным в WO 2005/030755 и WO 2006/005609 и показанным на схеме синтеза 1. Сначала соединение VIII взаимодействием с фениловым эфиром хлормуравьиной кислоты в присутствии основания, такого как, например, пиридин, превращают в соответствующий фенилкарбамат IX.
Последующее взаимодействие с амином X при необходимости