Способ рентгенофлуоресцентного определения микроэлементов с предварительным их концентрированием из сверхмалых проб воды и водных растворов
Иллюстрации
Показать всеИзобретение относится к способу рентгенофлуоресцентного определения микроэлементов и может быть использовано при анализе природных вод и техногенных растворов. Заявленный способ включает предварительное концентрирование микроэлементов из сверхмалых проб воды и водных растворов. Микрогранулу гидрофильного материала помещают на предварительно натянутую рентгенопрозрачную гидрофобную пленку, берут каплю из анализируемого раствора и наносят ее на указанную пленку с покрытием указанной микрогранулы. Проводят испарение указанной капли, а затем анализ микрогранулы с помощью рентгенофлуоресцентного микроанализатора с фокусирующей рентгеновской линзой. При этом пленку перед помещением на нее микрогранулы смазывают нерастворимым в воде и водных растворах жидким поверхностно-активным веществом. В каплю анализируемого раствора вводят от 1 до 5% концентрированной азотной или хлорной кислоты или берут эту каплю из анализируемого раствора, в который предварительно введена азотная или хлорная кислота до достижения ее концентрации от 1 до 5%. Заявленное изобретение обеспечивает уменьшение аналитических ошибок. 2 з.п. ф-лы, 1 табл., 8 ил., 4 пр.
Реферат
Изобретение относится к области инструментального химического анализа, более конкретно - к способу рентгенофлуоресцентного определения микроэлементов с предварительным их концентрированием из сверхмалых проб воды и водных растворов.
Известен ряд способов анализа воды и водных растворов рентгеноспектральными методами, в которых с целью исключения мешающих эффектов при регистрации соответствующих спектров, а также с целью уменьшения пределов обнаружения аналитов определяемые компоненты переводят тем или иным способом в твердую фазу с одновременным их концентрированием. Например, используют комбинированные схемы анализа растворов, включающие сорбционное концентрированно микроэлементов и их последующее определение в фазе сорбента (Ю.А.Золотов, Г.И.Цизин, С.Г.Дмитриенко, Е.И.Моросанова. Сорбционное концентрирование микрокомпонентов из растворов. Применение в неорганическом анализе, М., "Наука", 2007, с.320 [1]; О.Б.Моходоева, Г.В.Мясоедова, И.В.Кубракова. Сорбционное концентрирование в комбинированных методах определения благородных металлов, Ж. аналит. химии, 2007, Т.62, №7, с.679-695 [2]; Р.Х.Хамизов, А.Н.Груздева, М.Г.Токмачев, Г.И.Цизин, Н.А.Тихонов, М.А.Кумахов. Высокочувствительный рентгенофлуоресцентный анализ растворов с использованием сорбционной накопительной микросистемы, Ж. аналит. химии, 2009, Т.64, №9, с.939-943 [3]; K.V.Oskolok and O.V.Monogarova. X-Ray Fluorescence and Atomic Emission Determination of Cobalt in Water Using Polyurethane Foam Sorbents, Moscow University Chemistry Bulletin, 2011, Vol.66, No.3, p.179-183 [4]). Используют также методы контролируемого испарения жидкой фазы на специальных поверхностях (Takao Moriyama. Trace heavy element analysis for wastewater and river water by X-ray fluorescence spectrometry. Examples for ppm to sub ppm level analysis of heavy elements. // The Rigaku J., 2009, Vol.25, No.1, p.13-14, [5]).
Среди известных способов следует выделить способы рентгеноспектрального микроанализа, в которых за счет использования сфокусированного пучка электронов в эмиссионном рентгеноспектральном методе или сфокусированного первичного рентгеновского излучения в рентгенофлуоресцентном методе обеспечивается возможность определения элементов из анализируемых проб (мишеней) микроскопического масштаба (С.Г.Прутченко, Г.А.Григорьева, Ю.Я.Томашпольский. Способ определения содержания примесных химических элементов в природных и промышленных водах и устройство пробоотборника. Патент РФ №2152614, опубл. 10.07.2000 [6]; A.P.Morovov, L.D.Danilin, V.V.Zhmailo, V.N.Funin, Yu.V.Ignat'ev, N.V.Pilipenko, M.G.Vasin, V.V.Nazarov, V.V.Chulkov. Thin film sorbents for TXRF analysis, Advances in X-Ray Analysis, 2000, V.42, p.119-125 [7]; А.А.Болотоков, М.А.Кумахов, А.Н.Груздева, Р.Х.Хамизов, Е.Б.Подгорная. О возможности рентгенофлуоресцентного микроанализа растворов с предварительным концентрированием. Сорбционные и хроматографические процессы, 2011, T.11, Вып.1, с.88-99 [8]).
В частности, в соответствии со способом [6] определяемые элементы концентрируют на не содержащих эти элементы и маскирующие примеси ионитах в виде 1-5 гранул размером 10-1000 мкм с помощью прокачки анализируемых растворов через специальную кассету (пробоотборник) с указанными гранулами, а затем проводят электронно-зондовый рентгеноспектральный микроанализ отдельных гранул ионитов. Данный способ характеризуется следующими недостатками: необходимость использования таких дорогостоящих и малодоступных приборов как электронно-зондовые растровые микроскопы с рентгеноспектральными анализаторами: трудоемкая пробоподготовка, относительно большие пробы исходных анализируемых растворов; аналитические ошибки, связанные с трудностью пересчета содержания элементов, определяемых в твердой фазе, на их содержание в исходном анализируемом растворе в условиях отсутствия количественного извлечения в ходе сорбционного концентрирования; большие времена осуществления полного химико-аналитического цикла, включая пробоподготовку и измерение: более одного часа.
В способе [7] определяемые элементы концентрируют из анализируемых растворов на сорбционных материалах, выполненных в виде тонких пленок, а затем проводят их рентгенофлуоресцентный анализ с использованием рентгеноспектрального анализатора с полным внешним отражением (TXRF), снабженного рентгенооптическим узлом, включающим монохроматирующие зеркала из многослойных гетероструктур. Способ позволяет сократить объем пробы исходного раствора до одной капли, однако все остальные перечисленные выше недостатки способа [6] присущи и способу [7].
Наиболее близким к предлагаемому является способ рентгенофлуоресцентного определения микроэлементов с предварительным их концентрированием из сверхмалых проб воды и водных растворов [8]. В соответствии с этим способом на рентгенопрозрачную гидрофобную пленку помещают микрогранулу гидрофильного материала и каплю анализируемого раствора весьма малого объема (от одного до нескольких микролитров) так, чтобы она покрывала указанную микрогранулу. Каплю испаряют естественным образом или с помощью специальных приспособлений, например, инфракрасной лампы, а микрогранулу, покрытую остатками от испарения капли, анализируют с помощью рентгенофлуоресцентного микроанализатора, рентгенооптическая схема которого собрана на основе фокусирующих рентгеновских линз - линз Кумахова (M.A.Kumakhov. Capillary optics and their use in X-ray analysis, X-ray Spectrom., 2000, V.29, p.343-348 [9]). Способ [8] основан на эффекте, обнаруженном его авторами и состоящем в том, что капля водного раствора при ее испарении на гидрофобной поверхности "стягивается" вокруг указанной микрогранулы так, что определяемые компоненты в конечном итоге практически полностью переносятся на гидрофильную поверхность этой микрогранулы. Если, например, взята микрогранула диаметром 10 мкм и объемом меньше 1 нл, а капля имеет объем 1 мкл, то степень концентрирования превышает три порядка. Другой особенностью, определяющей одно из преимуществ этого способа, является то, что в нем достигается высокая чувствительность за счет исключения фонового рентгеновского излучения. Для этого облучению первичным рентгеновским пучком подвергают единичную микрогранулу, размещенную на предварительно натянутой, например на торец полого цилиндра, рентгенопрозрачной гидрофобной пленке. Способ [8] осуществляют с использованием специального прибора - рентгенофлуоресцентного микроанализатора, включающего рентгенооптический узел с острофокусной маломощной рентгеновской трубкой и поликапиллярной линзой, полупроводниковый детектор с АЦП и выходом на персональный компьютер, предметный столик, а также оптический узел, обеспечивающий юстировку предметного столика для позиционирования мишени (микрогранулы) в нужную точку для облучения первичным рентгеновским пучком. Способ может быть также осуществлен и на других рентгенофлуоресцентных приборах после их дополнительной комплектации рентгенооптическим узлом с фокусирующей линзой. Главным условием является обеспечение легкореализуемой возможности слежения на мониторе компьютера за всеми манипуляциями, включая размещение на пленке микрогранулы, нанесение на нее капли раствора и позиционирование мишени, а также слежения за процессом высыхания капли и оставляемым им следом. Помимо упрощения и удешевления приборного обеспечения и уменьшения объема анализируемого раствора до одной капли, способ [8] позволяет существенно облегчить пробоподготовку и сократить время анализа до 30 мин и меньше.
Однако этому способу при использовании его для анализа ряда растворов присущи ошибки, связанные с количественным переносом определяемых элементов из исходной жидкой фазы на (или в) твердую фазу, непосредственно облучаемую рентгеновским пучком. К этому приводят два фактора:
- если в анализируемом растворе содержатся водорастворимые поверхностно-активные вещества, то в следе от испарения капли на гидрофобной пленке остаются аналитически значимые количества определяемых элементов;
- если в анализируемом растворе содержатся малорастворимые вещества, то в ходе испарения они могут выпадать в виде микрокристаллов в "поле" следа от капли еще до того, как эта капля полностью испарится и "стянет" все содержимое вокруг гидрофильной микрогранулы. Тогда указанные микрокристаллы, тоже обладая определенными гидрофильными свойствами, сами начинают служить дополнительными центрами концентрирования компонентов, содержащихся в исходной капле. Это приводит к потере части компонентов для их аналитического определения.
Оба указанных фактора характерны для природных вод, поэтому способ [8] имеет ограничения при анализе природных вод.
Предлагаемое изобретение направлено на достижение технического результата, заключающегося в уменьшении аналитических ошибок, обусловленных обоими указанными факторами.
Способ рентгенофлуоресцентного определения микроэлементов с предварительным их концентрированием из сверхмалых проб воды и водных растворов по предлагаемому изобретению, как и наиболее близкий к нему известный способ [8], включает стадии:
- помещения микрогранулы гидрофильного материала на предварительно натянутую рентгенопрозрачную гидрофобную пленку,
- взятия капли из анализируемого раствора и
- нанесения ее на указанную пленку таким образом, чтобы указанная микрогранула оказалась покрытой анализируемым раствором,
- испарения указанной капли и анализа микрогранулы с помощью рентгенофлуоресцентного микроанализатора с фокусирующей рентгеновской линзой.
Для достижения названного выше технического результата в предлагаемом способе, в отличие от указанного наиболее близкого к нему известного, указанную пленку перед помещением на нее микрогранулы гидрофильного материала смазывают нерастворимым в воде и водных растворах жидким поверхностно-активным веществом, а в указанную каплю анализируемого раствора вводят от 1 до 5% концентрированной азотной или хлорной кислоты или берут эту каплю из анализируемого раствора, в который предварительно введена азотная или хлорная кислота до достижения ее концентрации от 1 до 5%.
Смазывание рентгенопрозрачной гидрофобной пленки нерастворимым в воде и водных растворах жидким поверхностно-активным веществом препятствует адсорбции компонентов анализируемого раствора, а применение азотной или хлорной кислоты, концентрирующейся в ходе испарения капли, позволяет одновременно достигать двух результатов: разрушать водорастворимые поверхностно-активные вещества, содержащиеся в исходном анализируемом растворе, и не давать осаждаться микро- и нанокристаллам малорастворимых примесей на поверхности пленки.
Данные кислоты не содержат с своем составе элементов, мешающих определению. При этом использование азотной кислоты предпочтительнее, так как она содержит только легкие элементы, которые не определяются методом энергодисперсионного рентгенофлуоресцентного анализа.
В качестве рентгенопрозрачной гидрофобной пленки могут быть использованы любые пленки для рентгенофлуоресцентного анализа, например из следующих материалов: лавсан (майлар), фторопласт (тефлон), поликарбонат.
В качестве нерастворимых поверхностно-активных веществ предпочтительным является использование любой из гомологического ряда жирных органических кислот от пентановой (валериановой) кислоты до нонановой (пеларгоновой) кислоты). Данные кислоты полностью нерастворимы в воде, что является необходимым условием для использования их в предлагаемом способе.
Предлагаемое изобретение иллюстрируется примерами 1-4 и фигурами 1-8, на которых показаны:
- на фиг.1 - фотография микрорентгенофлуоресцентного спектрометра MX-10, использованного в описываемых ниже примерах;
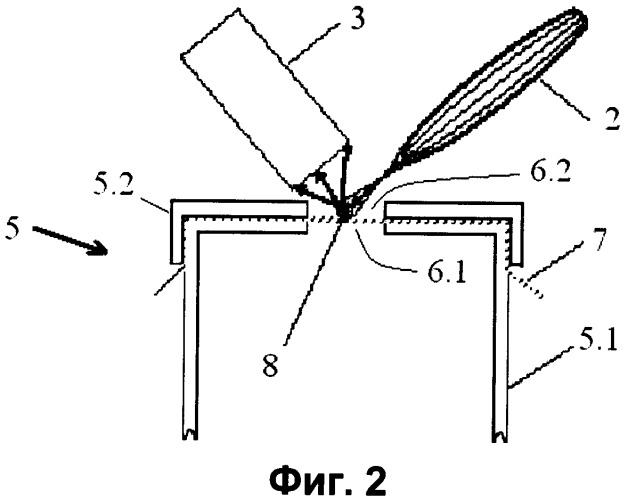
- на фиг.2 - схема получения спектра флуоресценции от микрогранулы гидрофильного материала с использованием прибора МХ-10;
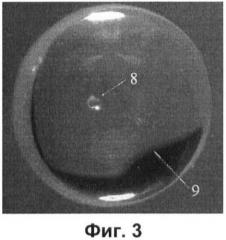
- на фиг.3 - фотография микрогранулы гидрофильного материала с нанесенной на нее каплей анализируемого раствора;
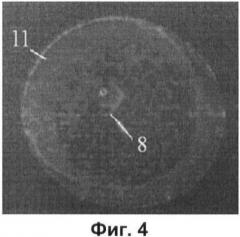
- на фиг.4, относящейся к примеру 1, - след после испарения капли анализируемого раствора, нанесенной на гранулу гидрофильного материала;
- на фиг.5 - спектр флуоресценции микрогранулы гидрофильного материала в случае, иллюстрируемом фиг.4;
- на фиг.6, относящейся к примеру 2, - след после испарения капли анализируемого раствора, в которую предварительно была внесена азотная кислота;
- на фиг.7, относящейся к примеру 3, - след после испарения капли анализируемого раствора при предварительном смазывании места под каплей нерастворимым в воде и водных растворах жидким поверхностно-активным веществом и добавлении азотной кислоты в анализируемый раствор, из которого взята капля;
- на фиг.8, относящейся к примерам 3 и 4, - спектр флуоресценции в случае, иллюстрируемом фиг.7, и случае, отличающемся от него тем, что азотную кислоту вносят непосредственно в каплю анализируемого раствора.
При получении спектра флуоресценции в примерах 1-4 использовался производимый ООО "Институт физической оптики" (Москва, www.xrayoptic.ru) микрорентгенофлуоресцентный спектрометр MX-10, имеющий фокальное пятно размером 26 мкм. На фотографии фиг.1 показаны входящие в состав этого прибора рентгеновская трубка 1, рентгеновская линза (линза Кумахова) 2, полупроводниковый детектор 3 рентгенофлуоресцентного излучения, цифровой микроскоп 4 и предметный столик 10.
В данном приборе реализуется метод энергодисперсионного рентгенофлуоресцентного анализа.
Основные технические характеристики прибора MX-10 представлены в таблице:
| Источник рентгеновского излучения | Рентгеновская трубка с медным анодом |
| Напряжение на трубке, кВ | До 35 |
| Ток трубки, мкА | До 200 |
| Мощность трубки, Вт | До 5 |
| Охлаждение | Воздушное |
| Локальность, мкм | 10-30 |
| Время анализа, сек | От 10 |
| Оптическое увеличение | 90× |
| Вес, кг | 3 |
| Размеры, мм | 200×200×400 |
| Анализируемые элементы | От Al до U |
| Предел обнаружения элементов (в зависимости от элемента), % | 0,003÷100 |
| Интерфейсы | USB |
| Управление | Программное |
Во всех описываемых ниже примерах использовалась схема получения спектра флуоресценции от микрогранулы гидрофильного материала, представленная на фиг.2.
На этой фигуре показаны держатель 5 образцов, натянутая на держателе 5 рентгенопрозрачная гидрофобная пленка 7, размещенная на пленке 7 микрогранула 8 гидрофильного материала с нанесенной на нее каплей анализируемого раствора, а также входящие в состав прибора MX-10 рентгеновская линза 2 (линза Кумахова) для фокусирования излучения на микрогрануле 8 и детектор 3 рентгенофлуоресцентного излучения.
Использовался держатель 5 образцов, изготовленный из фторопласта в виде пустотелого цилиндра 5.1 высотой 20 мм и диаметром 30 мм и надеваемого на него более короткого цилиндра 5.2. Оба цилиндра имеют в торце одинаковые соосные отверстия 6.1, 6.2 диаметром 10 мм. Между указанными цилиндрами во время сборки натягивали, как показано на фиг.2, рентгенопрозрачную гидрофобную пленку 7 толщиной 6 мкм, изготовленную из майлара. Держатель 5 размещали на предметном столике 10 (фиг.1).
Микрогранулу 8 гидрофильного материала, в качестве которого использовался сорбент Sac8, размещали на участке пленки 7 над отверстием 6.1.
Использовались следующие режимные параметры прибора MX-10: напряжение на трубке - 30 кВ, ток трубки - 100 мкА, время анализа - 300 сек.
Пример 1 (по наиболее близкому известному способу [8] для сравнения с ним предлагаемого)
А. Микрогранулу 8 указанного сорбента фиксировали в фокусе цифрового микроскопа 4, следя за всеми манипуляциями на экране компьютера.
Б. С использованием аналитического микрошприца покрывали микрогранулу 8 каплей анализируемого модельного раствора водопроводной воды объемом 1 мкл, содержащей одинаковые количества микрокомпонентов (по 0,2 мг/л): железа, марганца, кобальта и никеля при их совместном присутствии. На фиг.3 капля 9, нанесенная на микрогранулу 8, показана с 90-кратным увеличением.
В. Осуществляли испарение указанной капли в течение 20 мин естественным путем.
Г. Проводили анализ микрогранулы 8, используя рентгенофлуоресцентный микроанализатор MX-10, при фокусировании на ней излучения рентгеновской трубки 1 с помощью линзы 2.
После испарения на пленке 7 в условиях примера 1 оставался след 11 капли, окружающий микрогранулу 8 (см. микрофотографию на фиг.4). Видно, что этот след "размазан" по всей первоначальной площади капли, и он не "стягивается" вокруг микрогранулы 8.
На фиг.5 представлен спектр флуоресценции микрогранулы 8, полученный при выполнении пункта Г примера 1. В нем практически отсутствуют пики, соответствующие введенным в модельный раствор микроэлементам.
Пример 2
Проводили процесс по пунктам А, Б, В, Г примера 1, за исключением того, что перед осуществлением пункта Б брали анализируемый раствор объемом 1 мл и добавляли в него 0,1 мл азотной кислоты квалификации ОСЧ с концентрацией 30%, после перемешивания отбирали каплю с помощью микрошприца и накрывали микрогранулу 8.
На фиг.6 показан результат испарения капли объемом 1 мкл после выполнения пункта В в условиях примера 2 (след 12 капли после ее испарения).
Видно, что добавление азотной кислоты позволило уменьшить след от испарения воды по сравнению с фиг.4, но, как и в предыдущем случае, след размазан хаотично.
Получаемый при выполнении пункта Г спектр практически такой же, как на фиг.5, т.е. как и в условиях примера 1 для наиболее близкого известного способа [8].
Пример 3
Проводили процесс, как описано в примере 2 (т.е. по пунктам А, Б, В, Г примера 1 с учетом отмеченного выше отличия от него примера 2), однако перед осуществлением пункта А пленку 7 смазывали нерастворимым в воде и водных растворах жидким поверхностно-активным веществом, в качестве которого использовали пеларгоновую кислоту.
На фиг.7 показан результат после выполнения пункта В в условиях примера 3 (след 13 капли после ее испарения), а на фиг.8 представлен спектр флуоресценции, полученный при выполнении пункта Г. Хорошо видны пики микроэлементов, содержащихся в модельном растворе.
Пример 4
Проводили процесс, как описано в примере 3, с той разницей, что после осуществления пункта Б азотную кислоту с концентрацией 30% вносили не в анализируемый раствор, из которого брали каплю, а добавляли ее в количестве 0,1 мкл непосредственно в каплю.
Результат после выполнения пункта В в условиях примера 4 и спектр флуоресценции, полученный при выполнении пункта Г, практически совпадают с представленными на фиг.7 и 8 для примера 3. Пики микроэлементов, содержащихся в модельном растворе, хорошо видны на полученном спектре.
Следует заметить, что использование в экспериментах конкретного экземпляра прибора MX-10, имеющего рентгеновскую трубку с медным анодом, не позволило провести анализ модельного раствора с введением в него более тяжелых элементов. Совершенно очевидно, что при наличии трубки, например, с молибденовым анодом, такие элементы, например, Cu и Zn, тоже были бы успешно определены.
Сопоставление данных, полученных в описанных примерах, показывает, что совместное использование особенностей предлагаемого способа, а именно - смазывание места "высадки" капли пеларгоновой кислотой и добавление в анализируемый раствор азотной кислоты обеспечивают достижение технического результата, названного выше перед изложением сущности изобретения. Капля анализируемого раствора, испаряясь, стягивается в точку вокруг микрогранулы 8, благодаря чему спектр рентгенофлуоресценции имеет хорошо различимые пики определяемых элементов. Достигается высокая чувствительность при анализе природных вод и техногенных растворов, включая промышленные сточные воды, в экологических, технологических или иных целях, в сочетании с простотой и экспрессностью метода.
Источники информации
1. Ю.А.Золотов, Г.И.Цизин, С.Г.Дмитриенко, Е.И.Моросанова. Сорбционное концентрирование микрокомпонентов из растворов. Применение в неорганическом анализе, М., "Наука", 2007, с.320.
2. О.Б.Моходоева, Г.В.Мясоедова, И.В.Кубракова. Сорбционное концентрирование в комбинированных методах определения благородных металлов, Ж. аналит. химии, 2007, Т.62, №7, с.679-695.
3. Р.Х.Хамизов, А.Н.Груздева, М.Г.Токмачев, Г.И.Цизин, Н.А.Тихонов, М.А.Кумахов. Высокочувствительный рентгенофлуоресцентный анализ растворов с использованием сорбционной накопительной микросистемы, Ж. аналит. химии, 2009, Т.64, №9, с.939-943.
4. K.V.Oskolok and O.V.Monogarova. X-Ray Fluorescence and Atomic Emission Determination of Cobalt in Water Using Polyurethane Foam Sorbents, Moscow University Chemistry Bulletin, 2011, Vol.66, №3, p.179-183.
5. Takao Moriyama. Trace heavy element analysis for wastewater and river water by X-ray fluorescence spectrometry. Examples for ppm to sub ppm level analysis of heavy elements. // The Rigaku J., 2009, Vol.25, №1, p.l3-14.
6. С.Г.Прутченко, Г.А.Григорьева, Ю.Я.Томашпольский. Способ определения содержания примесных химических элементов в природных и промышленных водах и устройство пробоотборника. Патент РФ №2152614, опубл. 10.07.2000.
7. A.P.Morovov, L.D.Danilin, V.V.Zhmailo, V.N.Funin, Yu.V.Ignat'ev, N.V.Pilipenko, M.G.Vasin, V.V.Nazarov, V.V.Chulkov. Thin film sorbents for TXRF analysis, Advances in X-Ray Analysis, 2000, V.42, p.119-125.
8. А.А.Болотоков, М.А.Кумахов, А.Н.Груздева, Р.Х.Хамизов, Е.Б.Подгорная. О возможности рентгенофлуоресцентного микроанализа растворов с предварительным концентрированием. Сорбционные и хроматографические процессы, 2011, T.11, Вып.1, с.88-99.
9. M.A.Kumakhov. Capillary optics and their use in X-ray analysis, X-ray Spectrom., 2000, V.29, p.343-348.
1. Способ рентгенофлуоресцентного определения микроэлементов с предварительным их концентрированием из сверхмалых проб воды и водных растворов, включающий помещение микрогранулы гидрофильного материала на предварительно натянутую рентгенопрозрачную гидрофобную пленку, взятие капли из анализируемого раствора и нанесение ее на указанную пленку с покрытием указанной микрогранулы, испарение указанной капли и анализ указанной микрогранулы с помощью рентгенофлуоресцентного микроанализатора с фокусирующей рентгеновской линзой, отличающийся тем, что указанную пленку перед помещением на нее микрогранулы гидрофильного материала смазывают нерастворимым в воде и водных растворах жидким поверхностно-активным веществом, а в указанную каплю анализируемого раствора вводят от 1 до 5% концентрированной азотной или хлорной кислоты или берут эту каплю из анализируемого раствора, в который предварительно введена азотная или хлорная кислота до достижения ее концентрации от 1 до 5%.
2. Способ по п.1, отличающийся тем, что в качестве рентгенопрозрачной гидрофобной пленки используют пленку из группы материалов: майлар, фторопласт, полиэтилен, поликарбонат.
3. Способ по п.1 или 2, отличающийся тем, что в качестве нерастворимого в воде и водных растворах жидкого поверхностно-активного вещества используют любую из гомологического ряда жирных органических кислот от пентановой кислоты до нонановой кислоты.