Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к способу оценки возможности энтерального питания у больных с абдоминальным сепсисом. Сущность способа заключается в том, что первоначально опорожняют желудок, после чего в желудок вводят маркер, в качестве которого используют ацетаминофен. Через 15-40 минут определяют его концентрацию в плазме крови, по которой определяют возможность полного энтерального питания при абдоминальном сепсисе. При значениях ацетоминофена до 4 мкг/мл проведение назогастрального питания у больных считают невозможным, а при значении маркера более 6 мкг/мл проведение назогастрального питания у больных считают возможным. Использование заявленного способа позволяет повысить эффективность и безболезненность определения возможности энтерального питания при абдоминальном сепсисе. 2 з.п. ф-лы, 1 табл., 3 пр.
Реферат
Предлагаемое изобретение «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» относится к медицине, а именно к анестезиологии и реаниматологии, и может быть использовано для оценки функции желудочно-кишечного тракта при различных формах кишечной недостаточности, в частности при абдоминальном сепсисе.
Известны способы диагностики послеоперационных нарушений моторно-эвакуаторной функции желудочно-кишечного тракта, базирующиеся на данных аускультации фанендоскопом, баллонографии, иономанометрии, прямой миографии а также использования специальных зондов (см. Панков В.И. Профилактика и лечение послеоперационных динамических нарушений моторики желудочно-кишечного тракта. Дисс. д-ра наук. Рязань, 1980 г.).
Недостатками известных методов являются низкая эффективность и информативность, которая не обеспечивает возможности определения оптимального объема энтерального питания при абдоминальном сепсисе, а также высокая себестоимость, необходимость специального обучения обслуживающего персонала, болезненность для пациента, осложнения и побочные реакции.
Данные недостатки обусловлены тем, что из-за тяжести состояния больных такие малоинформативные методы трудно переносимы, содержат субъективные составляющие информации и не пригодны для динамического мониторинга моторики желудочно-кишечного тракта и не обеспечивают возможности определения оптимального объема энтерального питания при абдоминальном сепсисе.
Известен способ диагностики желудочно-кишечного тракта с использованием маркера (см. Miyauchi Т, Ishikawa M, Tashiro S, Hisaeda H, Nagasawa H, Himeno K (1997 г.) «Acetaminophen absorption test as a marker of small bowel transplant rejection». Transplantation 63: 1179-1182), когда при трансплантации кишечника у крыс в качестве маркера отторжения трансплантата использовали способность кишечника абсорбировать ацетаминофен из ее просвета. При этом во время оперативного вмешательства крысам устанавливался зонд непосредственно в кишечник. В последующем в первые, третьи и седьмые сутки в этот зонд вводили ацетаминофен в дозировке 0,15 г/кг и спустя 15 минут измеряли концентрацию парацетамола в сыворотке крови животного. На основании секционного материала они сравнили способность кишечника абсорбировать ацетаминофен. Выяснилось, что даже при минимальных морфологических изменениях в трансплантате снижается способность кишечника абсорбировать ацитоминофен. Полученные результаты позволили рекомендовать этот тест как высокочувствительный метод ранней диагностики отторжения трансплантата кишечника.
Недостатком данного способа является низкая эффективность и отсутствие возможности определения оптимального объема энтерального питания при абдоминальном сепсисе.
Данный недостаток обусловлен отсутствием оценки эвакуаторной способности желудка и отсутствием определения оптимального объема энтерального питания, а также тем, что в период исследования не учитывался суточный сброс по назогастральному зонду и поэтому не определяется оптимальный объем энтерального питания при абдоминальном сепсисе.
Известен способ оценки эвакуаторной способности желудка (См. Heading R.C., Nimmo J., Prescott and Tothill P. Br.J.Hharmac. 1973, 47, 415-421). Сущность известного способа заключается в следующем. У выздоравливающих больных определяли скорость опорожнения желудка, используя метод сцинтиграфии, а полученные значения сравнивали с изменением концентрации ацетаминофена в плазме крови и в моче после приема этими же пациентами 1,5 г препарата через рот. Полученные результаты доказали, что имеется высокая корреляционная зависимость между временем опорожнения желудка и временем регистрации пиковых значений концентрации ацетаминофена в плазме крови и моче. Таким образом, время максимальных значений парацетамола в плазме крови и в моче напрямую зависело от скорости эвакуации желудочного содержимого в тонкий кишечник.
Недостатками данного способа являются высокая сложность и себестоимость, низкая эффективность, наличие послеоперационных осложнений и побочных реакций и отсутствие возможности определения оптимального объема энтерального питания при абдоминальном сепсисе.
Данные недостатки обусловлены тем, что в известном способе слишком большая продолжительность исследования по времени, концентрация ацетаминофена в сыворотке крови регистрируется на протяжении 8 часов, а в моче его метаболиты определяют на протяжении суток, кроме того, исследования выполнялись у больных без абдоминального сепсиса, не учитывался в период исследований суточный сброс по назогастральному зонду, не был выделен оптимальный промежуток времени, в котором изменение концентрации ацеминофена в сыворотке крови наиболее информативно отражало эвакуаторную способность желудка. Поскольку абдоминальный сепсис часто сопровождается развитием тубулоинтерстициального нефрита, данный эффект значительно ограничивает использование методики пo определению метаболитов ацетаминофена в моче.
Наиболее близким по технической сущности к заявляемому техническому решению является принятый за прототип способ нутритивной поддержки при критических состояниях (См. Лейдерман И.Н. и др. «Современная концепция нутритивной поддержки при критических состояниях». 5 ключевых проблем, «Интенсивная терапия №1, 2005) [http://www.multis.ru/N1-2005.htlm], в котором определяют показания к энтеральному питанию по количеству маркера в крови.
Недостатком известного способа является низкая эффективность, высокая себестоимость.
Данный недостаток обусловлен отсутствием прогнозорования объема энтерального питания и функции желудочно-кишечного тракта у больных с абдоминальным сепсисом (перитонитом), кроме того в качестве маркера не используют дешевый и доступный препарат - ацетаминофен.
Задачей заявляемого изобретения является разработка способа, позволяющего оценить возможность и объем энтерального питания и функции желудочно-кишечного тракта у больных с абдоминальным сепсисом (перитонитом).
Техническим результатом заявляемого изобретения «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» является техническая простота, снижение себестоимости и безболезненности для пациента, определение оптимального объема энтерального питания при абдоминальном сепсисе и отсутствие послеоперационных осложнений и побочных реакций.
Поставленный технический результат достигается тем, что в известном способе оценки возможности энтерального питания у больных с абдоминальным сепсисом, путем определения показания к энтеральному питанию по количеству маркера в крови, согласно изобретению, первоначально опорожняют желудок, после чего в желудок вводят маркер, в качестве которого используют ацетаминофен в количестве 0,5 грамма, через 15-40 минут, после поступления в желудок маркера, определяют его концентрацию в плазме крови, по которой определяют возможность полного энтерального питания при абдоминальном сепсисе, при этом при значениях ацетаминофена до 6 мкг/мл проведение назогастрального питания у больных считают невозможным из-за нарушения эвакуации из желудка или снижения всасывательной способности кишечника, а при значении маркера более 6 мкг/мл проведение назогастрального питания у больных считают возможным, т.к. больные усваивают более 1000 мл/сут питания, вводимого назогастрально, причем первоначальное опорожнение желудка проводят с помощью назогастрального зонда, а концентрацию ацетаминофена в плазме крови определяют иммуноферментным анализатором, используя технологию флуоресцентного поляризационного иммуноанализа.
Между отличительными признаками и достигнутым техническим результатом существует следующая причинно-следственная связь.
В отличие от аналогов и прототипа преимуществом предлагаемого изобретения «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» является повышение точности определения объема энтерального питания, который может усвоить больной при абдоминальном сепсисе (перитоните), высокая эффективность и безболезненность для больного пациента, отсутствие осложнений и побочных реакций, поскольку в качестве маркера применяют известный испытанный многими годами применения ацетаминофен (парацетамол) в количестве 0,5 грамм, не дающий осложнений и побочных реакций. По концентрации предложенного маркера-цетаминофена в плазме крови после введения ацетаминофена в желудок оценивают эвакуаторную способность желудка и всасывательную способность кишечника и определяют объем энтерального питания, который может усвоить больной при абдоминальном сепсисе, при этом при значениях ацетаминофена до 6 мкг/мл проведение назогастрального питания у больных считают невозможным из-за нарушения эвакуации из желудка или снижения всасывательной способности кишечника, а при значении маркера более 6 мкг/мл проведение назогастрального питания у больных считают возможным, т.к. больные усваивают более 1000 мл/сут питания вводимого назогастрально. В данном случае следует заметить, что сложность проведения энтерального питания, например, при абдоминальном сепсисе связана с развитием у пациентов синдрома кишечной недостаточности, который характеризуется сочетанием расстройств ее моторной, эвакуаторной, секреторной, переваривающей и всасывающей функции (см. Гельфанд Б.Р., 1992; Савельев B.C., 1993; и др.). Таким образом, чтобы оценить возможности проведения энтерального питания необходимо знать эвакуаторную способность желудка и способность кишечника всасывать нутриенты, поэтому регистрацию концентрации маркера-ацетаминофена в плазме крови проводят в определенный временной интервал, именно через 15-40 минут после поступления ацетаминофена в желудок, в котором выделяют информативные значения концентрации маркера-ацетаминофена, т.е. определяют его концентрацию в плазме крови, при которой возможно полное энтеральное питание, или, например, при значениях ацетаминофена до 6 мкг/мл проведение назогастрального питания у больных считают невозможным из-за нарушения эвакуации из желудка или снижения всасывательной способности кишечника. Использование при первоначальном опорожнении желудка обычного назогастрального зонда, а для определения концентрации ацетаминофена в плазме крови применение иммуноферментного анализатора с использованием технологии флуоресцентного поляризационного иммуноанализа также снижает себестоимость. Дополнительным техническим результатом является также то, что использование в качестве маркера ацетаминофена в стабильном минимальном количестве 0,5 грамма позволяет оценить не только эвакуаторную способность желудка, но и всасывательную способность кишечника. Основными преимуществами предлагаемого изобретения «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» являются техническая простота, поскольку «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» не требует дорогостоящего оборудования и специального обучения персонала, не требует специального расчета количества маркера, что значительно снижает себестоимость предлагаемого способа. Преимуществом предлагаемого способа оценки возможности энтерального питания у больных с абдоминальным сепсисом является также высокая эффективность, атравматичность и безболезненность для больного пациента, отсутствие осложнений и побочных реакций, поскольку по состоянию больного выделяют возможность определенного объема энтерального питания, который может усвоить больной при абдоминальном сепсисе, что отражено в примерах проведенного лечения на пациентах - людях различного возраста. Следует заметить, что преимуществами предлагаемого способа оценки возможности энтерального питания у больных с абдоминальным сепсисом являются не только техническая простота, а также то, что исключается, в отличие от аналогов и прототипа предварительная, в том числе хирургическая, обработка и находит широкое применение обычный доступный и дешевый лечебный препарат ацетаминофен (парацетамол), что способствует, в совокупности признаков, достижению технического результата, т.е. снижению себестоимости при минимизации компонентов, повышению эффективности, поскольку очень быстро определяется степень адекватного баланса энергии путем определения концентрации ацетаминофена в плазме крови, через 15-40 мин после его введения в желудок и, конечно, основное - это то, что определяется оптимальный объем энтерального питания при абдоминальном сепсисе. Надо заметить, что в настоящий момент общепризнанной считается необходимость проведения нутритивной поддержки всех пациентов, находящихся в тяжелом состоянии и\или имеющих белково-энергетическую недостаточность.
Проведенный заявителем анализ уровня техники, включающий поиск по патентным и научно-техническим источникам информации и выявление источников, содержащих сведения об аналогах заявленного изобретения «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом», позволил установить, что заявитель не обнаружил источник, характеризующийся признаками, тождественными совокупности всех существенных признаков заявленного изобретения.
По имеющимся у заявителя сведениям, совокупность существенных признаков заявляемого изобретения «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» не известна из уровня техники, что позволяет сделать вывод о соответствии изобретения критерию "новизна". Определение из перечня выявленных аналогов и прототипа, как наиболее близких по совокупности признаков аналогов, позволил выявить совокупность существенных, по отношению к усматриваемому заявителем техническому результату, отличительных признаков в заявляемом способе оценки возможности энтерального питания у больных с абдоминальным сепсисом, изложенных в формуле изобретения. Следовательно, заявленное изобретение «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» соответствует критерию "новизна".
Для проверки соответствия заявленного изобретения критерию "изобретательский уровень" заявитель провел дополнительный поиск известных решений, чтобы выявить признаки, совпадающие с отличительными от прототипа признаками заявленного способа оценки возможности энтерального питания у больных с абдоминальным сепсисом. Результаты поиска показали, что заявленный «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» не вытекает для специалиста явным образом из известного уровня техники, поскольку из уровня техники, определенного заявителем, не выявлено влияние предусматриваемых существенными признаками заявленного изобретения преобразований для достижения технического результата.
Следовательно, заявленное изобретение «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» соответствует критерию "изобретательский уровень".
Таким образом, изложенные сведения свидетельствуют о выполнении при использовании заявленного способа оценки возможности энтерального питания у больных с абдоминальным сепсисом совокупности условий в том виде, как заявляемый способ охарактеризован в формуле изобретения, т.е. подтверждена возможность его осуществления с помощью технических средств в описанных в заявке примерах. Средства, воплощающие заявленный способ оценки возможности энтерального питания у больных с абдоминальным сепсисом, при его осуществлении, способны обеспечить достижение усматриваемого заявителем технического результата, а именно снижение себестоимости, повышение эффективности, определение оптимального объема энтерального питания при абдоминальном сепсисе, а также снижение процента послеоперационных осложнений, следовательно, заявленное изобретение «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» соответствует условию "промышленная применимость".
Сущность заявляемого изобретения «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» поясняется примерами конкретного выполнения и рисунками:
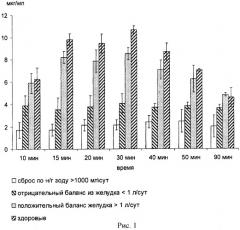
- на рис.1 показана динамика концентрации ацетаминофена в плазме крови у здоровых людей и у больных пациентов при абдоминальном сепсисе;
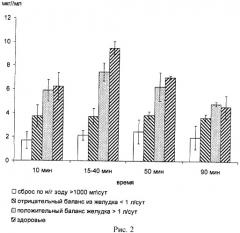
- на рис.2 показана динамика концентрации ацетаминофена в плазме крови у здоровых людей и у больных пациентов при абдоминальном сепсисе со средней концентрацией ацетаминофена в плазме крови в интервале 15-40 мин.
Примеры конкретного выполнения.
Важным фактором выживаемости больных с абдоминальным сепсисом (перитонитом) является достижение адекватного баланса энергии. В настоящий момент общепризнанной считается необходимость проведения нутритивной поддержки всех пациентов, находящихся в тяжелом состоянии и\или имеющих белково-энергетическую недостаточность. Учитывая высокий расход энергии и выраженную белковую недостаточность, становится понятным, почему трофическая поддержка больного с развившимся синдромом полиорганной недостаточности при распространенных формах абдоминального сепсиса (перитонита) - один из наиболее трудно решаемых компонентов программы интенсивной терапии.
Заявляемый «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» осуществляли следующим образом. У больных с абдоминальным сепсисом устанавливали назогастральный зонд и опорожняли желудок, после этого в него вводили 0,5 гр ацетаминофена (перфалган - действующее вещество парацетамол, производитель «Бристол-Майерс Сквибб», Франция) и через 10, 15, 20, 30, 40, 50 и 90 минут (рис.1) проводили забор 5 мл венозной крови. На иммуноферментном анализаторе AxSYM «ABBOT Laboratories» USA, используя технологию флуоресцентного поляризационного иммуноанализа, определяли концентрацию ацетаминофена в плазме крови каждой партии забора венозной крови, взятой через упомянутые выше временные интервалы (рис.1). В дальнейшем на протяжении 24 часов регистрировали баланс введенного и выделенного по назогастральному зонду питания. Таким образом, установили, что концентрация ацетаминофена в плазме крови у здоровых людей, в промежуток времени с 15 мин по 40 мин, после приема 0,5 гр ацетаминофена через рот, была в пределах от 7,21 мкг/мл до 12, 2 мкг/мл. У больных при абдоминальном сепсисе, у которых баланс введенного в назогастральный зонд был положительным и суммарно пациенты усвоили >1000 мл/сут питания (Нутрикомп АНД Браун файбер, производитель Б.Браун Медикал, Чили), показатели ацетаминофена в плазме крови в тот же временной промежуток колебались от 6,0 мкг/мл до 11,1 мкг/мл. Если баланс введенного в назогастральный зонд был отрицательным и сброс по назогастральному зонду был более 1000 мл/сут, показатели концентрации ацетаминофена в плазме крови были менее 4 мкг/мл (рис.2).
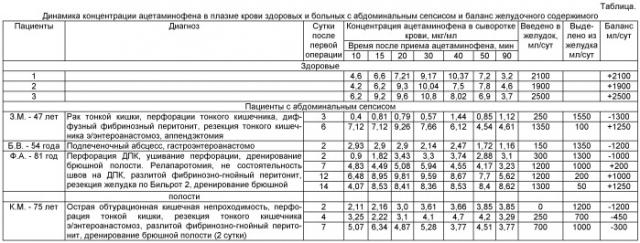
Пример №1 (таблица). Наблюдение проведено за 3-мя практически здоровыми людьми, составляющими контрольную группу. Задача исследования: установить закономерности поступления ацетаминофена в кровь из желудочно-кишечного тракта при нормально функционирующем кишечнике. Для достижения поставленной задачи утром в 10.00 на голодный желудок трем, практически здоровым, добровольцам в возрасте 27 и 32 лет, 44 года дали выпить 0,5 гр парацетамола через рот. В 10.10, 10.15, 10.20, 10.30, 10.40, 10.50 и в 11.30 затем проводили забор 5 мл венозной крови, в плазме которой определяли концентрацию ацетаминофена. Было установлено, что в данной группе во всех наблюдениях (см. таблицу) максимальные значения регистрировались в интервале с 15 до 40 минут и колебались в диапазоне от 6,2 мкг/мл до 10,8 мкг/мл. В дальнейшем каждый доброволец учитывал объем съеденного и выпитого в эти сутки.
Пример №2 (таблица). Больной З.М., 47 лет, был доставлен 01.02.11 в Медсанчасть с жалобами на интенсивные боли в правых отделах живота, поясничной области, тошноту, сухость во рту, слабость. SIRS (Systemic inflammatory response syndrome) 3 признака - ЧДД (Частота дыхательных движений) 22 в мин, температура 38,2°С, ЧСС (Частота сердечных сокращений) 108 уд./мин. Во время операции 01.02.11. обнаружили на петлях кишечника больше в правой половине налет фибрина. При ревизии в 70 см от связки Трейца, циркулярная опухоль, практически закрывающая просвет кишки, на брыжеечном крае перфорация. Изменения червеобразного отростка по типу флегмонозных. Произвели выделение петли кишки, несущей опухоль на протяжении 60 см. Провели резекцию тонкой кишки аппаратами УО-60, концы кишки укрыли кисетными и серозными швами. Провели анастомоз бок в бок 40 см от связки Трейца шириной 7 см, 2-рядно. Провели аппендэктомию лигатурно-инвагинационным способом. Диагноз после операции: рак тонкой кишки с перфорацией. Диффузный фибринозный перитонит. Абдоминальный сепсис. 03.02.11 провели опорожнение желудка, в него ввели 0,5 г ацетаминофена (перфалган - действующее вещество ацетаминофен (парацетамол), производитель «Бристол-Майерс Сквибб», Франция), через 10, 15, 20, 30, 40, 50 и 90 минут забирали по 5 мл венозной крови. Определили, что максимальное значение концентрации ацетаминофена в плазме крови - 1,44 мкг/мл приходилось на 40 минуту. За последующие сутки в назогастральный зонд ввели 250 мл питания (Нутрикомп АНД Браун файбер, производитель Б.Браун Медикал, Чили), при этом было выделено 1550 мл/сут. Таким образом, сброс по желудочному зонду составил 1350 мл/сут. Исследование повторили 07.02.11. Максимальное значение концентрации ацетаминофена в плазме крови - 9,26 мкг/мл регистрируется на 20 мин, а во временной интервал с 15 мин по 40 мин показатель концентрации ацетаминофена в плазме крови был всегда >6 мкг/мл. За последующие сутки в назогастральный зонд ввели 1350 мл/сут питания, а сброс по нему составил 100 мл/сут. Таким образом, пациент усвоил введенное ему питание. Данный пример иллюстрирует, что примененный предложенный способ оценки возможности энтерального питания у больных с абдоминальным сепсисом позволил определить, что на третьи сутки после операции больному показано только парентеральное питание, а на седьмые сутки возможно полное энтеральное питание.
Пример №3 (таблица). Больная Ф.А., 81 год, поступила в Медсанчасть 01.03.11 с клиникой острого живота. В этот же день выполнили операцию - ушивание язвы ДПК (двенадцатиперстной кишки). Дальнейшее течение осложнилось развитием тяжелого сепсиса с полиорганной недостаточностью. Максимальное значение по интегральной шкале оценки тяжести состояния АРАСНЕ II (Acute physiology and Chronic Health Evaluation) составило 22 балла, а по SOFA (Sepsis-related Organ Failure Assessments Score/ Sequential Organ Failure Assessment) 6 баллов. Провели релапаротомию 08.03.11, ушивание несостоятельности швов ДПК, санацию и дренирование брюшной полости. Сформировали лапаростому. Разлитой фибринозно-гнойный перитонит. Перитонит не разрешался и 12.03.11 провели повторную релапаротомию, на которой после отсечения пряди сальника от язвы, у верхнего края ушитой язвы обнаружили подтекание желудочного содержимого. Выполнили резекцию желудка по Бильрот 2. Пациентку выписали из стационара 22.03.11. Во время нахождения больной в стационаре 04.03.11, 09.03.11, 14.03.11 и 16.06.11 проводили оценку возможности энтерального питания с использованием предлагаемого способа. В период наиболее выраженных патофизиологических сдвигов и проявления синдрома кишечной недостаточности (04.03.11) максимальную концентрацию ацетаминофена в плазме крови (3,74 мкг/мл) регистрировали на 40 мин. Назогастральный сброс составил 1300 мл/сут. В этот период возможно было только полное парентеральное питание. Исследования, проводимые 09.03.11, показали, что концентрация ацетаминофена в плазме крови в период с 15 мин по 40 мин была больше 4 мкг/мл, но меньше 6 мкг/мл. В последующие 24 часа в желудок было введено 1200 мл указанного выше парентерального питания, сброс из желудка составил 1000 мл/сут, т.е. в этот период возможно было смешанное питание. Исследования, которые проводили на 2 и 4 сутки после последней операции (резекции желудка) убедительно показывали, что при положительном балансе вводимого в желудок >1000 мл/сут в интервале с 15 мин по 40 мин концентрация ацетаминофена в плазме крови была больше 6 мкг/мл.
Таким образом, заявляемый способ позволил установить, что в норме после приема 0,5 гр ацетаминофена препарат, проходя желудок, всасывается в верхних отделах тонкого кишечника и его концентрация в плазме крови в интервале с 15 мин до 40 мин всегда выше 6 мкг/мл (пример № 1). Развитие синдрома кишечной недостаточности при абдоминальном сепсисе сопровождается снижением эвакуаторной способности желудка и всасывательной функции кишечника. Примеры №2 и №3 убедительно демонстрировали связь между выраженностью синдрома кишечной недостаточности и способностью ацетаминофена проникать в кровь из желудочно-кишечного тракта, т.е. эмпирически был выявлен информативный временной промежуток, в который значения концентрации ацетаминофена наиболее информативно отражают выраженность синдрома кишечной недостаточности. Определены количественные показатели концентрации ацетаминофена в плазме крови, которые способны прогнозировать баланс между введенным и выделенным из желудка в последующие сутки. С учетом этого количественного показателя доктор аргументировано определит объем энтерального питания в предстоящие сутки при составлении программы нутритивной поддержки, способствующей предупреждению осложнений. Предложенный способ определил возможность необходимости у больных с перитонитом аргументировано назначать энтеральное питание с учетом выраженности синдрома кишечной недостаточности. При смешанном типе нутритивной поддержки учитывали, какой объем энтерального питания может усвоить пациент для расчета необходимого количества парентерального питания, поскольку:
- при концентрации ацетаминофена в плазме крови больше 6 мкг/мл больные усваивали более 1000 мл/сут питания, вводимого назогастрально;
- при значениях ацетаминофена менее 4 мкг/мл проведение назогастрального питания у больных невозможно из-за нарушения его эвакуации из желудка или снижения всасывательной способности кишечника.
Предлагаемый «Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом» обеспечивает достижение поставленного заявителем технического результата, поскольку способ технически прост, эффективен, снижает себестоимость, является безболезненным для пациента, исключает осложнения и побочные реакции, а эффективность подтверждается тем, он обеспечивает определение оптимального объема энтерального питания, поскольку позволил установить закономерность изменения концентрации в сыворотке крови у больных с абдоминальным сепсисом от эвакуаторной способности желудка и всасывательной способности тонкого кишечника. Кроме того, отслежена также закономерность между количеством усвоенного энтерального питания и способностью абсорбировать ацетаминофен из кишечника. Полученные данные позволяют наиболее точно определить возможный объем предстоящего энтерального питания больных с абдоминальным сепсисом.
1. Способ оценки возможности энтерального питания у больных с абдоминальным сепсисом путем определения показания к энтеральному питанию по количеству маркера в крови, отличающийся тем, что первоначально опорожняют желудок, после чего в желудок вводят маркер, в качестве которого используют ацетаминофен в количестве 0,5 г, через 15-40 мин после поступления в желудок маркера определяют его концентрацию в плазме крови, по которой определяют возможность полного энтерального питания при абдоминальном сепсисе, при этом при значениях ацетаминофена до 4 мкг/мл проведение назогастрального питания у больных считают невозможным из-за нарушения эвакуации из желудка или снижения всасывательной способности кишечника, а при значении маркера более 6 мкг/мл проведение назогастрального питания у больных считают возможным, так как больные усваивают более 1000 мл/сут питания вводимого назогастрально.
2. Способ по п.1, отличающийся тем, что первоначальное опорожнение желудка проводят с помощью назогастрального зонда.
3. Способ по п.1, отличающийся тем, что концентрацию ацетаминофена в сыворотке крови определяют иммуноферментным анализатором, используя технологию флуоресцентного поляризационного иммуноанализа.